文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷老教材)
黄金卷06
(考试时间:50分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Bi 209
第Ⅰ卷
一、单项选择题:共7题,每题6分,共42分。每题只有一个选项最符合题意。
1.化学与人类生产、生活、社会可持续发展等密切相关。下列说法正确的是
A.中国空间站的食物可谓太空一绝,航天员喜欢吃的“宫保鸡丁”的主要成分是有机物
B.“可燃冰”是一种有待大量开发的新能源,开采过程中发生大量泄漏不会对环境产生影响
C.清华大学打造的世界首款异构融合类脑芯片——天机芯的主要材料与光导纤维的相同
D.用于制造“山东舰”上舰载机降落拦阻索的特种钢属于新型无机非金属材料
2.用N 代表阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,1.12L苯含有C-H键的数目为0.3 N
A
B.25°C时K (CaSO)=9×10-6,则该温度下CaSO 饱和溶液中含有3×10-3N 个Ca2+
sp 4 4 A
C.46 克C HO分子中含极性键数目一定是7N
2 6 A
D.在反应KClO+6HCl= KCl+3Cl ↑+3H O中,每生成3 molCl 转移的电子数为5N
3 2 2 2 A
3.一种麻醉剂的分子结构式如图所示。其中,X的原子核只有1个质子;元素Y、Z、W原子序数依次增
大,且均位于X的下一周期;元素E的原子比W原子多8个电子。下列说法不正确的是
A. 是一种强氧化性酸 B.非金属性:
C.Y、W、E的氢化物中只有极性键 D. 中,Z的化合价为 价
4.有机物M是合成抗过敏药物色甘酸钠的中间体,结构简式如下图。下列关于该有机物的说法正确的是
A.属于芳香烃 B.能与NaOH溶液反应
C.苯环上的一氯取代物有4种 D.所有碳原子不可能共平面
5.2022 年中国团队在巴塞罗那获得“镁未来技术奖”。一种以MgCl -聚乙烯醇为电解液的镁电池如图所
2
示。下 列说法不正确的是A.放电时,正极的电极反应式为Mg2+ +2e- +V O=MgVO
2 5 2 5
B.放电一段时间后,聚乙烯醇中的c(Mg2+)几乎保持不变
C.充电时,Mg2+ 嵌入VO 晶格中
2 5
D.若将电解液换成MgCl 水溶液,工作时电池可能产生鼓包
2
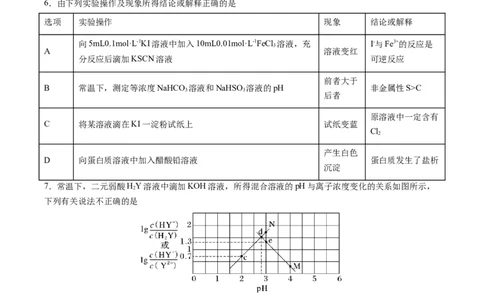
6.由下列实验操作及现象所得结论或解释正确的是
选项 实验操作 现象 结论或解释
向5mL0.1mol·L-1KI溶液中加入10mL0.01mol·L-1FeCl 溶液,充 I-与Fe3+的反应是
3
A 溶液变红
分反应后滴加KSCN溶液 可逆反应
前者大于
B 常温下,测定等浓度NaHCO 溶液和NaHSO 溶液的pH 非金属性S>C
3 3
后者
原溶液中一定含有
C 将某溶液滴在KI一淀粉试纸上 试纸变蓝
Cl
2
产生白色
D 向蛋白质溶液中加入醋酸铅溶液 蛋白质发生了盐析
沉淀
7.常温下,二元弱酸HY溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示,
2
下列有关说法不正确的是
A.曲线M表示pH与lg 的变化关系
B.NaHY溶液显酸性
C.交点d对应的pH=2.8
D.e点溶液中:c(HY-)>c(H Y)>c(Y2-)>c(H+)>c(OH-)
2
第Ⅱ卷
二、非选择题:包括必考题和选考题两部分,共58分。
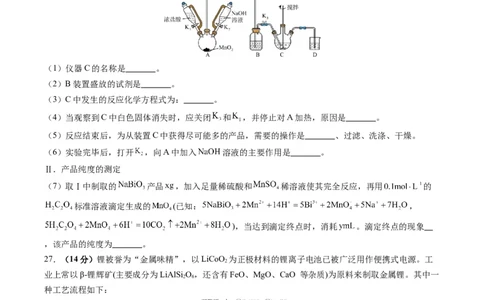
(一)必考题(共43分)26.(14分)铋酸钠 是一种新型有效的光催化剂,也被广泛应用于制药业。某兴趣小组设计实
验制取铋酸钠并探究其应用。
Ⅰ.制取铋酸钠
利用白色且难溶于水的 在 溶液中,在充分搅拌的情况下与 反应制备 ,实验装置
如下图(加热和夹持仪器已略去)。
已知: 粉末呈浅黄色,不溶于冷水,遇沸水或酸溶液迅速分解。
请按要求回答下列问题:
(1)仪器C的名称是 。
(2)B装置盛放的试剂是 。
(3)C中发生的反应化学方程式为: 。
(4)当观察到C中白色固体消失时,应关闭 和 ,并停止对A加热,原因是 。
(5)反应结束后,为从装置C中获得尽可能多的产品,需要的操作是 、过滤、洗涤、干燥。
(6)实验完毕后,打开 ,向A中加入 溶液的主要作用是 。
Ⅱ.产品纯度的测定
(7)取Ⅰ中制取的 产品 ,加入足量稀硫酸和 稀溶液使其完全反应,再用 的
标准溶液滴定生成的 (已知: ,
),当达到滴定终点时,消耗 。滴定终点的现象
,该产品的纯度为 。
27.(14分)锂被誉为“金属味精”,以LiCoO 为正极材料的锂离子电池已被广泛用作便携式电源。工
2
业上常以β-锂辉矿(主要成分为LiAlSi O,还含有FeO、MgO、CaO 等杂质)为原料来制取金属锂。其中一
2 6
种工艺流程如下:
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
氢氧化物 Fe(OH) Al(OH) Mg(OH)
3 3 2
开始沉淀pH 2.7 3.7 9.6完全沉淀pH 3.7 4.7 11
②Li CO 在不同温度下的溶解度如下表:
2 3
温度/ °C 0 10 20 50 75 100
LiCO 的溶解度/g 1.539 1.406 1.329 1.181 0.866 0.728
2 3
请回答下列问题:
(1)β-锂辉矿在处理前要粉碎,其主要目的是 ;用氧化物形式表示LiAlSi O 的组成:
2 6
。
(2)写出反应I中发生氧化还原反应的化学方程式: 。
(3)调节pH=5的作用是除去 。
(4)反应IV生成LiCO 沉淀结束后,实验室中通常得到纯净的LiCO 沉淀的操作名称蒸发浓缩,冷却结
2 3 2 3
晶、 、 、干燥,为了提高所得LiCO 沉淀的产率要使用 洗涤(选填
2 3
“热水”或“冷水”)。
(5)反应II加入碳酸钙,CaCO 是一种难溶物质,其K =2.8×10—9。CaCl 溶液与NaCO 溶液混合可形成
3 sp 2 2 3
CaCO 沉淀,现将等体积的CaCl 溶液与NaCO 溶液混合,若混合前NaCO 溶液的浓度为2.8 ×10—
3 2 2 3 2 3
4mol/L,则生成沉淀所需原CaCl 溶液的最小浓度为 mol/L。
2
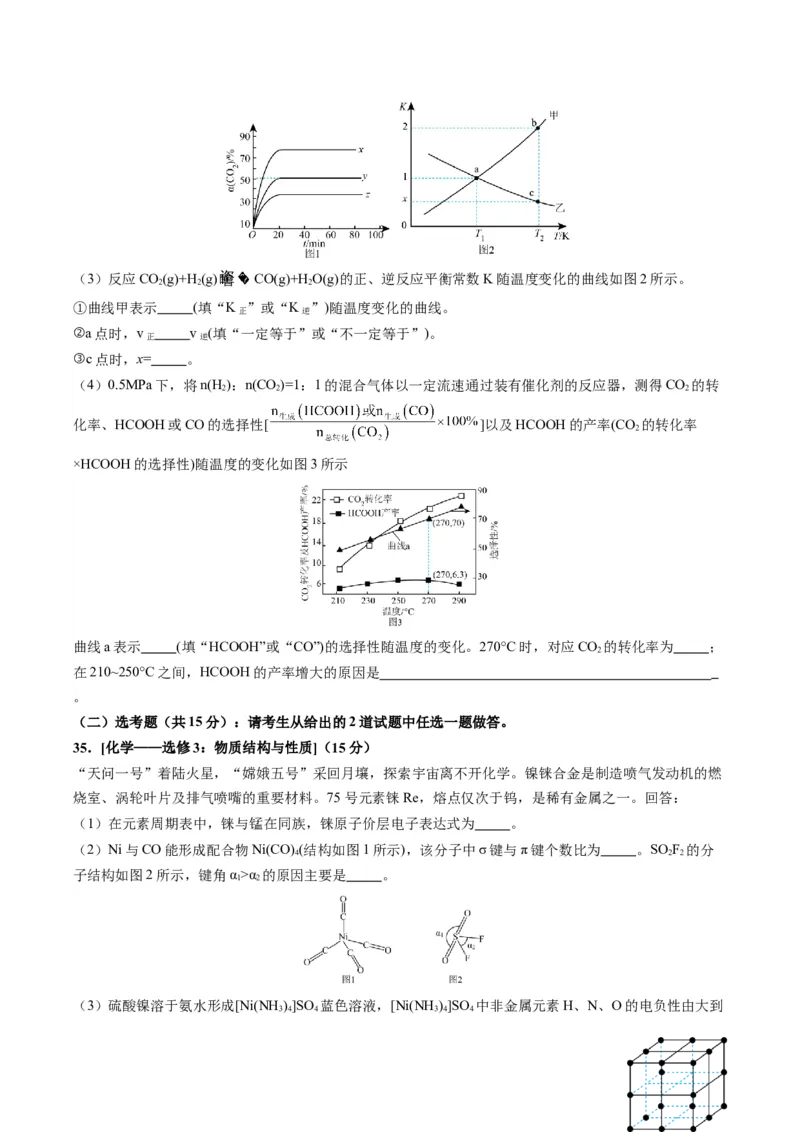
28.(15分)将CO 转化为甲烷、甲醇、甲酸等有机物是实现“碳中和”重要途径。在催化下CO 加氢合
2 2
成甲酸发生反应Ⅰ,同时还伴有反应Ⅰ发生。
Ⅰ.CO(g)+H(g) HCOOH(g) ΔH=-30.9kJ·mol-1
2 2 1
Ⅱ.CO(g)+H(g) CO(g)+HO(g) ΔH
2 2 2 2
回答下列问题:
(1)已知298K时,部分物质的相对能量如下表所示,则CO(g)的相对能量为 kJ·mol-1。
2
物质 H(g) HCOOH(g) HO(g) CO(g)
2 2
相对能量/(kJ·mol-1) 0 -423.9 -242 -110
(2)已知气体A的压强转化率表示为α(A)=(1- )×100%,p 为A的初始分压,p 为某时刻A的分压。保
0 1
持323K、恒温恒压,CO(g)、H(g)投料比为1:1,CO 初始分压分别为p MPa、p MPa和p MPa(p
2 2 2 0-a 0-b 0-c 0-
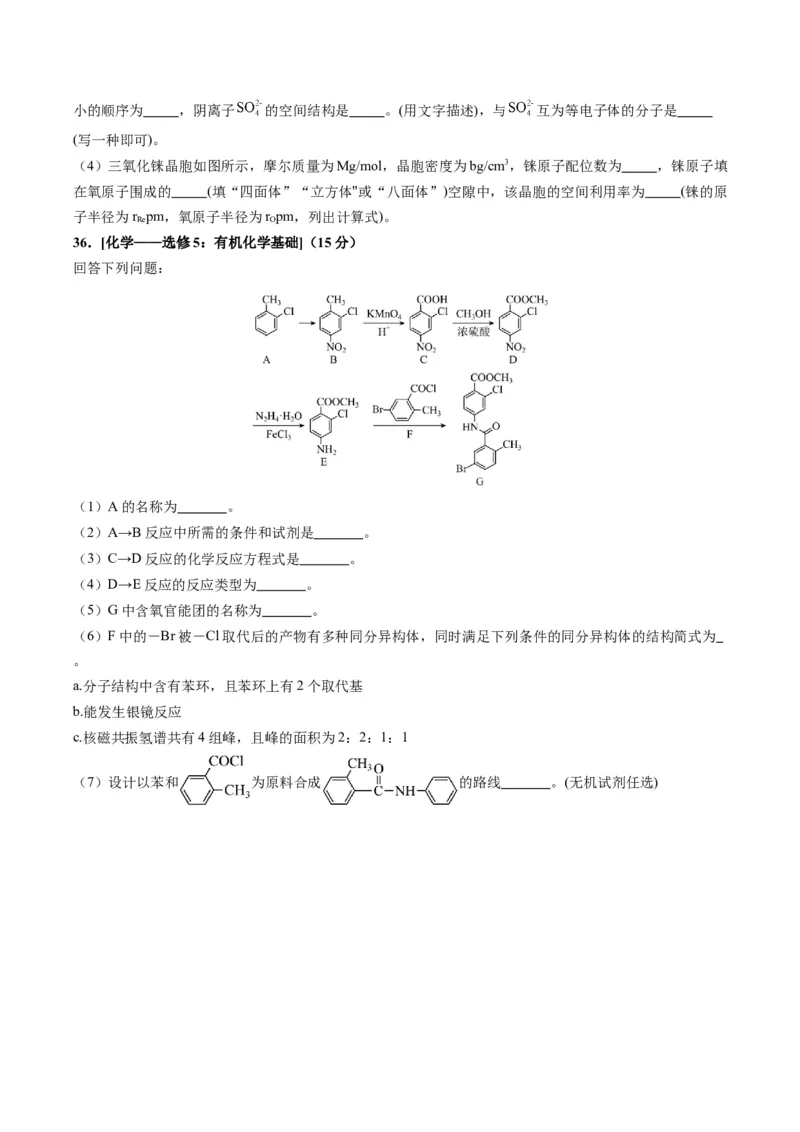
α 的原因主要是 。 1 2 (3)硫酸镍溶于氨水形成[Ni(NH )]SO 蓝色溶液,[Ni(NH )]SO 中非金属元素H、N、O的电负性由大到 3 4 4 3 4 4小的顺序为 ,阴离子 的空间结构是 。(用文字描述),与 互为等电子体的分子是 (写一种即可)。 (4)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子配位数为 ,铼原子填 在氧原子围成的 (填“四面体”“立方体"或“八面体”)空隙中,该晶胞的空间利用率为 (铼的原 子半径为r pm,氧原子半径为r pm,列出计算式)。 Re O 36.[化学——选修5:有机化学基础](15分) 回答下列问题: (1)A的名称为 。 (2)A→B反应中所需的条件和试剂是 。 (3)C→D反应的化学反应方程式是 。 (4)D→E反应的反应类型为 。 (5)G中含氧官能团的名称为 。 (6)F中的-Br被-Cl取代后的产物有多种同分异构体,同时满足下列条件的同分异构体的结构简式为 。 a.分子结构中含有苯环,且苯环上有2个取代基 b.能发生银镜反应 c.核磁共振氢谱共有4组峰,且峰的面积为2:2:1:1 (7)设计以苯和 为原料合成 的路线 。(无机试剂任选)