文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(全国卷旧教材)
黄金卷06
(考试时间:50分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Bi 209
第Ⅰ卷
一、单项选择题:共7题,每题6分,共42分。每题只有一个选项最符合题意。
1.化学与人类生产、生活、社会可持续发展等密切相关。下列说法正确的是
A.中国空间站的食物可谓太空一绝,航天员喜欢吃的“宫保鸡丁”的主要成分是有机物
B.“可燃冰”是一种有待大量开发的新能源,开采过程中发生大量泄漏不会对环境产生影响
C.清华大学打造的世界首款异构融合类脑芯片——天机芯的主要材料与光导纤维的相同
D.用于制造“山东舰”上舰载机降落拦阻索的特种钢属于新型无机非金属材料
【答案】A
【详解】A.“宫保鸡丁”主要成分鸡肉属于蛋白质,蛋白质属于有机物,A正确;
B.“可燃冰”开采过程中发生泄漏的气体是甲烷,甲烷是引起温室效应的气体之一,B错误;
C.天机芯的主要材料是半导体材料晶体硅,光导纤维的主要成分是具有良好光学特性的二氧化硅,二者
不同,C错误;
D.特种钢属于金属材料,不属于新型无机非金属材料,D错误。
故选A。
2.用N 代表阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,1.12L苯含有C-H键的数目为0.3 N
A
B.25°C时K (CaSO)=9×10-6,则该温度下CaSO 饱和溶液中含有3×10-3N 个Ca2+
sp 4 4 A
C.46 克C HO分子中含极性键数目一定是7N
2 6 A
D.在反应KClO+6HCl= KCl+3Cl ↑+3H O中,每生成3 molCl 转移的电子数为5N
3 2 2 2 A
【答案】D
【详解】A.标况下苯不是气体,不能计算其物质的量,A错误;
B.没有说明饱和溶液的体积,不能计算其物质的量,B错误;
C.C HO若为甲醚,一个分子含有8个极性键,若为乙醇,一个分子含有7个极性键,故不能计算,C错
2 6
误;
D.反应中每生成3个氯气,转移5个电子,则每生成3mol氯气,转移5mol电子,D正确;
故选D。3.一种麻醉剂的分子结构式如图所示。其中,X的原子核只有1个质子;元素Y、Z、W原子序数依次增
大,且均位于X的下一周期;元素E的原子比W原子多8个电子。下列说法不正确的是
A. 是一种强氧化性酸 B.非金属性:
C.Y、W、E的氢化物中只有极性键 D. 中,Z的化合价为 价
【答案】C
【分析】依题意,X的原子核只有一个质子,则X为H,由分子结构式可知,Y可形成4个共价键,Z可
形成2个共价键,W可形成一个共价键,且X、Y、Z,子序数依次增大,均位于X的下一周期,也就是第
二周期,则可推断Y为C,Z为O,W为F;元素E的原子比W原子多8个电子,则E为Cl。
【详解】X为H,Y为C,Z为O,W为F,E为Cl。
A.HClO是一种强氧化性酸,A正确;
B.同周期元素,原子序数越大,非金属性越强,故非金属性:F>O>C>H,B正确;
C.C的氢化物中CHCH 中含有极性键和非极性键,故C错误;
3 3
D.ZW 为OF ,F的非金属性强于O的,F在化合物中一般显-1价,故O的化合价为+2价,故D正确;
2 2
故选C。
4.有机物M是合成抗过敏药物色甘酸钠的中间体,结构简式如下图。下列关于该有机物的说法正确的是
A.属于芳香烃 B.能与NaOH溶液反应
C.苯环上的一氯取代物有4种 D.所有碳原子不可能共平面
【答案】B
【详解】A.该物质分子中含有苯环,根据物质分子结构可知:该物质中含有C、H、O三种元素,因此属
于烃的衍生物,A错误;
B.该物质分子中含有酯基,因此能与NaOH溶液反应,B正确;
C.根据物质结构简式可知:在苯环上含有3种不同位置的H原子,处于苯环上的一氯取代物有3种,C错误;
D.苯分子是平面分子,-OCH 的O取代苯分子中H原子的位置,在苯分子平面上,与O原子连接的2个
3
C原子是V形结构,可能处于同一平面上;乙烯分子是平面分子,-CH 及酯基的C原子取代乙烯分子中H
3
原子的位置,在乙烯分子的平面上,乙烯平面与苯分子平面共直线,由于碳碳单键可以旋转,则该分子中
所有碳原子可能共平面,D错误;
故合理选项是B。
5.2022 年中国团队在巴塞罗那获得“镁未来技术奖”。一种以MgCl -聚乙烯醇为电解液的镁电池如图所
2
示。下 列说法不正确的是
A.放电时,正极的电极反应式为Mg2+ +2e- +V O=MgVO
2 5 2 5
B.放电一段时间后,聚乙烯醇中的c(Mg2+)几乎保持不变
C.充电时,Mg2+ 嵌入VO 晶格中
2 5
D.若将电解液换成MgCl 水溶液,工作时电池可能产生鼓包
2
【答案】C
【分析】图中装置,放电时Mg作负极,VO 作正极。
2 5
【详解】A.由图中可知,放电时负极电极式为: ,正极电极式为:Mg2+ +2e-
+V O=MgVO,A正确;
2 5 2 5
B.由放电时电池总反应式: 知,放电不影响电解质溶液的Mg2+浓度,故一段时间后,
聚乙烯醇中的c(Mg2+)几乎保持不变,B正确;
C.充电时阳极电极式为: , 从VO 中脱离,C错误;
2 5
D.若将电解液换成MgCl 水溶液,Mg能与水缓慢反应生成H,工作时电池可能产生鼓包,D正确;
2 2
故选C。
6.由下列实验操作及现象所得结论或解释正确的是
选项 实验操作 现象 结论或解释
向5mL0.1mol·L-1KI溶液中加入10mL0.01mol·L-1FeCl 溶液,充 I-与Fe3+的反应是
A 3 溶液变红
分反应后滴加KSCN溶液 可逆反应前者大于
B 常温下,测定等浓度NaHCO 溶液和NaHSO 溶液的pH 非金属性S>C
3 3 后者
原溶液中一定含有
C 将某溶液滴在KI一淀粉试纸上 试纸变蓝
Cl
2
产生白色
D 向蛋白质溶液中加入醋酸铅溶液 蛋白质发生了盐析
沉淀
【答案】A
【详解】A.根据化学方程式2Fe3++2I-=2Fe2++I 中的系数关系,实验操作中所给的FeCl 是不足的,所以溶
2 3
液变红说明溶液中依然有Fe3+,说明该反应是可逆反应,A正确;
B.测定等浓度NaHCO 溶液和NaHSO 溶液的pH,前者大于后者是因为 的水解程度大于电离程度,
3 3
溶液呈碱性, 的水解程度小于电离程度,溶液呈酸性,根据越弱越水解,说明碳酸酸性<亚硫酸酸性,
但亚硫酸不是S元素的最高价氧化物对应的水化物,所以不能说明非金属性S>C,B错误;
C.将某溶液滴在KI一淀粉试纸上,试纸变蓝,说明原溶液中含有氧化性物质,但不一定是氯气,C错误;
D.向蛋白质溶液中加入醋酸铅溶液,产生白色沉淀,醋酸铅溶液是重金属盐溶液,所以是蛋白质发生了
变性,D错误;
故选A。
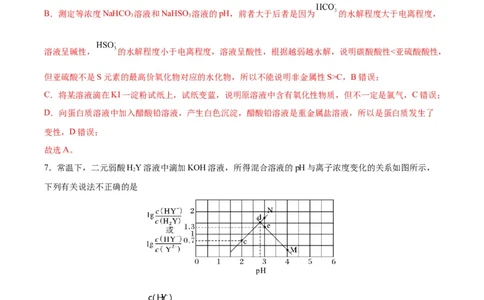
7.常温下,二元弱酸HY溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示,
2
下列有关说法不正确的是
A.曲线M表示pH与lg 的变化关系
B.NaHY溶液显酸性
C.交点d对应的pH=2.8
D.e点溶液中:c(HY-)>c(H Y)>c(Y2-)>c(H+)>c(OH-)
2
【答案】D
【详解】A.随着KOH溶液滴加,c(HY-)增大,c(HY)减小,继续滴加,c(HY-)减小,c(Y2-)增大,所以lg
2增大,用曲线N表示,lg 减小,用曲线M表示,A正确;
B.通过图中c点可得K =10-1.3,e点可得K =10-4.3,K = =10-12.7,K >K ,NaHY的电离程度大于其
a1 a2 h2 a2 h2
水解程度,所以溶液显酸性,B正确;
C.交点d时c(HY)=c(Y2-),K ·K = =10-5.6,则对应的pH=2.8,C正确;
2 a1 a2
D.e点溶液中:lg >lg ,c(HY)α 的原因主要是 。
1 2
(3)硫酸镍溶于氨水形成[Ni(NH )]SO 蓝色溶液,[Ni(NH )]SO 中非金属元素H、N、O的电负性由大到
3 4 4 3 4 4
小的顺序为 ,阴离子 的空间结构是 。(用文字描述),与 互为等电子体的分子是
(写一种即可)。
(4)三氧化铼晶胞如图所示,摩尔质量为Mg/mol,晶胞密度为bg/cm3,铼原子配位数为 ,铼原子填
在氧原子围成的 (填“四面体”“立方体"或“八面体”)空隙中,该晶胞的空间利用率为 (铼的原
子半径为r pm,氧原子半径为r pm,列出计算式)。
Re O【答案】(1)5d56s2
(2)1:1 双键
(3)O>N>H 正四面体 SiF
4
(4)6 八面体
【详解】(1)锰是25号元素,位于第四周期第VIIB族,价层电子排布式为3d54s2,铼与锰在同族,铼位
于第六周期VIIB族,则铼的价层电子表示式5d56s2。
(2)Ni(CO) 中Ni与4个CO形成4个配位键,属于σ键,CO分子与氮气分子互为等电子体,结构式为
4
碳氧三键,三键含有1个σ键与、2个π键,分子共含有8个σ键、8个π键,该分子中σ键与π键个数比
为1:1;SO F 键角α >α 的原因主要是双键成键电子对之间的排斥作用大于单键成键电子对之间的排斥作
2 2 1 2
用。
(3)Ni(NH )]SO 中非金属元素为H、N、O,根据元素周期律,同一周期中电负性从左至右依次增大,
3 4 4
一般化合物中H显正价,故电负性的顺序为O>N>H;阴离子 ,其中心原子S原子周围的价层电子对
数为: ,根据价层电子对互斥理论可知其的空间结构是正四面体; 是5原子32价电
子的微粒,5原子32价电子的微粒有 、 、 、SiF,其中SiF 为分子。
4 4
(4)根据物质的名称可知晶胞的化学式ReO,则Re与O的个数比为1:3,顶点的是铼原子,棱中心的是
3
O,离子晶体中配位数是某个微粒周围最近且等距离的异性电荷的微粒个数,每个铼原子的上下左右前后
都有一个等距的氧原子,故铼原子的配位数为6;铼原子填在了氧原子围成的八面体空隙中。根据已知可
得晶胞的体积是V= 。1个晶胞中有1个Re和3个O,二者的原子半径分别为r pm和r pm,阿
Re O伏加德罗常数值为N ,则ReO 晶胞中原子的体积占晶胞体积的百分率为 。
A 3
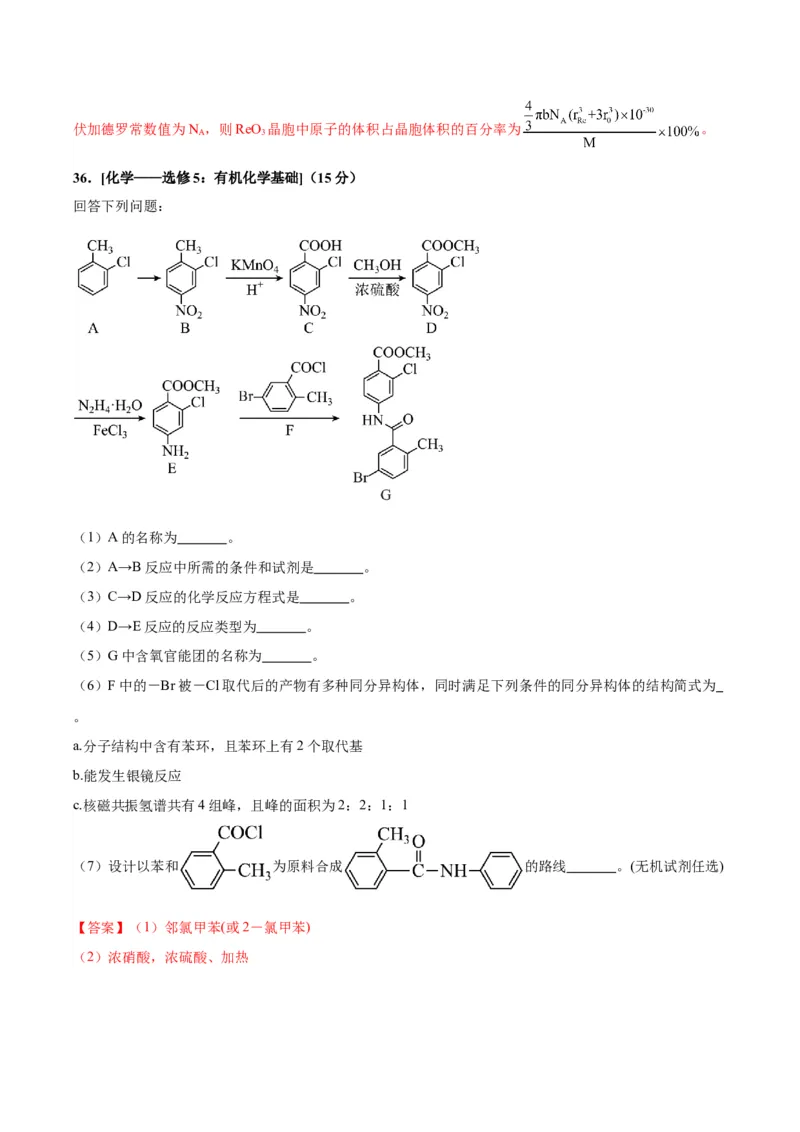
36.[化学——选修5:有机化学基础](15分)
回答下列问题:
(1)A的名称为 。
(2)A→B反应中所需的条件和试剂是 。
(3)C→D反应的化学反应方程式是 。
(4)D→E反应的反应类型为 。
(5)G中含氧官能团的名称为 。
(6)F中的-Br被-Cl取代后的产物有多种同分异构体,同时满足下列条件的同分异构体的结构简式为
。
a.分子结构中含有苯环,且苯环上有2个取代基
b.能发生银镜反应
c.核磁共振氢谱共有4组峰,且峰的面积为2:2:1:1
(7)设计以苯和 为原料合成 的路线 。(无机试剂任选)
【答案】(1)邻氯甲苯(或2-氯甲苯)
(2)浓硝酸,浓硫酸、加热(3) +CH OH +H O
3 2
(4)还原反应
(5)酯基、酰胺基
(6)
(7)
【分析】由结构简式分析,A发生硝化反应生成B,B和酸性高锰酸钾溶液发生氧化反应生成C,C和
CHOH发生酯化反应生成D,D发生还原反应生成E,E和F发生取代反应生成G,以此解答。
3
【详解】(1)根据习惯命名法或系统命名法可知其化学名称为邻氯甲苯或2-氯甲苯,故答案为:邻氯甲
苯(或2-氯甲苯)。
(2)根据A和B的结构简式可知A→B是硝化反应,所学的反应试剂和条件为浓硝酸,浓硫酸、加热,
故答案为:浓硝酸,浓硫酸、加热。
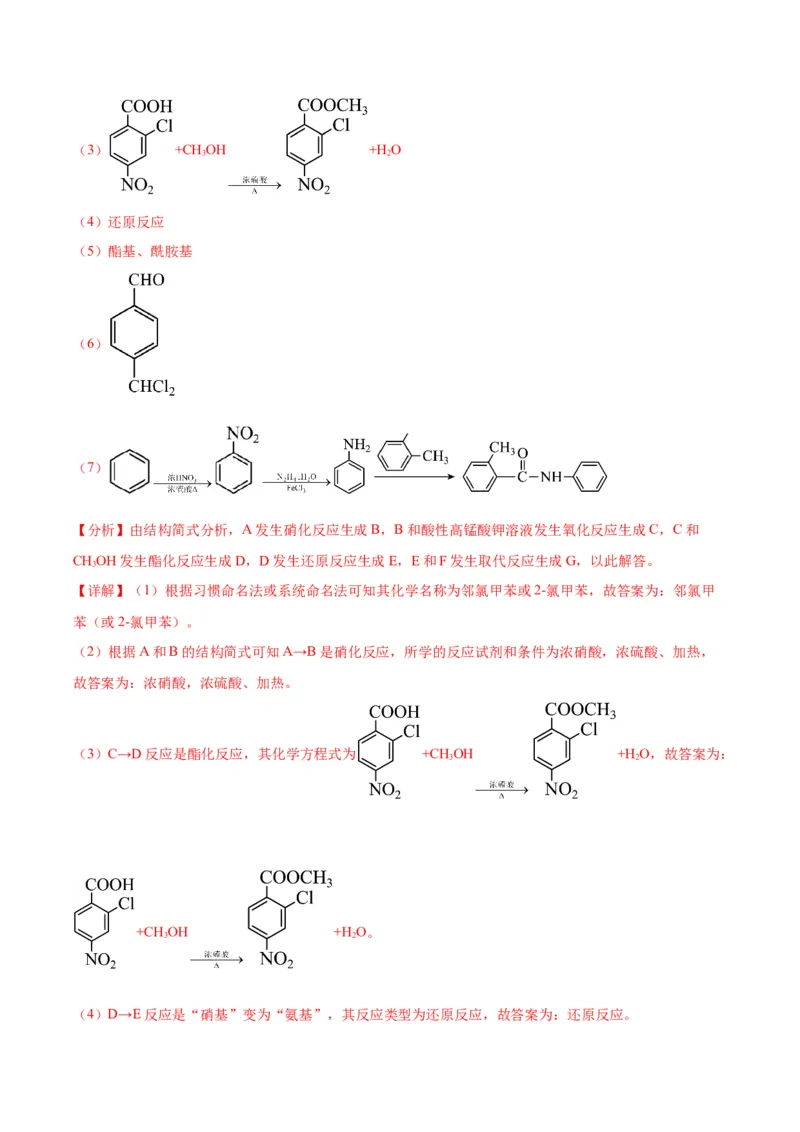
(3)C→D反应是酯化反应,其化学方程式为 +CH OH +H O,故答案为:
3 2
+CH OH +H O。
3 2
(4)D→E反应是“硝基”变为“氨基”,其反应类型为还原反应,故答案为:还原反应。(5)G中含氧官能团的名称是酯基和酰胺基,故答案为:酯基和酰胺基。
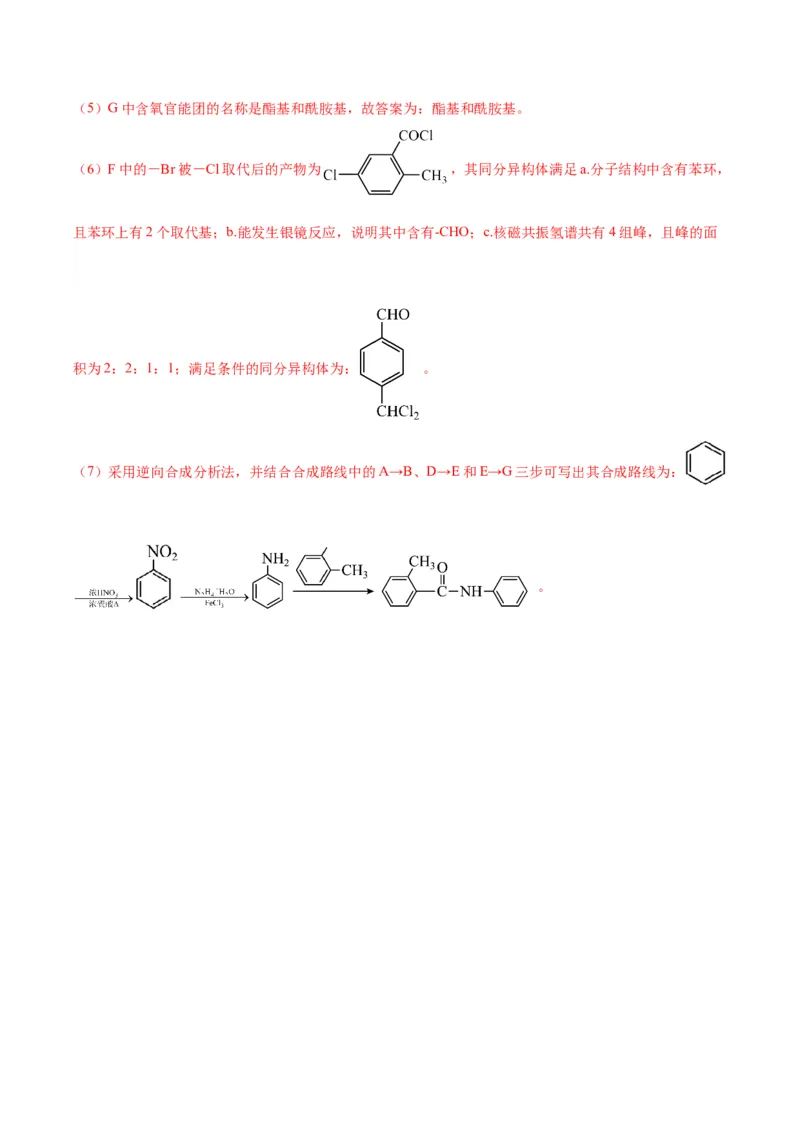
(6)F中的-Br被-Cl取代后的产物为 ,其同分异构体满足a.分子结构中含有苯环,
且苯环上有2个取代基;b.能发生银镜反应,说明其中含有-CHO;c.核磁共振氢谱共有4组峰,且峰的面
积为2:2:1:1;满足条件的同分异构体为: 。
(7)采用逆向合成分析法,并结合合成路线中的A→B、D→E和E→G三步可写出其合成路线为:
。