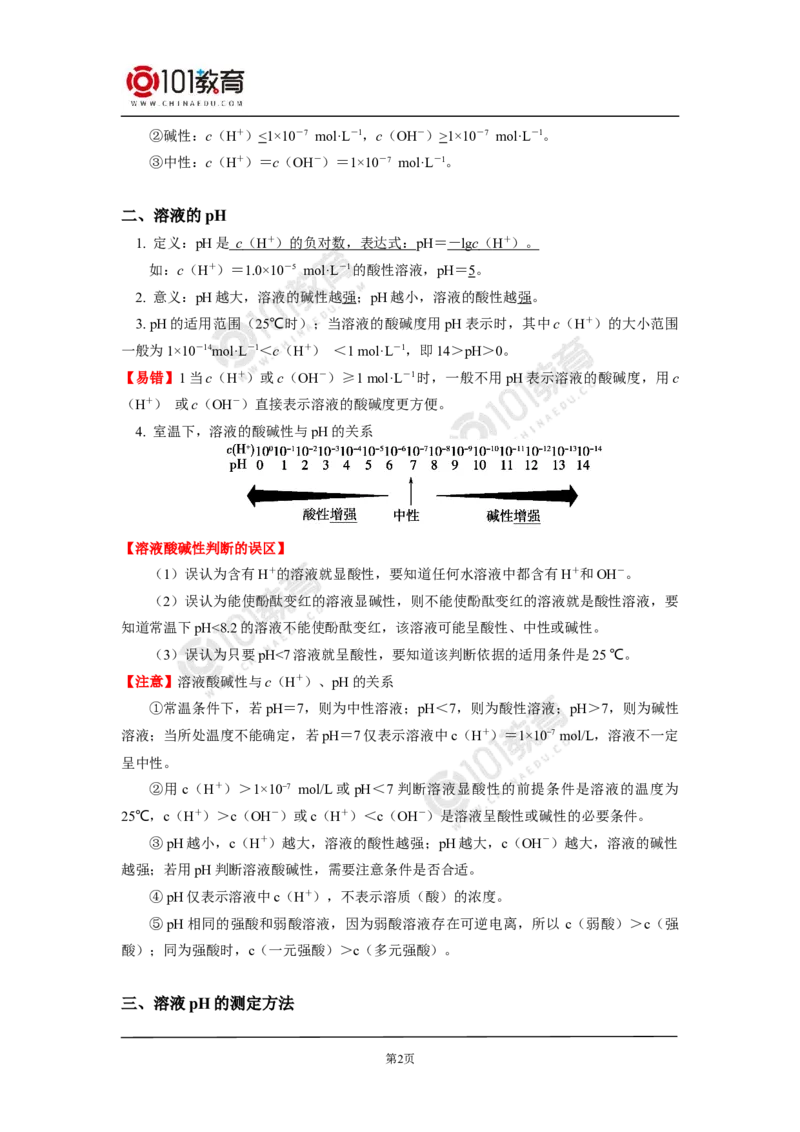
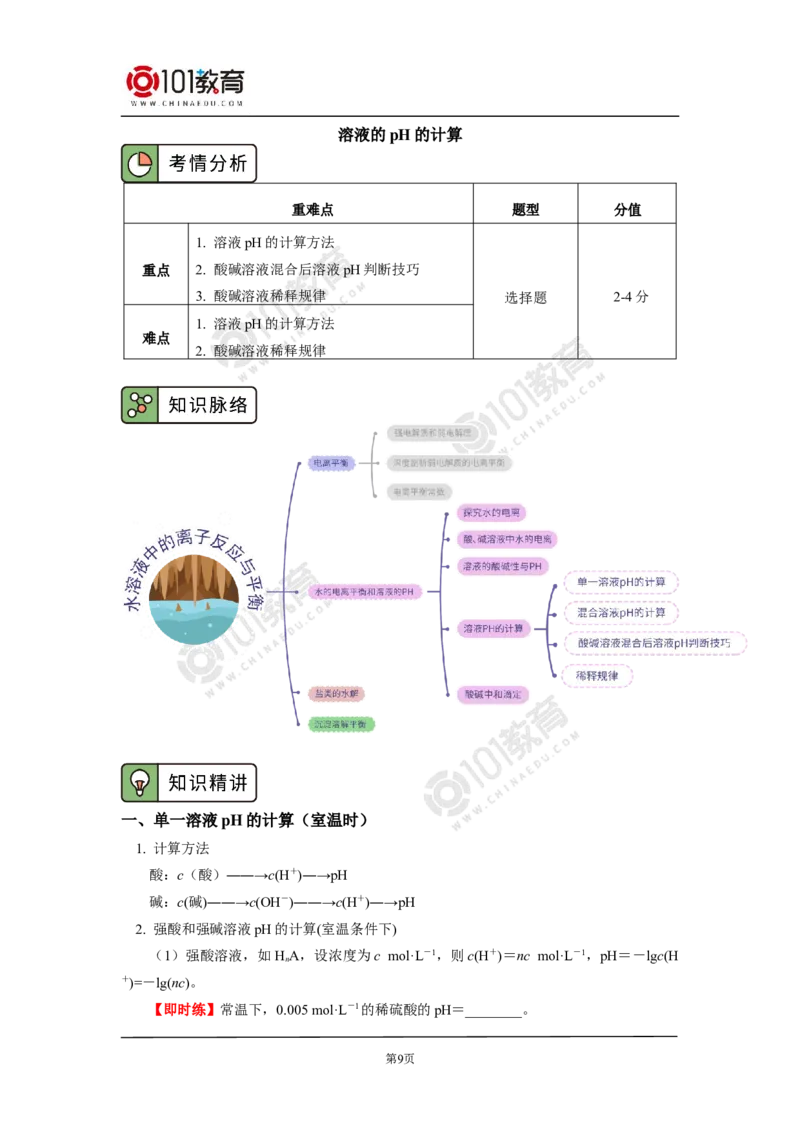
文档内容
溶液的酸碱性和pH
重难点 题型 分值
1. 掌握溶液酸碱性的判断方法
重点 2. 掌握pH的测定方法
3. 酸碱溶液稀释时图像问题
选择题 2-4分
1. 溶液酸碱性的判断方法
难点
2. 酸碱溶液稀释时图像问题
一、溶液酸碱性判断依据
1. 溶液的酸碱性的判断标准是 溶液中 c ( H + )与 c ( OH - )的相对大小 。
2. 溶液酸碱性与溶液中c(H+)和c(OH-)的关系:c(H+)=c(OH-),溶液呈中
性;c(H+)>c(OH-),溶液呈酸性,且c(H+)越大,酸性越强;c(H+)1×10-7 mol·L-1,c(OH-)<1×10-7 mol·L-1。
第1页②碱性:c(H+)<1×10-7 mol·L-1,c(OH-)>1×10-7 mol·L-1。
③中性:c(H+)=c(OH-)=1×10-7 mol·L-1。
二、溶液的pH
1. 定义:pH是 c ( H + )的负对数,表达式: pH= - l g c ( H + )。
如:c(H+)=1.0×10-5 mol·L-1的酸性溶液,pH=5。
2. 意义:pH越大,溶液的碱性越强;pH越小,溶液的酸性越强。
3. pH的适用范围(25℃时);当溶液的酸碱度用pH表示时,其中c(H+)的大小范围
一般为1×10-14mol·L-1<c(H+) <1 mol·L-1,即14>pH>0。
【易错】1当c(H+)或c(OH-)≥1 mol·L-1时,一般不用pH表示溶液的酸碱度,用c
(H+) 或c(OH-)直接表示溶液的酸碱度更方便。
4. 室温下,溶液的酸碱性与pH的关系
【溶液酸碱性判断的误区】
(1)误认为含有H+的溶液就显酸性,要知道任何水溶液中都含有H+和OH-。
(2)误认为能使酚酞变红的溶液显碱性,则不能使酚酞变红的溶液就是酸性溶液,要
知道常温下pH<8.2的溶液不能使酚酞变红,该溶液可能呈酸性、中性或碱性。
(3)误认为只要pH<7溶液就呈酸性,要知道该判断依据的适用条件是25 ℃。
【注意】溶液酸碱性与c(H+)、pH的关系
①常温条件下,若pH=7,则为中性溶液;pH<7,则为酸性溶液;pH>7,则为碱性
溶液;当所处温度不能确定,若pH=7仅表示溶液中c(H+)=1×10–7 mol/L,溶液不一定
呈中性。
②用c(H+)>1×10–7 mol/L或pH<7判断溶液显酸性的前提条件是溶液的温度为
25℃,c(H+)>c(OH-)或c(H+)<c(OH-)是溶液呈酸性或碱性的必要条件。
③pH越小,c(H+)越大,溶液的酸性越强;pH越大,c(OH-)越大,溶液的碱性
越强;若用pH判断溶液酸碱性,需要注意条件是否合适。
④pH仅表示溶液中c(H+),不表示溶质(酸)的浓度。
⑤pH相同的强酸和弱酸溶液,因为弱酸溶液存在可逆电离,所以 c(弱酸)>c(强
酸);同为强酸时,c(一元强酸)>c(多元强酸)。
三、溶液pH的测定方法
第2页1. pH试纸法
①种类
广泛pH试纸:其pH范围是 1 ~ 14 (最常用)。精密pH试纸:其pH范围较窄,可判
别0.2或0.3的pH差值。
专用pH试纸:用于酸性、中性或碱性溶液的专用pH试纸。
②使用方法:把一小块pH试纸放在玻璃片上,用玻璃棒蘸取待测液点在试纸的中央,
试纸变色后,与标准比色卡对照来确定溶液的pH。
2. pH计
pH计又称酸度计。
【想一想】用湿润的pH试纸测溶液的pH,结果一定偏高吗?
【答案】不一定,测酸液偏高,测碱液偏低,测中性溶液没有偏差。
例题1 下列说法正确的是( )
A. 不能使酚酞变红的溶液一定呈酸性
B. 某同学用pH试纸测得盐酸溶液的pH为10.6
C. 某溶液中加入甲基橙后变黄色,则溶液一定呈碱性
D. 某溶液中加入石蕊后变红色,加入甲基橙后呈黄色,则溶液pH在4.4~5之间
【答案】D
【解析】指示剂只能测定溶液pH的范围,如甲基橙的变色范围为3.1~4.4,当溶液的
pH大于4.4时均呈黄色,而石蕊的变色范围为5~8,在pH小于5时,溶液呈红色,所以
第3页C项错误,D项正确;酚酞的变色范围为8.2~10,在pH大于8.2时溶液呈红色,而小于8
时呈无色,故A项错误;常温下酸溶液的pH不可能大于7,故B项错误
例题2 等浓度的下列稀溶液:①乙酸 ②盐酸 ③碳酸 ④硫酸,它们的pH由小到
大排列正确的是( )
A. ①②③④ B. ③①②④
C. ④②③① D. ④②①③
【答案】D
【解析】盐酸、HSO 为强酸,等浓度时HSO 中的c(H+)大于盐酸,乙酸和碳酸为
2 4 2 4
弱酸,酸性:CHCOOH>H CO 。溶液的pH越小,则酸性越强,故pH由小到大的顺序为
3 2 3
④②①③。
25 ℃时,某溶液由水电离出的c(H+)=1×10-12 mol·L-1,则该溶液的pH可能为(
)
A. 12 B. 7
C. 6 D. 2
【答案】AD
【解析】水电离出的c (H+)=c (OH-),若为碱性溶液,则c(OH-)·c (H
水 水 水
+)=K =10-14,c(OH-)= =10-2 mol·L-1,pH=12。若为酸性溶液,则c(OH
w
-)=c (H+)=10-12 mol·L-1,c(H+)= =10-2 mol
水
(答题时间:40分钟)
一、选择题
1. 25 ℃时,向V mL pH=a的盐酸中,滴加pH=b的NaOH溶液10V mL时,溶液中的
Cl-和Na+的物质的量相等,则a+b的值是( )
A. 13 B. 14
C. 15 D. 不能确定
2. 313 K 时,水的 K =3.0×10-14,则在 313 K 时,c(H+)=10-7 mol·L-1的溶液
W
( )
第4页A. 呈酸性 B. 呈中性
C. 呈碱性 D. 无法判断
3. 用pH试纸测定溶液的pH,正确操作是( )
A. 将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色
卡对照
B. 将一小块试纸用蒸馏水润湿后放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,
再与标准比色卡对照
C. 将一小块试纸在待测液中蘸一下,取出后放在表面皿上,与标准比色卡对照
D. 将一小块试纸先用蒸馏水润湿后,再在待测液中蘸一下,取出后与标准比色卡对照
*4. 常温下,下列各组离子在指定溶液中能大量共存的是( )
A. pH=1的溶液中:Fe2+、NO、SO、Na+
B. 由水电离的c(H+)=1×10-14mol·L-1的溶液中:Ca2+、K+、Cl-、HCO
C. c(H+)/c(OH-)=1012的溶液中:NH、Al3+、NO、Cl-
D. c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO、SCN-
*5. 已知温度T时水的离子积常数为K ,该温度下,将浓度为a mol·L-1的一元酸HA与
w
b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A. a=b
B. 混合溶液的pH=7
C. 混合溶液中,c(H+)= mol·L-1
D. 混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
6. 下列叙述正确的是( )
A. 95 ℃纯水的pH<7,说明加热可导致水呈酸性
B. pH=3的醋酸溶液,稀释至10倍后pH=4
C. 0.2 mol·L-1的盐酸,与等体积水混合后pH=1
D. pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
二、填空题
7. 某温度下,纯水中 c(H+)=2×10-7 mol·L-1,则此溶液中c(OH-)为________
mol·L-1,该温度时的 K =________。如温度不变,滴入稀盐酸使 c(H+)=5.0×10-6
W
mol·L-1,则c(OH-)为________ mol·L-1。
8. 常温下,求算下列溶液中水电离出的c(H+)和c(OH-)。
(1)pH=2的HSO 溶液中,c(H+)=________,c(OH-)=________。
2 4
(2)pH=10的NaOH溶液中,c(H+)=________,c(OH-)=________。
*9. 有一学生在实验室测某溶液的pH,实验时,他先用蒸馏水润湿pH试纸,然后用洁
第5页净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作________(填“正确”或“错误”),其理由是__________
_______________________________________________________________;
(2)该操作是否一定有误差?______________________________________
______________________________________________________________;
(3)若用此方法分别测定c(OH-)相等的氢氧化钠溶液和氨水的pH,误差较大的
是________________,原因是_______________________________________
______________________________________________________________;
(4)只从下列试剂中选择实验所需的试剂,你能否区分 0.1 mol·L-1硫酸溶液和0.01
mol·L-1硫酸溶液?
________________(填“能”或“否”),简述操作过程:_______________
_______________________________________________________________。
试剂:a.紫色石蕊试液 b. 酚酞试液 c. 甲基橙溶液 d. 蒸馏水 e. 氯化钡溶液 f.
pH试纸
第6页1. 【答案】A
【解析】由HCl+NaOH===NaCl+HO知,当Cl-和Na+的物质的量相等时,HCl和
2
NaOH完全反应,即盐酸中的 n(H+)等于NaOH中的n(OH-),则10-a·V=10-14+
b·10V,则a+b=13。
2. 【答案】C
【解析】根据溶液中c(H+)与c(OH-)的相对大小判断。由K =c(H+)·c(OH
W
-)可得:c(OH-)= mol·L-1=3.0×10-7 mol·L-1,c(H+)n(H+),故OH-有剩余;剩余n(OH-)≈1×10-4V mol,c(OH-)=
5×10-5 mol·L-1,c(H+)=2×10-10 mol·L-1,pH=-lg(2×10-10)=10-lg 2=9.7。
三、酸、碱发生中和反应后溶液pH的判断技巧
1. 酸与碱的pH之和为14,等体积混合。
常温时
规律:谁弱谁过量,谁弱显谁性。
原因:酸和碱已电离出的H+与OH-恰好中和,谁弱谁的H+或OH-有储备(即物质过
量),还能继续电离。
2. 等体积强酸(pH)和强碱(pH)混合。
1 2
常温时
四、酸、碱溶液稀释规律
第10页1. 酸碱溶液稀释时pH的计算
(1)强酸溶液:pH=a,加水稀释10n倍,则pH=a+n。强碱溶液:pH=b,加水稀
释10n倍,则pH=b-n。
(2)弱酸溶液:pH=a,加水稀释10n倍,则a<pH<a+n。弱碱溶液:pH=b,加水
稀释10n倍,则b-n<pH<b。
(3)酸碱溶液无限稀释,pH只能接近于7,酸溶液的pH不可能大于7,碱溶液的pH
不可能小于7。
2. 酸碱溶液稀释时的图像规律
(1)起始物质的量浓度相同时的情况分析
物质的量浓度相同的一元强酸溶液和一元弱酸溶液,弱酸溶液的 pH大。稀释相同的
倍数,仍是弱酸溶液的pH大;稀释至相同的pH,强酸溶液中加的水多。pH变化情况如图
甲。
物质的量浓度相同的一元强碱溶液和一元弱碱溶液,强碱溶液的 pH大。稀释相同的
倍数,仍是强碱溶液的pH大;稀释至相同的pH,强碱溶液中加的水多。pH变化情况如图
乙。
(2)起始pH相同时的情况分析
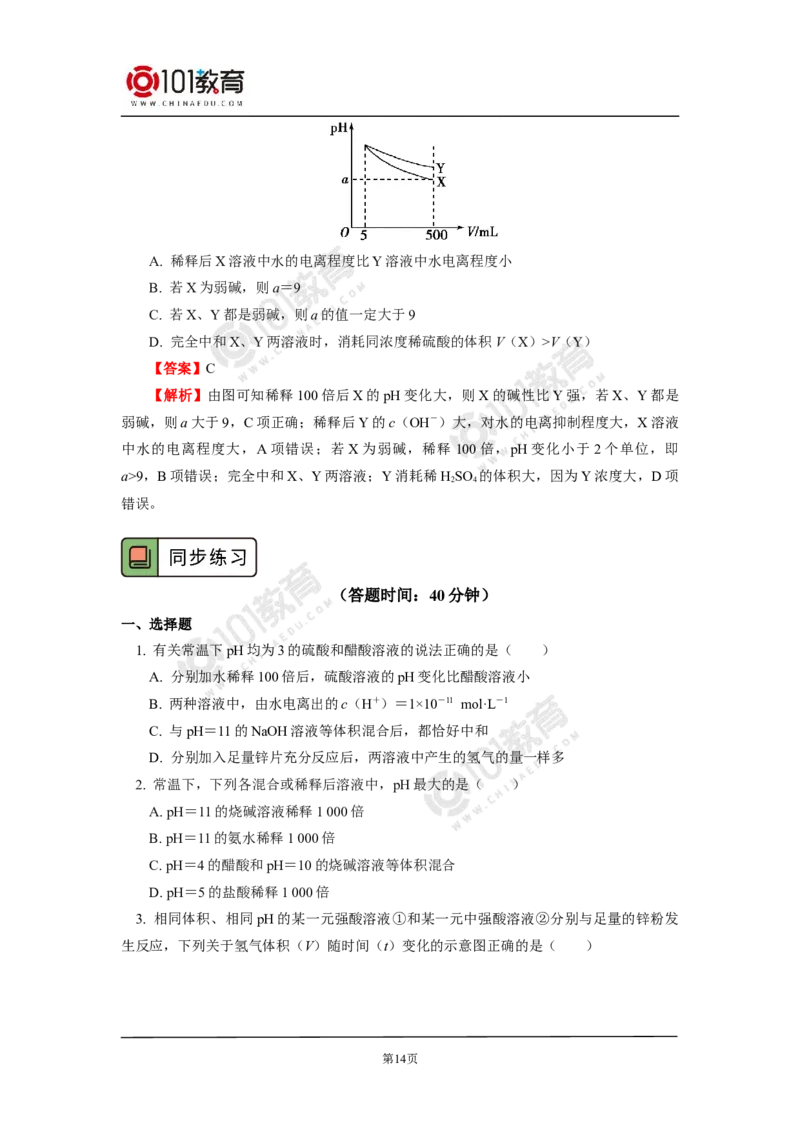
将pH相同的一元强酸溶液和弱酸溶液稀释同样的倍数,弱酸溶液的pH变化小,强酸
溶液的pH变化大;将pH相同的一元强酸溶液和弱酸溶液稀释后pH仍相同,则弱酸溶液
中所加的水比强酸溶液中的多。如图丙。
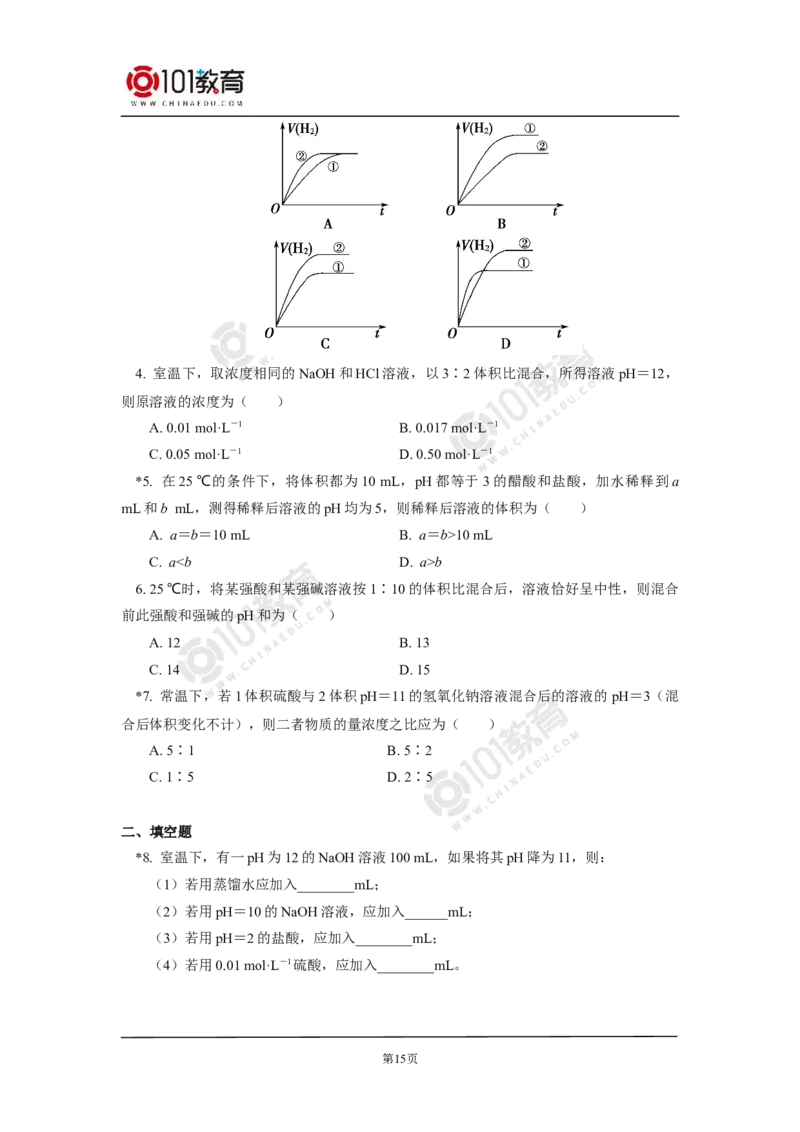
第11页将pH相同的一元强碱溶液和弱碱溶液稀释同样的倍数,强碱溶液的 pH变化大,弱碱
溶液pH变化小;将pH相同的一元强碱溶液和弱碱溶液稀释至相同的pH,则弱碱溶液中
所加的水比强碱溶液中的多。如图丁。
【小结】溶液pH计算口诀:无限稀释“7”为限;碱按碱、酸按酸;同强混合在中间;
异强混合看过量。
例题1 在一定体积pH=12的Ba(OH) 溶液中,逐滴加入一定物质的量浓度的
2
NaHSO 溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11。若反应后溶液的体积等于
4
Ba(OH) 溶液与NaHSO 溶液的体积之和,则Ba(OH) 溶液与NaHSO 溶液的体积比
2 4 2 4
是( )
A.1∶9 B. 1∶1
C. 1∶2 D. 1∶4
【答案】D
【解析】pH=12 的氢氧化钡溶液中 c(H+)=1×10-12 mol·L-1,c(OH-)=
mol·L-1=1×10-2mol·L-1,c[Ba(OH) ]=0.5×10-2 mol·L-1;反应后溶液pH=
2
11,c(H+)=1×10-11 mol·L-1,c(OH-)= mol·L-1=1×10-3 mol·L-1。设氢
第12页氧化钡溶液体积为 V L,硫酸氢钠溶液的体积为 V L。依题意知,n(Ba2+)=n
1 2
(SO)。由Ba(OH)+NaHSO=BaSO↓+NaOH+HO知,生成的氢氧化钠的物质的量
2 4 4 2
为n(NaOH)=n[Ba(OH) ]=0.5×10-2 V mol,0.5×10-2 V /(V +V )=1×10-3,
2 1 1 1 2
V∶V=1∶4。
1 2
例题2 常温下,0.1 mol·L-1某一元酸(HA)溶液中 =1×10-8,相同物质的
量浓度的某一元碱(BOH)溶液中 =1×1012,下列叙述正确的是( )
A. pH=a的HA溶液,稀释10倍,其pH=a+1
B. 等体积、等浓度的HA和BOH溶液恰好完全反应,溶液的pH=7
C. HA溶液的pH=3,BOH溶液的pH=13
D. 相同体积、相同pH的HA溶液和盐酸分别与足量Zn反应,生成氢气的物质的量相
同
【答案】C
【解析】常温下,0.1 mol·L-1 HA溶液中 =1×10-8、K =c(H+)·c(OH
W
-)=1×10-14,联立解得 c(H+)=10-3 mol·L-1,溶液的 pH=3,联立 =
1×1012、K =c(H+)c(OH-)=1×10-14,解得c(OH-)=0.1 mol·L-1,BOH溶液的pH
W
=13,故C正确;0.1 mol·L-1的HA溶液的pH=3,则HA为弱酸,弱酸稀释时会继续电
离出H+,则pH=a的HA溶液,稀释10倍后,pH的变化值小于1,即pH7,故B错误;HA为弱酸,在溶液中
只能部分电离出H+,pH相等的HA溶液和盐酸中,HA的物质的量浓度大于盐酸,则相同
体积、相同pH的HA溶液和盐酸分别与足量Zn反应,HA产生的氢气多,故D错误。
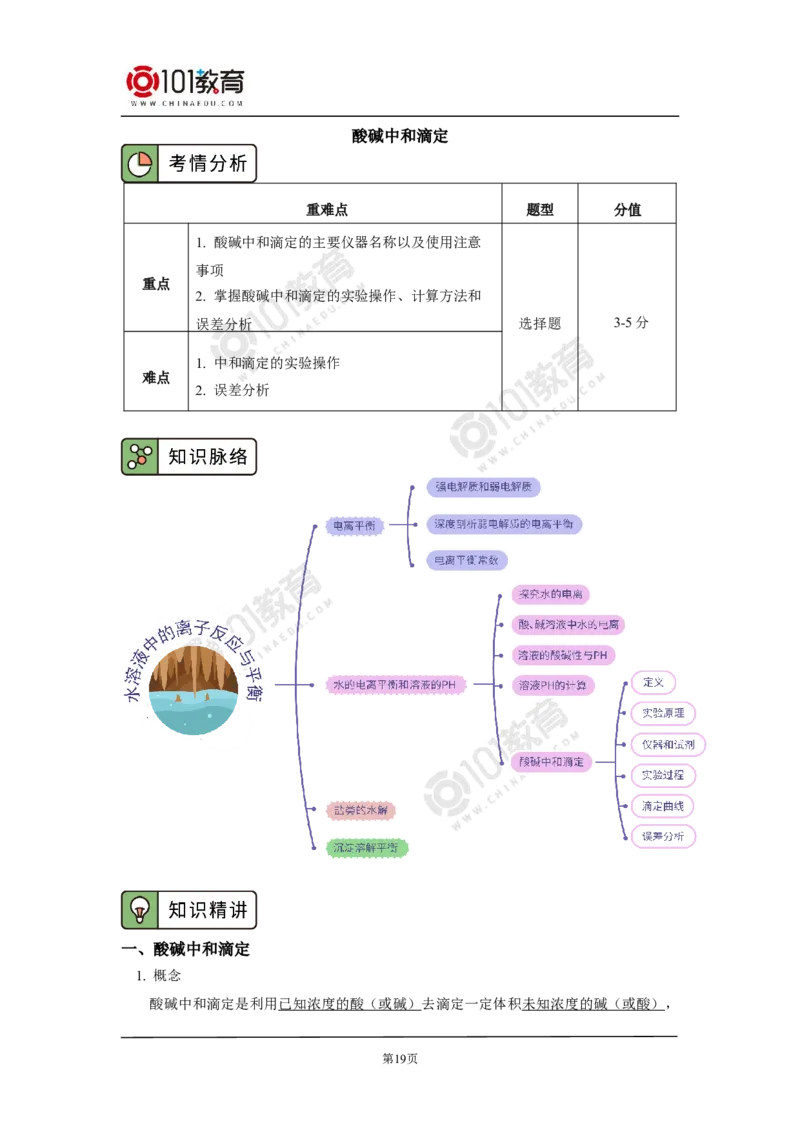
pH=11的X、Y两种碱溶液各5 mL,分别稀释至500 mL,其pH与溶液体积(V)的
关系如图所示,下列说法正确的是( )
第13页A. 稀释后X溶液中水的电离程度比Y溶液中水电离程度小
B. 若X为弱碱,则a=9
C. 若X、Y都是弱碱,则a的值一定大于9
D. 完全中和X、Y两溶液时,消耗同浓度稀硫酸的体积V(X)>V(Y)
【答案】C
【解析】由图可知稀释100倍后X的pH变化大,则X的碱性比Y强,若X、Y都是
弱碱,则a大于9,C项正确;稀释后Y的c(OH-)大,对水的电离抑制程度大,X溶液
中水的电离程度大,A项错误;若X为弱碱,稀释100倍,pH变化小于2个单位,即
a>9,B项错误;完全中和X、Y两溶液;Y消耗稀HSO 的体积大,因为Y浓度大,D项
2 4
错误。
(答题时间:40分钟)
一、选择题
1. 有关常温下pH均为3的硫酸和醋酸溶液的说法正确的是( )
A. 分别加水稀释100倍后,硫酸溶液的pH变化比醋酸溶液小
B. 两种溶液中,由水电离出的c(H+)=1×10-11 mol·L-1
C. 与pH=11的NaOH溶液等体积混合后,都恰好中和
D. 分别加入足量锌片充分反应后,两溶液中产生的氢气的量一样多
2. 常温下,下列各混合或稀释后溶液中,pH最大的是( )
A. pH=11的烧碱溶液稀释1 000倍
B. pH=11的氨水稀释1 000倍
C. pH=4的醋酸和pH=10的烧碱溶液等体积混合
D. pH=5的盐酸稀释1 000倍
3. 相同体积、相同pH的某一元强酸溶液①和某一元中强酸溶液②分别与足量的锌粉发
生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )
第14页4. 室温下,取浓度相同的NaOH和HCl溶液,以3∶2体积比混合,所得溶液pH=12,
则原溶液的浓度为( )
A. 0.01 mol·L-1 B. 0.017 mol·L-1
C. 0.05 mol·L-1 D. 0.50 mol·L-1
*5. 在25 ℃的条件下,将体积都为10 mL,pH都等于3的醋酸和盐酸,加水稀释到a
mL和b mL,测得稀释后溶液的pH均为5,则稀释后溶液的体积为( )
A. a=b=10 mL B. a=b>10 mL
C. ab
6. 25 ℃时,将某强酸和某强碱溶液按1∶10的体积比混合后,溶液恰好呈中性,则混合
前此强酸和强碱的pH和为( )
A. 12 B. 13
C. 14 D. 15
*7. 常温下,若1体积硫酸与2体积pH=11的氢氧化钠溶液混合后的溶液的pH=3(混
合后体积变化不计),则二者物质的量浓度之比应为( )
A. 5∶1 B. 5∶2
C. 1∶5 D. 2∶5
二、填空题
*8. 室温下,有一pH为12的NaOH溶液100 mL,如果将其pH降为11,则:
(1)若用蒸馏水应加入________mL;
(2)若用pH=10的NaOH溶液,应加入______mL;
(3)若用pH=2的盐酸,应加入________mL;
(4)若用0.01 mol·L-1硫酸,应加入________mL。
第15页第16页1. 【答案】B
【解析】硫酸是强电解质,完全电离,醋酸是弱电解质,加水稀释,醋酸继续电离出
H+,分别加水稀释100倍后,硫酸溶液的pH为5,醋酸溶液的pH小于5,所以硫酸溶液
的pH变化比醋酸溶液大,故A错误;pH均为3的醋酸和硫酸,溶液中c(H+)=1×10-3
mol·L-1,溶液中c(OH-)= mol·L-1=1×10-11 mol·L-1,溶液中c (H+)=c
水
(OH-),故两种溶液中,c (H+)=1×10-11 mol·L-1,故B正确;硫酸为强酸,pH=3
水
的硫酸与pH=11的氢氧化钠溶液等体积混合恰好中和,而醋酸为弱酸,若 pH=3的醋酸
与pH=11的氢氧化钠溶液等体积混合,醋酸过量,故C错误;硫酸是强电解质,完全电
离,醋酸是弱电解质,溶液中主要以醋酸分子形式存在,与足量的 Zn反应,醋酸提供的H
+大于硫酸,Zn与醋酸反应产生氢气的物质的量较大,故D错误。
2. 【答案】B
【解析】pH=11的烧碱溶液稀释1 000倍后,pH=8;pH=11的氨水稀释1 000倍后,
由于稀释促进电离,pH>8;pH=4的醋酸和pH=10的烧碱溶液等体积混合后,醋酸过量,
溶液呈酸性,pH<7;pH=5的盐酸稀释1 000倍后,pH接近7但小于7;所以B的pH最
大。
3. 【答案】C
【解析】相同体积、相同pH的一元强酸和一元中强酸中,H+浓度相等,所以刚开始
与锌反应的速率是相同的,随着反应的进行,中强酸继续电离,故反应速率较强酸快,排
除B、D;又因中强酸的物质的量浓度大于强酸,所以与足量的锌反应生成氢气的量较多,
排除A项。
4. 【答案】C
【解析】设原溶液的浓度为c,两者反应后碱过量,应先求c(OH-),c(OH-)=
=0.01 mol·L-1,解得c=0.05 mol·L-1。
5. 【答案】D
【解析】因为醋酸是弱酸,盐酸是强酸,在稀释相同体积后,醋酸的 pH变化相对盐
酸小,则当稀释后两者的pH仍相等,故a>b。
6. 【答案】B
【解析】强酸和强碱溶液按1∶10的体积比混合恰好呈中性,则说明酸溶液中的氢离
子浓度等于碱溶液中的氢氧根离子的浓度的10倍,故pH和为13,选B。
7. 【答案】B
【解析】HSO +2NaOH===Na SO +2HO,设硫酸的物质的量浓度为c mol·L-1,体
2 4 2 4 2
第17页积为V L,氢氧化钠溶液浓度为10-3 mol·L-1,体积为2V L,混合后pH=3,即c(H+)
= mol·L-1=10-3 mol·L-1,解得c= ×10-3,则二者物质的量浓度之比
应为5∶2,B项正确。
8. 【答案】(1)900 (2)1 000 (3)81.8 (4)42.86
【解析】(1)由c(OH-) =10-3 mol·L-1= ,得V(HO)
稀释 2
=0.9 L=900 mL。
(2)设加入pH=10的NaOH溶液的体积为x,c(OH-)=10-3 mol·L-1
=
得x=1 L=1 000 mL。
(3)设加入pH=2的盐酸的体积为y,
c(OH-)=10-3 mol·L-1
=
得y=0.081 8 L=81.8 mL。
(4)设加入硫酸的体积为z
c(OH-)=10-3 mol·L-1
=
得z=0.042 86 L=42.86 mL。
第18页酸碱中和滴定
重难点 题型 分值
1. 酸碱中和滴定的主要仪器名称以及使用注意
事项
重点
2. 掌握酸碱中和滴定的实验操作、计算方法和
误差分析 选择题 3-5分
1. 中和滴定的实验操作
难点
2. 误差分析
一、酸碱中和滴定
1. 概念
酸碱中和滴定是利用已知浓度的酸(或碱)去滴定一定体积未知浓度的碱(或酸),
第19页通过测定反应完全时消耗已知浓度的酸(或碱)的体积,从而推算出未知浓度的碱(或
酸)的浓度的方法。
2. 原理
中和反应中酸提供的H+与碱提供的OH-的物质的量相等。
H + + OH - == =H O 即c(H+)·V =c(OH-)·V
2 酸 碱
c(H+)=或 c(OH-)=。
3. 仪器及使用
(1)仪器
图1 图2 图3
(2)滴定管的使用(如图3):
①查漏:使用前先检查滴定管活塞是否漏水。
②润洗:在加入反应液之前,洁净的滴定管要用所要盛装的溶液润洗 2 ~ 3 遍。
③注液:分别将试剂加入到相应滴定管中,使液面位于滴定管2_ mL ~ 3 _mL 处。
④调液面:在滴定管下放一烧杯,调节活塞,使滴定管尖嘴部分充满反应液,然后调
节滴定管液面使其处于某一刻度,准确读取数值并记录。
⑤使用滴定管时,左手控制活塞(或碱式滴定管的玻璃球),滴定过程滴加溶液的速
度不能太快,一般以每秒 3 ~ 4 滴为宜。
4. 酸碱中和滴定操作(以NaOH溶液滴定盐酸为例)
(1)滴定的准备:
①滴定管:查漏、洗涤、润洗、装液、调液面、读数。
②锥形瓶:洗涤、装液、加指示剂。
(2)滴定操作:
①从酸式滴定管中放出一定体积的盐酸于锥形瓶中,并滴入 2 滴酚酞溶液。把锥形瓶
放在碱式滴定管下面。
②用左手控制碱式滴定管橡胶管内玻璃珠,右手不断旋转振荡锥形瓶,眼睛注视锥形
瓶内溶液颜色变化及滴定流速,当溶液由无色变为粉红色且半分钟内不褪色,记下滴定管
的读数。
③按上述操作重复2~3次。
【微点拨】酸式滴定管带有玻璃活塞,可装酸性、中性或强氧化性溶液;碱式滴定管
第20页带有装玻璃球的胶管,只能装碱性溶液。
二、指示剂的选择
(1)强酸与强碱相互滴定时,选甲基橙或酚酞都可以,但不能选石蕊试液(遇酸、碱颜
色变化不明显)。一般原则是:酸滴定碱,选甲基橙;碱滴定酸,选酚酞。
(2)滴定终点的判断(以NaOH溶液滴定未知浓度的盐酸为例):
若用酚酞作指示剂,当滴入最后一滴NaOH溶液时,溶液的颜色由无色突变为粉红色,
且半分钟内不褪色,说明达到滴定终点。
若用甲基橙作指示剂,当滴入最后一滴NaOH溶液时,溶液的颜色由红色变为橙色,
且半分钟内不变为原色,说明达到滴定终点。
三、酸碱中和滴定曲线
1. pH的突变
在酸碱反应过程中,溶液的pH会发生变化,对于强酸强碱的反应,开始时由于被中
和的酸(或碱)浓度较大,加入少量的碱(或酸)对其pH的影响不大。当反应接近终点
(pH≈7)时,很少量的碱(或酸)就会引起溶液 pH 突变 ,酸、碱的浓度不同,pH突变范
围不同。
2. 滴定曲线
酸碱滴定曲线是以酸碱混合过程中滴加酸(或碱)的量为横坐标,以溶液pH 为纵坐
标绘出一条溶液pH随酸(或碱)的滴加量而变化的曲线。
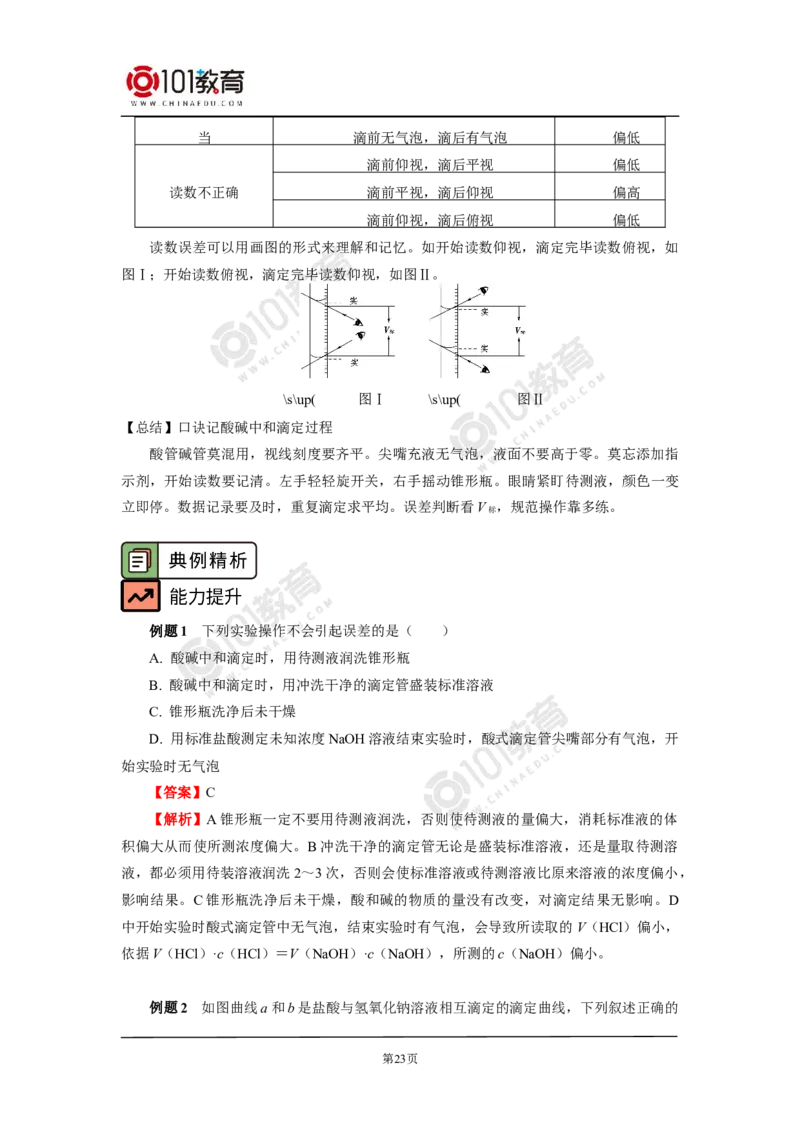
例如:以0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 HCl溶液为例,其
滴定曲线如图所示。
【想一想】滴定终点是反应终点吗?
【提示】不是,滴定终点是指示剂变色点。
四、误差分析
第21页1. 常用量器的读数方法及误差分析
(1)平视读数(如图a):实验室中用量筒、移液管或滴定管量取一定体积的液体,
读取液体体积时,视线应与凹液面最低点保持水平,视线与刻度的交点即为读数(即“凹
液面定视线,视线定读数”)。
(2)俯视读数(如图b):当使用量筒测量液体的体积时,由于俯视视线向下倾斜,
寻找交点的位置在凹液面的上方,读数高于正确的刻度线位置,即读数偏大。
(3)仰视读数(如图c):使用滴定管读数时,由于视线向上倾斜,寻找交点的位置
在液面的下方,因滴定管刻度标法与量筒不同,仰视时读数偏大。
2. 酸碱中和滴定中的误差分析
(1)误差分析依据
酸碱中和滴定是一个要求较高的定量实验,每一个不当或错误的操作都会引起误差。
对应一元酸与一元碱,由公式可知,V(待)是准确量取的体积,c(标)是标准溶液的浓
度,它们均为定值,所以V(待)的大小取决于标准溶液的体积的大小,标准溶液的体积
大则待测液的浓度大,标准溶液的体积小则待测液的浓度小。
分析误差要根据计算式:c =,当用标准液滴定待测液时,c 、V 均为定值,c
待测 标准 待测
的大小由V 的大小决定。
待测 标准
(2)常见误差分析
以盐酸标准溶液滴定未知浓度的碱溶液(酚酞作指示剂)为例,常见的因操作不正确
而引起的误差分析如下:
步骤 操作 误差分析
未用标准液润洗滴定管 偏高
未用待测液润洗移液管或所用的滴定
偏低
仪器的洗涤或润洗 管
用待测液润洗锥形瓶 偏高
洗涤后锥形瓶未干燥 无影响
标准液漏滴在锥形瓶外一滴 偏高
滴定时溅落液体 待测液溅出锥形瓶外一滴 偏低
将移液管下部的残留液吹入锥形瓶 偏高
尖嘴处气泡处理不 滴前有气泡,滴后无气泡 偏高
第22页当 滴前无气泡,滴后有气泡 偏低
滴前仰视,滴后平视 偏低
读数不正确 滴前平视,滴后仰视 偏高
滴前仰视,滴后俯视 偏低
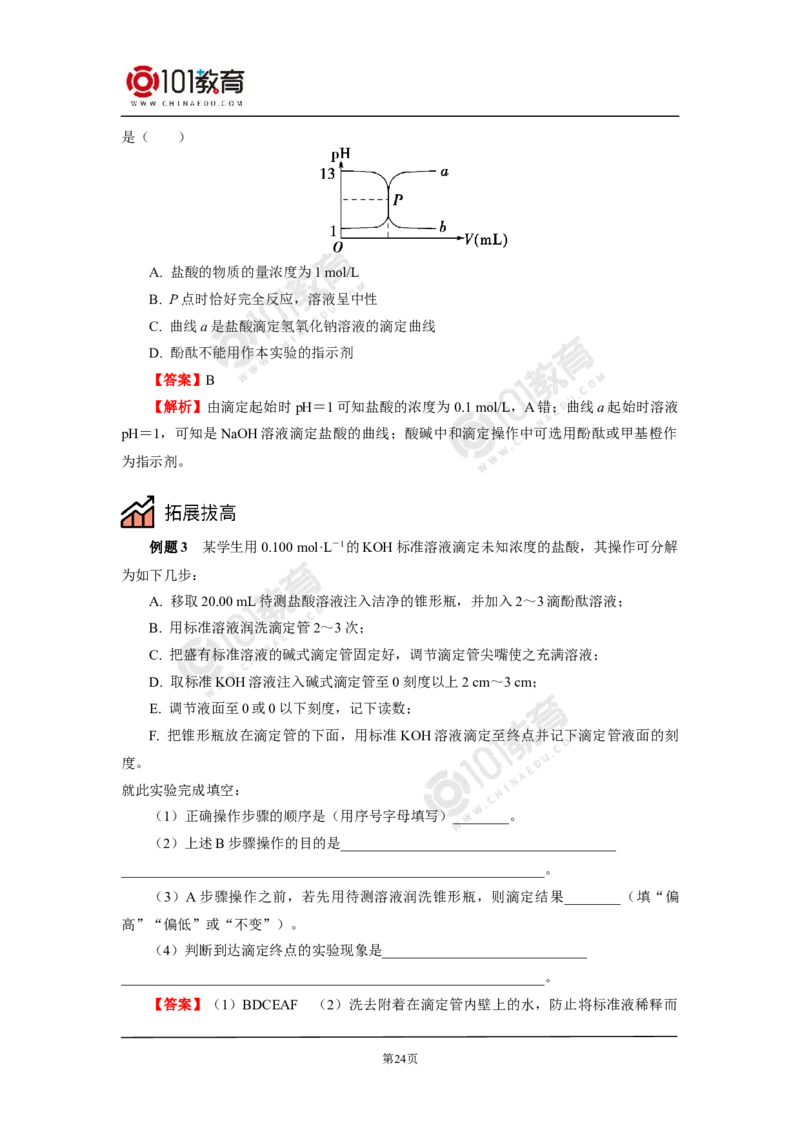
读数误差可以用画图的形式来理解和记忆。如开始读数仰视,滴定完毕读数俯视,如
图Ⅰ;开始读数俯视,滴定完毕读数仰视,如图Ⅱ。
\s\up( 图Ⅰ \s\up( 图Ⅱ
【总结】口诀记酸碱中和滴定过程
酸管碱管莫混用,视线刻度要齐平。尖嘴充液无气泡,液面不要高于零。莫忘添加指
示剂,开始读数要记清。左手轻轻旋开关,右手摇动锥形瓶。眼睛紧盯待测液,颜色一变
立即停。数据记录要及时,重复滴定求平均。误差判断看V ,规范操作靠多练。
标
例题1 下列实验操作不会引起误差的是( )
A. 酸碱中和滴定时,用待测液润洗锥形瓶
B. 酸碱中和滴定时,用冲洗干净的滴定管盛装标准溶液
C. 锥形瓶洗净后未干燥
D. 用标准盐酸测定未知浓度NaOH溶液结束实验时,酸式滴定管尖嘴部分有气泡,开
始实验时无气泡
【答案】C
【解析】A锥形瓶一定不要用待测液润洗,否则使待测液的量偏大,消耗标准液的体
积偏大从而使所测浓度偏大。B冲洗干净的滴定管无论是盛装标准溶液,还是量取待测溶
液,都必须用待装溶液润洗2~3次,否则会使标准溶液或待测溶液比原来溶液的浓度偏小,
影响结果。C锥形瓶洗净后未干燥,酸和碱的物质的量没有改变,对滴定结果无影响。D
中开始实验时酸式滴定管中无气泡,结束实验时有气泡,会导致所读取的V(HCl)偏小,
依据V(HCl)·c(HCl)=V(NaOH)·c(NaOH),所测的c(NaOH)偏小。
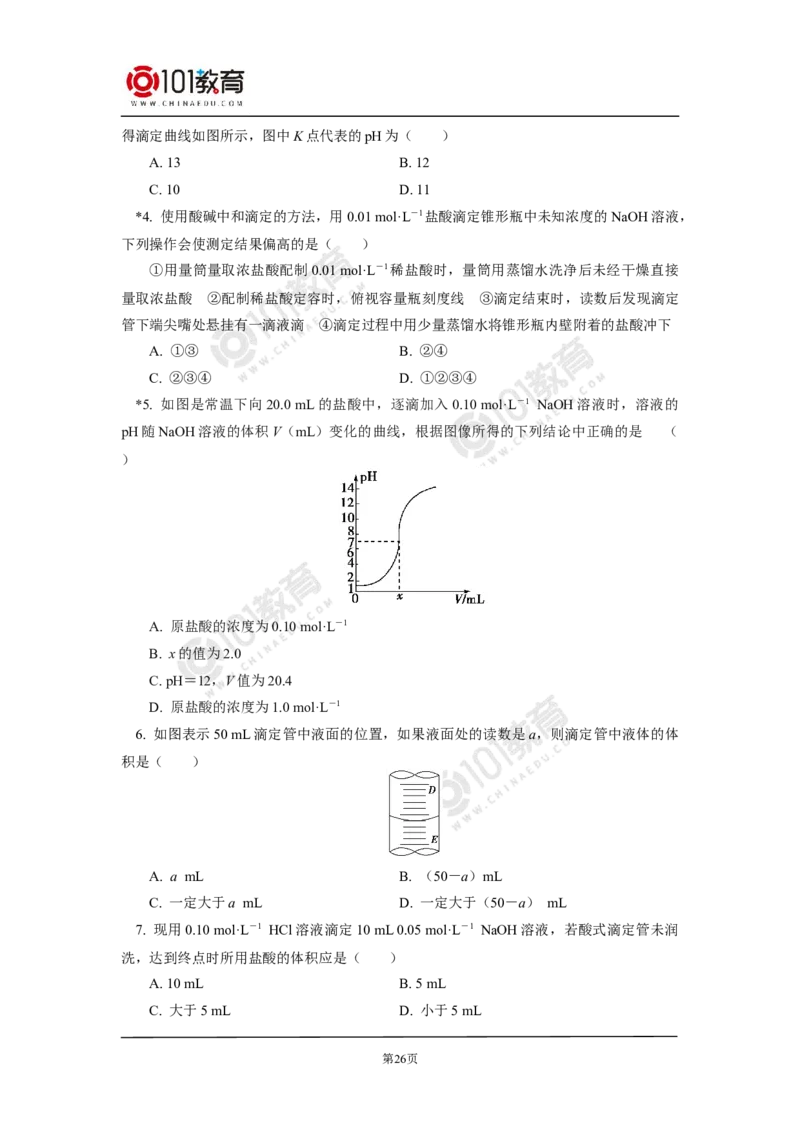
例题2 如图曲线a和b是盐酸与氢氧化钠溶液相互滴定的滴定曲线,下列叙述正确的
第23页是( )
A. 盐酸的物质的量浓度为1 mol/L
B. P点时恰好完全反应,溶液呈中性
C. 曲线a是盐酸滴定氢氧化钠溶液的滴定曲线
D. 酚酞不能用作本实验的指示剂
【答案】B
【解析】由滴定起始时pH=1可知盐酸的浓度为0.1 mol/L,A错;曲线a起始时溶液
pH=1,可知是NaOH溶液滴定盐酸的曲线;酸碱中和滴定操作中可选用酚酞或甲基橙作
为指示剂。
例题3 某学生用0.100 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解
为如下几步:
A. 移取20.00 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞溶液;
B. 用标准溶液润洗滴定管2~3次;
C. 把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D. 取标准KOH溶液注入碱式滴定管至0刻度以上2 cm~3 cm;
E. 调节液面至0或0以下刻度,记下读数;
F. 把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻
度。
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)________。
(2)上述B步骤操作的目的是_______________________________________
____________________________________________________________。
(3)A步骤操作之前,若先用待测溶液润洗锥形瓶,则滴定结果________(填“偏
高”“偏低”或“不变”)。
(4)判断到达滴定终点的实验现象是_____________________________
____________________________________________________________。
【答案】(1)BDCEAF (2)洗去附着在滴定管内壁上的水,防止将标准液稀释而
第24页带来误差 (3)偏高
(4)溶液由无色变为浅红色,且半分钟内不褪色
【解析】(1)本题考查的是酸碱中和滴定的实验操作过程。所以正确的操作顺序为:
BDCEAF。
(2)无论是盛放标准液还是待测液的滴定管都必须润洗,因为滴定管内壁上附着的蒸
馏水会对盛装的溶液稀释而引起测定误差。
(3)A步骤操作之前,若先用待测液润洗锥形瓶,将使锥形瓶内壁上附着待测液,导
致待测液的实际体积大于20.00 mL,最终在滴定过程中消耗的标准液偏多,使测定结果偏
高。
(4)本实验中采用酚酞作指示剂,故当溶液由无色变为浅红色,且半分钟内不褪色,
即达到了滴定终点。
(答题时间:40分钟)
一、选择题
1. 用NaOH溶液滴定盐酸时,由于滴定速率太快,当混合溶液变红时不知 NaOH是否过
量,判断它是否过量的方法是( )
A. 加入5 mL盐酸再进行滴定
B. 返滴一滴待测盐酸
C. 重新进行滴定
D. 以上方法均不适用
2. 下列是一段关于中和滴定的实验叙述:
(1)取一锥形瓶,用待测NaOH溶液润洗两次;
(2)在锥形瓶中放入25 mL待测NaOH溶液;
(3)加入几滴石蕊试剂作指示剂;
(4)取一支酸式滴定管,洗涤干净;
(5)直接往酸式滴定管中注入标准酸溶液,进行滴定;
(6)左手旋转滴定管的玻璃活塞,右手不停摇动锥形瓶;
(7)两眼注视着滴定管内盐酸溶液液面下降,直至滴定终点。
其中错误的是( )
A. (4)(6)(7) B. (1)(5)(6)(7)
C. (3)(5)(7) D. (1)(3)(5)(7)
3. 在25 ℃时,用0.125 mol·L-1的标准盐酸溶液滴定25.00 mL未知浓度的NaOH溶液所
第25页得滴定曲线如图所示,图中K点代表的pH为( )
A. 13 B. 12
C. 10 D. 11
*4. 使用酸碱中和滴定的方法,用0.01 mol·L-1盐酸滴定锥形瓶中未知浓度的NaOH溶液,
下列操作会使测定结果偏高的是( )
①用量筒量取浓盐酸配制0.01 mol·L-1稀盐酸时,量筒用蒸馏水洗净后未经干燥直接
量取浓盐酸 ②配制稀盐酸定容时,俯视容量瓶刻度线 ③滴定结束时,读数后发现滴定
管下端尖嘴处悬挂有一滴液滴 ④滴定过程中用少量蒸馏水将锥形瓶内壁附着的盐酸冲下
A. ①③ B. ②④
C. ②③④ D. ①②③④
*5. 如图是常温下向20.0 mL的盐酸中,逐滴加入0.10 mol·L-1 NaOH溶液时,溶液的
pH随NaOH溶液的体积V(mL)变化的曲线,根据图像所得的下列结论中正确的是 (
)
A. 原盐酸的浓度为0.10 mol·L-1
B. x的值为2.0
C. pH=12,V值为20.4
D. 原盐酸的浓度为1.0 mol·L-1
6. 如图表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体
积是( )
A. a mL B. (50-a)mL
C. 一定大于a mL D. 一定大于(50-a) mL
7. 现用0.10 mol·L-1 HCl溶液滴定10 mL 0.05 mol·L-1 NaOH溶液,若酸式滴定管未润
洗,达到终点时所用盐酸的体积应是( )
A. 10 mL B. 5 mL
C. 大于5 mL D. 小于5 mL
第26页二、填空题
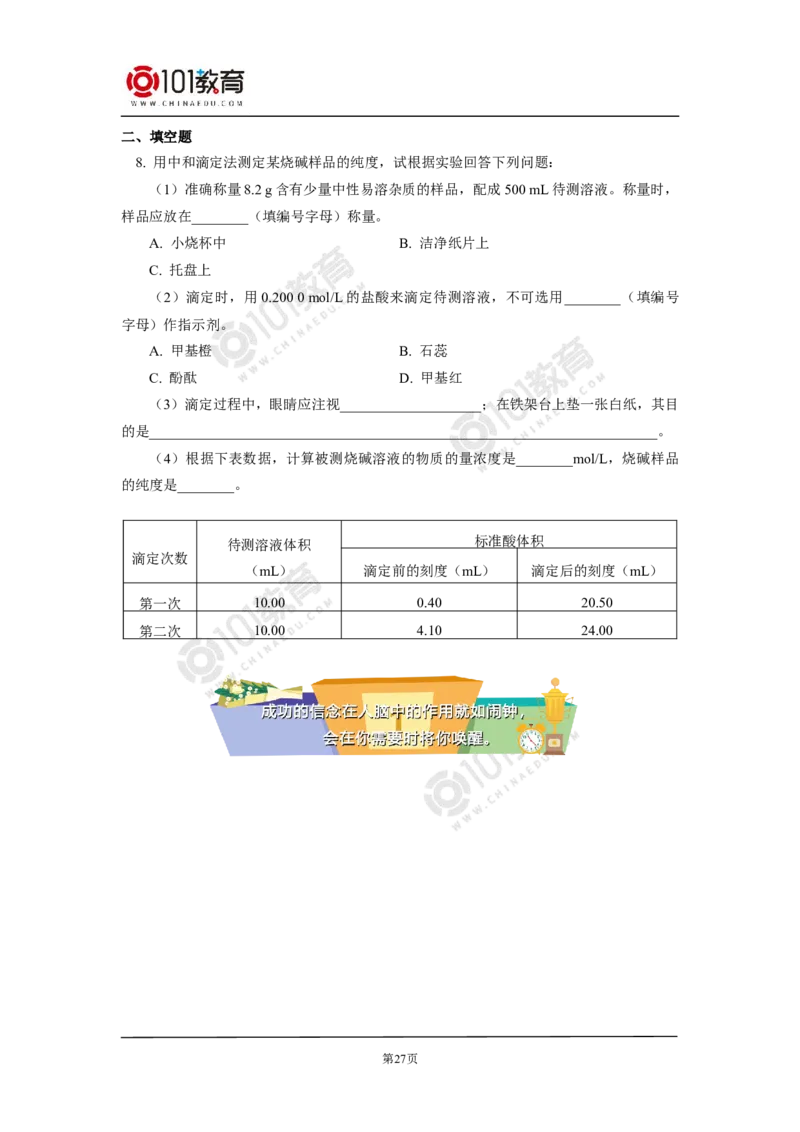
8. 用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,
样品应放在________(填编号字母)称量。
A. 小烧杯中 B. 洁净纸片上
C. 托盘上
(2)滴定时,用0.200 0 mol/L的盐酸来滴定待测溶液,不可选用________(填编号
字母)作指示剂。
A. 甲基橙 B. 石蕊
C. 酚酞 D. 甲基红
(3)滴定过程中,眼睛应注视____________________;在铁架台上垫一张白纸,其目
的是________________________________________________________________________。
(4)根据下表数据,计算被测烧碱溶液的物质的量浓度是________mol/L,烧碱样品
的纯度是________。
待测溶液体积 标准酸体积
滴定次数
(mL) 滴定前的刻度(mL) 滴定后的刻度(mL)
第一次 10.00 0.40 20.50
第二次 10.00 4.10 24.00
第27页1. 【答案】B
【解析】若NaOH过量,则返滴一滴待测盐酸,若红色消失,说明NaOH未过量,若
红色不消失,则说明NaOH过量。
2. 【答案】D
【解析】操作(1)的锥形瓶只能用水洗;操作(3)中不能用石蕊作为中和滴定的指
示剂,因为它的显色效果不明显;操作(5)中滴定管必须用标准液润洗后才能注入标准液;
操作(7)中两眼应主要注视锥形瓶中溶液颜色的变化。
3. 【答案】A
【解析】由图示可知,在V(HCl)=20.00 mL时,pH=7,HCl与NaOH恰好完全反
应 , 由 c ( HCl ) ·V ( HCl ) = c ( NaOH ) ·V ( NaOH ) , 知 c ( NaOH ) =
=0.1 mol·L-1,c(OH-)=0.1 mol·L-1,c(H
+)=10-13 mol·L-1,pH=13。
4. 【答案】A
【解析】①未干燥,相当于稀释盐酸,滴定时将消耗盐酸偏多,使结果偏高,③滴定
管下端尖嘴处悬挂有一滴盐酸,相当于消耗盐酸偏多,使结果偏高。
5. 【答案】A
【解析】当V(NaOH)=0 mL时,盐酸溶液的pH=1,因此c(HCl)=0.10 mol·L-
1;当反应后溶液pH=7时,HCl与NaOH恰好完全反应,因此n(HCl)=n(NaOH),
故 V ( NaOH ) = 20.0 mL ; 当 反 应 后 溶 液 pH = 12 时 ,
=1×10-2 mol·L-1,解得 V(NaOH)=
24.4 mL。
6. 【答案】D
【解析】滴定管的零刻度在上面,50 mL的刻度在下面,但刻度线以下仍有一部分容
积,因此液体体积一定是大于(50-a) mL。
7. 【答案】C
【解析】用0.10 mol·L-1 HCl溶液滴定10 mL 0.05 mol·L-1 NaOH溶液正好需5 mL
HCl溶液。现盐酸被稀释,其浓度小于0.10 mol·L-1,故中和NaOH所需体积大于5 mL。
8. 【答案】(1)A (2)B
(3)锥形瓶内溶液颜色的变化 便于观察锥形瓶内液体颜色的变化,减小滴定误差
(4)0.400 0 97.56%
【解析】(1)称量氢氧化钠等易潮解、腐蚀性强的试剂时,样品应放在小烧杯中;
第28页(2)酸碱中和滴定时,一般应选甲基橙、酚酞、甲基红等颜色变化较明显的指示剂,石蕊
在酸或碱溶液中颜色变化不明显,易造成误差;(4)由表中数据知,滴定时所用盐酸的体
积为20.00 mL,根据c(NaOH)= ,求得c(NaOH)=0.400 0 mol/L。
第29页