文档内容
第 1 章 有机化合物的结构特点与研究方法
第2节研究有机化合物的一般方法
第2课时
【学习目标】
1.了解有机化合物结构测定的一般步骤和程序,能进行确定有机化合物分子式的简单计算,形成宏观辨
识与微观探析的化学学科核心素养。
2.能利用官能团的化学检验方法鉴定官能团,培养证据推理与模型认知的化学学科核心素养。
3.初步了解一些测定有机化合物结构的现代手段,懂得有机化合物结构测定是有机化合物合成的重要
环节,培养科学态度与社会责任的化学学科核心素养。
【学习难点】
1.有机物结构测定方法了解
2. 有机物结构测定方法的原理
课前回忆:有机物的分离提纯,提纯有机物的方法:
蒸馏
分液
分离提纯
萃取
重结晶
一、确定元素种类
1. 定性分析——确定有什么元素。
将某有机物在O 中充分燃烧后,各元素对应的燃烧产物
2
C - C O ; N- N ; H - H O 。
2 2 2
2.定量分析——最简整数比
判断是否含有 氧元素 。
碳元素的质量与氢元素质量之和等于有机物的质量则该物质中无氧元素。碳元素的质量与氢元素质量之和
不等于有机物的质量则该物质中无氧元素。
①根据CO 的质量和HO的质量分别求出C元素和氢元素的质量;剩下的即为氧的质量。
2 2
②求C与H的个数比,或C、H与O的个数比,确定最简式。3.李比希元素分析流程图
1.分别说明A;B;C;D;E;F装置的作用分别是什么?
反应装置,净化装置,再反应装置,吸收装置,吸收装置,防污染装置
制取氧气,吸收水蒸气,物质充分燃烧,吸收水,吸收二氧化碳,防止空气中水和二氧化碳进入装置中
2 . 说明 Cu O 的作用:
作氧化剂,充分氧化为完全燃烧的一氧化碳
【例题】:
1、含C、H、O三元素的未知物A,经燃烧分析实验测定该未知物中碳的质量分数为 52.2%,氢的质量分数
为13.1%。试求该未知物A的实验式。
(1)计算该有机化合物中氧元素的质量分数:
ω(O ) = 100 % - 52.2 % - 13.1 % = 34.7 %
(2)计算该有机化合物分子内各元素原子的个数比:
N(C ) : N(H ) : N(O ) == 4. 3 : 1 3 : 2. 1 = 2 : 6 : 1
2.已知由C、H、O元素组成的某化合物9.2 g完全燃烧后可以得到17.6 g CO2和10.8 g H2O,通过计算确
定该化合物的实验式 。(写出解题过程)
17.6g 10.8g 9.2g-m(C)-m(H)
【 详 解 】 n (C) = =0.4 mol , n (H) = ×2=1.2 mol , n (O) = =
44g/mol 18g/mol 16g/mol
9.2g-0.4mol×12g/mol-1.2mol×1g/mol
=0. 2 mo l ,故 n (C ) ∶ n (H ) ∶ n (O) =N (C ) ∶ N (H ) ∶ N (O ) =
16g/mol
2 ∶ 6 ∶ 1 ,该化合物的实验式为 CH O 。
2 62.某仅由碳、氢、氧三种元素组成的有机化合物。取有机物样品1.8 g,在纯氧中完全燃烧,将产物先后
通过浓硫酸和碱石灰,两者分别增重1.08 g和2.64 g。试求该有机物的实验式 。
【答案】CH O;
2
1.08 g 2.64 g
【详解】已知m(H)= ×2=0.12 g,m(C)= ×12=0.72 1:2:1g
18 44
则m(O)=1.8g−0.12 g−0.72 g=0.96 g
0.72g 0.12g 0.96g
n(C):n(H):n(O)= : : =1:2:1
则 12g 1g 16g ,则其实验式为CH O;
2
mol mol mol
故答案为:CH O。
2
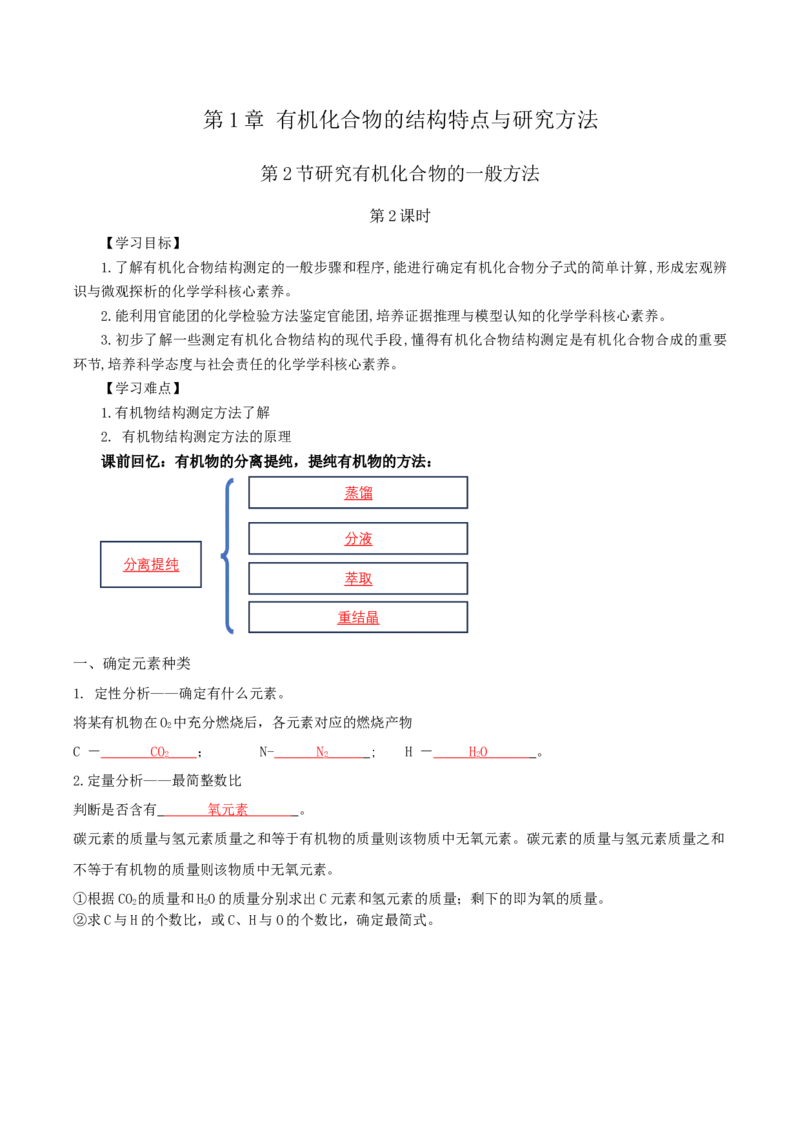
4.确定分子式—质谱法
离子因质量、电荷不同,在电场和磁
质谱仪用高能电子流等轰
有机分子失去电子形成带正电 场中运动行为不同
击
荷的分子离子和碎片离子等
少量样品 计算机分析
得到它们相对质量与电荷数比值 以质荷比为横坐标,
(质荷比) 以各类离子相对丰度
为纵坐标记录测试结
果,得到质谱图
二、确定分子式
已知最简比,测分子相对质量即可得分子式
1.质谱法测相对质量
质谱仪——可以精确测定相对分子质量。
原理:用高能电子流轰击样品,使分子失去电子变成带正电荷得分子离子和碎片离子,在磁场得作用下,
由于他们得相对质量不同而使其到达检测器的时间先后不同,其结果被记录为质谱图。
质谱图:横坐标表示碎片的质荷比,纵坐标表示碎片的相对丰度,峰上的数据表示碎片的相对质量。分子
离子的相对质量越大,质荷比就越大,到达检测器需要的时间就越长,因此质谱图中最右边的峰表示的就
是样品的相对分子质量。
①质荷比:是指离子的相对质量与其电荷的比值。
②质谱图中,质荷比的最大值表示样品分子的相对分子质量。求相对分子质量:的一些方法
① M=m/n
②有机蒸气的相对密度D=M/M 标准状况下,有机蒸气的密度为ρ g/L
1 2
③标准状况下,有机蒸气的密度为ρ g/L M=22.4L/mol × ρ g/L
某混合气体在标准状况下的密度为0.8g/L,该混合气体的平均相对分子质量为
19.7
2.某烃的蒸气密度是相同状况下氢气密度的80倍,该卤代烃的摩尔质量为:
180g/mol
3.某烃的蒸气密度是相同状况下甲烷密度的4.5倍,该卤代烃的摩尔质量为:
72g/mol
三、有机物分子结构确定
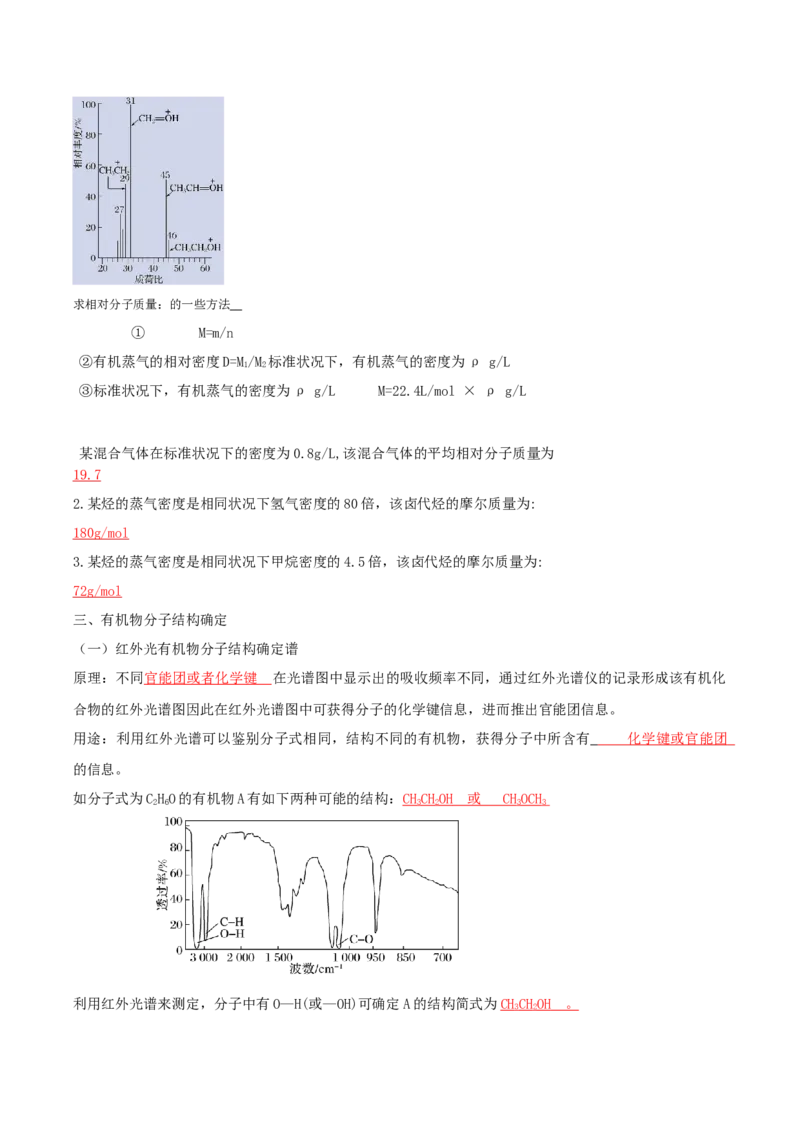
(一)红外光有机物分子结构确定谱
原理:不同官能团或者化学键 在光谱图中显示出的吸收频率不同,通过红外光谱仪的记录形成该有机化
合物的红外光谱图因此在红外光谱图中可获得分子的化学键信息,进而推出官能团信息。
用途:利用红外光谱可以鉴别分子式相同,结构不同的有机物,获得分子中所含有 化学键或官能团
的信息。
如分子式为CHO的有机物A有如下两种可能的结构:CHCH O H 或 C HOCH
2 6 3 2 3 3
利用红外光谱来测定,分子中有O—H(或—OH)可确定A的结构简式为CHCH O H 。
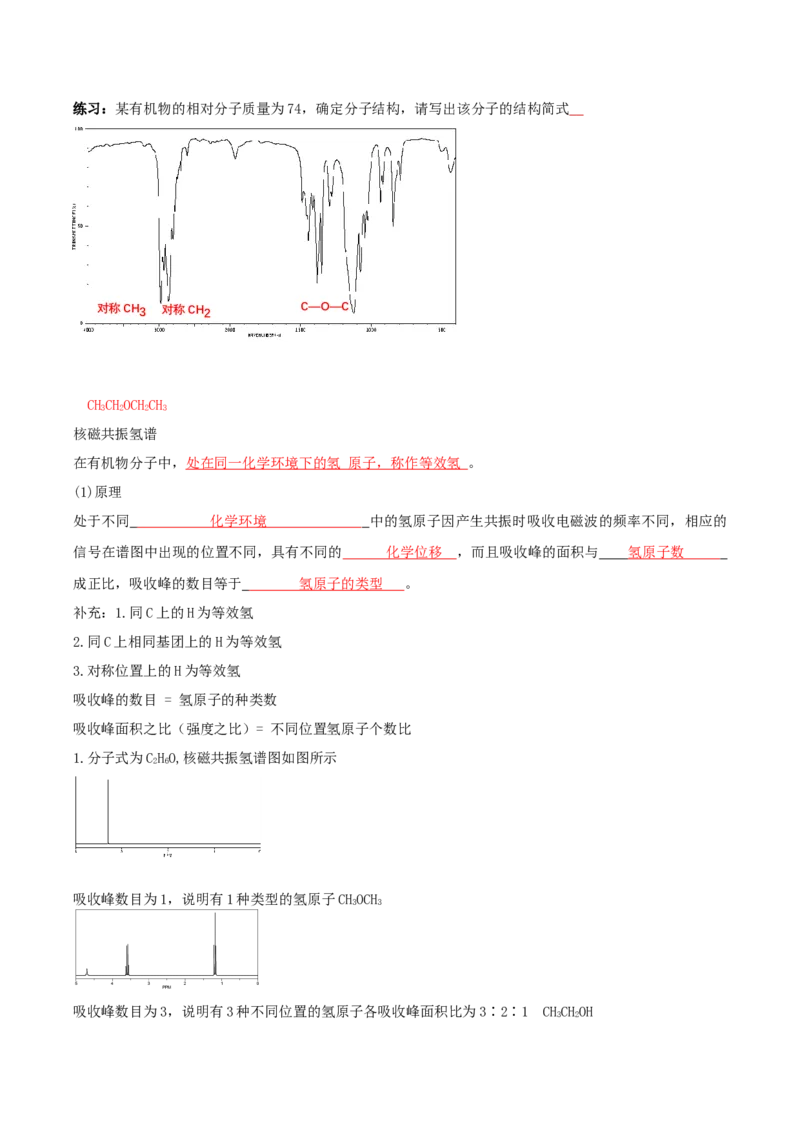
3 2练习:某有机物的相对分子质量为74,确定分子结构,请写出该分子的结构简式
对称CH3 对称CH2 C―O―C
CHCHOCHCH
3 2 2 3
核磁共振氢谱
在有机物分子中,处在同一化学环境下的氢 原子,称作等效氢 。
(1)原理
处于不同 化学环境 中的氢原子因产生共振时吸收电磁波的频率不同,相应的
信号在谱图中出现的位置不同,具有不同的 化学位移 ,而且吸收峰的面积与 氢原子数
成正比,吸收峰的数目等于 氢原子的类型 。
补充:1.同C上的H为等效氢
2.同C上相同基团上的H为等效氢
3.对称位置上的H为等效氢
吸收峰的数目 = 氢原子的种类数
吸收峰面积之比(强度之比)= 不同位置氢原子个数比
1.分子式为CHO,核磁共振氢谱图如图所示
2 6
吸收峰数目为1,说明有1种类型的氢原子CHOCH
3 3
5 4 3 2 1 0
PPM
吸收峰数目为3,说明有3种不同位置的氢原子各吸收峰面积比为3∶2∶1 CHCHOH
3 2CH 的几种核磁共振氢谱
4 8
扩展:核磁共振碳谱
在有机物分子中,不同处在同一化学环境下的碳原子化学位移不同。
分子式为CHO,核磁共振氢谱图如图所示
2 6
60 50 40 30 20 10 0
PPM
化学式: C HCH O H
3 2
60 50 40 30 20 10 0
PPM
化学式: C HOCH
3 3
扩展:X射线衍射
(1)原理
X 射线是一种波长很短(约 1 0 -1 0 m )的电磁波,它和晶体中的原子相互作用可以产生衍射谱图。
(2)用途
经过计算可以从中获得分子结构的有关数据,包括键长、键角等分子结构信息。将 X 射线衍射技术用于有机化合物(特别是复杂的生物大分子)晶体结构的测定,可以获得更为直接而详尽的结构信息。
课堂习题专练
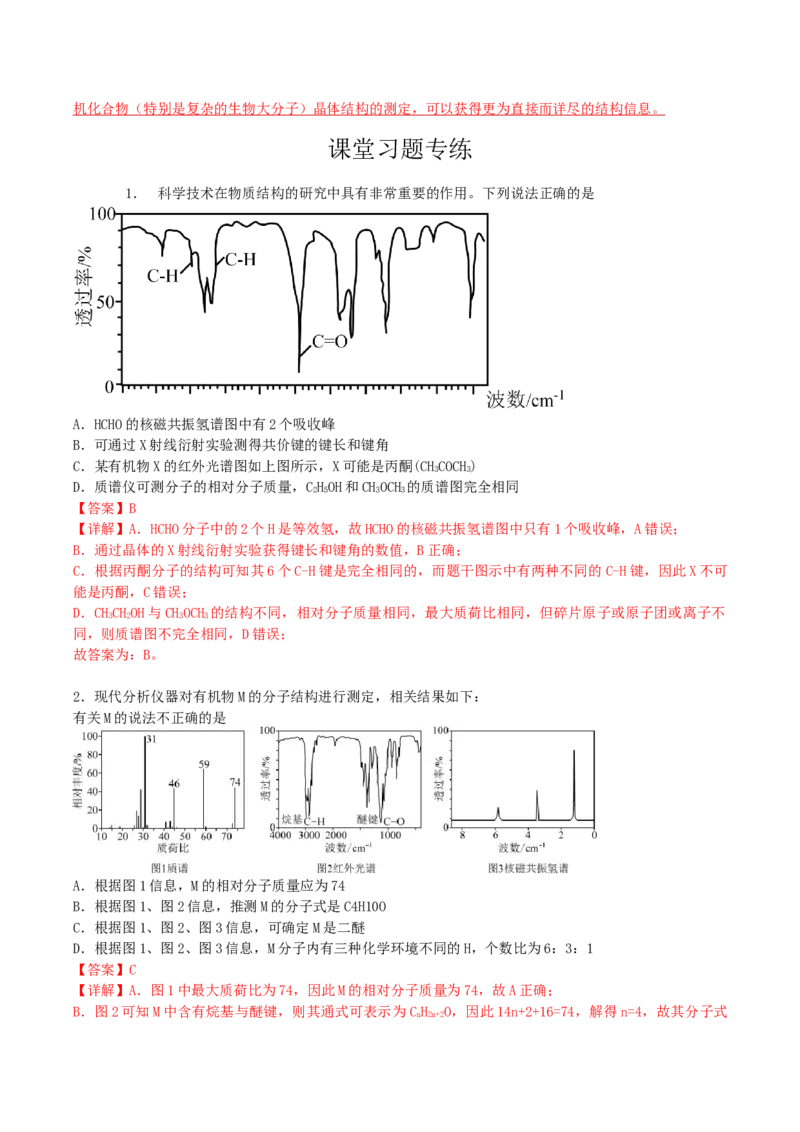
1. 科学技术在物质结构的研究中具有非常重要的作用。下列说法正确的是
A.HCHO的核磁共振氢谱图中有2个吸收峰
B.可通过X射线衍射实验测得共价键的键长和键角
C.某有机物X的红外光谱图如上图所示,X可能是丙酮(CHCOCH)
3 3
D.质谱仪可测分子的相对分子质量,CHOH和CHOCH 的质谱图完全相同
2 5 3 3
【答案】B
【详解】A.HCHO分子中的2个H是等效氢,故HCHO的核磁共振氢谱图中只有1个吸收峰,A错误;
B.通过晶体的X射线衍射实验获得键长和键角的数值,B正确;
C.根据丙酮分子的结构可知其6个C-H键是完全相同的,而题干图示中有两种不同的C-H键,因此X不可
能是丙酮,C错误;
D.CHCHOH与CHOCH 的结构不同,相对分子质量相同,最大质荷比相同,但碎片原子或原子团或离子不
3 2 3 3
同,则质谱图不完全相同,D错误;
故答案为:B。
2.现代分析仪器对有机物M的分子结构进行测定,相关结果如下:
有关M的说法不正确的是
A.根据图1信息,M的相对分子质量应为74
B.根据图1、图2信息,推测M的分子式是C4H10O
C.根据图1、图2、图3信息,可确定M是二醚
D.根据图1、图2、图3信息,M分子内有三种化学环境不同的H,个数比为6:3:1
【答案】C
【详解】A.图1中最大质荷比为74,因此M的相对分子质量为74,故A正确;
B.图2可知M中含有烷基与醚键,则其通式可表示为CH O,因此14n+2+16=74,解得n=4,故其分子式
n 2n+2为CH O,故B正确;
4 10
C.由图2可知M属于醚类,结合分子式CH O,可确定M是一元醚,故C错误;
4 10
D.由图3可知M中含有3种类型的氢原子,并且个数比为6:3:1,故D正确;
答案选C。
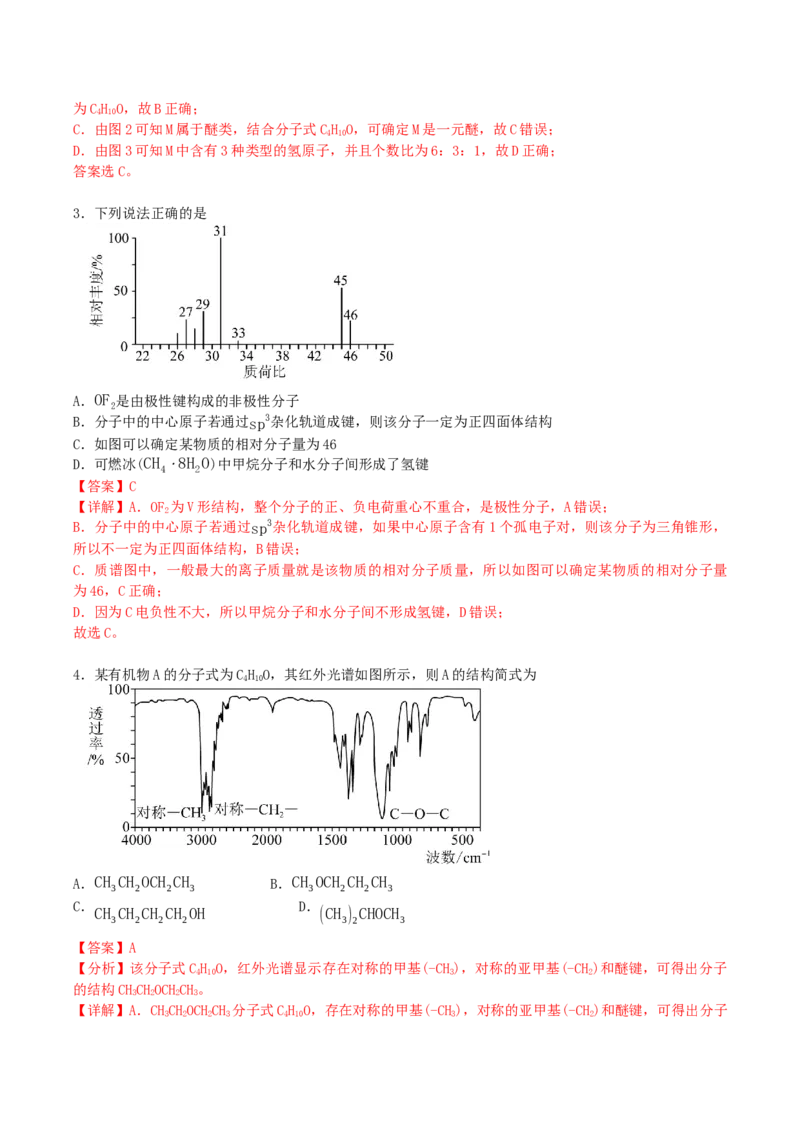
3.下列说法正确的是
A.OF 是由极性键构成的非极性分子
2
B.分子中的中心原子若通过sp3杂化轨道成键,则该分子一定为正四面体结构
C.如图可以确定某物质的相对分子量为46
D.可燃冰(CH ⋅8H O)中甲烷分子和水分子间形成了氢键
4 2
【答案】C
【详解】A.OF 为V形结构,整个分子的正、负电荷重心不重合,是极性分子,A错误;
2
B.分子中的中心原子若通过sp3杂化轨道成键,如果中心原子含有1个孤电子对,则该分子为三角锥形,
所以不一定为正四面体结构,B错误;
C.质谱图中,一般最大的离子质量就是该物质的相对分子质量,所以如图可以确定某物质的相对分子量
为46,C正确;
D.因为C电负性不大,所以甲烷分子和水分子间不形成氢键,D错误;
故选C。
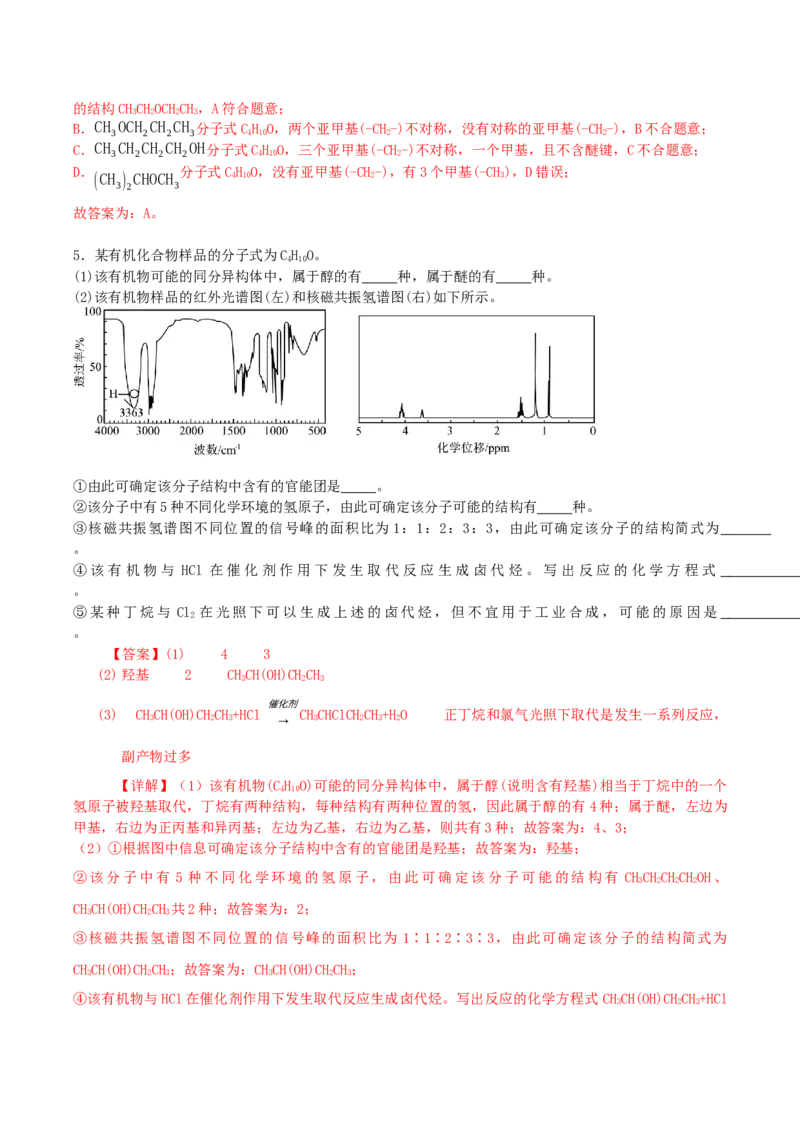
4.某有机物A的分子式为CH O,其红外光谱如图所示,则A的结构简式为
4 10
A.CH CH OCH CH B.CH OCH CH CH
3 2 2 3 3 2 2 3
C. D.
CH CH CH CH OH (CH ) CHOCH
3 2 2 2 3 2 3
【答案】A
【分析】该分子式CH O,红外光谱显示存在对称的甲基(-CH),对称的亚甲基(-CH)和醚键,可得出分子
4 10 3 2
的结构CHCHOCHCH。
3 2 2 3
【详解】A.CHCHOCHCH 分子式CH O,存在对称的甲基(-CH),对称的亚甲基(-CH)和醚键,可得出分子
3 2 2 3 4 10 3 2的结构CHCHOCHCH,A符合题意;
3 2 2 3
B.CH OCH CH CH 分子式CH O,两个亚甲基(-CH-)不对称,没有对称的亚甲基(-CH-),B不合题意;
3 2 2 3 4 10 2 2
C.CH CH CH CH OH分子式CH O,三个亚甲基(-CH-)不对称,一个甲基,且不含醚键,C不合题意;
3 2 2 2 4 10 2
D. 分子式CH O,没有亚甲基(-CH-),有3个甲基(-CH),D错误;
(CH ) CHOCH 4 10 2 3
3 2 3
故答案为:A。
5.某有机化合物样品的分子式为CH O。
4 10
(1)该有机物可能的同分异构体中,属于醇的有 种,属于醚的有 种。
(2)该有机物样品的红外光谱图(左)和核磁共振氢谱图(右)如下所示。
①由此可确定该分子结构中含有的官能团是 。
②该分子中有5种不同化学环境的氢原子,由此可确定该分子可能的结构有 种。
③核磁共振氢谱图不同位置的信号峰的面积比为1:1:2:3:3,由此可确定该分子的结构简式为
。
④该有机物与 HCl 在催化剂作用下发生取代反应生成卤代烃。写出反应的化学方程式
。
⑤某种丁烷与 Cl 在光照下可以生成上述的卤代烃,但不宜用于工业合成,可能的原因是
2
。
【答案】(1) 4 3
(2)羟基 2 CHCH(OH)CHCH
3 2 3
催化剂
(3) CHCH(OH)CHCH+HCl CHCHClCHCH+HO 正丁烷和氯气光照下取代是发生一系列反应,
3 2 3 → 3 2 3 2
副产物过多
【详解】(1)该有机物(CH O)可能的同分异构体中,属于醇(说明含有羟基)相当于丁烷中的一个
4 10
氢原子被羟基取代,丁烷有两种结构,每种结构有两种位置的氢,因此属于醇的有4种;属于醚,左边为
甲基,右边为正丙基和异丙基;左边为乙基,右边为乙基,则共有3种;故答案为:4、3;
(2)①根据图中信息可确定该分子结构中含有的官能团是羟基;故答案为:羟基;
②该分子中有 5 种不同化学环境的氢原子,由此可确定该分子可能的结构有 CHCHCHCHOH、
3 2 2 2
CHCH(OH)CHCH 共2种;故答案为:2;
3 2 3
③核磁共振氢谱图不同位置的信号峰的面积比为 1∶1∶2∶3∶3,由此可确定该分子的结构简式为
CHCH(OH)CHCH;故答案为:CHCH(OH)CHCH;
3 2 3 3 2 3
④该有机物与HCl在催化剂作用下发生取代反应生成卤代烃。写出反应的化学方程式 CHCH(OH)CHCH+HCl
3 2 3催化剂 催化剂
CHCHClCHCH+HO;故答案为:CHCH(OH)CHCH+HCl CHCHClCHCH+HO;
→ 3 2 3 2 3 2 3 → 3 2 3 2
⑤某种丁烷与Cl 在光照下可以生成上述的卤代烃,但不宜用于工业合成,可能的原因是正丁烷和氯气光
2
照下取代是发生一系列反应,副产物过多;故答案为:正丁烷和氯气光照下取代是发生一系列反应,副产
物过多。