文档内容
第二节 氯及其化合物
第2课时 氯气与碱的反应 氯离子的检验
基础巩固
1.下列生活中的物质与其有效成分的化学式、用途的对应关系中,不正确的是
选项 A B C D
生活中的物质 食盐 小苏打 复方氢氧化铝片 漂白粉
有效成分的化学式
用途 做调味品 做发酵粉 做抗酸药 做消毒剂
【答案】B
【解析】
A.食盐的主要成分是氯化钠,有咸味,可做调味品,故A正确;
B.小苏打的主要成分为碳酸氢钠,不是碳酸钠,故B错误;
C.氢氧化铝难溶于水,能够和盐酸反应,可以做抗酸药,故C正确;
D.漂白粉的有效成分为Ca(ClO) ,具有强氧化性,可做消毒剂,故D正确;
2
故选B。
2.如图所示,从a处通入新制备的 ,关闭b阀时,c处的干燥红色布条看不到明显现象;当打开b阀
后,c处红色布条逐渐褪色。d瓶中装的是( )
①浓硫酸 ②NaOH溶液 ③ ④饱和NaCl溶液
A.①③ B.②④ C.①② D.③④
【答案】C
【解析】本题解题关键在于明确HClO有漂白作用,干燥的 不具备漂白作用。先判断a处通入的
是否带有水蒸气。根据b阀打开时,红色布条褪色,说明a处通入的是潮湿的 ;潮湿的 在b阀关
闭后通过d,看不到c处红色布条有明显变化,说明d处溶液吸收了氯气或者吸收了潮湿氯气中的水蒸
气。因此正确选项为C。
3.发生氯气泄漏时,下列防护措施合理的是( )
①及时转移疏散人群,同时向有关部门如实报告事故有关情况 ②被转移人群应戴上用浓NaOH处理过
的口罩 ③用高压水枪向空中喷洒含碱性物质的水溶液 ④被转移人群应戴上用NaCO 处理过的口罩(湿
2 3
润)⑤将人群转移到地势较低的地方即可,不必走太远 ⑥及时清理现场,检查水源和食物等是否被污染
学科网(北京)股份有限公司⑦常温下氯气能溶解于水,所以只要向空气中喷洒水就可以解毒
A.②③④⑤ B.①③④⑥
C.①②⑤⑥ D.①③⑤⑦
【答案】 B
【解析】 NaOH为强碱,有强腐蚀性,②不合理;Cl 的密度比空气的大,不能将人群转移到地势较低
2
的地方,⑤不合理;Cl 溶解度不大且溶于水生成HCl,⑦不合理。
2
4.下列关于氯及其化合物的叙述正确的是
A.氯气无漂白性,而次氯酸有,因此氯水能使鲜花褪色而干燥的氯气不行
B.漂白粉的主要成分是Ca(ClO) ,主要用于杀菌消毒
2
C.工业生产中不是将氯气通入澄清石灰水中来制取漂白粉
D.漂白液和洁厕灵(主要含HCl)两种都是消毒剂,一起用效果更好
【答案】C
【解析】A. 氯气无漂白性,而次氯酸有,鲜花中含有水,因此干燥的氯气能使鲜花褪色,A错误;
B. 漂白粉的主要成分是Ca(ClO) 和CaCl ,有效成分是Ca(ClO) ,B错误;
2 2 2
C. 澄清石灰水是稀溶液,工业生产中将氯气通入澄清石灰乳中来制取漂白粉,C正确;
D. 一起用时,漂白液中NaClO和洁厕灵中HCl发生氧化还原反应生成氯气,氯气有毒,D错误;
故选C。
5.下列说法正确的是
A.漂白粉是纯净物,84消毒液是混合物,两者都可以长期保存
B.漂白粉中含有次氯酸,所以漂白粉能使有机色质褪色
C.工业上将氯气通入澄清石灰水中制取漂白粉
D.漂白粉在空气中容易失效的原因是Ca(ClO) 与CO 、H O反应生成的HClO不稳定
2 2 2
【答案】D
【解析】A.因漂白粉的主要成分是氯化钙和次氯酸钙,是混合物,Ca(ClO) 、NaClO能和空气中二氧化碳
2
反应,所以不能长期保存,故A错误;
B.漂白粉的主要有效成分为次氯酸钙,不含次氯酸,次氯酸酸性弱于碳酸,所以次氯酸钙与空气中二氧
化碳和水反应生成具有漂白性的次氯酸,能够使染料等有机色素褪色,故B错误;
C.因为澄清石灰水中氢氧化钙浓度太低成本较高,工业上通常用石灰乳与氯气反应制取漂白粉,故C错
误;
D.碳酸酸性大于HClO,强酸能和弱酸盐反应生成弱酸,漂白粉中Ca(ClO) 易与空气中的二氧化碳和水反
2
应生成碳酸钙和HClO,HClO见光易分解,导致漂白粉失效,故D正确;
故选:D。
6.下列关于含氯消毒剂的解释不正确的是
A.“84”消毒液不能与洁厕灵混合使用:2H++Cl-+ClO-=Cl ↑+H O
2 2
B.工业上将氯气通入石灰乳制取漂白粉:2Cl +2Ca(OH) =CaCl +Ca(ClO) +2H O
2 2 2 2 2
C.氯水应避光保存的原因是:2HClO H O+Cl ↑
2 2
学科网(北京)股份有限公司D.氯气意外发生泄漏,可用浸有一定浓度NaHCO 溶液的毛巾捂住鼻子,向高处转移
3
【答案】C
【解析】A.84消毒液含NaClO,洁厕灵含HCl,两者混用发生反应NaClO+2HCl=Cl ↑+NaCl+H O,A正确;
2 2
B.工业上用Cl 与石灰乳反应制漂白粉,B正确;
2
C.次氯酸见光易分解,2HClO 2HCl+O ↑,C错误;
2
D.NaHCO 溶液具有弱碱性,能与氯气反应,处在该环境中,可用浸有一定浓度NaHCO 溶液的毛巾捂住
3 3
鼻子,向高处转移,D正确;
故选C。
7.(2021·洮南市第一中学高一月考)某溶液中含有较大量的Cl-、 、OH-三种阴离子,如果只取一
次该溶液就能够分别将3种阴离子依次检验出来。下列实验操作的操作顺序中, 正确的是
①滴加Mg(NO) 溶液 ②过滤 ③滴加AgNO 溶液 ④滴加Ba(NO ) 溶液
3 2 3 3 2
A.①②④②③ B.④②③②① C.①②③②④ D.④②①②③
【答案】D
【解析】
检验氯离子选择硝酸银溶液;检验氢氧根离子,选择硝酸镁溶液;检验碳酸根离子选择硝酸钡溶液,用
三种试剂将三种离子检验出来,每加一种试剂能够检验出一种离子,此时要注意每加入一种试剂只能与
一种离子结合,来选择加入试剂顺序及操作步骤。
Cl-用含有AgNO 溶液检验,二者反应生成白色沉淀AgCl; 用Ba(NO ) 溶液检验,二者反应生成白
3 3 2
色沉淀BaCO ;OH-用Mg(NO) 溶液检验,二者反应生成白色沉淀Mg(OH) 。Cl-、 、OH-都和
3 3 2 2
AgNO 溶液反应, 、OH-都和Mg(NO) 溶液反应生成白色沉淀;只有 和Ba(NO ) 溶液反应生成
3 3 2 3 2
白色沉淀,为了防止干扰,应该先检验Ba(NO )、再检验OH-,故加入试剂顺序是④②①②③,故合理选
3 2
项是D。
8.“84”消毒液对新型冠状病毒具有消杀作用。如图所示为某品牌“84”消毒液使用说明的一部分,下列说法
错误的是
(主要成分)本品是以次氯酸钠(NaClO)为主要有效成分的消毒液。
(注意事项)
1.本品为外用消毒剂,不可内服。
2.本品对金属制品有腐蚀作用,对棉纺织品有漂白脱色作用。
3.密闭、避光、避热、置于阴凉处保存。
A.次氯酸钠中的Cl元素显+1价 B.“84”消毒液见光易变质
C.“84”消毒液能使品红溶液褪色 D.“84”消毒液能用不锈钢容器盛放
【答案】D
【解析】
A.次氯酸钠中Na为+1价、O为-1价,则Cl为+1价,A正确;
B.“84”消毒液会和空气中的CO 反应生成HClO,HClO见光易分解,从而导致变质,B正确;
2
学科网(北京)股份有限公司C.“84”消毒液具有强氧化性,具有漂白性,可以漂白品红溶液,C正确;
D.“84”消毒液对金属制品有腐蚀作用,不能用不锈钢容器盛放,D错误;
综上所述答案为D。
9.有关漂白粉和漂白液的说法正确的是_______(填序号)。
①工业上将氯气通入澄清石灰水制取漂白粉。
②漂白液的有效成分是NaClO,漂白粉的有效成分是Ca(ClO) 。
2
③漂白粉和Fe(OH) 胶体都常用于自来水的处理,二者的作用原理不相同。
3
④漂白粉在空气中久置不可能发生氧化还原反应。
⑤漂白粉在空气中久置变质,理由是漂白粉中的CaCl 与空气中的CO 反应生成CaCO 。
2 2 3
⑥漂白粉在空气中不稳定,所以可用于漂白纸张。
【答案】②③
【解析】
①不正确,漂白粉是将Cl 通入石灰乳中制得的混合物,反应的化学方程式为2Cl+2Ca(OH) =CaCl +
2 2 2 2
Ca(ClO) +2HO;
2 2
②正确,漂白液的有效成分是NaClO,漂白粉的主要成分是CaCl 、Ca(ClO) ,有效成分是Ca(ClO) ;
2 2 2
③正确,漂白粉用于自来水杀菌消毒,Fe(OH) 胶体用于除去水中的悬浮杂质,二者的作用原理不同;
3
④不正确,漂白粉在空气中久置的化学方程式为Ca(ClO) +HO+CO=CaCO +2HClO,2HClO 2HCl
2 2 2 3
+O↑,既有复分解反应,又有氧化还原反应;
2
⑤不正确,漂白粉在空气中失效原因是Ca(ClO) +HO+CO=CaCO +2HClO,而2HClO 2HCl+O↑;
2 2 2 3 2
⑥不正确,漂白粉能用于漂白纸张,与其强氧化性有关,与不稳定性无关。
则答案为: ②③。
10.(1)在某防空防灾演习现场,模拟一起大客车与一辆装有氯气的槽罐车发生追尾事故,造成槽罐翻落、
氯气泄露。人防办立即指挥专业救援队在事发地点,测定风向,进行事故处置。引导大客车上的乘客
_____________(填序号)
a.顺风向高处转移 b.顺风向低处转移
c.逆风向高处转移 d.逆风向低处转移
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现
象是 ________。
(3)为防止氯气尾气污染空气,根据氯气的性质,可用NaOH溶液吸收多余的氯气,原理是(用离子方程式
表示) ____________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的
有效成分是________(填化学式),长期露置于空气中的漂白粉会失效的原因,用化学反应方程式可表示为
________。
【答案】c 干燥的有色布条无明显变化,湿润的有色布条褪色 Cl+2OH-=ClO-+Cl-+HO
2 2
学科网(北京)股份有限公司Ca(ClO) Ca(ClO) +CO +HO=CaCO ↓+2HClO,2HClO 2HCl+O ↑
2 2 2 2 3 2
【解析】
(1)氯气有毒,且氯气的密度大于空气的密度,因此引导大客车上的乘客逆风高处转移,选项c正确;故
答案为c;
(2)氯气本身不具有漂白性,干燥的氯气不能使干燥的有色布条褪色,氯气遇到水产生次氯酸,次氯酸具
有强氧化性,具有漂白性,氯气能使湿润有色布条褪色;故答案为干燥的有色布条无明显变化,湿润的
有色布条褪色;
(3)Cl 能与NaOH发生歧化反应,其离子方程式为Cl+2OH-=Cl-+ClO-+HO;漂白粉的成分是CaCl
2 2 2 2
和Ca(ClO) ,其有效成分是Ca(ClO) ;碳酸的酸性强于次氯酸,漂白粉长期露置于空气中发生
2 2
Ca(ClO) +CO +HO=CaCO ↓+2HClO,2HClO 2HCl+O ↑;故答案为Cl+2OH-=Cl-+ClO-+HO;
2 2 2 3 2 2 2
Ca(ClO) ;Ca(ClO) +CO +HO=CaCO ↓+2HClO,2HClO 2HCl+O ↑。
2 2 2 2 3 2
能力提升
11.已知氯气和NaOH溶液在一定温度下能发生反应:Cl +2NaOH=NaCl+NaClO+H O,3Cl +
2 2 2
6NaOH=5NaCl+NaClO +3H O。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO 的
3 2 3
混合溶液,经测定ClO-与ClO 的个数比为1∶3,则氯气与氢氧化钠反应时,被还原的氯原子和被氧化的
氯原子的个数比为
A.21∶5 B.11∶3 C.3∶1 D.4∶1
【答案】D
【解析】根据ClO-与ClO 的个数之比1:3,由Cl 到ClO-,每个氯原子失去1个电子,由Cl 到ClO ,每个
2 2
氯原子失去5个电子,一共失去1+3×5=16个电子;由Cl 到Cl-,每个氯原子得到1个电子,需要16个原
2
子才能得到16个电子,所以,被还原的氯原子和被氧化的氯原子的个数比=16:(1+3)=4:1;
故答案为D。
12.某学生做如下实验:第一步,在淀粉KI溶液中滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即
变蓝:第二步,在上述蓝色溶液中,滴加足量的NaSO 溶液,蓝色逐渐消失,并检测到有硫酸钠生成。
2 3
下列叙述中该同学对实验原理的解释和所得结论不正确的是
A.氧化性:HC1O>I >SO
2
B.淀粉KI溶液变蓝是因为I-被HClO氧化为I,I 遇淀粉变蓝
2 2
C.蓝色消失的原因是NaSO 溶液具有漂白性
2 3
D.若将足量NaSO 溶液加入氯水中,氯水褪色
2 3
【答案】C
【解析】
在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝,说明NaClO将KI氧
学科网(北京)股份有限公司化为单质碘;加入足量的亚硫酸钠溶液,蓝色逐渐消失,说明碘单质将NaSO 氧化为NaSO ,自身成为
2 3 2 4
碘离子。
A.第一步反应生成了碘单质,说明氧化性:ClO−>I,第二步碘被NaSO 还原,说明氧化性:ClO−>I
2 2 3 2
>SO ,故A正确;
B.根据以上分析知,淀粉−KI溶液变蓝是因为I−被ClO−氧化为I,I 使淀粉变蓝,故B正确;
2 2
C.根据以上分析知,蓝色消失的原因是NaSO 溶液具有还原性,故C错误;
2 3
D.亚硫酸钠具有还原性,能被强氧化剂氯气氧化生成硫酸钠,同时氯气被还原为氯离子,所以氯水褪色,
故D正确;
故选:C。
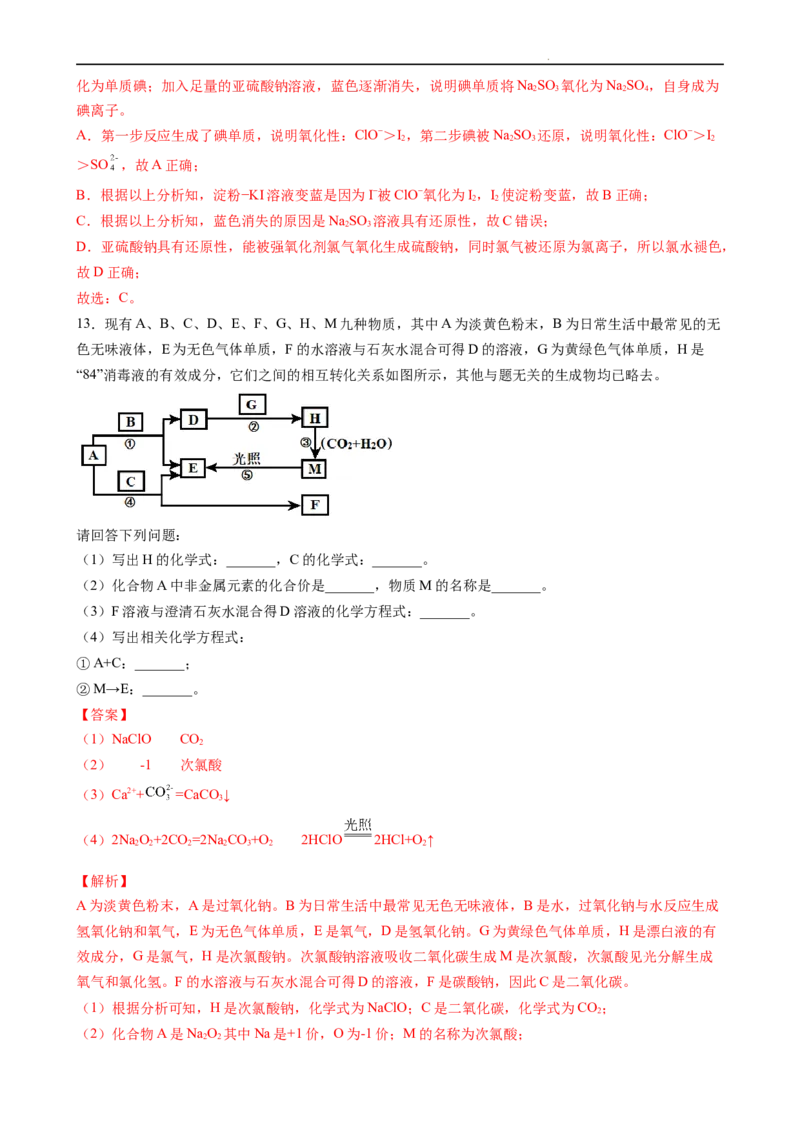
13.现有A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,B为日常生活中最常见的无
色无味液体,E为无色气体单质,F的水溶液与石灰水混合可得D的溶液,G为黄绿色气体单质,H是
“84”消毒液的有效成分,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。
请回答下列问题:
(1)写出H的化学式:_______,C的化学式:_______。
(2)化合物A中非金属元素的化合价是_______,物质M的名称是_______。
(3)F溶液与澄清石灰水混合得D溶液的化学方程式:_______。
(4)写出相关化学方程式:
①A+C:_______;
②M→E:_______。
【答案】
(1)NaClO CO
2
(2) -1 次氯酸
(3)Ca2++ =CaCO ↓
3
(4)2NaO+2CO =2Na CO+O 2HClO 2HCl+O ↑
2 2 2 2 3 2 2
【解析】
A为淡黄色粉末,A是过氧化钠。B为日常生活中最常见无色无味液体,B是水,过氧化钠与水反应生成
氢氧化钠和氧气,E为无色气体单质,E是氧气,D是氢氧化钠。G为黄绿色气体单质,H是漂白液的有
效成分,G是氯气,H是次氯酸钠。次氯酸钠溶液吸收二氧化碳生成M是次氯酸,次氯酸见光分解生成
氧气和氯化氢。F的水溶液与石灰水混合可得D的溶液,F是碳酸钠,因此C是二氧化碳。
(1)根据分析可知,H是次氯酸钠,化学式为NaClO;C是二氧化碳,化学式为CO;
2
(2)化合物A是NaO 其中Na是+1价,O为-1价;M的名称为次氯酸;
2 2
学科网(北京)股份有限公司(3)F是碳酸钠,其溶液与澄清石灰水混合得D溶液的离子方程式为Ca2++ =CaCO ↓;
3
(4)两个化学方程式分别为:2Na O+2CO =2Na CO+O 、2HClO 2HCl+O ↑;
2 2 2 2 3 2 2
14.为了探究氯水能否和碳酸钙发生化学反应,某学生设计如下实验:
实验一:向盛有饱和氯水的锥形瓶中加入大理石,并充分振荡,观察到氯水的黄绿色褪去并同时产生气
体。
实验二:取实验一后锥形瓶中清液,进行如下实验:
①该清液滴在有色布条上有极强的漂白作用。
②该清液中滴加碳酸钠溶液产生白色沉淀。
③该清液中滴加盐酸可产生大量气体。
实验三:该学生设想用下列装置收集实验二中产生的气体做进一步检验。
回答下列问题:
(1)在实验二中,清液滴在有色布条上有极强的漂白作用说明该清液中含有________________(写化学式);
清液中滴加碳酸钠溶液产生白色沉淀说明该清液中含有________;清液中滴加盐酸产生的气体是
________(用化学式表示)。
(2)实验三中,洗气装置内的洗涤液一般用________溶液,用装置________收集。
(3) 该 学 生 通 过 上 述 实 验 , 写 出 了 氯 水 和 碳 酸 钙 反 应 的 化 学 方 程 式 :
_____________________________________________________。
【答案】(1)HClO Ca2+ Cl
2
(2)饱和NaCl B
(3)CaCO+2Cl+HO===2HClO+CaCl+CO↑
3 2 2 2 2
【解析】氯气溶于水,发生反应:Cl+HO===HCl+HClO;生成的HCl与CaCO 发生反应:2HCl+
2 2 3
CaCO===CaCl+CO↑+HO,滴加盐酸产生Cl 发生反应:HCl+HClO===Cl↑+HO。实验三中为了减少
3 2 2 2 2 2 2
Cl 的溶解用饱和NaCl溶液吸收杂质气体,用排液法收集气体,应将导管口插入试管口。
2
学科网(北京)股份有限公司学科网(北京)股份有限公司