文档内容
第二章 海水中的重要元素—钠和氯
第二节 氯及其化合物 课时作业
第二课时 氯气的实验室制法
基础达标
1.实验室制取Cl 时,能用于干燥Cl 的试剂是( )
2 2
A.碱石灰 B.浓硫酸 C.固体烧碱 D.生石灰
2.下列说法中正确的是( )
A.用鼻子对着盛有氯气的瓶口,就可以嗅到氯气的气味
B.用向下排空气法可以收集到纯净的氯气
C.贮氯罐意外泄漏,应沿逆风方向疏散群众
D.氯气车间液氯泄漏时,应弯腰逃离氯气泄漏区域
3.实验室用浓盐酸和MnO 制取Cl 下列说法中错误的是( )
2 2
A.可以用浓硫酸干燥Cl B.可以用排饱和食盐水法收集Cl
2 2
C.该反应需要加热 D.用NaOH溶液除去Cl 中混有的HCl
2
4.如图是实验室制备氯气的发生装置,其中装置名称不正确的是( )
A.长颈漏斗 B.铁架台 C.圆底烧瓶 D.酒精灯
5.实验室用下列两种方法制取氯气:①用含292gHCl的浓盐酸与足量的MnO 反应;
2
②用174gMnO 与足量浓盐酸反应。若不考虑HCl的挥发,则反应后所得氯气的质量(
2
)
A.方法①比方法②多 B.方法②比方法①多
C.两种方法一样多 D.无法比较
6.在实验室可利用浓盐酸与二氧化锰共热制氯气,制备装置中须安装分液漏斗而不能
使用长颈漏斗,有关原因叙述错误的是( )A.防止氯气通过漏斗扩散到空气中造成污染 B.便于控制加入浓盐酸的量
C.因长颈漏斗加热时容易破裂 D.尽量避免HCl挥发到空气中
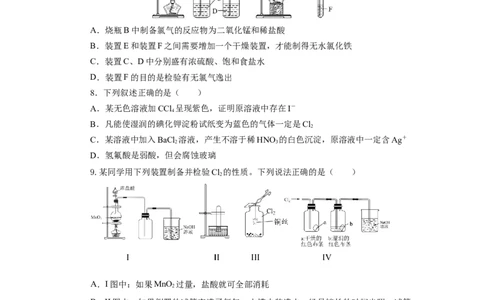
7.利用如图装置可用氯气与金属铁反应制备无水氯化铁,该铁合物呈棕红色、易潮
解,100℃升华。下列有关说法正确的是( )
A.烧瓶B中制备氯气的反应物为二氧化锰和稀盐酸
B.装置E和装置F之间需要增加一个干燥装置,才能制得无水氯化铁
C.装置C、D中分别盛有浓硫酸、饱和食盐水
D.装置F的目的是检验有无氯气逸出
8.下列叙述正确的是( )
A.某无色溶液加CCl 呈现紫色,证明原溶液中存在I-
4
B.凡能使湿润的碘化钾淀粉试纸变为蓝色的气体一定是Cl
2
C.某溶液中加入BaCl 溶液,产生不溶于稀HNO 的白色沉淀,原溶液中一定含Ag+
2 3
D.氢氟酸是弱酸,但会腐蚀玻璃
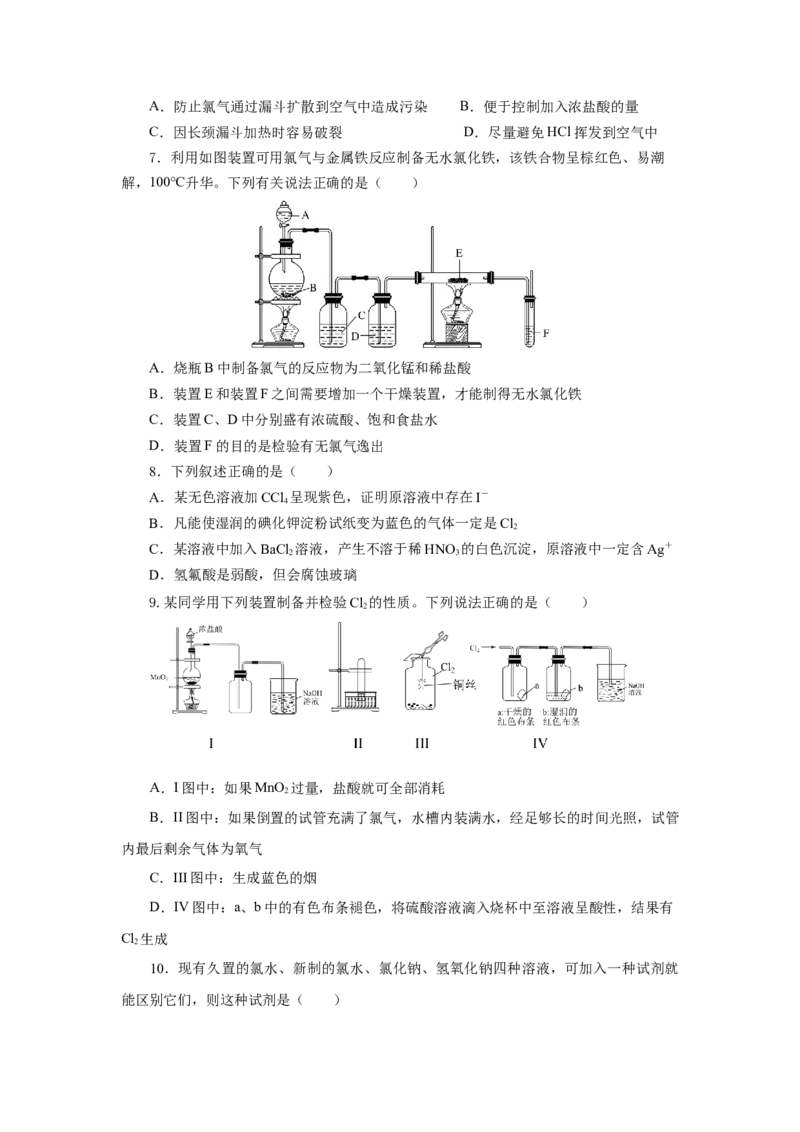
9.某同学用下列装置制备并检验Cl 的性质。下列说法正确的是( )
2
A.I图中:如果MnO 过量,盐酸就可全部消耗
2
B.II图中:如果倒置的试管充满了氯气,水槽内装满水,经足够长的时间光照,试管
内最后剩余气体为氧气
C.III图中:生成蓝色的烟
D.IV图中:a、b中的有色布条褪色,将硫酸溶液滴入烧杯中至溶液呈酸性,结果有
Cl 生成
2
10.现有久置的氯水、新制的氯水、氯化钠、氢氧化钠四种溶液,可加入一种试剂就
能区别它们,则这种试剂是( )A.硝酸银溶液 B.酚酞溶液 C.紫色石蕊溶液 D.饱和食盐水
能力提升
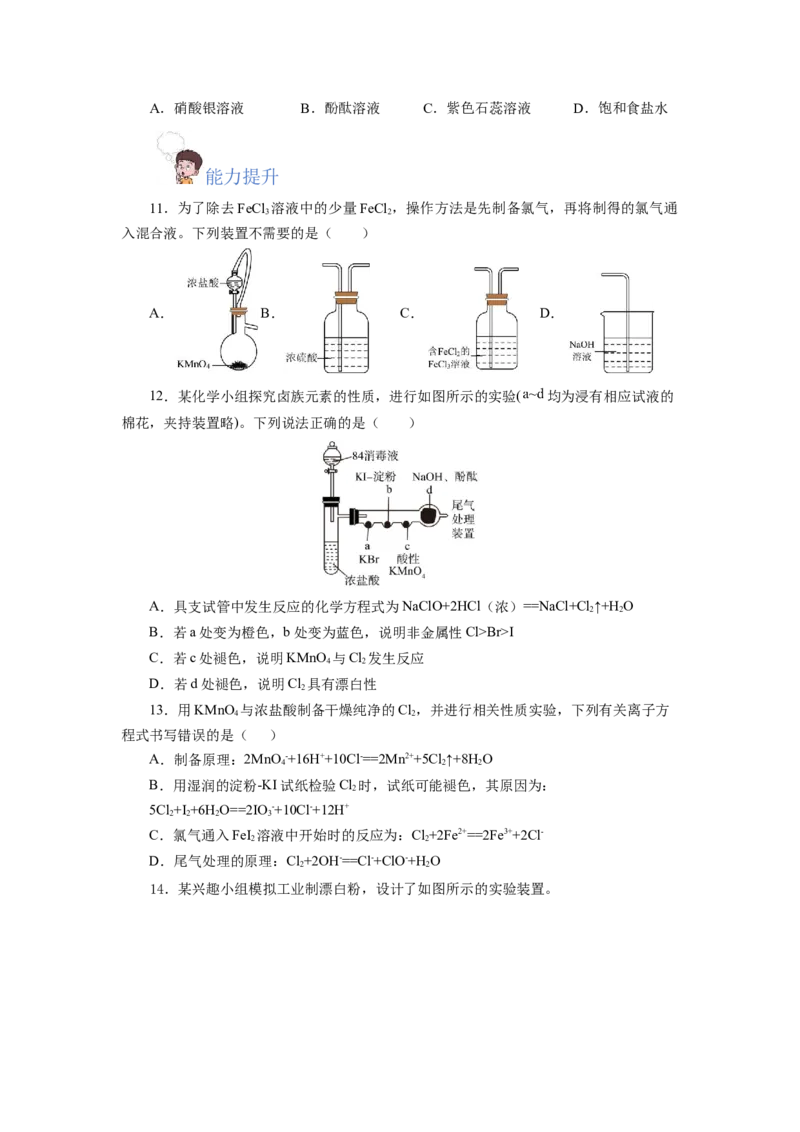
11.为了除去FeCl 溶液中的少量FeCl ,操作方法是先制备氯气,再将制得的氯气通
3 2
入混合液。下列装置不需要的是( )
A. B. C. D.
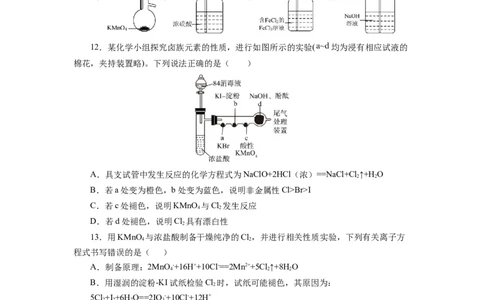
12.某化学小组探究卤族元素的性质,进行如图所示的实验( 均为浸有相应试液的
棉花,夹持装置略)。下列说法正确的是( )
A.具支试管中发生反应的化学方程式为NaClO+2HCl(浓)==NaCl+Cl ↑+H O
2 2
B.若a处变为橙色,b处变为蓝色,说明非金属性Cl>Br>I
C.若c处褪色,说明KMnO 与Cl 发生反应
4 2
D.若d处褪色,说明Cl 具有漂白性
2
13.用KMnO 与浓盐酸制备干燥纯净的Cl,并进行相关性质实验,下列有关离子方
4 2
程式书写错误的是( )
A.制备原理:2MnO -+16H++10Cl-==2Mn2++5Cl↑+8H O
4 2 2
B.用湿润的淀粉-KI试纸检验Cl 时,试纸可能褪色,其原因为:
2
5Cl+I +6H O==2IO -+10Cl-+12H+
2 2 2 3
C.氯气通入FeI 溶液中开始时的反应为:Cl+2Fe2+==2Fe3++2Cl-
2 2
D.尾气处理的原理:Cl+2OH-==Cl-+ClO-+H O
2 2
14.某兴趣小组模拟工业制漂白粉,设计了如图所示的实验装置。已知:①氯气和碱反应放出热量;
②温度高时,6Cl+6Ca(OH) =5CaCl +Ca(ClO)+6H O。
2 2 2 3 2 2
请回答下列问题:
(1)圆底烧瓶内发生反应的离子方程式为_________________________________;装置
乙中饱和食盐水的作用是________________________________。
(2)漂白粉在空气中失效的原因是
_____________________________________________、
_______________________________________________(用化学方程式表示)。
(3)该小组制得的漂白粉中CaCl 的量远大于Ca(ClO) 的量,其主要原因是
2 2
____________;为提高Ca(ClO) 的含量,可采取的措施是
2
_____________________________(任写一种即可)。
直击高考
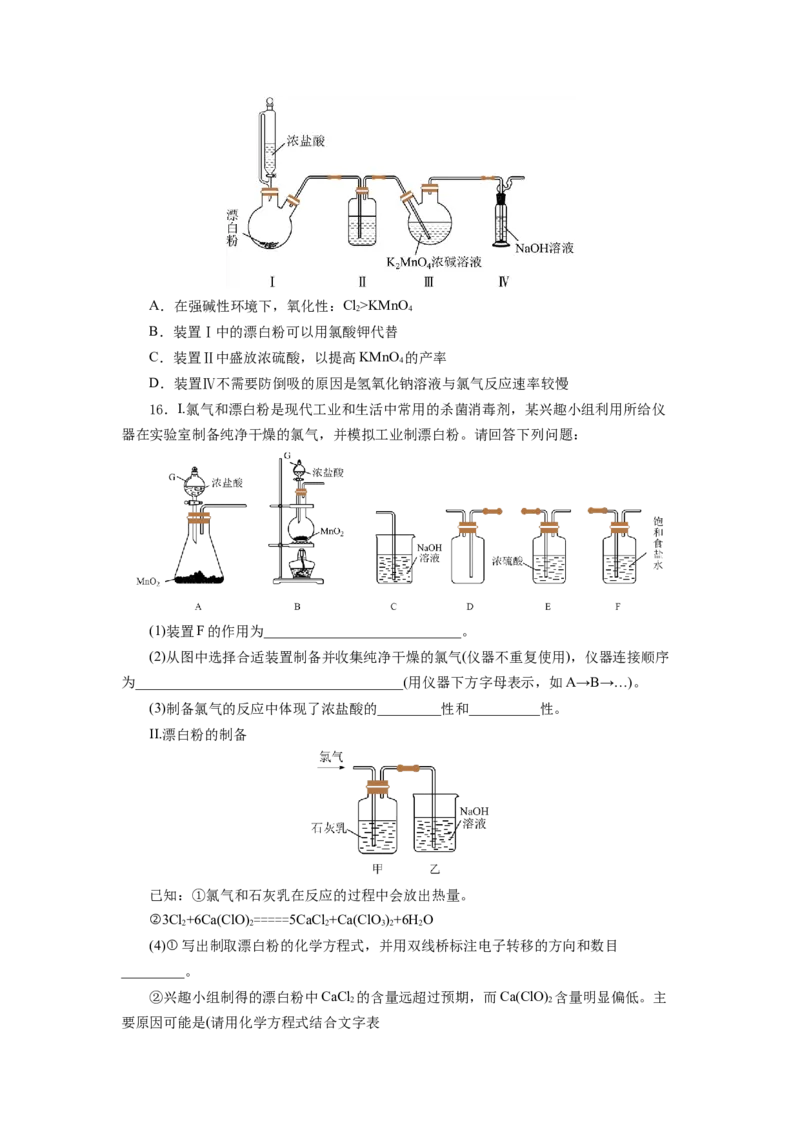
15.锰酸钾(K MnO )在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
2 4
3MnO 2-+2H O==2MnO-+MnO↓+4OH-。利用Cl 氧化KMnO 制备KMnO 的装置如图
4 2 4 2 2 2 4 4
所示(夹持装置略)。下列说法错误的是( )A.在强碱性环境下,氧化性:Cl>KMnO
2 4
B.装置Ⅰ中的漂白粉可以用氯酸钾代替
C.装置Ⅱ中盛放浓硫酸,以提高KMnO 的产率
4
D.装置Ⅳ不需要防倒吸的原因是氢氧化钠溶液与氯气反应速率较慢
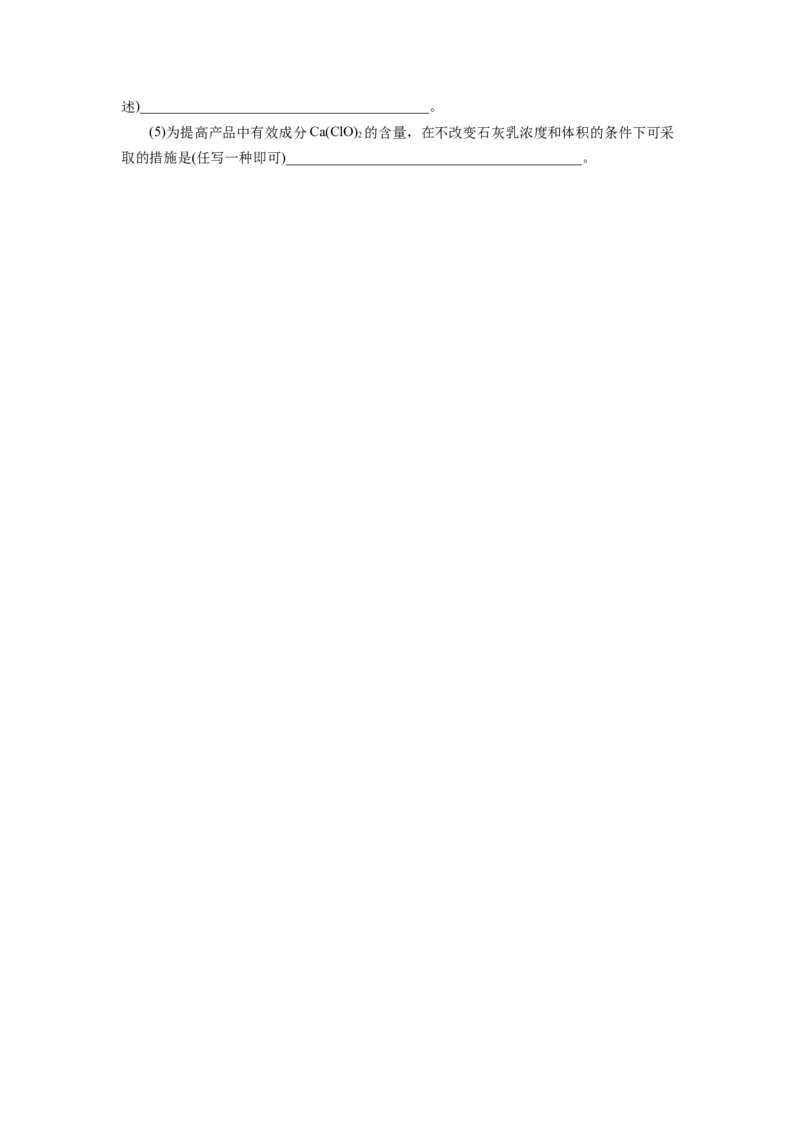
16.I.氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,某兴趣小组利用所给仪
器在实验室制备纯净干燥的氯气,并模拟工业制漂白粉。请回答下列问题:
(1)装置F的作用为____________________________。
(2)从图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用),仪器连接顺序
为______________________________________(用仪器下方字母表示,如A→B→…)。
(3)制备氯气的反应中体现了浓盐酸的_________性和__________性。
II.漂白粉的制备
已知:①氯气和石灰乳在反应的过程中会放出热量。
②3Cl +6Ca(ClO) =====5CaCl +Ca(ClO)+6H O
2 2 2 3 2 2
(4)①写出制取漂白粉的化学方程式,并用双线桥标注电子转移的方向和数目
_________。
②兴趣小组制得的漂白粉中CaCl 的含量远超过预期,而Ca(ClO) 含量明显偏低。主
2 2
要原因可能是(请用化学方程式结合文字表述)_________________________________________。
(5)为提高产品中有效成分Ca(ClO) 的含量,在不改变石灰乳浓度和体积的条件下可采
2
取的措施是(任写一种即可)__________________________________________。