文档内容
化学试题
相对原子质量:H-1 C-12 O-16 S-32
一、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选
项中,只有一项是符合题目要求的。
1. 下列物品中,由金属材料制成的是
A. 纯棉毛巾 B. 铁制剪刀 C. 橡胶导管 D. 陶瓷坩
埚
2. 我国神舟载人飞船供氧系统中含有下列物质,其中属于氧化物的是
A. O B. CO C. NaOH D. NaCO
2 2 2 3
3. 从植物“地不容”中提取抑制新冠病毒的新药—千金藤素,需用到5%的NaCO 溶液。若
2 3
配制100g该溶液,需要称取NaCO 的质量为
2 3
A. 95g B. 90g C. 20g D. 5 g
4. 我国的下列科技新成果,不属于化学研究范畴的是
A. 实现从一氧化碳到蛋白质的人工合成 B. 实现从二氧化碳到淀粉的人工合
成
C. C 与金属铜复合催化低温合成乙二醇 D. 射电望远镜捕获世界最大快速射
60
电暴
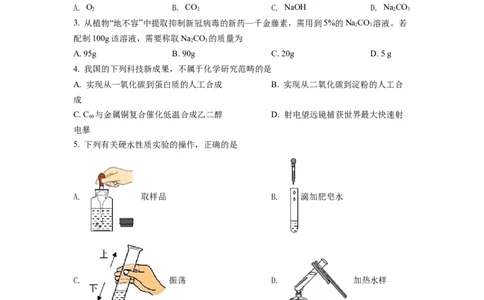
5. 下列有关硬水性质实验的操作,正确的是
A. 取样品 B. 滴加肥皂水
C. 振荡 D. 加热水样
6. “平衡膳食要会看标签。”某品牌巧克力标签如下,“营养素参考值”是指每100g食品中营
养素的含量占该营养素每日推荐摄入量的百分率。下列说法错误的是
营养成分表
项目 每100g 营养素参考值/%
能量 2300kJ 27
蛋白质 6.7g 11脂肪 34.7g 58
碳水化合物 55.7g 19
.
A 食用该巧克力可有效补充能量
B. 食用10g该巧克力可提供蛋白质0.67g
C. 食用50g该巧克力已超过脂肪日推荐摄入量
D. 仅食用该巧克力无法满足均衡营养的需要
7. 某海水淡化系统(如下图)工作时,蒸发腔中的水在光热作用下变为水蒸气,太阳能风扇
将水蒸气吹到冷凝腔冷凝,实现海水淡化。下列说法错误的是
A. 光热作用下,水分子运动速率加快
B. 液态水变为水蒸气,水分子间的间隔变大
C. 水蒸气冷凝为水,水分子本身变小
D. 海水变为淡水,水分子化学性质不变
8. 硫辛酸(C H OS)被称为“万能抗氧化剂”,广泛用于治疗和预防心脏病等多种疾病。下
8 14 2 2
列有关硫辛酸的说法错误的是
A. 属于有机化合物 B. 碳元素质量分数最大
C. 由4种元素组成 D. 含有1个氧分子
9. 我国古代常用灰吹法炼银(如下图),其过程为:将矿物银熔于铅形成银铅块,通过焙烧
使铅氧化成PbO进入炉灰,灰吹得银。下列说法错误的是
A. 银是活泼金属
B. 银铅块属于混合物
C. PbO中Pb的化合价为+2
D. 灰吹法炼银过程含有化学变化
10. 下列实验方案能达到实验目的的是实验目的 实验方案
A 鉴别(NH )SO 和KSO 取样,与熟石灰混合研磨,闻气味
4 2 4 2 4
B 检验二氧化碳是否集满 将燃着的木条伸入集气瓶中
C 除去氮气中的少量氧气 将气体通过灼热 的木炭
D 探究锌、铁、铜的金属活动性顺序 将铜丝、铁丝分别插入硫酸锌溶液中
A. A B. B C. C D. D
二、非选择题:本题共8小题,共70分。
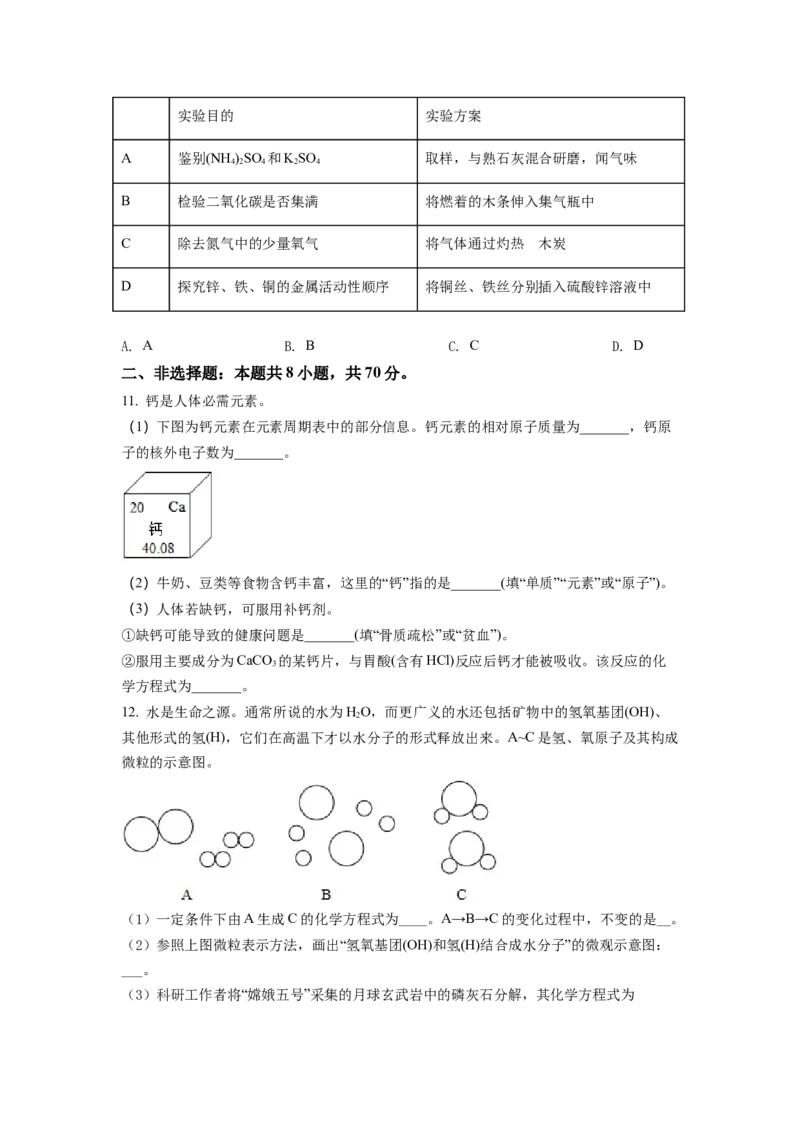
11. 钙是人体必需元素。
(1)下图为钙元素在元素周期表中的部分信息。钙元素的相对原子质量为_______,钙原
子的核外电子数为_______。
(2)牛奶、豆类等食物含钙丰富,这里的“钙”指的是_______(填“单质”“元素”或“原子”)。
(3)人体若缺钙,可服用补钙剂。
①缺钙可能导致的健康问题是_______(填“骨质疏松”或“贫血”)。
②服用主要成分为CaCO 的某钙片,与胃酸(含有HCl)反应后钙才能被吸收。该反应的化
3
学方程式为_______。
12. 水是生命之源。通常所说的水为HO,而更广义的水还包括矿物中的氢氧基团(OH)、
2
其他形式的氢(H),它们在高温下才以水分子的形式释放出来。A~C是氢、氧原子及其构成
微粒的示意图。
(1)一定条件下由A生成C的化学方程式为____。A→B→C的变化过程中,不变的是__。
(2)参照上图微粒表示方法,画出“氢氧基团(OH)和氢(H)结合成水分子”的微观示意图:
___。
(3)科研工作者将“嫦娥五号”采集的月球玄武岩中的磷灰石分解,其化学方程式为。则X的化学式为____。
(4)理论上,通过测量外星球矿样中氢元素的质量,可换算出矿样中水的质量。若1.0g
某矿样含氢的质量为8.0×10-5g,则含水的质量m(HO)=____g
2
13. 兴趣小组用稀盐酸清洗铁夹表面的铁锈(主要成分为氧化铁),并进行保护实验。
(1)除铁锈的反应属于_______(填基本反应类型)。
(2)铁夹在稀盐酸中浸泡较长时间,有气体产生。产生气体的化学方程式为_______。
(3)将清洗过的铁夹进行“发蓝”处理,形成致密的氧化物保护膜,其主要成分与铁在氧气
中燃烧的产物相同,该氧化物的化学式为_______。
(4)验证废液显酸性,可选用的一种试剂或用品是_______。
(5)用氢氧化钠中和废液中的盐酸,反应的化学方程式为_______。
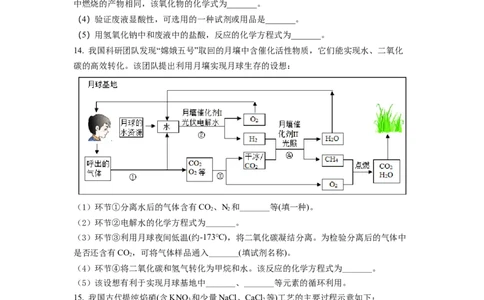
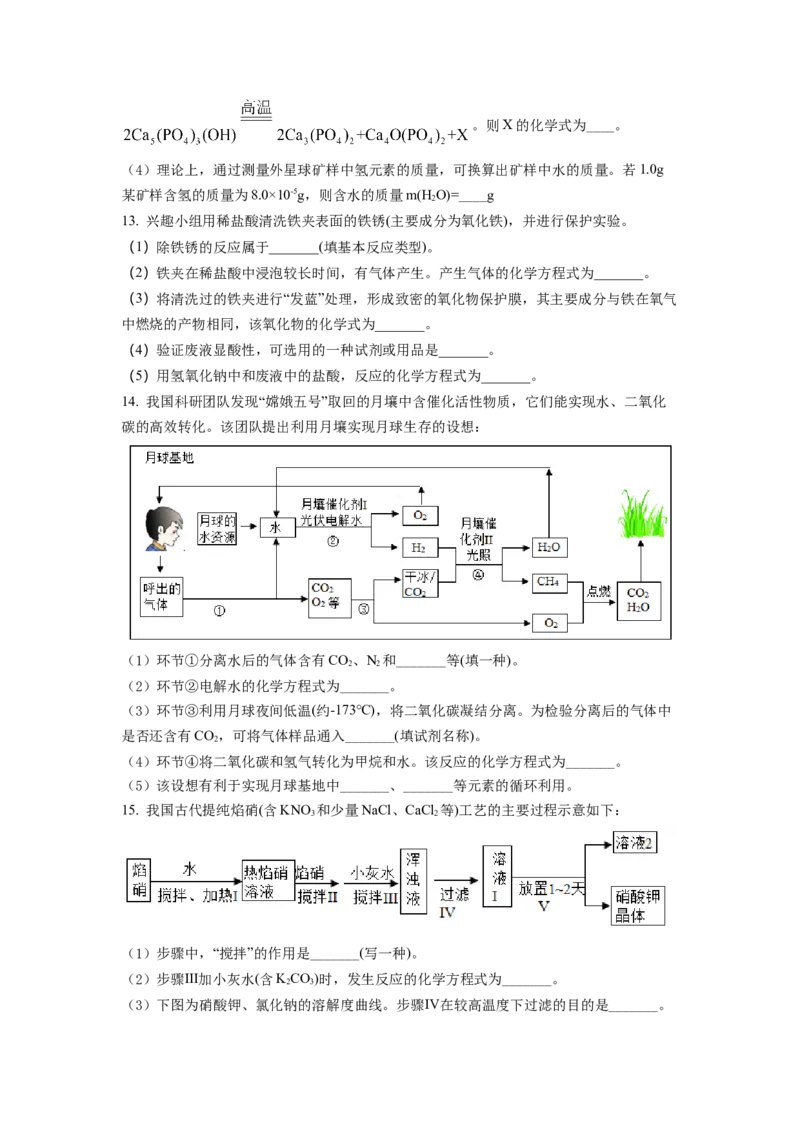
14. 我国科研团队发现“嫦娥五号”取回的月壤中含催化活性物质,它们能实现水、二氧化
碳的高效转化。该团队提出利用月壤实现月球生存的设想:
(1)环节①分离水后的气体含有CO、N 和_______等(填一种)。
2 2
(2)环节②电解水的化学方程式为_______。
(3)环节③利用月球夜间低温(约-173℃),将二氧化碳凝结分离。为检验分离后的气体中
是否还含有CO,可将气体样品通入_______(填试剂名称)。
2
(4)环节④将二氧化碳和氢气转化为甲烷和水。该反应的化学方程式为_______。
(5)该设想有利于实现月球基地中_______、_______等元素的循环利用。
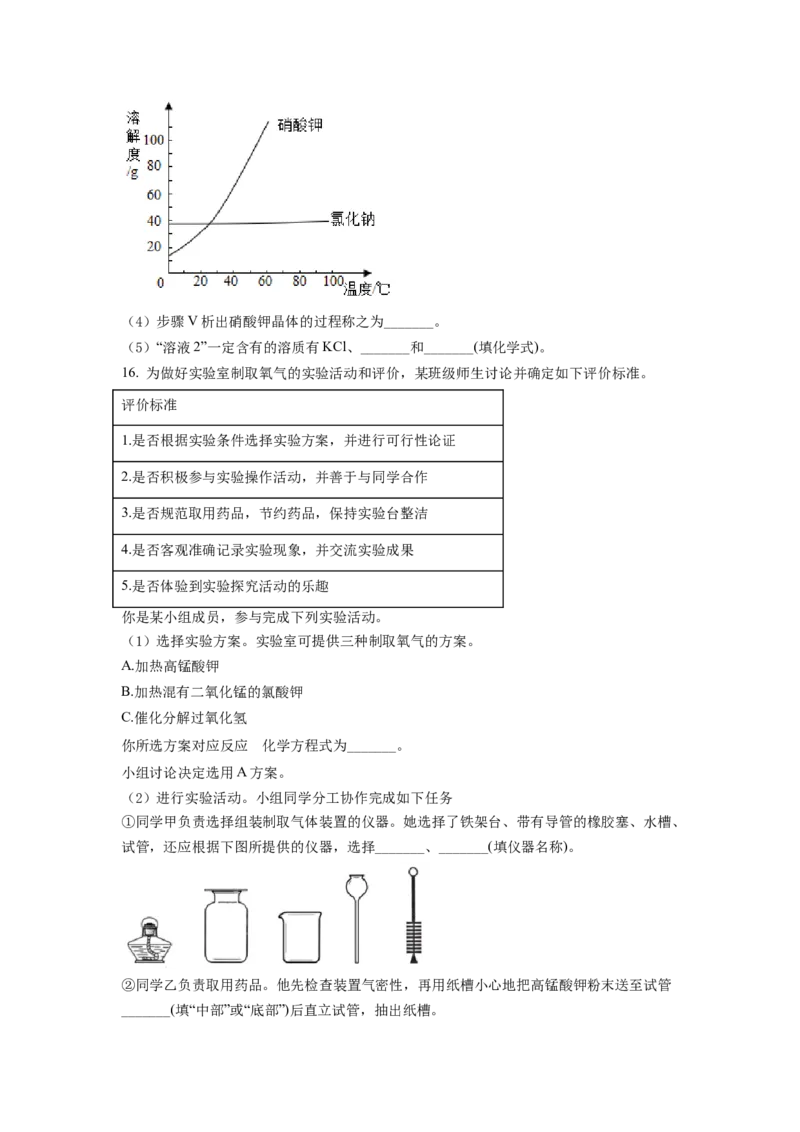
15. 我国古代提纯焰硝(含KNO 和少量NaCl、CaCl 等)工艺的主要过程示意如下:
3 2
(1)步骤中,“搅拌”的作用是_______(写一种)。
(2)步骤Ⅲ加小灰水(含KCO)时,发生反应的化学方程式为_______。
2 3
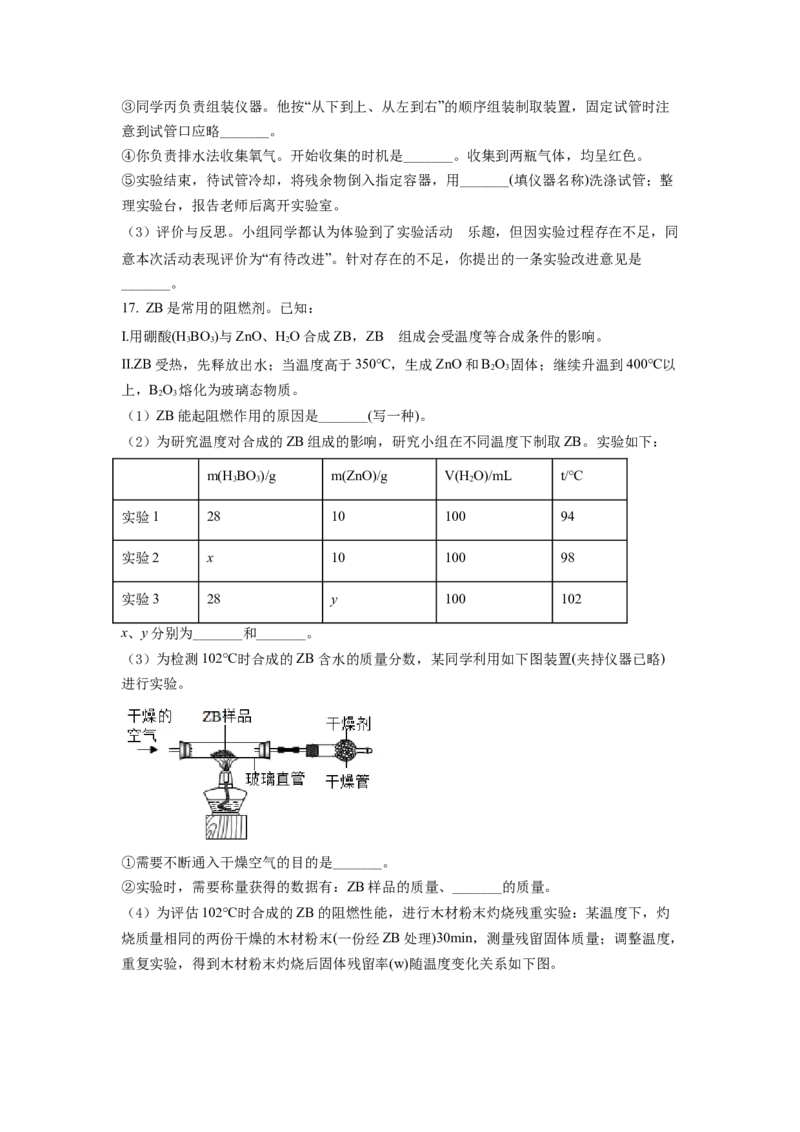
(3)下图为硝酸钾、氯化钠的溶解度曲线。步骤Ⅳ在较高温度下过滤的目的是_______。(4)步骤V析出硝酸钾晶体的过程称之为_______。
(5)“溶液2”一定含有的溶质有KCl、_______和_______(填化学式)。
16. 为做好实验室制取氧气的实验活动和评价,某班级师生讨论并确定如下评价标准。
评价标准
1.是否根据实验条件选择实验方案,并进行可行性论证
2.是否积极参与实验操作活动,并善于与同学合作
3.是否规范取用药品,节约药品,保持实验台整洁
4.是否客观准确记录实验现象,并交流实验成果
5.是否体验到实验探究活动的乐趣
你是某小组成员,参与完成下列实验活动。
(1)选择实验方案。实验室可提供三种制取氧气的方案。
A.加热高锰酸钾
B.加热混有二氧化锰的氯酸钾
C.催化分解过氧化氢
你所选方案对应反应 化的学方程式为_______。
小组讨论决定选用A方案。
(2)进行实验活动。小组同学分工协作完成如下任务
①同学甲负责选择组装制取气体装置的仪器。她选择了铁架台、带有导管的橡胶塞、水槽、
试管,还应根据下图所提供的仪器,选择_______、_______(填仪器名称)。
②同学乙负责取用药品。他先检查装置气密性,再用纸槽小心地把高锰酸钾粉末送至试管
_______(填“中部”或“底部”)后直立试管,抽出纸槽。③同学丙负责组装仪器。他按“从下到上、从左到右”的顺序组装制取装置,固定试管时注
意到试管口应略_______。
④你负责排水法收集氧气。开始收集的时机是_______。收集到两瓶气体,均呈红色。
⑤实验结束,待试管冷却,将残余物倒入指定容器,用_______(填仪器名称)洗涤试管;整
理实验台,报告老师后离开实验室。
(3)评价与反思。小组同学都认为体验到了实验活动 乐的趣,但因实验过程存在不足,同
意本次活动表现评价为“有待改进”。针对存在的不足,你提出的一条实验改进意见是
_______。
17. ZB是常用的阻燃剂。已知:
I.用硼酸(H BO)与ZnO、HO合成ZB,ZB 的组成会受温度等合成条件的影响。
3 3 2
Ⅱ.ZB受热,先释放出水;当温度高于350℃,生成ZnO和B O 固体;继续升温到400℃以
2 3
上,B O 熔化为玻璃态物质。
2 3
(1)ZB能起阻燃作用的原因是_______(写一种)。
(2)为研究温度对合成的ZB组成的影响,研究小组在不同温度下制取ZB。实验如下:
m(HBO)/g m(ZnO)/g V(H O)/mL t/℃
3 3 2
实验1 28 10 100 94
实验2 x 10 100 98
实验3 28 y 100 102
x、y分别为_______和_______。
(3)为检测102℃时合成的ZB含水的质量分数,某同学利用如下图装置(夹持仪器已略)
进行实验。
①需要不断通入干燥空气的目的是_______。
②实验时,需要称量获得的数据有:ZB样品的质量、_______的质量。
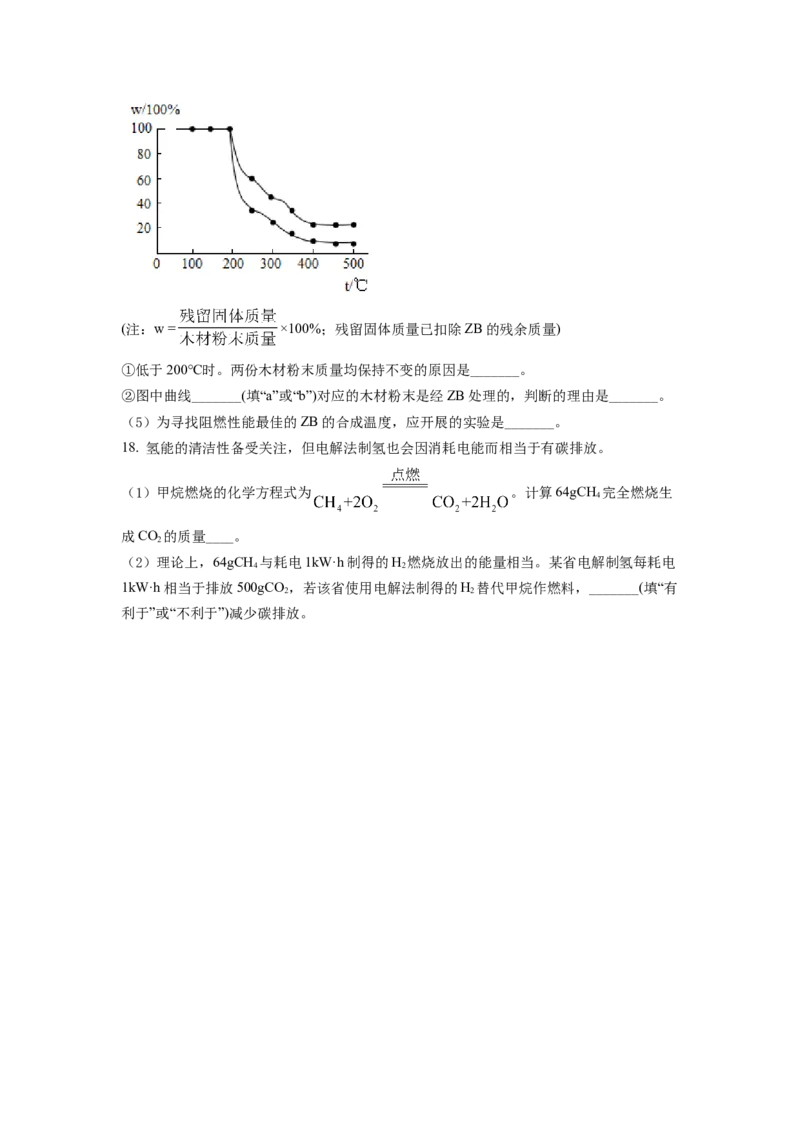
(4)为评估102℃时合成的ZB的阻燃性能,进行木材粉末灼烧残重实验:某温度下,灼
烧质量相同的两份干燥的木材粉末(一份经ZB处理)30min,测量残留固体质量;调整温度,
重复实验,得到木材粉末灼烧后固体残留率(w)随温度变化关系如下图。(注:w = ×100%;残留固体质量已扣除ZB的残余质量)
①低于200℃时。两份木材粉末质量均保持不变的原因是_______。
②图中曲线_______(填“a”或“b”)对应的木材粉末是经ZB处理的,判断的理由是_______。
(5)为寻找阻燃性能最佳的ZB的合成温度,应开展的实验是_______。
18. 氢能的清洁性备受关注,但电解法制氢也会因消耗电能而相当于有碳排放。
(1)甲烷燃烧的化学方程式为 。计算64gCH 完全燃烧生
4
成CO 的质量____。
2
(2)理论上,64gCH 与耗电1kW·h制得的H 燃烧放出的能量相当。某省电解制氢每耗电
4 2
1kW·h相当于排放500gCO,若该省使用电解法制得的H 替代甲烷作燃料,_______(填“有
2 2
利于”或“不利于”)减少碳排放。