AI精准分割子宫内膜癌MRI肿瘤:媲美专家水平,助力精准诊疗新突破
近日,一项发表于Scientific Reports的研究,利用3D卷积神经网络(3D CNN) 实现子宫内膜癌MRI肿瘤全自动分割,其精度与一致性达到人类专家水平,为子宫内膜癌术前风险分层、个性化治疗提供了强有力的技术支撑。
一、研究背景:临床痛点与技术需求
-
疾病现状子宫内膜癌多数早期患者可通过手术治愈,但约15%会出现复发,预后极差;术前MRI是评估肿瘤局部侵犯的核心手段,肿瘤体积、纹理特征是预测高危疾病与生存期的重要指标。
-
临床痛点人工全容积肿瘤分割工作量极大,无法在日常临床中常规开展,亟需自动化、高精度的分割工具替代人工。
-
技术趋势深度学习与CNN在医学影像领域应用广泛,3D MRI成像更适合癌症术前规划,基于3D CNN的肿瘤自动分割成为研究热点。
二、研究核心内容:AI分割结果与专家高度一致
本研究纳入139例子宫内膜癌患者术前盆腔MRI数据,采用3D U-Net模型完成肿瘤自动分割,通过多维度指标验证AI性能,核心结果通过图表直观呈现:
1. Figure 1:3D肿瘤分割可视化对比
-
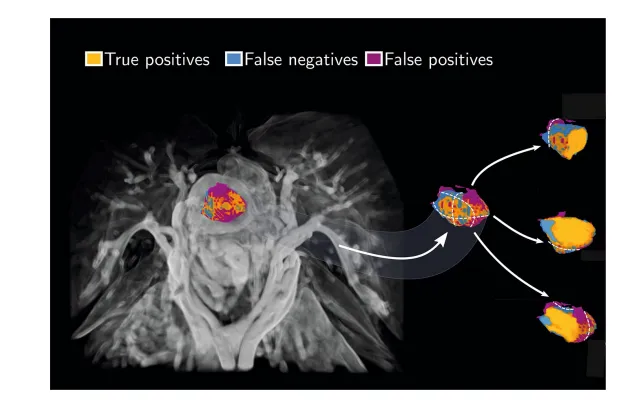
左侧:AI分割与人工分割的3D体积渲染,橙色为真阳性(一致区域),蓝色为假阴性、紫色为假阳性(差异区域); -
右侧:3组轴位MRI切片+肿瘤局部放大,清晰展示AI与人工分割轮廓; -
关键发现:AI分割误差主要集中在肿瘤边缘,核心肿瘤区域识别高度精准。
2. Figure 2:2D肿瘤轮廓分割一致性
-
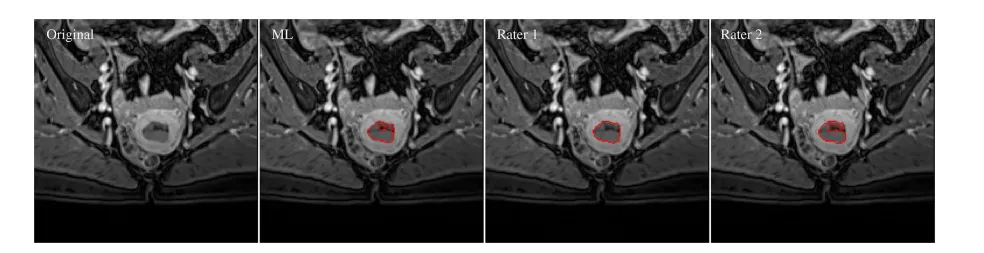
红色实线为AI、专家1、专家2的肿瘤分割轮廓,叠加在MRI VIBE序列图像上; -
量化结果:DSC_ML,R1=0.96、DSC_ML,R2=0.89、DSC_R1,R2=0.90,AI与专家轮廓重合度极高。
3. Figure 3:肿瘤体积测量无显著差异
-
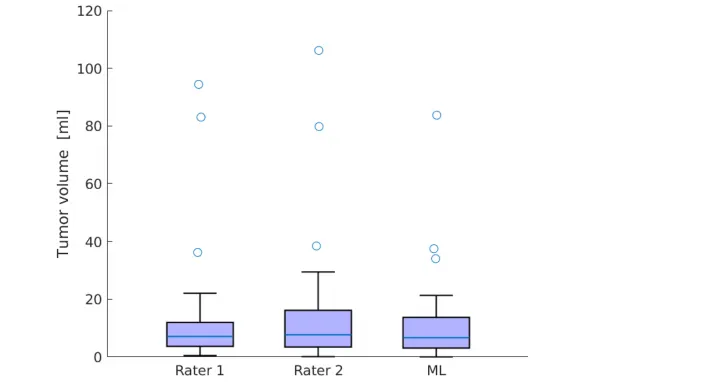
箱线图展示专家1、专家2、AI测量的肿瘤体积分布; -
统计结果:Friedman检验p=0.28,三者中位肿瘤体积无统计学差异,AI体积测量无明显偏差。
4. Figure 4:Bland-Altman分析:体积一致性卓越
-
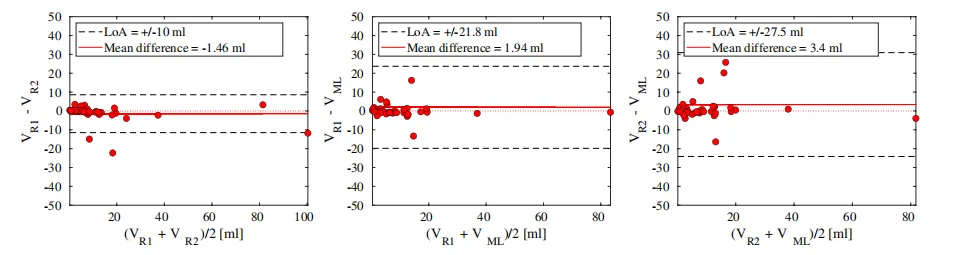
左图:专家1 vs 专家2,95%一致性界限±10ml,偏倚-1.46ml; -
中图:专家1 vs AI,95%一致性界限±21.8ml,偏倚1.94ml; -
右图:专家2 vs AI,95%一致性界限±27.5ml,偏倚3.4ml; -
关键结论:AI与专家的肿瘤体积测量一致性极高,组内相关系数(ICC)无显著差异。
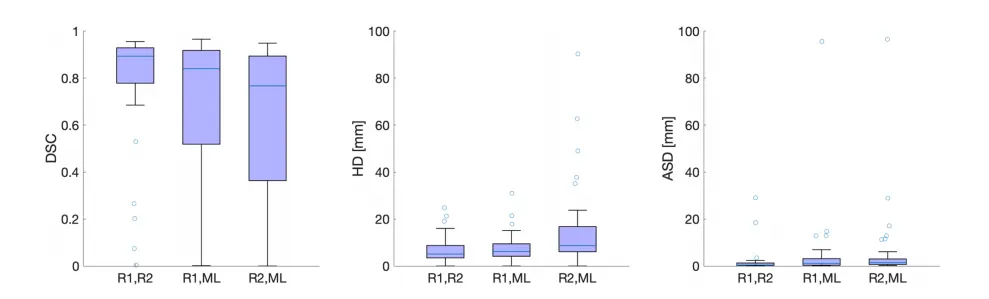
5. Figure 5 + Table 1:分割精度多指标验证
-
DSC(戴斯相似系数):专家间中位0.89,AI与专家1为0.84,无显著差异(p=0.08); -
HD(豪斯多夫距离):专家间中位5.15mm,AI与专家1为6.39mm,无显著差异(p=0.60); -
ASD(平均表面距离):专家间中位0.42mm,AI与专家1为1.08mm,无显著差异(p=0.05); -
亚型分析:子宫内膜样癌分割效果最优,非子宫内膜样癌因样本量小,差异无统计学意义。
三、实验及分析方法流程总结
-
研究对象139例经病理确诊的子宫内膜癌患者,2009-2019年于挪威霍克兰大学医院行术前盆腔MRI,分为训练集84例、验证集21例、测试集34例。
-
MRI数据采集使用1.5T/3T西门子扫描仪,采用T1-VIBE脂肪抑制序列,统一参数扫描,DICOM格式转换为NIfTI格式。
-
人工分割标准两位盆腔影像经验丰富的放射科专家独立完成肿瘤3D分割,互盲操作,结果作为金标准。
-
AI模型构建基于3D U-Net架构,Keras+TensorFlow框架,加入旋转、缩放、水平翻转等数据增强,输入尺寸(192,192,32)体素,RMSprop优化器训练,早停法防止过拟合。
-
评价指标
-
体积一致性:Friedman检验、Bland-Altman、ICC; -
分割精度:DSC、HD、ASD; -
统计学检验:Wilcoxon符号秩检验,显著性水平α=0.05。
四、研究结论与展望
核心结论
-
3D CNN可实现子宫内膜癌MRI肿瘤全自动分割,肿瘤体积测量、轮廓分割精度达到人类专家水平; -
AI分割误差仅集中在肿瘤边缘,核心区域识别可靠,可稳定提取肿瘤体积与全容积纹理特征; -
该工具可替代人工分割,实现实时全容积放射组学分析,助力术前风险分层与个性化治疗。
未来展望
-
扩大样本量,开展多中心、前瞻性研究,纳入不同设备、不同人群数据,提升模型泛化性; -
结合半监督、弱监督学习,减少人工标注工作量,进一步提升分割精度; -
推进临床转化,将AI分割工具整合到MRI诊断流程,实现子宫内膜癌精准诊疗落地。
论文基础信息
-
DOI:10.1038/s41598-020-80068-9 -
发表期刊:Scientific Reports(Nature旗下) -
发表单位:挪威NORCE研究中心、霍克兰大学医院、卑尔根大学、美国梅奥诊所等
 夜雨聆风
夜雨聆风




