文档内容
专练 40 化学平衡的移动及影响因素
授课提示:对应学生用书79页
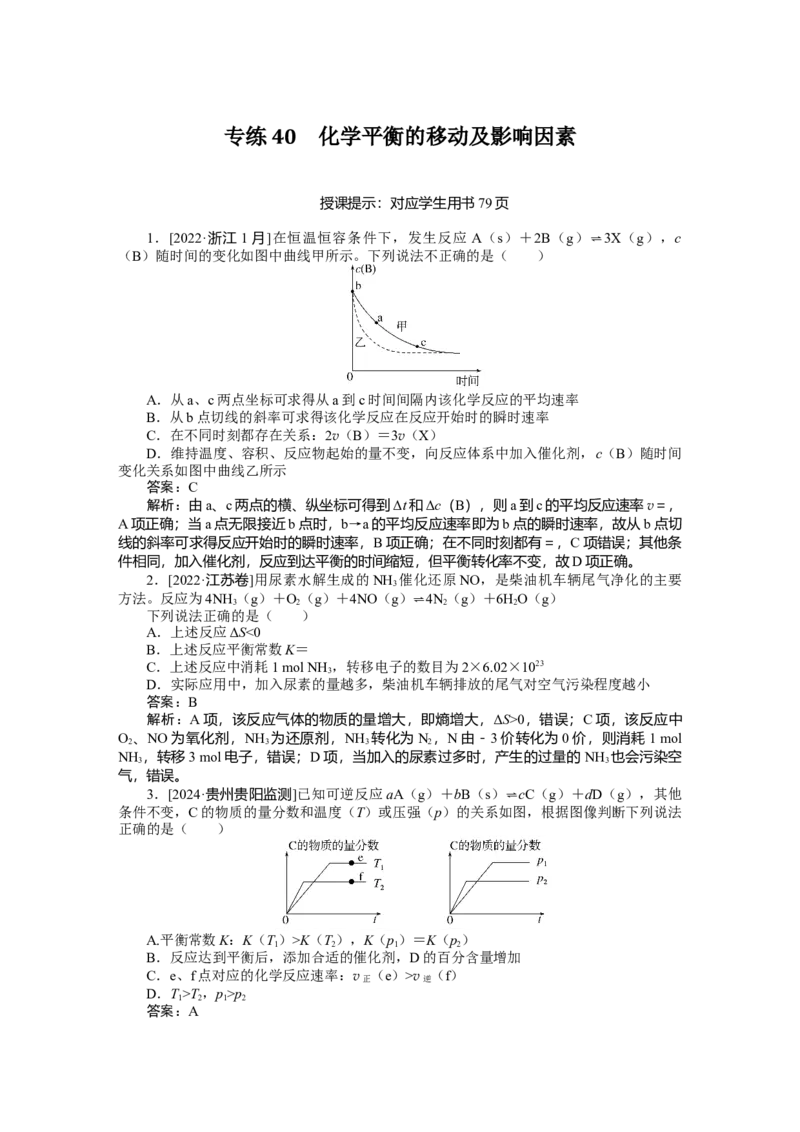
1.[2022·浙江1月]在恒温恒容条件下,发生反应 A(s)+2B(g) ⇌3X(g),c
(B)随时间的变化如图中曲线甲所示。下列说法不正确的是( )
A.从a、c两点坐标可求得从a到c时间间隔内该化学反应的平均速率
B.从b点切线的斜率可求得该化学反应在反应开始时的瞬时速率
C.在不同时刻都存在关系:2v(B)=3v(X)
D.维持温度、容积、反应物起始的量不变,向反应体系中加入催化剂,c(B)随时间
变化关系如图中曲线乙所示
答案:C
解析:由a、c两点的横、纵坐标可得到Δt和Δc(B),则a到c的平均反应速率v=,
A项正确;当a点无限接近b点时,b→a的平均反应速率即为b点的瞬时速率,故从b点切
线的斜率可求得反应开始时的瞬时速率,B项正确;在不同时刻都有=,C项错误;其他条
件相同,加入催化剂,反应到达平衡的时间缩短,但平衡转化率不变,故D项正确。
2.[2022·江苏卷]用尿素水解生成的NH 催化还原NO,是柴油机车辆尾气净化的主要
3
方法。反应为4NH
3
(g)+O
2
(g)+4NO(g) ⇌4N
2
(g)+6H
2
O(g)
下列说法正确的是( )
A.上述反应ΔS<0
B.上述反应平衡常数K=
C.上述反应中消耗1 mol NH ,转移电子的数目为2×6.02×1023
3
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
答案:B
解析:A项,该反应气体的物质的量增大,即熵增大,ΔS>0,错误;C项,该反应中
O 、NO为氧化剂,NH 为还原剂,NH 转化为N ,N由-3价转化为0价,则消耗1 mol
2 3 3 2
NH ,转移3 mol电子,错误;D项,当加入的尿素过多时,产生的过量的NH 也会污染空
3 3
气,错误。
3.[2024·贵州贵阳监测]已知可逆反应aA(g)+bB(s) ⇌cC(g)+dD(g),其他
条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图,根据图像判断下列说法
正确的是( )
A.平衡常数K:K(T)>K(T),K(p)=K(p)
1 2 1 2
B.反应达到平衡后,添加合适的催化剂,D的百分含量增加
C.e、f点对应的化学反应速率:v正 (e)>v逆 (f)
D.T>T,p>p
1 2 1 2
答案:A解析:根据“先拐先平数值大”,知T>T ,T→T ,温度降低,C的物质的量分数增
2 1 2 1
大,平衡向正反应方向移动,平衡常数增大,故K(T )>K(T ),由于平衡常数只与温度
1 2
有关,故K(p )=K(p ),A项正确;反应达到平衡后,添加合适的催化剂,平衡不移
1 2
动,D的百分含量不变,B项错误;e点对应温度小于 f点对应温度,故 v (e)T,p>p,D项错误。
2 1 2 1
4.[角度创新]一定温度下,在一密闭容器中发生反应:2SO
2
(g)+O
2
(g) ⇌2SO
3
(g),c(SO )随时间(t)变化如图所示。
2
400 ℃时压强对SO 的转化率的影响如表。
2
压强 0.1 MPa 0.5 MPa 1 MPa 10 MPa
SO 的转化率 99.2% 99.6% 99.7% 99.9%
2
下列说法正确的是( )
A.a点的v逆 大于b点的v逆
B.t 时刻改变的条件一定是增大c(SO )
2 2
C.化学平衡常数d点与e点相等
D.硫酸工业中,SO 催化氧化制SO 时采用高压提高生产效益
2 3
答案:C
解析:a点时反应向正反应方向进行,b点时反应达到平衡状态,从a点到b点,正反
应速率逐渐减小,逆反应速率逐渐增大,故a点的v 小于b点的v ,A项错误;t 时c
逆 逆 2
(SO )突然增大,随后逐渐减小,说明平衡向正反应方向移动,故t 时刻改变的条件可以
2 2
是增大c(SO ),还可以是增大压强,B项错误;化学平衡常数只与温度有关,反应温度
2
不变,平衡常数不变,因此d点和e点的化学平衡常数相等,C项正确;根据表中提供的数
据可知,增大压强对SO 的转化率影响不大,但增大压强对工业设备要求高,同时生产成本
2
增大,因此硫酸工业中,SO 催化氧化制SO 时采用高压不能提高生产效益,D项错误。
2 3
5.[2024·广州市综合测试]反应R(g) ⇌P(g)在有水和无水条件下,反应历程如图。
图中M表示中间产物,TS表示过渡态。其他条件相同时,下列说法正确的是( )
A.在有水条件下,反应更快达到平衡
B.有水和无水时,反应分别分3步和2步进行
C.反应达到平衡时,升高温度,P的浓度增大
D.无水条件下R的平衡转化率比有水条件下大
答案:A
解析:在有水条件下,反应的活化能低,反应速率快,反应更快达到平衡,A项正确;
有水和无水时,均只有1种中间产物,反应均分2步进行,B项错误;R(g)⇌P(g)为放
热反应,反应达到平衡时,升高温度,平衡逆向移动,P的浓度减小,C项错误;水为该反
应的催化剂,催化剂不影响平衡移动,故R的平衡转化率不变,D项错误。
6.[2024·云南玉溪通海二中高三月考]在某一恒温体积可变的密闭容器中发生如下反应:
A(g)+B(g) ⇌2C(g) ΔH<0。t
1
时刻达到平衡后,在t
2
时刻改变某一条件,其反应
过程如图所示。下列说法正确的是( )A.0~t
2
时间段内,v正 >v逆
B.Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ
C.t 时刻改变的条件可能是向密闭容器中加C
2
D.Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ<Ⅱ
答案:C
解析:0~t 时,反应正向进行,v >v ,t~t 时,反应达到平衡,v =v ,A错误;
1 正 逆 1 2 正 逆
t 时刻改变条件后达到平衡时,逆反应速率不变,说明和原平衡等效,A的体积分数Ⅰ=Ⅱ,
2
B错误;向密闭容器中加C,逆反应速率瞬间增大,再次建立的平衡与原平衡等效,说明和
原平衡相同,符合图形,C正确;由于温度不变,所以Ⅰ、Ⅱ两过程达到平衡时,平衡常数
相等,D错误。
7.下列对化学平衡移动的分析中,不正确的是( )
①有气体参加的反应达到平衡时,若减小反应容器容积,平衡向气体体积增大的方向移
动
②有气体参加的反应达到平衡时,在恒压反应容器中充入稀有气体,平衡不会发生移动
③已达到平衡的反应C(s)+H
2
O(g) ⇌CO(g)+H
2
(g),当增加反应物物质的量
时,平衡一定向正反应方向移动
④已达到平衡的反应N
2
(g)+3H
2
(g) ⇌2NH
3
(g),当增大N
2
的浓度时,平衡向正
反应方向移动,H 的转化率一定升高
2
A.①④ B.①②③
C.②③④ D.①②③④
答案:B
解析:有气体参加的反应达到平衡时,若减小反应容器容积,相当于增大压强,则平衡
向气体体积减小的方向移动,故①错误;有气体参加的反应达到平衡时,在恒压反应容器中
充入稀有气体,则容器的容积增大,相当于减小压强,平衡向气体体积增大的方向移动,故
②错误;已达到平衡的反应C(s)+H
2
O(g)⇌CO(g)+H
2
(g),C为固体,当增加反
应物碳的物质的量时,平衡不移动,故③错误;已达到平衡的反应N (g)+3H (g)
2 2
⇌2NH
3
(g),当增大N
2
的浓度时,平衡向正反应方向移动,H
2
的转化率一定升高,故④
正确。故选B。
8.[2024·江西赣县三中月考]温度为T℃时,在容积为2 L的恒容密闭容器中发生反应:
1
2NO(g)+O
2
(g) ⇌2NO
2
(g) ΔH<0。实验测得:v正 =v消耗 (NO)=2v消耗 (O
2
)=k
正
·c2(NO)·c(O
2
),v逆 =v消耗 (NO
2
)=k
逆
·c2(NO
2
),k
正
、k
逆
为速率常数,受温度影
响。不同时刻测得容器中n(NO)、n(O)如表:
2
时间/s 0 1 2 3 4 5
n(NO)/mol 0.20 0.10 0.08 0.065 0.06 0.06
n(O)/mol 0.10 0.05 0.04 0.032 5 0.03 0.03
2
下列说法正确的是( )
A.0~2 s内,该反应的平均速率v(NO)=0.03 mol·L-1·s-1
B.其他条件不变,往原容器中再通入0.20 mol NO和0.10 mol O ,则达到新的平衡时
2
NO 体积分数减小
2
C.其他条件不变,移走部分NO ,则平衡正向移动,平衡常数增大
2
D.当温度改变为T℃时,若k =k ,则T<T
2 正 逆 2 1
答案:A
解析:根据表格数据可知:在0~2 s内,Δn(NO)=0.20 mol-0.08 mol=0.12 mol,
则该反应的平均速率v(NO)==0.03 mol·L-1·s-1,A项正确;其他条件不变,往该恒容密
闭容器中再通入0.20 mol NO和0.10 mol O ,相当于增大体系的压强,由于正反应是气体体
2
积减小的反应,增大压强,平衡正向移动,达到新的平衡时NO 体积分数增大,B项错误;
2温度不变,化学平衡常数不变,C项错误;k 、k 为速率常数,受温度影响,温度为T℃
正 逆 1
时,列三段式:
2NO(g)+O
2
(g)⇌2NO
2
(g)
0.1 0.05 0
0.07 0.035 0.07
0.03 0.015 0.07
化学平衡常数K==≈363>1,此时v =v ,即=K,说明k >k ,若k =k ,则
正 逆 正 逆 正 逆
K减小,平衡逆向移动,由于正反应为放热反应,则改变条件是升高温度,所以T >T ,D
2 1
项错误。
9.已知:A(g)+2B(g) ⇌3C(g) ΔH<0,向一恒温恒容的密闭容器中充入1 mol
A和3 mol B发生反应,t 时达到平衡状态Ⅰ,在t 时改变某一条件,t 时重新达到平衡状态
1 2 3
Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是( )
A.容器内压强不变,表明反应达到平衡
B.t 时改变的条件:向容器中加入C
2
C.平衡时A的体积分数φ:φ(Ⅱ)<φ(Ⅰ)
D.平衡常数K:K(Ⅱ)φ(Ⅰ),C错误;化学平衡常数只与温度有关,温度
不变,平衡常数不变,即K(Ⅱ)=K(Ⅰ),D错误。
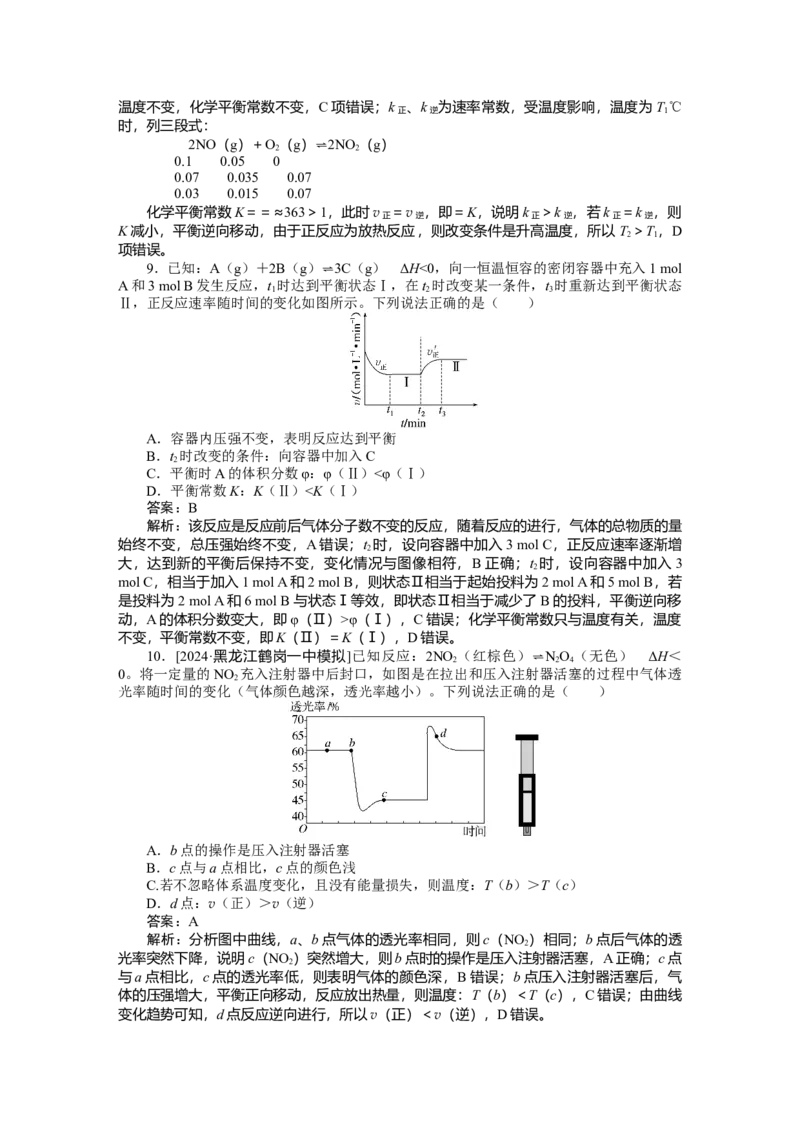
10.[2024·黑龙江鹤岗一中模拟]已知反应:2NO
2
(红棕色) ⇌N
2
O
4
(无色) ΔH<
0。将一定量的NO 充入注射器中后封口,如图是在拉出和压入注射器活塞的过程中气体透
2
光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是( )
A.b点的操作是压入注射器活塞
B.c点与a点相比,c点的颜色浅
C.若不忽略体系温度变化,且没有能量损失,则温度:T(b)>T(c)
D.d点:v(正)>v(逆)
答案:A
解析:分析图中曲线,a、b点气体的透光率相同,则c(NO )相同;b点后气体的透
2
光率突然下降,说明c(NO )突然增大,则b点时的操作是压入注射器活塞,A正确;c点
2
与a点相比,c点的透光率低,则表明气体的颜色深,B错误;b点压入注射器活塞后,气
体的压强增大,平衡正向移动,反应放出热量,则温度:T(b)<T(c),C错误;由曲线
变化趋势可知,d点反应逆向进行,所以v(正)<v(逆),D错误。