文档内容
专练 61 物质的制备与性质实验
授课提示:对应学生用书121页
一、选择题
1.
[2024·全国甲卷]四瓶无色溶液NH NO 、NaCO 、Ba(OH) 、AlCl ,它们之间的反
4 3 2 3 2 3
应关系如图所示。其中a、b、c、d代表四种溶液,e和g为无色气体,f为白色沉淀。下列
叙述正确的是( )
A.a呈弱碱性
B.f可溶于过量的b中
C.c中通入过量的e可得到无色溶液
D.b和d反应生成的沉淀不溶于稀硝酸
答案:B
解析:由分析知,a为NH NO ,NH水解使溶液呈酸性,A错误;Al(OH) 可与强
4 3 3
碱反应生成四羟基合铝酸根离子,故可溶于过量的Ba(OH) 中,B正确;AlCl 与过量的
2 3
NH 反应生成Al(OH) 白色沉淀,C错误;Ba(OH) 和NaCO 反应生成BaCO ,
3 3 2 2 3 3
BaCO 可以溶于稀硝酸生成二氧化碳和Ba(NO ),D错误。
3 3 2
2.[2024·安徽卷]仅用下表提供的试剂和用品,不能实现相应实验目的的是( )
选项 实验目的 试剂 用品
MgCl 溶液、AlCl 溶液、
A 比较镁和铝的金属性强弱 2 3 试管、胶头滴管
氨水
试管、橡胶塞、导管、乳
乙醇、乙酸、浓硫酸、饱 胶管、铁架台(带铁
B 制备乙酸乙酯
和NaCO 溶液 夹)、碎瓷片、酒精灯、
2 3
火柴
制备
C CuSO 溶液、氨水 试管、胶头滴管
[Cu(NH )]SO 溶液 4
3 4 4
烧杯、胶头滴管、石棉
利用盐类水解制备Fe
D 饱和FeCl 溶液、蒸馏水 网、三脚架、酒精灯、火
(OH) 胶体 3
3 柴
答案:A
解析:向MgCl2溶液、AlCl3溶液中分别滴加氨水,均产生白色沉淀,且氨水过量沉
淀不溶解,无法比较Mg(OH)2、Al(OH)3的碱性强弱,即无法比较Mg和Al的金属
性强弱,A项符合题意;乙醇和乙酸在浓硫酸催化、加热条件下发生酯化反应生成乙酸乙
酯和水,饱和Na2CO3溶液可溶解乙醇、吸收乙酸、降低乙酸乙酯的溶解度,实验用品正
确,B项不符合题意;向硫酸铜溶液中逐滴加入氨水,先产生蓝色Cu(OH)2沉淀,后沉
淀溶解,得到[Cu(NH3)4]SO4溶液,实验用品正确,C项不符合题意;向沸水中滴加饱和FeCl3溶液,继续煮沸至溶液呈红褐色停止加热,得到氢氧化铁胶体,实验用品正确,
D项不符合题意。
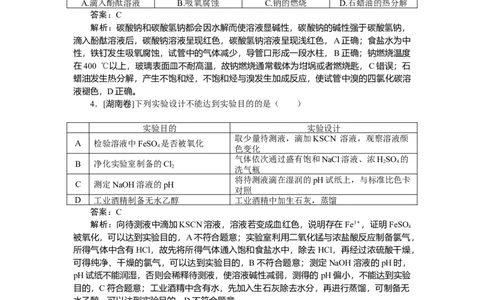
3.[2022·湖北卷]下列实验装置(部分夹持装置略)或现象错误的是( )
A.滴入酚酞溶液 B.吸氧腐蚀 C.钠的燃烧 D.石蜡油的热分解
答案:C
解析:碳酸钠和碳酸氢钠都会因水解而使溶液显碱性,碳酸钠的碱性强于碳酸氢钠,
滴入酚酞溶液后,碳酸钠溶液呈现红色,碳酸氢钠溶液呈现浅红色,A正确;食盐水为中
性,铁钉发生吸氧腐蚀,试管中的气体减少,导管口形成一段水柱,B正确;钠燃烧温度
在400 ℃以上,玻璃表面皿不耐高温,故钠燃烧通常载体为坩埚或者燃烧匙,C错误;石
蜡油发生热分解,产生不饱和烃,不饱和烃与溴发生加成反应,使试管中溴的四氯化碳溶
液褪色,D正确。
4.[湖南卷]下列实验设计不能达到实验目的的是( )
实验目的 实验设计
取少量待测液,滴加KSCN 溶液,观察溶液颜
A 检验溶液中FeSO 是否被氧化
4 色变化
气体依次通过盛有饱和NaCl溶液、浓HSO 的
B 净化实验室制备的Cl 2 4
2 洗气瓶
将待测液滴在湿润的pH试纸上,与标准比色卡
C 测定NaOH溶液的pH
对照
D 工业酒精制备无水乙醇 工业酒精中加生石灰,蒸馏
答案:C
解析:向待测液中滴加KSCN溶液,溶液若变成血红色,说明存在Fe3+,证明FeSO
4
被氧化,可以达到实验目的,A不符合题意;实验室利用二氧化锰与浓盐酸反应制备氯气,
所得气体中含有HCl,故先将所得气体通入饱和食盐水中,除去 HCl,再经过浓硫酸干燥,
可得纯净、干燥的氯气,可以达到实验目的,B不符合题意;测定NaOH溶液的pH时,
pH试纸不能润湿,否则会稀释待测液,使溶液碱性减弱,测得的 pH偏小,不能达到实验
目的,C符合题意;工业酒精中含有水,先加入生石灰除去水分,再进行蒸馏,可制备无
水乙醇,可以达到实验目的,D不符合题意。
5.[2024·衡水中学二调]从某含有FeCl 、FeCl 、CuCl 的工业废液中回收铜并制备氯
2 3 2
化铁晶体的流程如下:
则下列说法正确的是( )
A.试剂a是铁、试剂b是稀硫酸
B.操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同
C.试剂c是氯气,相应的反应为:2Fe2++Cl===2Fe3++2Cl-
2
D.用酸性KMnO 溶液可检验溶液W中是否还有Fe2+
4答案:C
解析:由最终得到FeCl 及其流程图可以知道,b为盐酸,若为硫酸会引入硫酸根杂质
3
离子,故A错误;上述分析可以知道,操作Ⅰ、Ⅱ是过滤,操作Ⅲ是结晶,过滤,所用仪
器不同,故B错误;滤液X,滤液Z中均含有FeCl ,c为氯气氧化亚铁离子为铁离子的反
2
应为: 2Fe2++Cl===2Fe3++2Cl-,故C正确;亚铁离子、氯离子都可以被高锰酸钾溶液
2
氧化,用酸性KMnO 溶液不能检验溶液W中是否还有Fe2+,故D错误。
4
6.[2024·长春实验中学高三开学考试]下列实验中,现象和结论都正确的是( )
实验 现象 结论
将SO 通入BaCl 溶液,然 产生白色沉淀,白色沉淀 所得沉淀为BaSO,后转
A 2 2 3
后滴入稀硝酸 不消失 化为BaSO
4
将浓硫酸滴入含少量水的 得黑色蓬松的固体及刺激 该过程中浓硫酸仅体现吸
B
蔗糖中,并搅拌 性气味气体 水性和脱水性
用黄豆粒大小的金属钠分
C 前者反应更剧烈 羟基的活动性:水>乙醇
别与水、乙醇反应
向10 mL 0.1 mol·L-1
NaOH溶液中加入1 mL 0.1
Cu(OH) 比
D mol·L-1 MgCl 溶液,再向 产生蓝色沉淀 2
2 Mg(OH) 更难溶
混合液MgCl 中滴加0.1 2
2
mol·L-1 CuCl 溶液
2
答案:C
解析:将SO 通入BaCl 溶液,不会产生白色沉淀,A错误;将浓硫酸滴入含少量水的
2 2
蔗糖中,得黑色蓬松的固体及刺激性气味气体,该过程中浓硫酸体现吸水性、脱水性和强
氧化性,B错误;金属钠与水反应比乙醇与水反应剧烈,说明羟基的活动性:水>乙醇,C
正确;向 10 mL 0.1 mol·L-1 NaOH溶液中加入 1 mL 0.1 mol·L-1 MgCl 溶液,产生 Mg
2
(OH) 后,NaOH过量,所以再向混合液中滴加0.1 mol·L-1 CuCl 溶液产生蓝色沉淀,
2 2
并不是Mg(OH) 沉淀转化成Cu(OH) 沉淀,D错误。
2 2
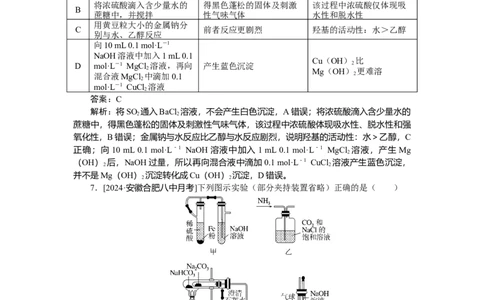
7.[2024·安徽合肥八中月考]下列图示实验(部分夹持装置省略)正确的是( )
A.图甲可用于制备氢氧化亚铁
B.图乙可用于制备NaHCO
3
C.图丙可用于验证碳酸钠和碳酸氢钠的稳定性
D.图丁可用于证明Cl 能溶于水或与NaOH溶液反应
2
答案:D
解析:图甲中左侧盛放稀硫酸的试管侧面导管应有一个止水夹,且导管应插入液面以下,打开止水夹,利用Fe粉和稀硫酸反应产生的氢气排尽装置内的空气,之后关闭止水夹,
将硫酸亚铁溶液压入氢氧化钠溶液中制取氢氧化亚铁,A项错误;氨气极易溶于水,应有
防倒吸装置,且应先通入氨气,再通入二氧化碳,B项错误;碳酸氢钠稳定性较差,应放
在温度较低的小试管中,C项错误;将胶头滴管中NaOH溶液挤入烧瓶中,若Cl 能溶于水
2
或与NaOH溶液反应,则气球会鼓起来,D项正确。
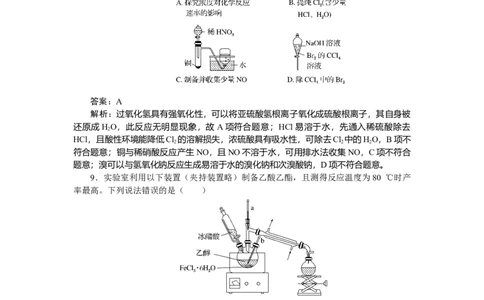
8.[2024·湖北省八市高三联考]下列图示装置不能达到实验目的的是( )
答案:A
解析:过氧化氢具有强氧化性,可以将亚硫酸氢根离子氧化成硫酸根离子,其自身被
还原成HO,此反应无明显现象,故 A项符合题意;HCl易溶于水,先通入稀硫酸除去
2
HCl,且酸性环境能降低Cl 的溶解损失,浓硫酸具有吸水性,可除去Cl 中的HO,B项不
2 2 2
符合题意;铜与稀硝酸反应产生NO,且NO不溶于水,可用排水法收集NO,C项不符合
题意;溴可以与氢氧化钠反应生成易溶于水的溴化钠和次溴酸钠,D项不符合题意。
9.实验室利用以下装置(夹持装置略)制备乙酸乙酯,且测得反应温度为80 ℃时产
率最高。下列说法错误的是( )
A . 若 实 验 过 程 中 乙 醇 为 C HOH , 则 实 验 原 理 为 CHCOOH +
2 3
CHCHOHCHCO18OCH CH+HO
3 3 2 3 2
B.可选用FeCl ·6H O替代浓硫酸作催化剂的原因可能是Fe3+水解提供质子
3 2
C.图中冷却装置可换成冷凝效果更好的球形冷凝管
D.控制反应温度在80 ℃时,要时刻观察温度计b的示数
答案:C
解析:
去情境抓关键 分析判断由羟酸与醇发生酯化反应的原理可知,羧酸
提供的羧基上的羟基与乙醇提供的羟基上的
实验中乙醇为CHCHOH
3 H结合生成水,CHCHOH中18O在产物乙酸
3
乙酯中,A正确
酯化反应需要催化剂提供H+,Fe3+易发生水
用FeCl ·6H O替代浓硫酸作催化剂
3 2 解产生H+,B正确
球形冷凝管倾斜放置时会形成多个积液区
生成的乙酸乙酯在冷凝管中冷凝为液态,被 域,不利于液体顺利流下,导致乙酸乙酯的
烧瓶收集 产率降低,故在蒸馏装置中不可以替代直形
冷凝管,C错误
温度计b应插入液面以下,且要时刻观察温
反应温度为80 ℃时产率最高
度计b的示数以确保反应更充分,D正确
二、非选择题
10.[2022·辽宁卷]HO 作为绿色氧化剂应用广泛,氢醌法制备HO 原理及装置如下:
2 2 2 2
已知:HO、HX等杂质易使Ni催化剂中毒。回答下列问题:
2
(1)A中反应的离子方程式为
________________________________________________________________________。
(2)装置B应为 (填序号)。
(3)检查装置气密性并加入药品,所有活塞处于关闭状态。开始制备时,打开活塞
,控温45 ℃。一段时间后,仅保持活塞b打开,抽出残留气体。随后关闭活塞b,打开活
塞 ,继续反应一段时间。关闭电源和活塞,过滤三颈烧瓶中混合物,加水萃取,
分液,减压蒸馏,得产品。
(4)装置F的作用为
________________________________________________________________________。
(5)反应过程中,控温45 ℃的原因为
________________________________________________________________________
________________________________________________________________________。
(6)氢醌法制备HO 总反应的化学方程式为
2 2
________________________________________________________________________
________________________________________________________________________。(7)取2.50 g产品,加蒸馏水定容至100 mL,摇匀。取20.00 mL于锥形瓶中,用
0.050 0 mol·L-1酸性KMnO 标准溶液滴定。平行滴定三次,消耗标准溶液体积分别为
4
19.98 mL、20.90 mL、20.02 mL。假设其他杂质不干扰结果,产品中HO 质量分数为
2 2
。
答案:(1)Zn+2H+===Zn2++H↑
2
(2)② (3) a、b c、d
(4)防止外界水蒸气进入C中使催化剂中毒
(5)适当升温加快反应速率,同时防止温度过高HO 分解
2 2
(6)H+O=====HO
2 2 2 2
(7)17%
解析:从HO 的制备原理图可知,反应分两步进行,第一步为H 在Ni催化作用下与
2 2 2
乙基蒽醌反应生成乙基蒽醇,第二步为O 与乙基蒽醇反应生成HO 和乙基蒽醌。启普发
2 2 2
生器A为制取H 的装置,产生的H 中混有HCl和HO,需分别除去后进入C中发生第一
2 2 2
步反应。随后氧气源释放的氧气经D干燥后进入C中发生反应生成HO 和乙基蒽醌,F中
2 2
装有浓HSO ,与C相连,防止外界水蒸气进入C中,使催化剂Ni中毒。(2)A中出来
2 4
的H 中含有HCl和水蒸气,结合已知信息可知,必须在装置B中将其除去,碱石灰同时吸
2
收HCl和水蒸气,故应选②。(3)开始制备时,打开活塞a、b,A中产生的H 进入C中,
2
在Ni催化作用下与乙基蒽醌反应生成乙基蒽醇,一段时间后,关闭a,仅保持活塞b打开,
将残留H 抽出,随后关闭活塞b,打开活塞c、d,将O 通入C中与乙基蒽醇反应生成
2 2
HO 和乙基蒽醌。(4)HO容易使Ni催化剂中毒,实验中需要保持C装置为无水环境,
2 2 2
F的作用为防止外界水蒸气进入C中。(5)适当升温加快反应速率,同时防止温度过高
HO 分解,所以反应过程中控温45 ℃。(6)氢醌法制备HO ,H 和O 是反应物,乙基
2 2 2 2 2 2
蒽醌和Ni是催化剂,故总反应的化学方程式为H +O=====HO 。(7)消耗标准溶液体
2 2 2 2
积为20.90 mL的误差过大,应舍去,故平均消耗标准溶液的体积为×(19.98 mL+20.02
mL)=20.00 mL,结合2MnO+5HO +6H+===2Mn2++5O↑+8HO可知,反应的 n
2 2 2 2
(HO )=n(MnO)=×20.00×10-3 L×0.050 0 mol·L-1=2.5×10-3 mol,故产品中HO
2 2 2 2
质量分数为×100%=17%。