文档内容
座号
2012 年河南省初中学业水平暨高级中等学校招生考试试卷
化 学
注意事项:
1.本试卷共4页,满分50分,考试时间50分钟。请用钢笔或圆珠笔直接答在试卷上。
2.答卷前将密封线内的项目填写清楚。
题 号 一 二 三 四 总 分
分 数
相对原子质量 H-1 C-12 O-16 S-32 Ca-40 Fe-56
得 分 评卷人
一、选择题 (本题包括10个小题,每小题1分,共10分)
下列各题,每题只有一个选项符合题意,请将正确选项的标号
填入题后括号内。
1.生活中的下列变化属于物理变化的是【 】
A.粮食酿酒 B.铁钉生锈 C.蜡烛燃烧 D.水的蒸发
A.废旧电池 B.空玻璃酒瓶
C.废弃铁锅 D.一次性塑料饭盒
3.分子、原子、离子等都是构成物质的微粒。下列物质由离子构成的是 【 】
A.氯化钠 B.黄金 C.金刚石 D.干冰
4.下列物质在氧气里燃烧,能生成有刺激性气味的气体的是 【 】
A.铁丝 B.硫 C.镁条 D.木炭
5.我们的衣、食、住、行中蕴含着丰富的化学知识。下列说法不正确的是 【 】
A.衣料中的棉、羊毛等都属于合成有机高分子材料
B.食用加碘食盐和强化铁酱油可补充某些人体必需微量元素
C.建造高楼大厦时所用到的钢和生铁属于铁的两种合金
D.宇通客车用天然气代替汽油作燃料可减少空气污染
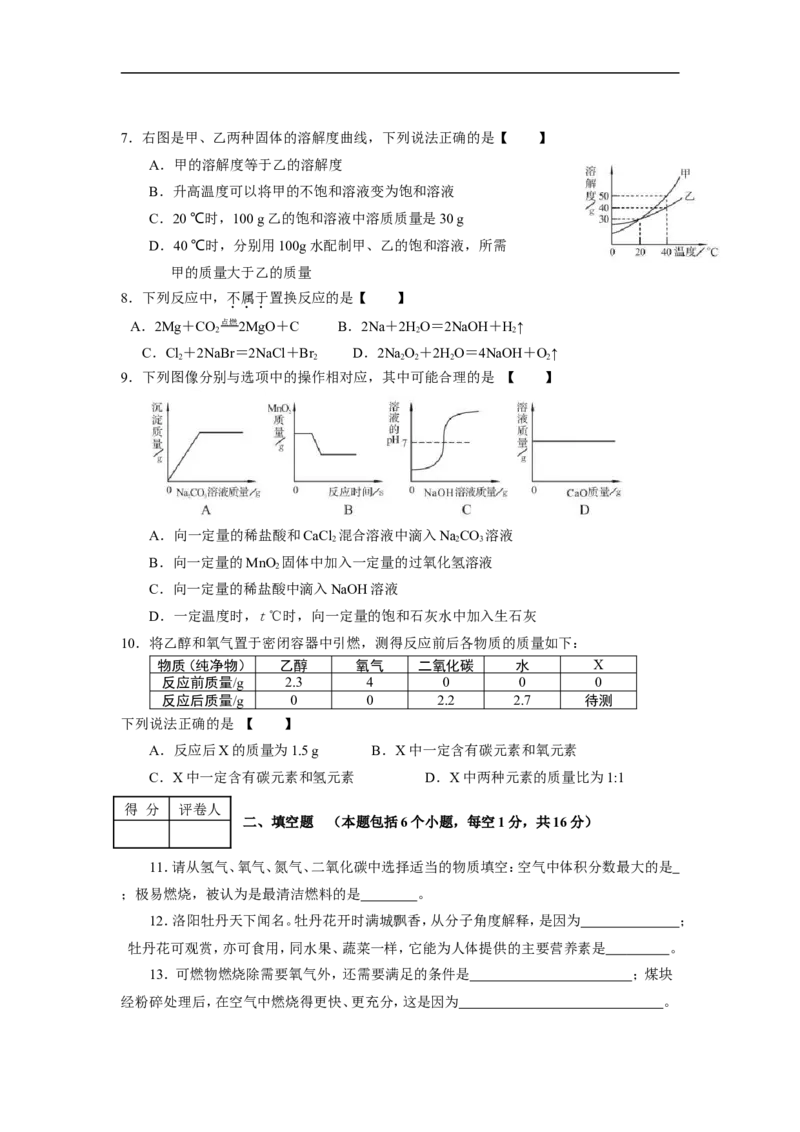
6.下列图示的实验操作正确的是 【 】7.右图是甲、乙两种固体的溶解度曲线,下列说法正确的是【 】
A.甲的溶解度等于乙的溶解度
B.升高温度可以将甲的不饱和溶液变为饱和溶液
C.20 ℃时,100 g乙的饱和溶液中溶质质量是30 g
D.40 ℃时,分别用100g水配制甲、乙的饱和溶液,所需
甲的质量大于乙的质量
8.下列反应中,不属于置换反应的是【 】
A.2Mg+CO 点燃 2MgO+C B.2Na+2HO=2NaOH+H↑
2 2 2
C.Cl+2NaBr=2NaCl+Br D.2NaO+2HO=4NaOH+O↑
2 2 2 2 2 2
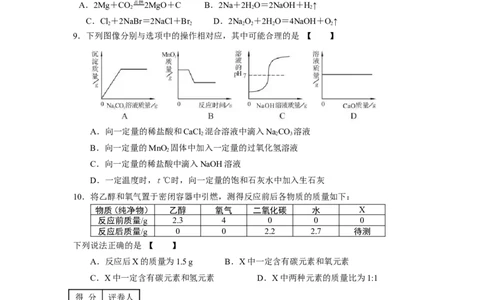
9.下列图像分别与选项中的操作相对应,其中可能合理的是 【 】
A.向一定量的稀盐酸和CaCl 混合溶液中滴入NaCO 溶液
2 2 3
B.向一定量的MnO 固体中加入一定量的过氧化氢溶液
2
C.向一定量的稀盐酸中滴入NaOH溶液
D.一定温度时,t℃时,向一定量的饱和石灰水中加入生石灰
10.将乙醇和氧气置于密闭容器中引燃,测得反应前后各物质的质量如下:
物质(纯净物) 乙醇 氧气 二氧化碳 水 X
反应前质量/g 2.3 4 0 0 0
反应后质量/g 0 0 2.2 2.7 待测
下列说法正确的是 【 】
A.反应后X的质量为1.5 g B.X中一定含有碳元素和氧元素
C.X中一定含有碳元素和氢元素 D.X中两种元素的质量比为1:1
得 分 评卷人
二、填空题 (本题包括6个小题,每空1分,共16分)
11.请从氢气、氧气、氮气、二氧化碳中选择适当的物质填空:空气中体积分数最大的是
;极易燃烧,被认为是最清洁燃料的是 。
12.洛阳牡丹天下闻名。牡丹花开时满城飘香,从分子角度解释,是因为 ;
牡丹花可观赏,亦可食用,同水果、蔬菜一样,它能为人体提供的主要营养素是 。
13.可燃物燃烧除需要氧气外,还需要满足的条件是 ;煤块
经粉碎处理后,在空气中燃烧得更快、更充分,这是因为 。14.右图是某输液瓶标签上的部分内容。由此可知,葡萄糖由 种元素
组成,其中碳元素的质量分数为 。要把10 g这种葡萄糖溶液稀释为2%
的溶液,需要水的质量为 g。
15.明矾可用于净水,是因为明矾溶于水生成的胶状物可以 悬浮于
水中的杂质,使水澄清;新型自来水消毒剂ClO 可由下列反应制取:Cl +2X=
2 2
2NaCl+2ClO ,则X的化学式为 ;除去硬水中过多的 (填离子符号)和
2
Mg2+就可得到软水。
16.甲、乙、丙、丁是常见的化合物,它们有如右图所示转化关系
(部分物质已略去)。甲是相对分子质量为16的有机物;乙是最常见
的溶剂;丁是白色难溶固体,其中金属元素的质量分数为40%。则甲的化学式为 ;反
应②和③的化学方程式分别为 、 ;试剂A中溶质
在生产或生活中的一种用途是 。
得 分 评卷人
三、简答题 (本题包括4个小题,共14分)
17.(2分)右图是某物质分解的微观示意图。
(1)图中属于化合物的是 。
(2)写出该反应的化学方程式。
18.(4分)请用所学化学知识解释下列原理。
(1)洗涤剂能除去油污,是因为它具有 功能。
(2)在铁制品表面涂油、刷漆或镀铬等都能防止铁生锈,其原理是什么?
(3)用化学方程式表示含Mg(OH) 的药物治疗胃酸过多症的原理。
2
(4)用化学方程式表示“联合制碱法”中的如下反应 :向饱和食盐水中先后通入足量
NH 和CO,生成小苏打(在该溶液中难溶)和一种氮肥。
3 2
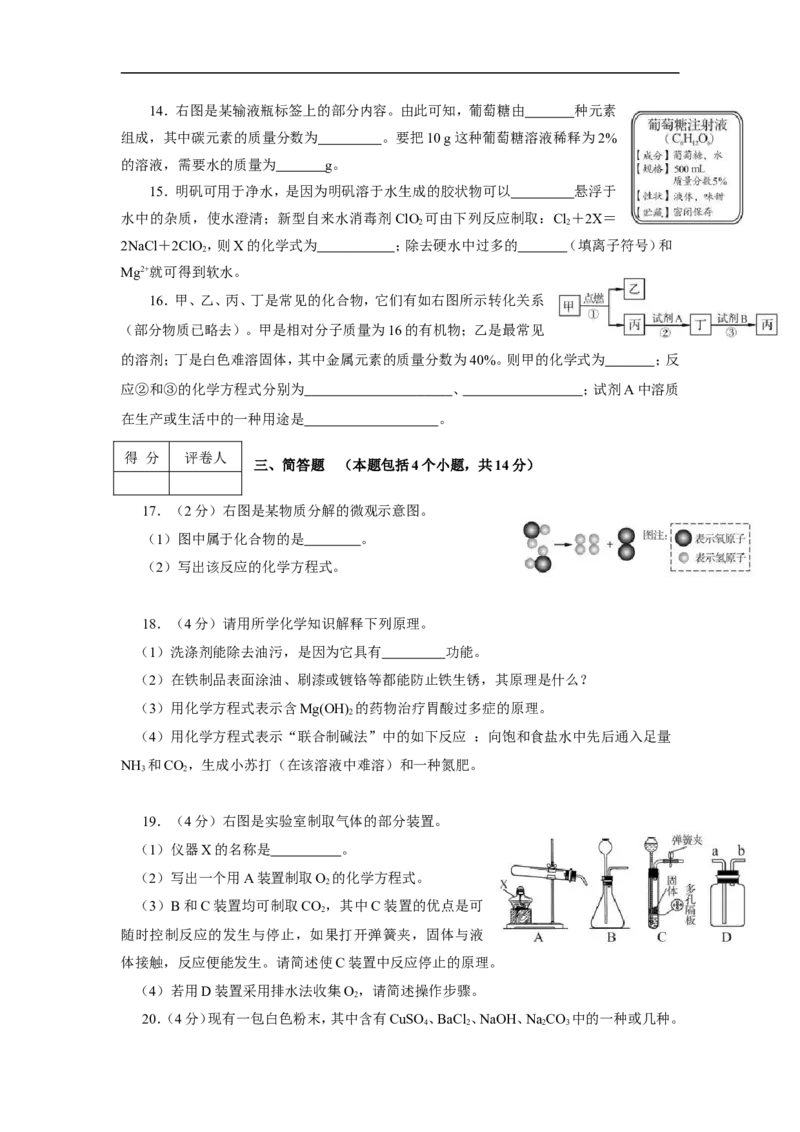
19.(4分)右图是实验室制取气体的部分装置。
(1)仪器X的名称是 。
(2)写出一个用A装置制取O 的化学方程式。
2
(3)B和C装置均可制取CO ,其中C装置的优点是可
2
随时控制反应的发生与停止,如果打开弹簧夹,固体与液
体接触,反应便能发生。请简述使C装置中反应停止的原理。
(4)若用D装置采用排水法收集O,请简述操作步骤。
2
20.(4分)现有一包白色粉末,其中含有CuSO 、BaCl 、NaOH、NaCO 中的一种或几种。
4 2 2 3某化学小组为确定白色粉末的成分,进行了如下实验:(I)取一定量白色粉末,加入足量水,
振荡,得到无色透明溶液;(II)取少量(I)的溶液,加入足量盐酸,有气泡产生。(提示:BaCO
3
难溶于水;NaCO 的水溶液呈碱性)
2 3
(1)该白色粉末中肯定含有什么物质?可能含有什么物质?
(2)为确定可能含有的物质是否存在,还需做什么实验?请写出简要的实验步骤。
得 分 评卷人 四、综合应用题 (共10分)
21.金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)右图是铝的原子结构示意图。下列说法不正确的是 。
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
(2)某化学小组用一定量AgNO 和Cu(NO ) 混合溶液进行了右图实验 ,
3 3 2
并对溶液A和固体B的成分进行了分析和实验探究。
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO ) ② Zn (NO )、AgNO ③ Zn (NO )、Cu(NO )
3 2 3 2 3 3 2 3 2
④Zn (NO )、AgNO、Cu(NO )
3 2 3 3 2
【交流讨论】不合理的猜想是 (填标号),其理由是
。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 现 象 有关反应的化学方程式
取少量固体B, 有气泡产生
滴加
(3)右图是工业炼铁示意图。其中,焦炭的作用是燃烧提供能量和
;有铁生成的化学方程式为 。
(4)某工厂利用废铁屑与废硫酸起反应来制取硫酸亚铁。现有废硫酸49 t
(H SO 的质量分数为10%),与足量废铁屑起反应,可生产硫酸亚铁的质量是多少?
2 42012年河南省初中学业水平暨高级中等学校招生考试
化学试题参考答案及评分标准
注意事项:
1.答出其他合理答案,请参照评分标准给分。
2.没有特别要求写化学式的,写化学式或名称均得分。
一、选择题 (每小题1分,共10分)
题号 1 2 3 4 5 6 7 8 9 10
答案 D C A B A C D D C B
二、填空题 (每空1分,共16分)
11.氮气(或N) 氢气(或H)
2 2
12.分子在不断地运动使香味扩散 维生素
13.三 40% 15
14.温度达到可燃物的着火点 煤粉与氧气(或空气)有更大的接触面
15.吸附 NaClO Ca2+
2
16.CH CO+ Ca(OH) == CaCO↓+H O CaCO+2HCl== CaCl + CO↑+ H O等
4 2 2 3 2 3 2 2 2
灭火(或作气体肥料等)
三、简答题 (共14分)
17.(2分)(1)水(或HO) (2)2HO 通电 2H↑+ O ↑
2 2 2 2
18.(4分)(1)乳化
(2)覆盖保护层,起到隔绝氧气(或空气)和水的作用。
(3)Mg(OH) +2HCl =MgCl+2HO
2 2 2
(4)NaCl+H O+NH +CO == NaHCO ↓+NHCl
2 3 2 3 4
19.(4分)(1)酒精灯
(2)2KMnO △ KMnO + MnO + O ↑或2KClO 2KCl+ 3O↑
4 2 4 2 2 3 2
(3)当用弹簧夹夹住胶皮管时,产生的气体使试管内的压强增大,液体被压回长颈漏斗中,
与固体反应物脱离,反应便会停止。
(4)先将集气瓶装满水,再将O 从b口通入。
2
20.(4分)(1)肯定含有NaCO;可能含有NaOH。
2 3
(2)取少量(I)的溶液,加入足量BaCl 溶液(或CaCl 溶液),静置,取上层清液滴加酚酞溶
2 2液。
四、综合应用题 (共10分)
21.(1)C(1分) (2)②(1分) 猜想②中无Cu(NO ),说明Cu(NO ) 已与Zn反应生
3 2 3 2
成Cu,而Cu能与AgNO 反应,故也不可能有AgNO 【或Zn应先与AgNO 反应后与
3 3 3
Cu(NO ) 反应,当有AgNO 剩余时,溶质中一定含有Cu(NO )】(1分)
3 2 3 3 2
实验步骤 现象 有关反应的化学方程式
Zn+2HCl=ZnCl+H↑
2 2
稀盐酸(或稀硫酸等)
(或Zn+HSO =ZnSO +H↑)
2 4 4 2
(1分)
(1分)
(3)制取CO(1分) Fe O+3CO高温 2Fe+3CO(1分)
2 3 2
(4)解:设可生产硫酸亚铁的质量为x。
Fe+HSO =FeSO +H↑ (1分)
2 4 4 2
98 152
49 t×10% x
98:152=49 t×10%:x (列成为竖式) (1分)
x=7.6 t (1分)
答:可生产硫酸亚铁7.6 t。