文档内容
3. 2021年10月4日,美国两位科学家因为发现了温度和触觉受体荣获诺贝尔生
姓
理学或医学奖,他们利用辣椒素来识别皮肤神经末梢中对热有反应的传感器。辣
名 椒素的结构如图所示,下列有关说法正确的是( )
密山市高级中学 2023-2024 学年度高三联考期末考试
化学试卷
注意事项:1.考试期间,注意考试时间
A.分子式为
2.禁止在试卷上乱写乱画
B.分子中甲基上的一氯取代物有三种
一、单项选择题(50分)
C.它的含有苯环的同分异构体中可能含有两个碳碳双键
1.古今化学多有异曲同工之处,下列叙述所涉及的原理不同的是( )
D.能使溴水和酸性高锰酸钾溶液褪色,且反应类型相同
曲为酒之骨,凡酿酒必资曲药
A 纳米酶用于生物传感器、疾病诊断与治疗 4.利用如图所示装置进行实验(夹持装置略),b中现象能证明a中产物生成的是(
成信
)
铝合金用作火箭、飞船和空间站主体结构材
B 铜柔锡柔,合两柔则为刚
料 b中检测试剂及现
a中反应
象
为宅煮糖,宅垣忽坏,去土而
C 啤酒和白酒中加入食品胶体作澄清剂
糖白 A 淀粉-KI溶液变蓝
浓 分解生成
以火烧之,紫青烟起,乃真硝
D 使用X射线衍射技术推测晶体的分子排列 与NaOH乙醇溶液
石也 B 溴水褪色
生成乙烯
A.A B.B C.C D.D
浓NaOH与 溶液生
2.大连理工大学课题组通过 催化,使 反应体系在温 C 石蕊溶液变红
成
和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
木炭与浓 反应生
D 澄清石灰水浑浊
成
, 是阿伏加德罗常数的值,下列有关说法
A.A B.B C.C D.D
正确的是( )
5.丙烯酸乙酯( )天然存在于菠萝等水果中,是一种食品用合
A.标准状况下,2.24LNO中含有电子数为3
成香料。某小组设计如图装置制备丙烯酸乙酯(加热仪器省略)。下列说法错误的
是( )
B.消耗0.3molNO则生成的 中 键数目为0.75
C.生成3.4g 能消除CO的数目为0.5
D.0.5molCO、0.2moINO和0.3mol 在容器中反应转移电子数为
————
班
级
————
学
号
————-A.
B.
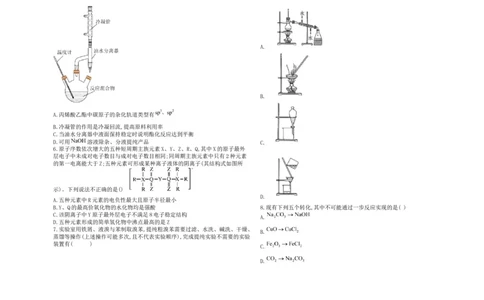
A.丙烯酸乙酯中碳原子的杂化轨道类型有
B.冷凝管的作用是冷凝回流,提高原料利用率
C.当油水分离器中液面保持稳定时说明酯化反应达到平衡
D.可用 溶液除杂、分液提纯产品 C.
6.原子序数依次增大的五种短周期主族元素X、Y、Z、R、Q,其中X的原子最外
层电子中未成对电子数目与成对电子数目相同;同周期主族元素中只有2种元素
的第一电离能大于Z;五种元素可形成某种离子液体的阴离子(其结构式如图所
示)。下列说法不正确的是()
D.
A.五种元素中R元素的电负性最大且原子半径最小
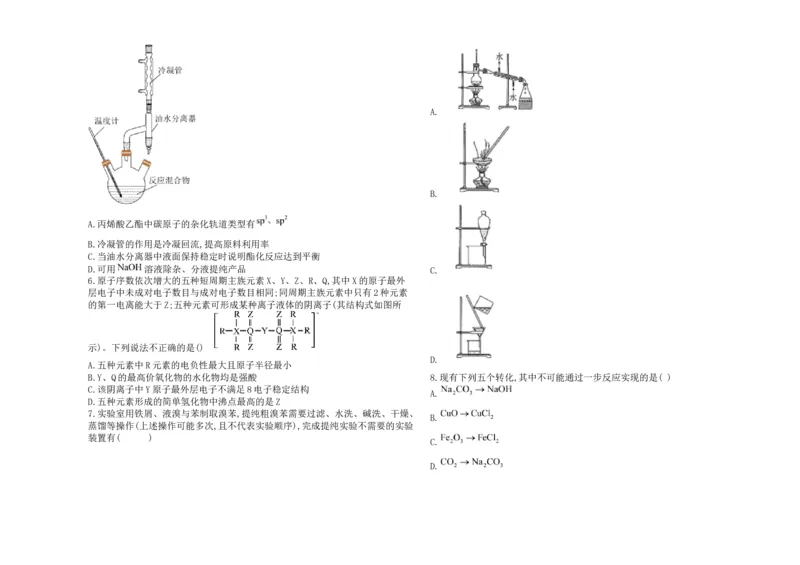
B.Y、Q的最高价氧化物的水化物均是强酸 8.现有下列五个转化,其中不可能通过一步反应实现的是( )
C.该阴离子中Y原子最外层电子不满足8电子稳定结构
A.
D.五种元素形成的简单氢化物中沸点最高的是Z
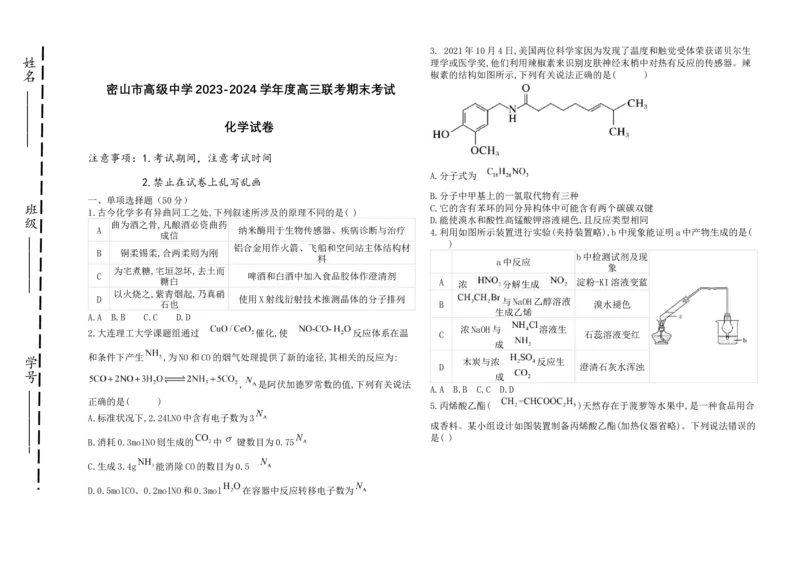
7.实验室用铁屑、液溴与苯制取溴苯,提纯粗溴苯需要过滤、水洗、碱洗、干燥、
B.
蒸馏等操作(上述操作可能多次,且不代表实验顺序),完成提纯实验不需要的实验
装置有( )
C.
D.C,G在空气中放置极易生锈。则A是___,B是___,C是__,D是___,E是___,
9.利用辉锑矿(主要成分为 ,含 、MgO、 等杂质)为原料制
F是____,G是____ 。
备SbOCl的工艺流程如图所示。还原性: 。 12.(5分)CO2、碳酸盐、有机物等均是自然界碳循环中的重要物质。回答下列
问题:
(1)下列物质属于化合物但不属于电解质的是______(填字母)。
A.石墨 B.汽油 C.乙醇D.碳酸
(2)倍半碳酸钠(Na2CO3·NaHCO3·2H2O)在水溶液中的电离方程式为
__________________________。
(3)金属钠在足量CO2中燃烧生成常见的盐和单质,写出反应的化学方程式:
下列说法正确的是( ) ____________。
(4)铜器表面的难溶物Cu2(OH)2CO3可用稀硫酸洗涤除去,该反应的离子方程式
A.“溶浸”中浸出渣的主要成分为
为________________。
B.“还原”加入Sb的目的是将 还原为Fe
(5)工业上制取金刚砂的反应为: ,该反应中氧化剂
与还原剂的物质的量之比为______。
C.“水解”时发生的主要反应为:
13.(13分)A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如
D.可采用边加热、边搅拌的形式促进 的水解 下的反应关系:
10. 室温下,下列实验方案、实验现象及实验结论均正确的是( )
实验现
选项 实验方案 实验结论
象
出现红
A 将饱和 滴入 溶液中 褐色溶 制得 胶体 ⑴若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要 物质。处理C物
液
质可得到有价值的化学品,写出该化学品中的1种酸和1种盐的名称________、
用 计分别测 和 饱和溶液 前者小 酸性: _________。
B
于后者 ⑵若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条
的
件下反应生成的A是大气主要成分,写出该反应的化学方程式____________
向 浓度都为 出现黄
C ⑶若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起
色沉淀
混合溶液中滴加2滴 温室效应的主要气体。判断单质A的元素在周期表中的位置是________。
固体表 写④反应离子方程式___________。
D 将浓硫酸滴入胆矾晶体中 浓硫酸有脱水性
面变白
⑷若A是应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。
A.A B.B C.C D.D
C的溶液用于蚀刻印刷铜电路板,写该反应的离子方程式_______________。
二、填空题(25分)
三、计算题(14分)
11.(7分)有七种金属:钾、锌、铁、锡、铜、银、铂,它们的标号分别为A、
14.(8分)将铜与Fe2O3的混合物共28.8g加入300mL2.00mol·L-1的稀硫酸中,
B、C、D、E、F、G。①常温下,只有A和水反应生成氢气;②D、E、G都能和稀
充分反应后剩余固体的质量为6.40g。请计算:
硫酸反应生成氢气,B、C、F无此性质;③C、F组成原电池时,F为正极;④在
⑴混合物加入稀硫酸中,发生反应的离子方程式为____________。
G的硫酸盐溶液中加入D,发现D溶解,G析出;⑤将G、E接触放置,E不易锈
⑵混合物中铜的物质的量为____________mol。
蚀;⑥以铂作电极,电解相同浓度的B和C的硝酸盐溶液时,在阴极上首先得到
⑶反应后的溶液中最多消耗锌片的质量为____________g。15.(6分)(1)一杯咖啡中含有0.194g咖啡因(分子式C8H10N4O2,M=194g/
mol),你知道其中有_______个咖啡因分子;这些咖啡因分子中的N原子的物质
的量为_________.
(2)经检测一瓶泉水样品,1.0L样品中含4.8×10﹣2g Mg2+,那么该泉水中
Mg2+的物质的量浓度为____________.含1.0mol Mg的这种泉水的体积是
_________L.
(3)0.2mol H2S,在标准状况下的体积约为_______L;相同质量的CH4和H2S
中分子个数比为____________.
对温室气体二氧化碳的研究一直是科技界关注的重点。 (4)写出写出钙化作用的离子方程式____________。
四、实验题(11分) (5)电解完成后,a室的pH值______(“变大”、“变小”或“几乎不变”);
I.在催化剂存在下用H2还原CO2是解决温室效应的重要手段之一,相关反应如 其间b室发生反应的离子方程式为____________。
下:
主反应:CO2(g)+4H2(g)=CH4(g)+2H2O(g) △H1①
副反应:CO2(g)+H2(g)=CO(g)+H2O(g) △H2=+41.2kJ/mol
已知H2和CH4的燃烧热分别为-285.5kJ·mol-1和-890.0kJ·mol-1
H2O(l)=H2O(g) △H=+44 kJ·mol-1
(1)△H1=______kJ·mo l-1。
(2)有利于提高CH4平衡产率的反应条件是(至少写两条)_________。工业上
提高甲烷反应选择性的关键因素是_____________。
(3)T℃时,若在体积恒为2L的密闭容器中同时发生上述反应,将物质的量之
和为5mol的H2和CO2以不同的投料比进行反应,结果如图所示。若a、b表示
反应物的转化率,则表示H2转化率的是______,c、d分别表示CH4(g)和CO(g)
的体积分数,由图可知=______时,甲烷产率最高。若该条件下CO的产率趋于
0,则T℃时①的平衡常数K=________。
II.溶于海水的CO295%以HCO3-形式存在。在海洋中,通过如下左图钙化作用实
现碳自净。密山市高级中学 2023-2024 学年度高三联考期末考试
化学试卷答案
1-5 D C C C D
6-10 C B C C C
11. 钾铜银锌锡铂
12.(1)C
( 2 ) ( 或
)
(3)
(4)
(5)1∶2
13.(1) 硫酸、硫酸铵(钙)
(2) 4NH +6NO==5N +6H O (一定条件)
3 2 2
(3) 第 三 周 期 Ⅲ A 族 AlO - +2H O+CO ==Al(OH) ↓ +
2 2 2 3
HCO -
3
(4) Cu+2Fe3+=Cu2+ +2Fe2+
14. (1)Fe2O3 + 6H+ = 2Fe3+ + 3H2O 或 2Fe3+ +Cu =
2Fe2+ +Cu2+
(2)0.2
(3)3915.(1)0.001NA 0.004mol
(2)0.002mol/L 500L
(3)4.48L 17:8
16. (1)-164.0
(2)降低温度,增大压强 催化剂
(3)b 4 100
(4)2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O
(5)几乎不变 H++ HCO3-= CO2↑+H2O