文档内容
B.m=2n-1
襄阳五中 2025 届高三下学期 5 月适应性考试(一)
C.三聚氰胺为极性分子,能溶于水
化 学 试 题
D.一定条件下,三聚氰胺与甲醛反应还可得到网状聚合物
6.下列对事实的解释错误的是
命题人: 杨襄 审题人: 朱海军、周少红
事实 解释
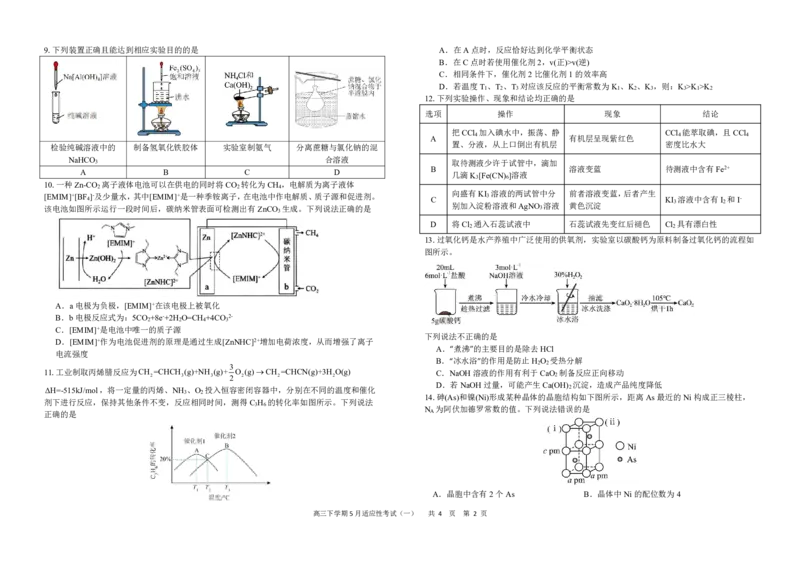
可能用到的相对原子质量H-1 C-12 O-16 N-14 F-19 Na-23 Sb-122 As-75 Ni-59
A 聚乙炔用于制备导电高分子材料 高分子的共轭大π键体系为电荷传递提供了通路
一、选择题:本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一
项是符合题目要求的。 B 正戊烷的沸点高于异戊烷 异戊烷分子支链多,分子间距大,范德华力弱
1.化学与生活密切相关。下列说法错误的是
C NO的极性大于CO N-O键的极性大于C-O键
A.核桃中富含硬脂酸、油酸和亚油酸,此三种酸均为十八碳酸
B.原油中的含硫化合物,可使输送原油的钢管发生化学腐蚀
D 表面活性剂可降低水的表面张力
表面活性剂在水面形成单分子膜,破坏了水分子间
C.甘油和矿物油均可作护肤品的保湿剂,二者的保湿原理不相同 的氢键
D.有机玻璃的主要成分为聚甲基丙烯酸甲酯,可通过缩聚反应制得 7.NH 催化还原氮氧化物是目前应用最广泛的烟气脱硝技术。用活化的V O 作催化剂,NH
3 2 5 3
2.下列化学用语说法正确的是 将NO还原成N 的一种反应历程如图所示。下列说法错误的是
2
A.邻羟基苯甲醛分子内氢键可表示为 B.2-甲基-1-丁醇的键线式:
C.硫氰化氢(HSCN)的球棍模型可能为 D.乙醇的分子式:C H OH
2 5
3.设N 为阿伏加德罗常数的值。下列说法错误的是
A
A.1molFe与1molCl 充分反应,转移电子数为2N
2 A
B.1LpH=9的CH COONa溶液中,由水电离的OH-数目为10-5N
3 A
C.0.5molXeF 中Xe的价层电子对数为3N
4 A
D.1mol液态水中水分子间的氢键数目小于2N
A
4.下列反应的离子方程式书写正确的是
A.工业制漂白粉:Cl
2
+2OH-=Cl-+ClO-+H
2
O A.反应Ⅰ对总反应速率影响不大
B.向NaHS溶液中滴加Cu(NO
3
)
2
溶液:HS-+Cu2+=CuS↓+H+ B.增大NH
3
浓度会影响催化剂对NO的吸附
C.向Na
2
[Be(OH)
4
]溶液中通入过量CO
2
:[Be(OH)
4
]2-+2CO
2
=Be(OH)
2
↓+2HCO
3
- C.整个历程中涉及极性键和非极性键的断裂和形成
D.消耗标准状况下11.2LO 时,整个过程转移6mol电子
2
8 . X、Y、Z、P、Q为原子序数依次增大的前三周期元素,其中只有一种是金属元素,X、Y、
D.向 溶液中加入少量盐酸:
P位于三个不同周期,Y、Z处于不同主族,5种元素形成的化合物如图所示。下列说法错误的
5.三聚氰胺和甲醛在一定条件下反应得到线性聚合物的化学方程式如图。下列说法正确的是 是
A.单质沸点:P>Q>Z>X B.同周期元素中,第一电离能介于P、Q之间的有4种
A.三聚氰胺分子中碳、氮原子杂化方式均为sp2 C.键角:ZX v(逆)
C.相同条件下,催化剂2比催化剂1的效率高
D.若温度T 、T 、T 对应该反应的平衡常数为K 、K 、K ,则:K >K >K
1 2 3 1 2 3 3 1 2
12.下列实验操作、现象和结论均正确的是
选项 操作 现象 结论
把CCl 加入碘水中,振荡、静 CCl 能萃取碘,且CCl
A 4 有机层呈现紫红色 4 4
置、分液,从上口倒出有机层 密度比水大
检验纯碱溶液中的 制备氢氧化铁胶体 实验室制氨气 分离蔗糖与氯化钠的混
NaHCO 3 合溶液 取待测液少许于试管中,滴加
B 溶液变蓝 待测液中含有Fe2+
A B C D 几滴K [Fe(CN) ]溶液
3 6
10.一种Zn-CO 离子液体电池可以在供电的同时将CO 转化为CH ,电解质为离子液体
2 2 4
[EMIM]+[BF 4 ]-及少量水,其中[EMIM]+是一种季铵离子,在电池中作电解质、质子源和促进剂。 C
向盛有KI
3
溶液的两试管中分 前者溶液变蓝,后者产生
KI 溶液中含有I 和I-
该电池如图所示运行一段时间后,碳纳米管表面可检测出有ZnCO 生成。下列说法正确的是
别加入淀粉溶液和AgNO
3
溶液 黄色沉淀 3 2
3
D 将Cl 通入石蕊试液中 石蕊试液先变红后褪色 Cl 具有漂白性
2 2
13.过氧化钙是水产养殖中广泛使用的供氧剂,实验室以碳酸钙为原料制备过氧化钙的流程如
图所示。
A.a电极为负极,[EMIM]+在该电极上被氧化
B.b电极反应式为:5CO +8e-+2H O=CH +4CO 2-
2 2 4 3
C.[EMIM]+是电池中唯一的质子源
下列说法不正确的是
D.[EMIM]+作为电池促进剂的原理是通过生成[ZnNHC]2+增加电荷浓度,从而增强了离子
A.“煮沸”的主要目的是除去HCl
电流强度
B.“冰水浴”的作用是防止H O 受热分解
2 2
3
11.工业制取丙烯腈反应为CH =CHCH (g)+NH (g)+ O (g)CH =CHCN(g)+3H O(g) C.NaOH溶液的作用有利于CaO 制备反应正向移动
2 3 3 2 2 2 2 2
D.若NaOH过量,可能产生Ca(OH) 沉淀,造成产品纯度降低
ΔH=-515kJ/mol,将一定量的丙烯、NH 、O 投入恒容密闭容器中,分别在不同的温度和催化 2
3 2
14.砷(As)和镍(Ni)形成某种晶体的晶胞结构如下图所示,距离As最近的Ni构成正三棱柱,
剂下进行反应,保持其他条件不变,反应相同时间,测得C H 的转化率如图所示。下列说法
3 6
N 为阿伏加德罗常数的值。下列说法错误的是
正确的是 A
A.晶胞中含有2个As B.晶体中Ni的配位数为4
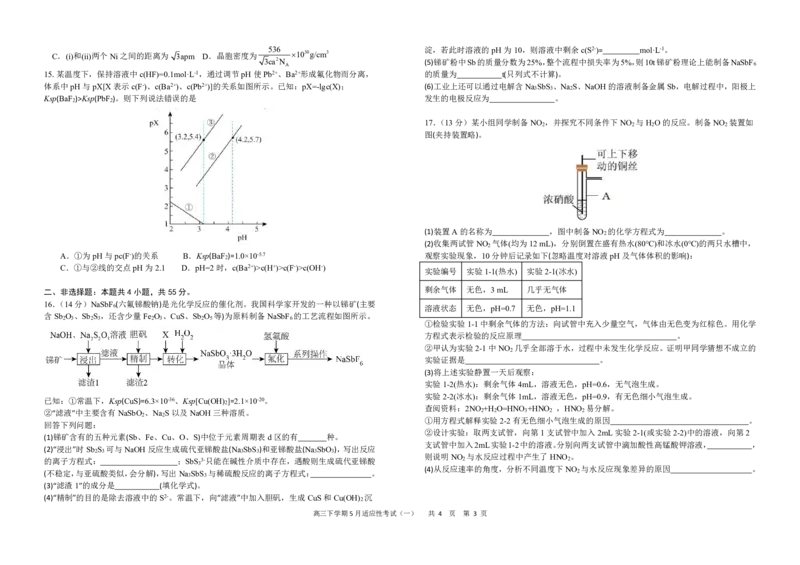
高三下学期5月适应性考试(一) 共 4 页 第 2 页536 淀,若此时溶液的pH为10,则溶液中剩余c(S2-)= mol·L-1。
C.(i)和(ii)两个Ni之间的距离为 apm D.晶胞密度为 1030g/cm3
3ca2N (5)锑矿粉中Sb的质量分数为25%,整个流程中损失率为5%,则10t锑矿粉理论上能制备NaSbF
A 6
15.某温度下,保持溶液中c(HF)=0.1mol·L-1,通过调节pH使Pb2+、Ba2+形成氟化物而分离, 的质量为 t(只列式不计算)。
体系中pH与pX[X表示c(F-)、c(Ba2+)、c(Pb2+)]的关系如图所示。已知:pX=-lgc(X); (6)工业上还可以通过电解含Na SbS 、Na S、NaOH的溶液制备金属Sb,电解过程中,阳极上
3 3 2
Ksp(BaF )>Ksp(PbF )。则下列说法错误的是 发生的电极反应为 。
2 2
17.(13分)某小组同学制备NO ,并探究不同条件下NO 与H O的反应。制备NO 装置如
2 2 2 2
图(夹持装置略)。
(1)装置A的名称为 ,图中制备NO 的化学方程式为 。
2
(2)收集两试管NO 气体(均为12mL),分别倒置在盛有热水(80℃)和冰水(0℃)的两只水槽中,
2
A.①为pH与pc(F-)的关系 B.Ksp(BaF )=1.0×10-5.7 观察实验现象,10分钟后记录如下(忽略温度对溶液pH及气体体积的影响):
2
C.①与②线的交点pH为2.1 D.pH=2时,c(Ba2+)>c(H+)>c(F-)>c(OH-)
实验编号 实验1-1(热水) 实验2-1(冰水)
二、非选择题:本题共4小题,共55分。 剩余气体 无色,3mL 几乎无气体
16.(14分)NaSbF (六氟锑酸钠)是光化学反应的催化剂。我国科学家开发的一种以锑矿(主要
6 溶液状态 无色,pH=0.7 无色,pH=1.1
含Sb O 、Sb S ,还含少量Fe O 、CuS、Sb O 等)为原料制备NaSbF 的工艺流程如图所示。
2 3 2 3 2 3 2 5 6
①检验实验1-1中剩余气体的方法:向试管中充入少量空气,气体由无色变为红棕色。用化学
方程式表示检验的反应原理 。
②甲认为实验2-1中NO 几乎全部溶于水,过程中未发生化学反应。证明甲同学猜想不成立的
2
实验证据是 。
(3)将上述实验静置一天后观察:
实验1-2(热水):剩余气体4mL,溶液无色,pH=0.6,无气泡生成。
实验2-2(冰水):剩余气体1mL,溶液无色,pH=0.9,有无色细小气泡生成。
已知:①常温下,Ksp(CuS)=6.3×10-36、Ksp[Cu(OH) ]=2.1×10-20。
2
查阅资料:2NO +H O=HNO +HNO ,HNO 易分解。
②“滤液”中主要含有NaSbO 、Na S以及NaOH三种溶质。 2 2 3 2 2
2 2
①用方程式解释实验2-2有无色细小气泡生成的原因 。
回答下列问题:
②设计实验:取两支试管,向第1支试管中加入2mL实验2-1(或实验2-2)中的溶液,向第2
(1)锑矿含有的五种元素(Sb、Fe、Cu、O、S)中位于元素周期表d区的有 种。
支试管中加入2mL实验1-2中的溶液。分别向两支试管中滴加酸性高锰酸钾溶液, ,
(2)“浸出”时Sb S 可与NaOH反应生成硫代亚锑酸盐(Na SbS )和亚锑酸盐(Na SbO ),写出反应
2 3 3 3 3 3
则说明NO 与水反应过程中产生了HNO 。
的离子方程式: ;SbS 3-只能在碱性介质中存在,遇酸则生成硫代亚锑酸 2 2
3
(4)从反应速率的角度,分析不同温度下NO 与水反应现象差异的原因 。
(不稳定,与亚硫酸类似,会分解),写出Na SbS 与稀硫酸反应的离子方程式: 。 2
3 3
(3)“滤渣1”的成分是 (填化学式)。
(4)“精制”的目的是除去溶液中的S2-。常温下,向“滤液”中加入胆矾,生成CuS和Cu(OH) 沉
2
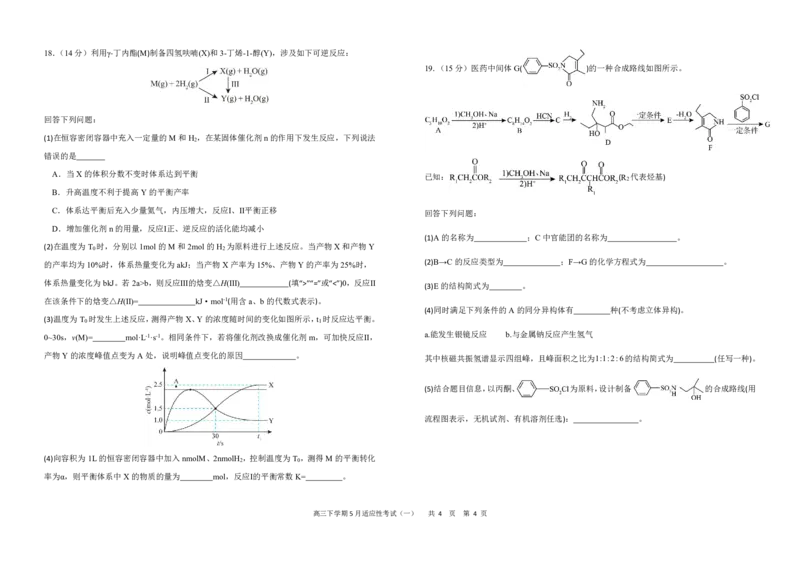
高三下学期5月适应性考试(一) 共 4 页 第 3 页18.(14分)利用γ-丁内酯(M)制备四氢呋喃(X)和3-丁烯-1-醇(Y),涉及如下可逆反应:
19.(15分)医药中间体G( )的一种合成路线如图所示。
回答下列问题:
(1)在恒容密闭容器中充入一定量的M和H ,在某固体催化剂n的作用下发生反应,下列说法
2
错误的是
A.当X的体积分数不变时体系达到平衡
已知: (R 代表烃基)
2
B.升高温度不利于提高Y的平衡产率
C.体系达平衡后充入少量氦气,内压增大,反应Ⅰ、Ⅱ平衡正移
回答下列问题:
D.增加催化剂n的用量,反应Ⅰ正、逆反应的活化能均减小
(1)A的名称为 ;C中官能团的名称为 。
(2)在温度为T 时,分别以1mol的M和2mol的H 为原料进行上述反应。当产物X和产物Y
0 2
的产率均为10%时,体系热量变化为akJ;当产物X产率为15%、产物Y的产率为25%时,
(2)B→C的反应类型为 ;F→G的化学方程式为 。
体系热量变化为bkJ。若2a>b,则反应Ⅲ的焓变△H(Ⅲ) (填“>”“=”或“<”)0,反应Ⅱ
(3)E的结构简式为 。
在该条件下的焓变△H(Ⅱ)= kJ·mol-1(用含a、b的代数式表示)。
(4)同时满足下列条件的A的同分异构体有 种(不考虑立体异构)。
(3)温度为T 时发生上述反应,测得产物X、Y的浓度随时间的变化如图所示,t 时反应达平衡。
0 1
0~30s,v(M)= mol·L-1·s-1。相同条件下,若将催化剂改换成催化剂m,可加快反应Ⅱ,
a.能发生银镜反应 b.与金属钠反应产生氢气
产物Y的浓度峰值点变为A处,说明峰值点变化的原因 。
其中核磁共振氢谱显示四组峰,且峰面积之比为1:1:2:6的结构简式为 (任写一种)。
(5)结合题目信息,以丙酮、 为原料,设计制备 的合成路线(用
流程图表示,无机试剂、有机溶剂任选): 。
(4)向容积为1L的恒容密闭容器中加入nmolM、2nmolH ,控制温度为T ,测得M的平衡转化
2 0
率为α,则平衡体系中X的物质的量为 mol,反应Ⅰ的平衡常数K= 。
高三下学期5月适应性考试(一) 共 4 页 第 4 页