文档内容
宁德一中 2024 届高三第一次检测高三化学考试
本试卷共8页,20题,满分100分。考试用时75分钟
相对原子质量:H1 Li7 C12 N14 O16 Na23 Al27 Cl35.5 S32 Fe56 Cu64 P31
一、选择题(本题共16小题,每题3分,共48分,每小题只有一个选项符合题意。)
1. 广东是岭南文化的集萃地。下列有关岭南文化的说法不正确的是
A. “海丝文化”:海上丝绸贸易用于交易的银锭中仅存在离子键
B. “茶艺文化”:沏泡功夫茶利用了萃取原理,水作萃取剂
C. “建筑文化”:制作博古梁架时,在木材上雕刻花纹的过程主要发生物理变化
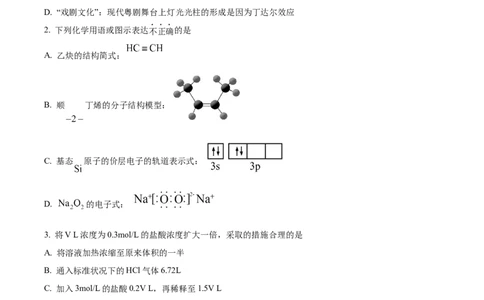
D. “戏剧文化”:现代粤剧舞台上灯光光柱的形成是因为丁达尔效应
2. 下列化学用语或图示表达不正确的是
A. 乙炔的结构简式:
B. 顺 丁烯的分子结构模型:
C. 基态 原子的价层电子的轨道表示式:
D. 的电子式:
3. 将V L浓度为0.3mol/L的盐酸浓度扩大一倍,采取的措施合理的是
A. 将溶液加热浓缩至原来体积的一半
B. 通入标准状况下的HCl气体6.72L
C. 加入3mol/L的盐酸0.2V L,再稀释至1.5V L
D. 加入等体积0.9mol/L的盐酸,混合均匀
4. ClO沸点3.8°C,熔点-116°C,是很好的氯化剂,利用HgO+2Cl =HgCl +ClO可以制备高纯度的ClO。
2 2 2 2 2
下列说法正确的是(N 为阿伏加德罗常数)
A
A. 标准状况下,2.24LCl O含有分子数为0.1N
2 A
B. 0.2mol氯气与足量的HgO反应,转移电子数为0.2N
A
C. HgO与稀硝酸反应的离子方程式为O2-+2H+=H O
2
D. ClO与氢氧化钠溶液反应的离子方程式为ClO+2OH-=Cl-+ClO-+H O
2 2 2
第1页/共9页
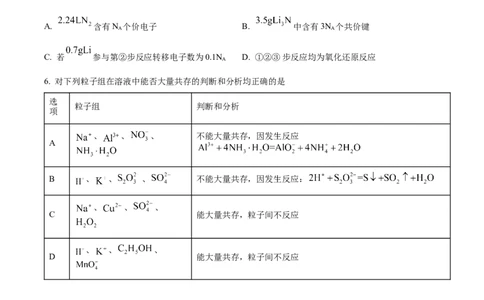
学科网(北京)股份有限公司5. 南京大学科研团队首次发现氨还原过程中的多米诺效应:即一旦完成第①步,将自发完成后续步骤,反
应过程示意图如下。N 表示阿伏加德罗常数的值,下列说法正确的是
A
A. 含有N 个价电子 B. 中含有3N 个共价键
A A
C. 若 参与第②步反应转移电子数为0.1N D. ①②③步反应均为氧化还原反应
A
6. 对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
选
粒子组 判断和分析
项
、 、 、 不能大量共存,因发生反应
A
B 、 、 、 不能大量共存,因发生反应:
、 、 、
C 能大量共存,粒子间不反应
、 、 、
D 能大量共存,粒子间不反应
A. A B. B C. C D. D
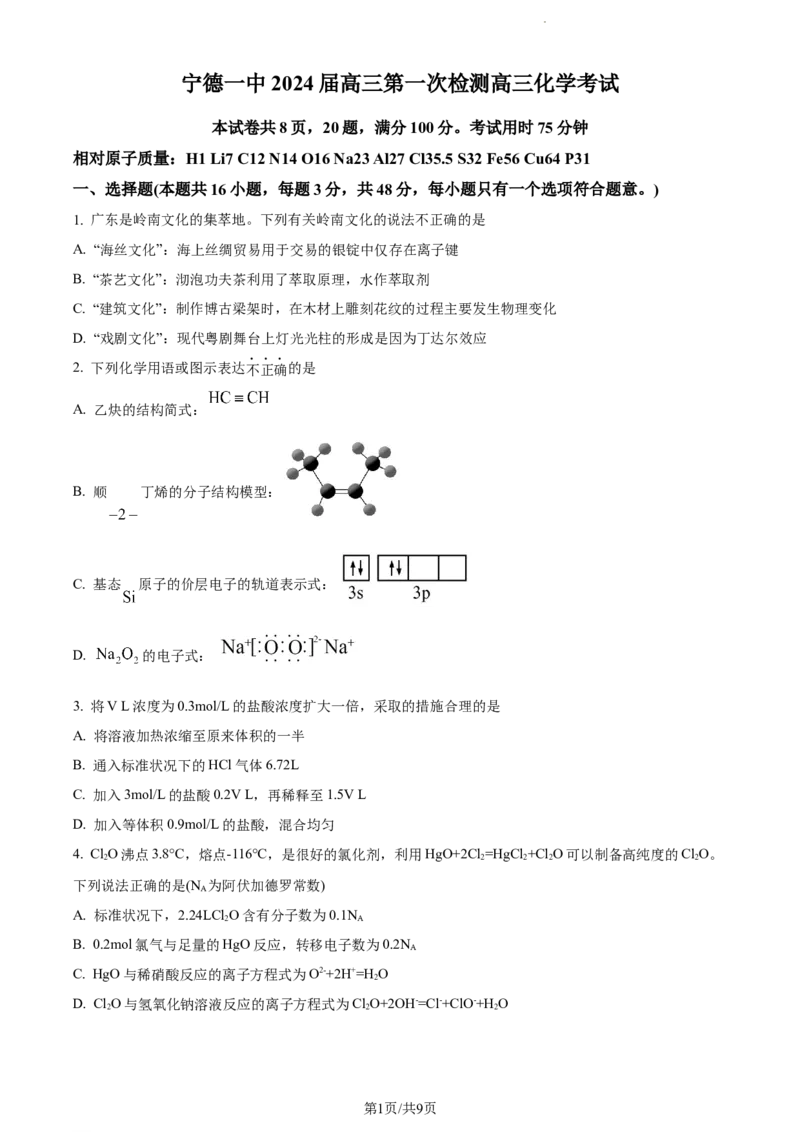
7. 崖柏素具天然活性,有酚的通性,结构如图。关于 崖柏素的说法错误的是
第2页/共9页
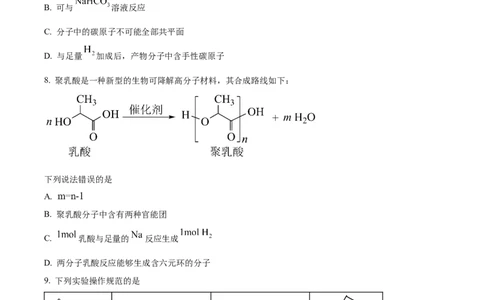
学科网(北京)股份有限公司A. 可与溴水发生取代反应
B. 可与 溶液反应
C. 分子中的碳原子不可能全部共平面
D. 与足量 加成后,产物分子中含手性碳原子
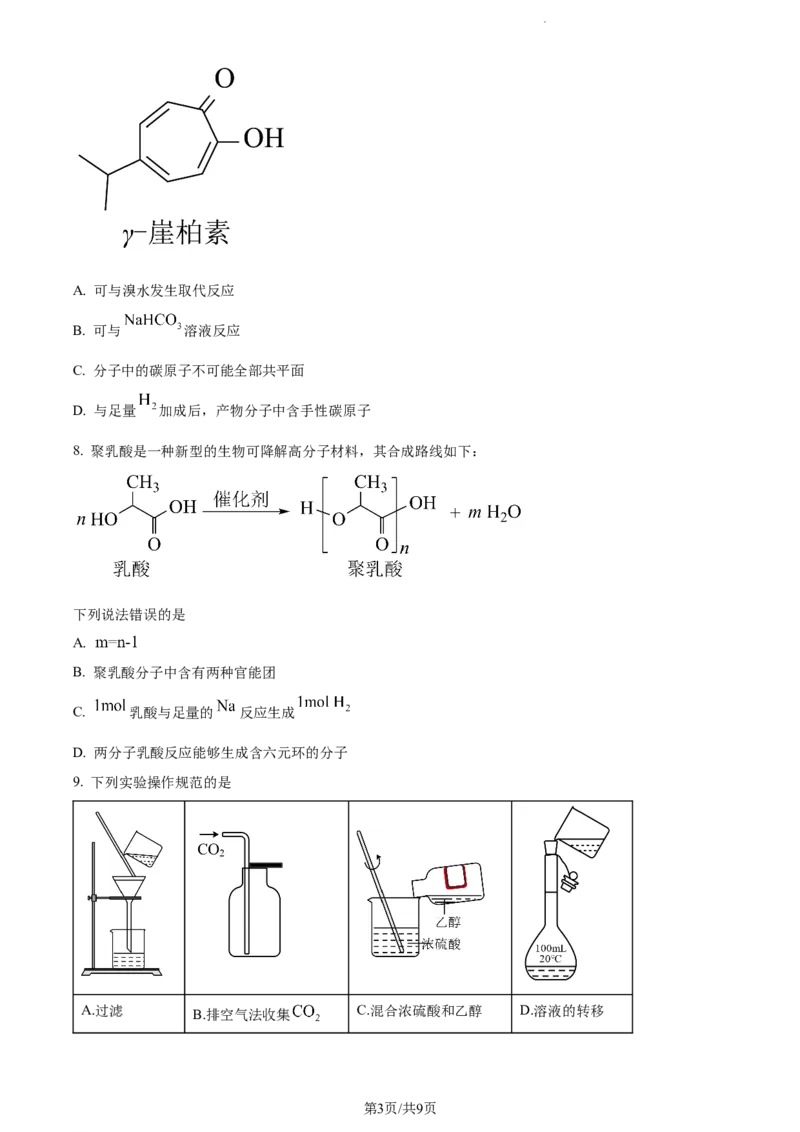
8. 聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法错误的是
A.
B. 聚乳酸分子中含有两种官能团
C. 乳酸与足量的 反应生成
D. 两分子乳酸反应能够生成含六元环的分子
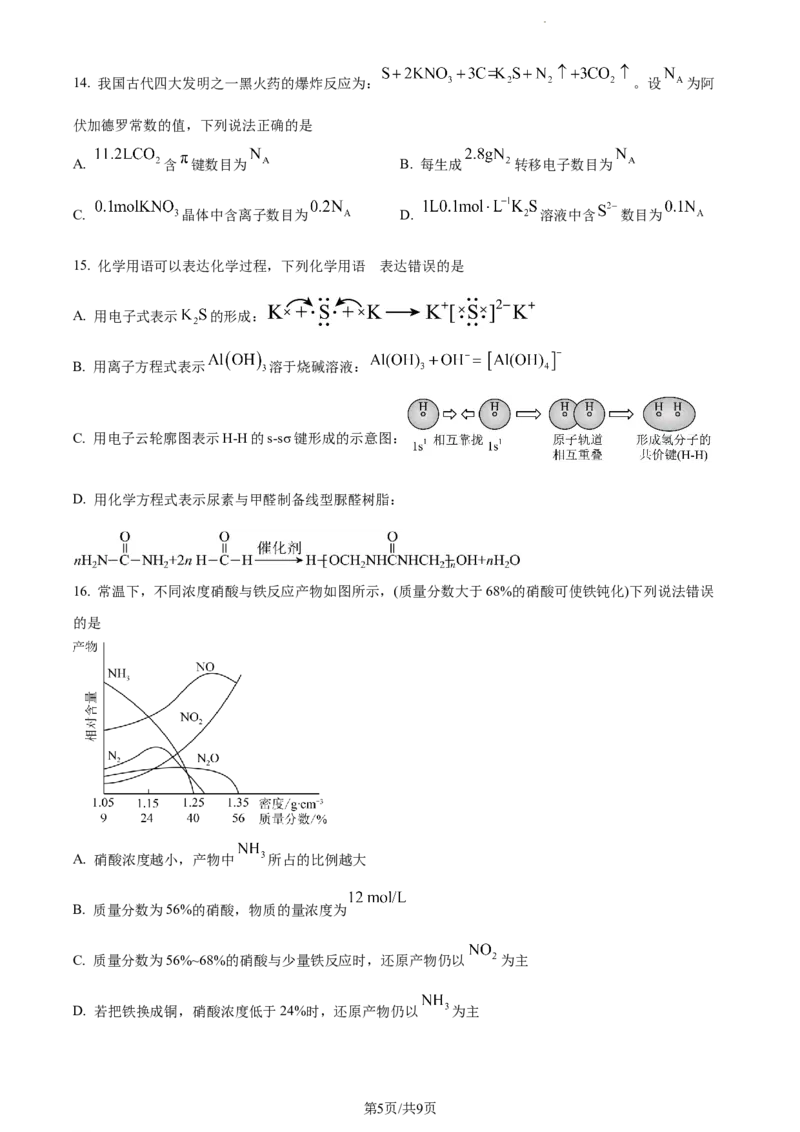
9. 下列实验操作规范的是
A.过滤 C.混合浓硫酸和乙醇 D.溶液的转移
B.排空气法收集
第3页/共9页
学科网(北京)股份有限公司A. A B. B C. C D. D
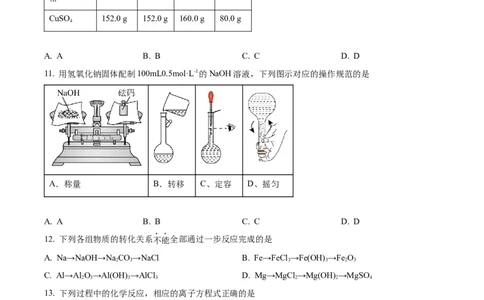
10. 实验中需用1.0mol·L-1的CuSO 溶液950mL,配制时选用容量瓶的规格和称取药品的质量分别为
4
选项 A B C D
容量瓶规
1000 mL 950 mL 1000 mL 500 mL
格
CuSO 152.0 g 152.0 g 160.0 g 80.0 g
4
A. A B. B C. C D. D
11. 用氢氧化钠固体配制100mL0.5mol·L-1的NaOH溶液,下列图示对应的操作规范的是
A.称量 B.转移 C、定容 D、摇匀
A. A B. B C. C D. D
12. 下列各组物质的转化关系不能全部通过一步反应完成的是
A. Na→NaOH→Na CO→NaCl B. Fe→FeCl →Fe(OH) →Fe O
2 3 3 3 2 3
C. Al→Al O→Al(OH) →AlCl D. Mg→MgCl →Mg(OH) →MgSO
2 3 3 3 2 2 4
13. 下列过程中的化学反应,相应的离子方程式正确的是
A. 用碳酸钠溶液处理水垢中的硫酸钙: +CaSO =CaCO +
4 3
B. 酸性高锰酸钾溶液和草酸溶液反应:2 +16H++5 ═2Mn2++10CO ↑+8H O
2 2
C. 硫酸铝溶液中滴加少量氢氧化钾溶液:Al3++4OH-= +2H O
2
D. 氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓
第4页/共9页
学科网(北京)股份有限公司14. 我国古代四大发明之一黑火药的爆炸反应为: 。设 为阿
伏加德罗常数的值,下列说法正确的是
A. 含 键数目为 B. 每生成 转移电子数目为
C. 晶体中含离子数目为 D. 溶液中含 数目为
的
15. 化学用语可以表达化学过程,下列化学用语 表达错误的是
A. 用电子式表示 的形成:
B. 用离子方程式表示 溶于烧碱溶液:
C. 用电子云轮廓图表示H-H的s-sσ键形成的示意图:
D. 用化学方程式表示尿素与甲醛制备线型脲醛树脂:
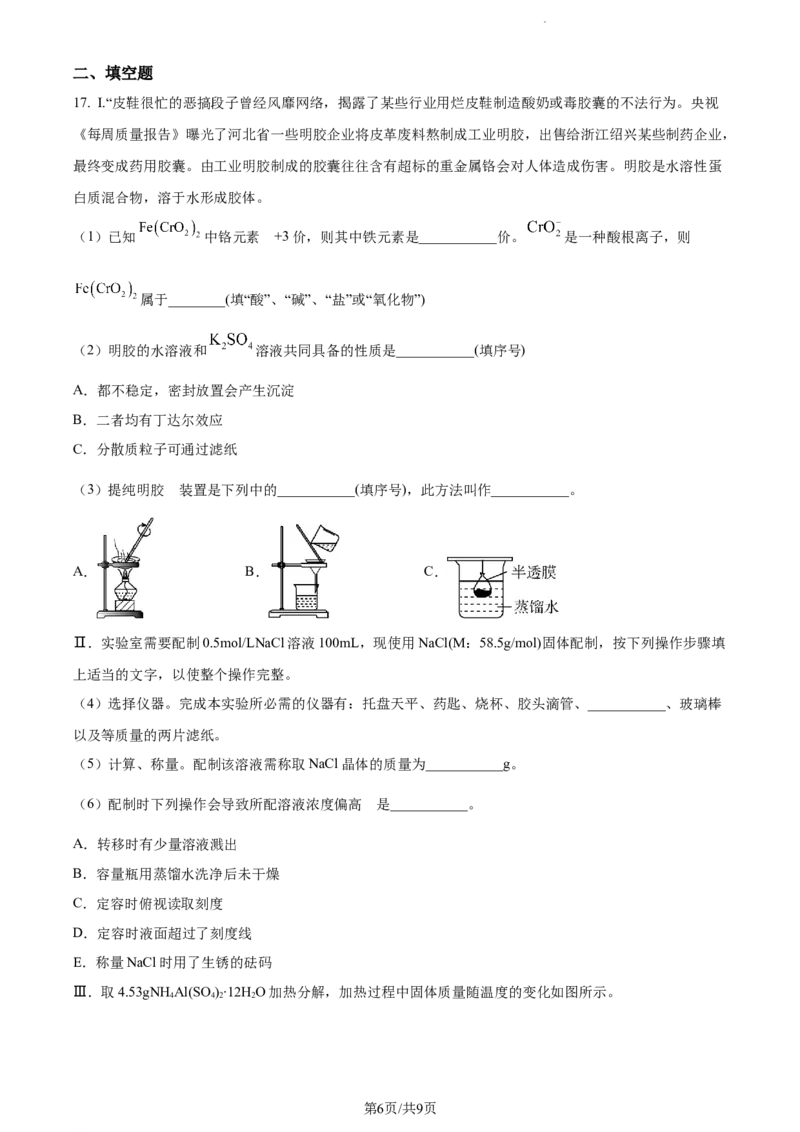
16. 常温下,不同浓度硝酸与铁反应产物如图所示,(质量分数大于68%的硝酸可使铁钝化)下列说法错误
的是
A. 硝酸浓度越小,产物中 所占的比例越大
B. 质量分数为56%的硝酸,物质的量浓度为
C. 质量分数为56%~68%的硝酸与少量铁反应时,还原产物仍以 为主
D. 若把铁换成铜,硝酸浓度低于24%时,还原产物仍以 为主
第5页/共9页
学科网(北京)股份有限公司二、填空题
17. I.“皮鞋很忙的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视
《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,
最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬会对人体造成伤害。明胶是水溶性蛋
白质混合物,溶于水形成胶体。
是
(1)已知 中铬元素 +3价,则其中铁元素是___________价。 是一种酸根离子,则
属于________(填“酸”、“碱”、“盐”或“氧化物”)
(2)明胶的水溶液和 溶液共同具备的性质是___________(填序号)
A.都不稳定,密封放置会产生沉淀
B.二者均有丁达尔效应
C.分散质粒子可通过滤纸
的
(3)提纯明胶 装置是下列中的___________(填序号),此方法叫作___________。
A. B. C.
Ⅱ.实验室需要配制0.5mol/LNaCl溶液100mL,现使用NaCl(M:58.5g/mol)固体配制,按下列操作步骤填
上适当的文字,以使整个操作完整。
(4)选择仪器。完成本实验所必需的仪器有:托盘天平、药匙、烧杯、胶头滴管、___________、玻璃棒
以及等质量的两片滤纸。
(5)计算、称量。配制该溶液需称取NaCl晶体的质量为___________g。
的
(6)配制时下列操作会导致所配溶液浓度偏高 是___________。
A.转移时有少量溶液溅出
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线
E.称量NaCl时用了生锈的砝码
Ⅲ.取4.53gNHAl(SO )∙12H O加热分解,加热过程中固体质量随温度的变化如图所示。
4 4 2 2
第6页/共9页
学科网(北京)股份有限公司的
(7)硫酸铝铵晶体在300℃、633℃分解生成 固体分别为___________、___________。(填化学式)
18. 草酸可作还原剂、沉淀剂、金属除锈剂、织物漂白剂等。实验室用电石(主要成分CaC ,少量CaS杂
2
质)为原料制取HC O·2H O的装置如图所示。已知:CaC +2H O→Ca(OH) +C H↑。请回答下列问题:
2 2 4 2 2 2 2 2 2
(1)装置B中的试剂名称是___________。
(2)装置D的作用是___________。
(3)装置C中生成HC O 的化学方程式为___________。
2 2 4
(4)从装置C中得到产品,需经过蒸发浓缩、冷却结晶、过滤、洗涤及干燥;其中洗涤的具体操作是
___________。
(5)准确称取10.0g产品于锥形瓶中,加入适量蒸馏水溶解,再加入少量稀硫酸,然后用1.00mol·L-1酸性
KMnO 标准洛液进行滴定,消耗标准溶液20.00mL。草酸溶液与酸性高锰酸钾溶液反应的离子方程式为
4
___________(杂质不参与反应),产品中HC O·2H O(摩尔质量为126g/mo1)的质量分数为___________%。
2 2 4 2
19. 硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根( )可看作是 中的一个O原子被S
原子取代的产物。
(1)基态S原子价层电子排布式是___________。
(2)比较S原子和O原子的第一电离能大小,从原子结构的角度说明理由:___________。
(3)同位素示踪实验可证实 中两个S原子的化学环境不同,实验过程为
。过程ii中, 断裂的只有硫硫键,若过程i所用试剂是
第7页/共9页
学科网(北京)股份有限公司Na32SO 和 ,过程ii含硫产物是___________。
2 3
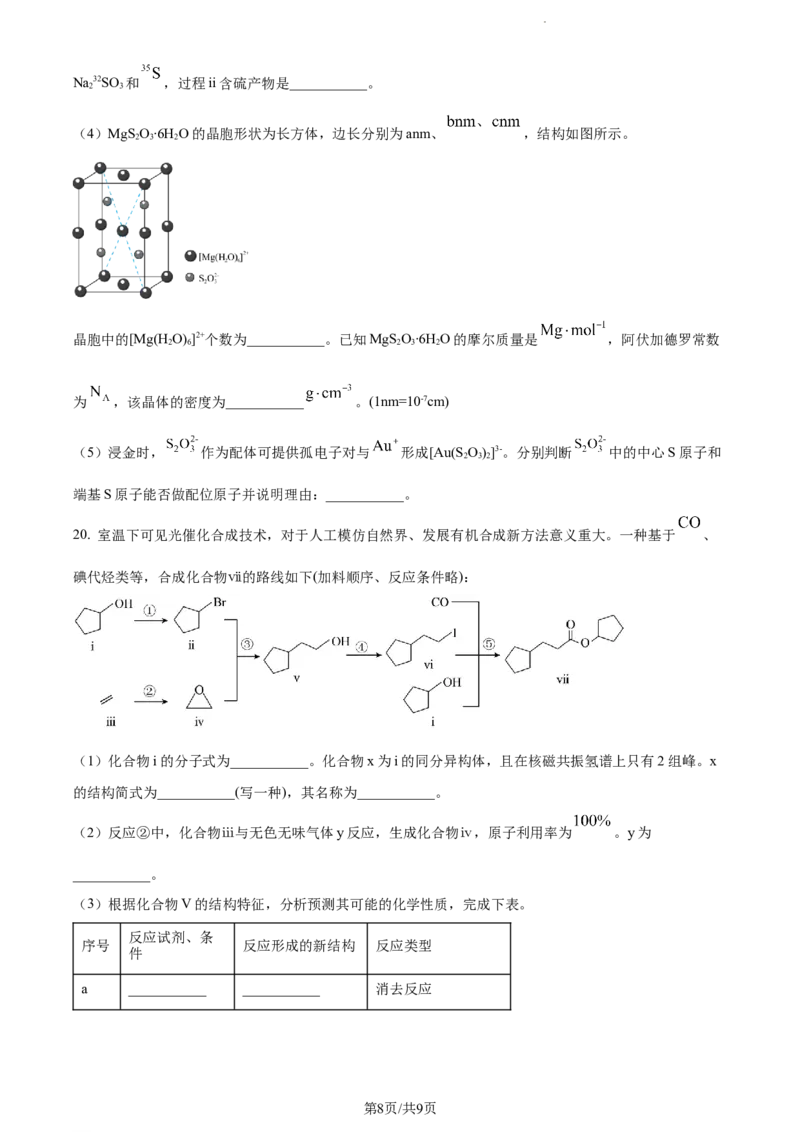
(4)MgS O∙6H O的晶胞形状为长方体,边长分别为anm、 ,结构如图所示。
2 3 2
晶胞中的[Mg(H O) ]2+个数为___________。已知MgS O∙6H O的摩尔质量是 ,阿伏加德罗常数
2 6 2 3 2
为 ,该晶体的密度为___________ 。(1nm=10-7cm)
(5)浸金时, 作为配体可提供孤电子对与 形成[Au(S O)]3-。分别判断 中的中心S原子和
2 3 2
端基S原子能否做配位原子并说明理由:___________。
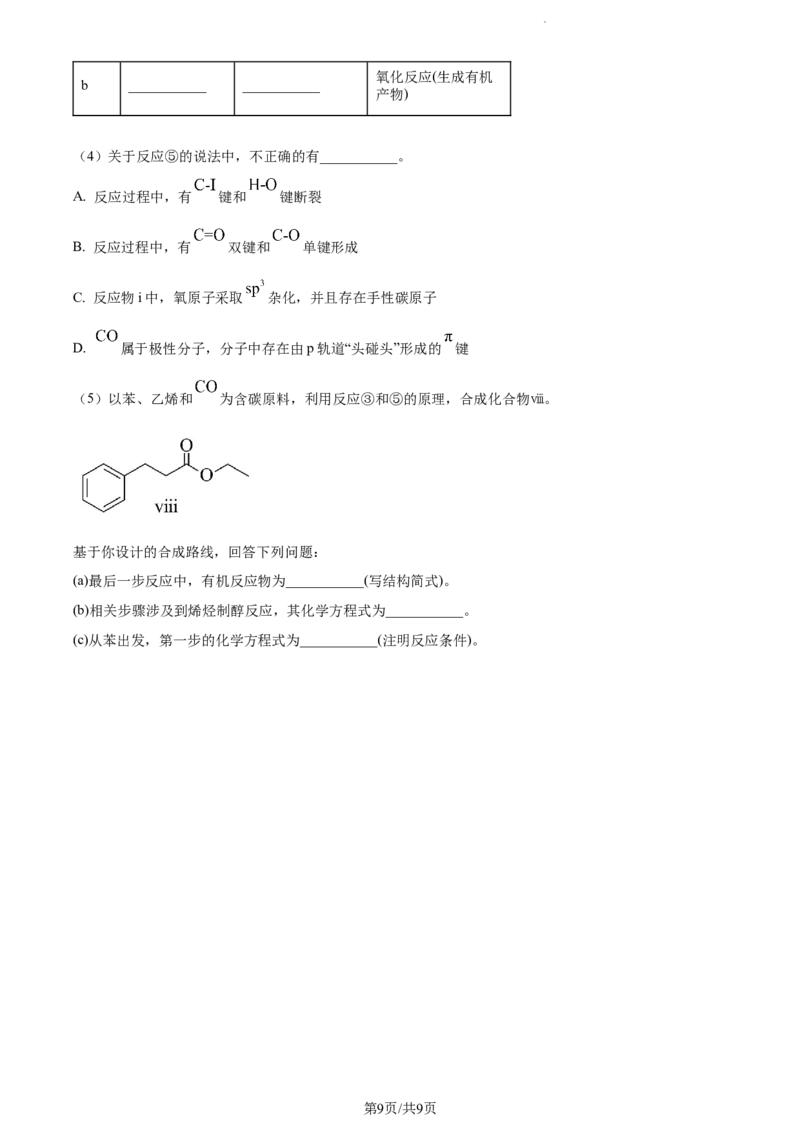
20. 室温下可见光催化合成技术,对于人工模仿自然界、发展有机合成新方法意义重大。一种基于 、
碘代烃类等,合成化合物ⅶ的路线如下(加料顺序、反应条件略):
(1)化合物i的分子式为___________。化合物x为i的同分异构体,且在核磁共振氢谱上只有2组峰。x
的结构简式为___________(写一种),其名称为___________。
(2)反应②中,化合物ⅲ与无色无味气体y反应,生成化合物ⅳ,原子利用率为 。y为
___________。
(3)根据化合物V的结构特征,分析预测其可能的化学性质,完成下表。
反应试剂、条
序号 反应形成的新结构 反应类型
件
a ___________ ___________ 消去反应
第8页/共9页
学科网(北京)股份有限公司氧化反应(生成有机
b ___________ ___________
产物)
(4)关于反应⑤的说法中,不正确的有___________。
A. 反应过程中,有 键和 键断裂
B. 反应过程中,有 双键和 单键形成
C. 反应物i中,氧原子采取 杂化,并且存在手性碳原子
D. 属于极性分子,分子中存在由p轨道“头碰头”形成的 键
(5)以苯、乙烯和 为含碳原料,利用反应③和⑤的原理,合成化合物ⅷ。
基于你设计的合成路线,回答下列问题:
(a)最后一步反应中,有机反应物为___________(写结构简式)。
(b)相关步骤涉及到烯烃制醇反应,其化学方程式为___________。
(c)从苯出发,第一步的化学方程式为___________(注明反应条件)。
第9页/共9页
学科网(北京)股份有限公司