文档内容
选择性必修1 第一章 第二节 反应热的计算 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
1. 已知25 ℃、101 kPa下,1 mol水蒸发为水蒸气需要吸热44.01 kJ。
2HO(l)===2H (g)+O(g) ΔH=+571.66 kJ·mol-1
2 2 2
C(s)+HO(g)===CO(g)+H(g) ΔH=+131.29 kJ·mol-1
2 2
则反应C(s)+O(g)===CO(g)的反应热为( )
2
A.ΔH=-396.36 kJ·mol-1 B.ΔH=-198.55 kJ·mol-1
C.ΔH=-154.54 kJ·mol-1 D.ΔH=-110.53 kJ·mol-1
2. 白磷在氧气中燃烧的能量变化如图所示,下列说法正确的是( )
A.ΔH 是白磷的燃烧热
1
B. 图示中ΔH = ΔH+ΔH
3 1 2
C.+3价磷的氧化物被氧化是吸热反应
D.1 mol白磷在氧气中完全燃烧放出的热量为ΔH
3
3. 在1 200 ℃时,天然气脱硫工艺中会发生下列反应:
①HS(g)+O(g)==SO (g)+HO(g) ΔH
2 2 2 2 1
②2HS(g)+SO (g)== S(g)+2HO(g) ΔH
2 2 2 2 2
③HS(g)+O(g) ==S(g)+HO(g) ΔH
2 2 2 3
④2S(g) == S(g) ΔH,则ΔH 的正确表达式为( )
2 4 4
A.ΔH=(ΔH+ΔH-3ΔH) B.ΔH=(3ΔH-ΔH-ΔH)
4 1 2 3 4 3 1 2
C.ΔH=(ΔH+ΔH-3ΔH) D.ΔH=(ΔH-ΔH-3ΔH)
4 1 2 3 4 1 2 3
4. 发射火箭时使用的燃料可以是液氢和液氧,已知下列热化学方程式:
①H(g)+O(g)==HO(l) ΔH=-285.8 kJ·mol-1
2 2 2 1
②H(g)==H(l) ΔH=-0.92kJ·mol-1
2 2 2
③O(g)==O(l)ΔH=-6.84 kJ·mol-1
2 2 3
④HO(l)==HO(g) ΔH=+44.0 kJ·mol-1
2 2 4
则反应H(l)+O(l)==HO(g)的反应热ΔH为( )
2 2 2
A.+237.46 kJ·mol-1 B.-474.92 kJ·mol-1
C.-118.73 kJ·mol-1 D.-237.46 kJ·mol-1
5. 已知:△(g)+H(g)→CH CHCH(g) ΔH=-157 kJ·mol-1。已知环丙烷(g)的燃烧热ΔH=-2
2 3 2 3
092 kJ·mol-1,丙烷(g)的燃烧热ΔH=-2 220 kJ·mol-1,1 mol液态水蒸发为气态水的焓变为ΔH
=+44 kJ·mol-1。则2 mol氢气完全燃烧生成气态水的ΔH(kJ·mol-1)为( )
A.-658 B.-482 C.-329 D.-285
6. Li/Li O体系的能量循环如图所示。下列说法正确的是( )
2
A.ΔH<0
3
1
学科网(北京)股份有限公司B.ΔH+ΔH+ΔH=ΔH
3 4 5 6
C.ΔH>ΔH
6 5
D.ΔH+ΔH+ΔH+ΔH+ΔH+ΔH=0
1 2 3 4 5 6
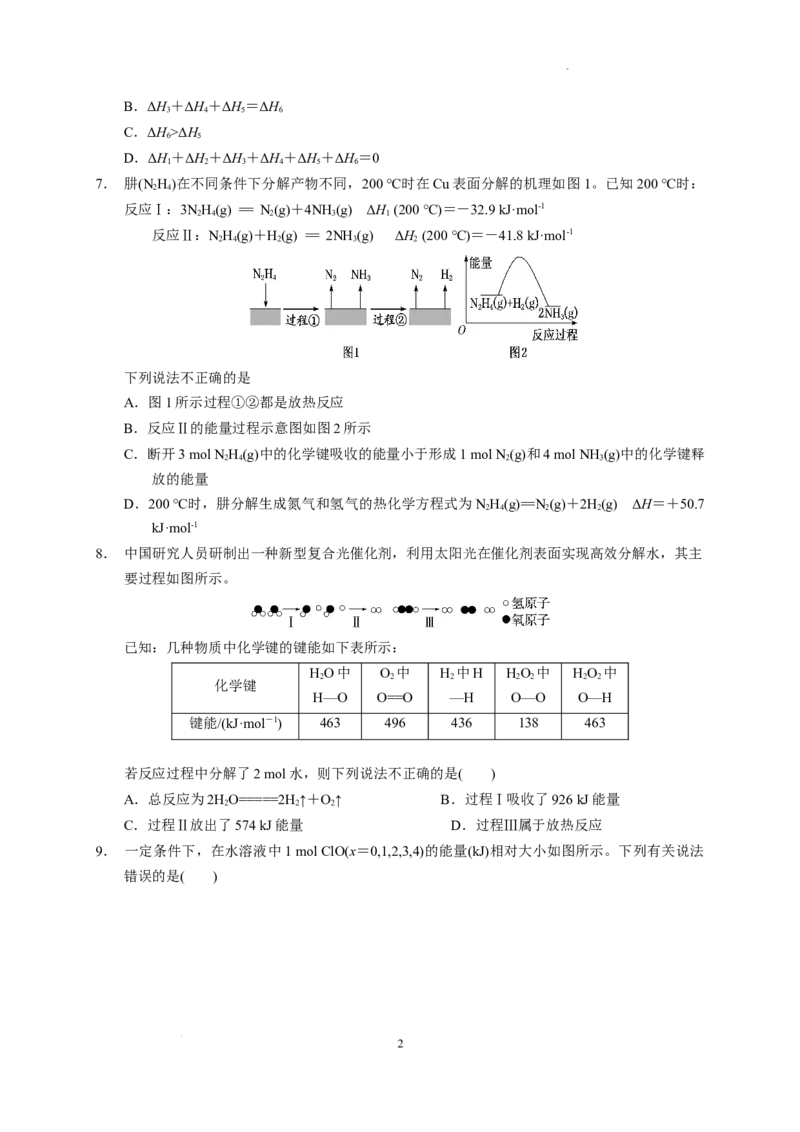
7. 肼(N H)在不同条件下分解产物不同,200 ℃时在Cu表面分解的机理如图1。已知200 ℃时:
2 4
反应Ⅰ:3NH(g) == N(g)+4NH (g) ΔH (200 ℃)=-32.9 kJ·mol-1
2 4 2 3 1
反应Ⅱ:NH(g)+H(g) == 2NH (g) ΔH (200 ℃)=-41.8 kJ·mol-1
2 4 2 3 2
下列说法不正确的是
A.图1所示过程①②都是放热反应
B.反应Ⅱ的能量过程示意图如图2所示
C.断开3 mol N H(g)中的化学键吸收的能量小于形成1 mol N (g)和4 mol NH (g)中的化学键释
2 4 2 3
放的能量
D.200 ℃时,肼分解生成氮气和氢气的热化学方程式为NH(g)==N(g)+2H(g) ΔH=+50.7
2 4 2 2
kJ·mol-1
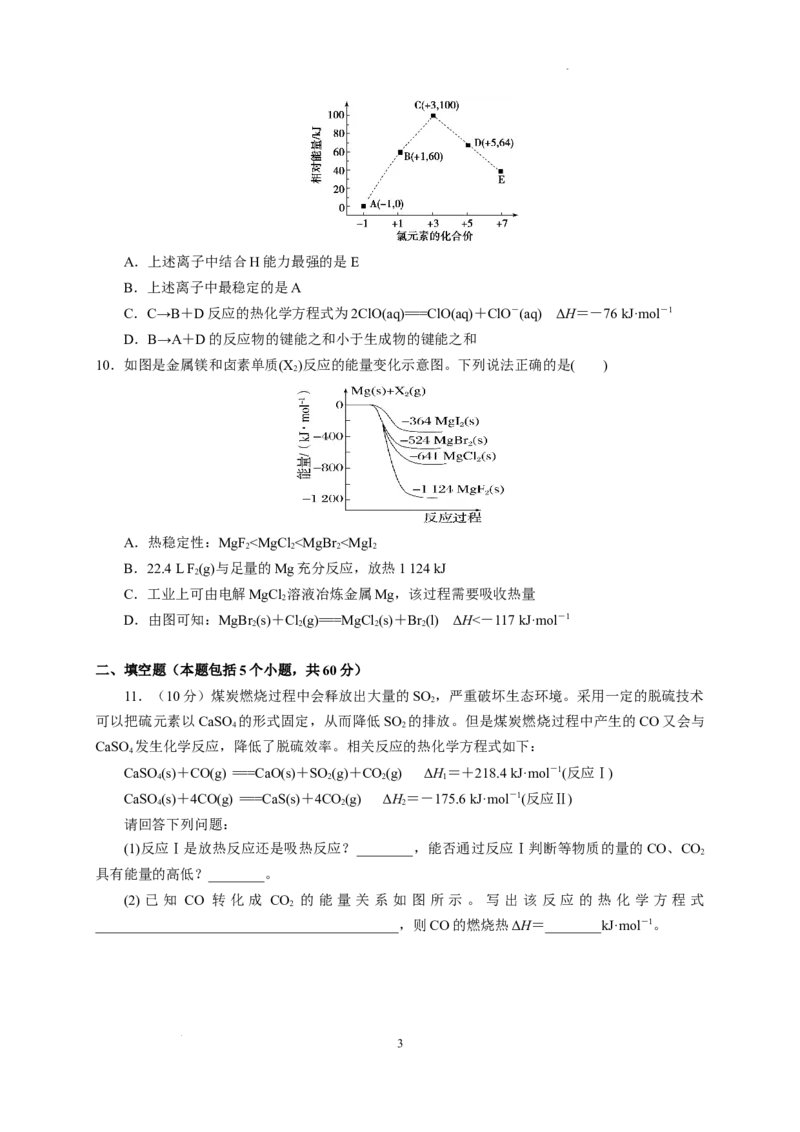
8. 中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,其主
要过程如图所示。
已知:几种物质中化学键的键能如下表所示:
HO中 O 中 H 中H HO 中 HO 中
2 2 2 2 2 2 2
化学键
H—O O==O —H O—O O—H
键能/(kJ·mol-1) 463 496 436 138 463
若反应过程中分解了2 mol水,则下列说法不正确的是( )
A.总反应为2HO=====2H↑+O↑ B.过程Ⅰ吸收了926 kJ能量
2 2 2
C.过程Ⅱ放出了574 kJ能量 D.过程Ⅲ属于放热反应
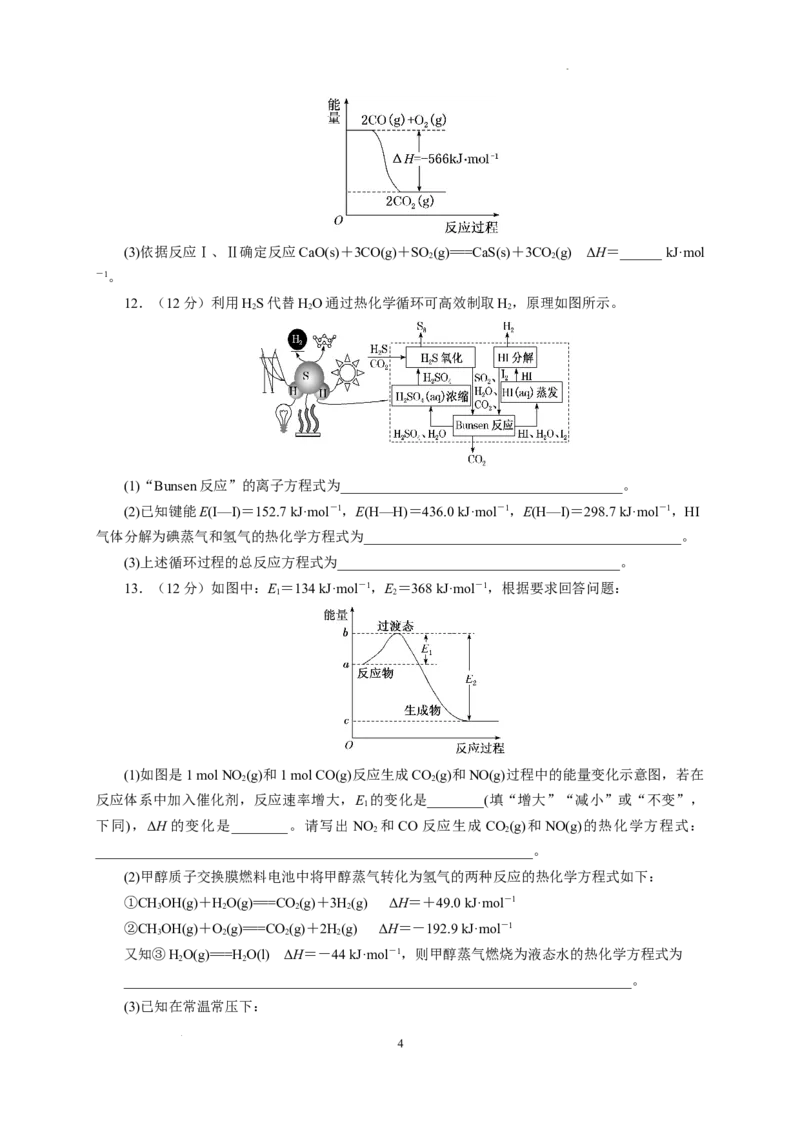
9. 一定条件下,在水溶液中1 mol ClO(x=0,1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法
错误的是( )
2
学科网(北京)股份有限公司A.上述离子中结合H能力最强的是E
B.上述离子中最稳定的是A
C.C→B+D反应的热化学方程式为2ClO(aq)===ClO(aq)+ClO-(aq) ΔH=-76 kJ·mol-1
D.B→A+D的反应物的键能之和小于生成物的键能之和
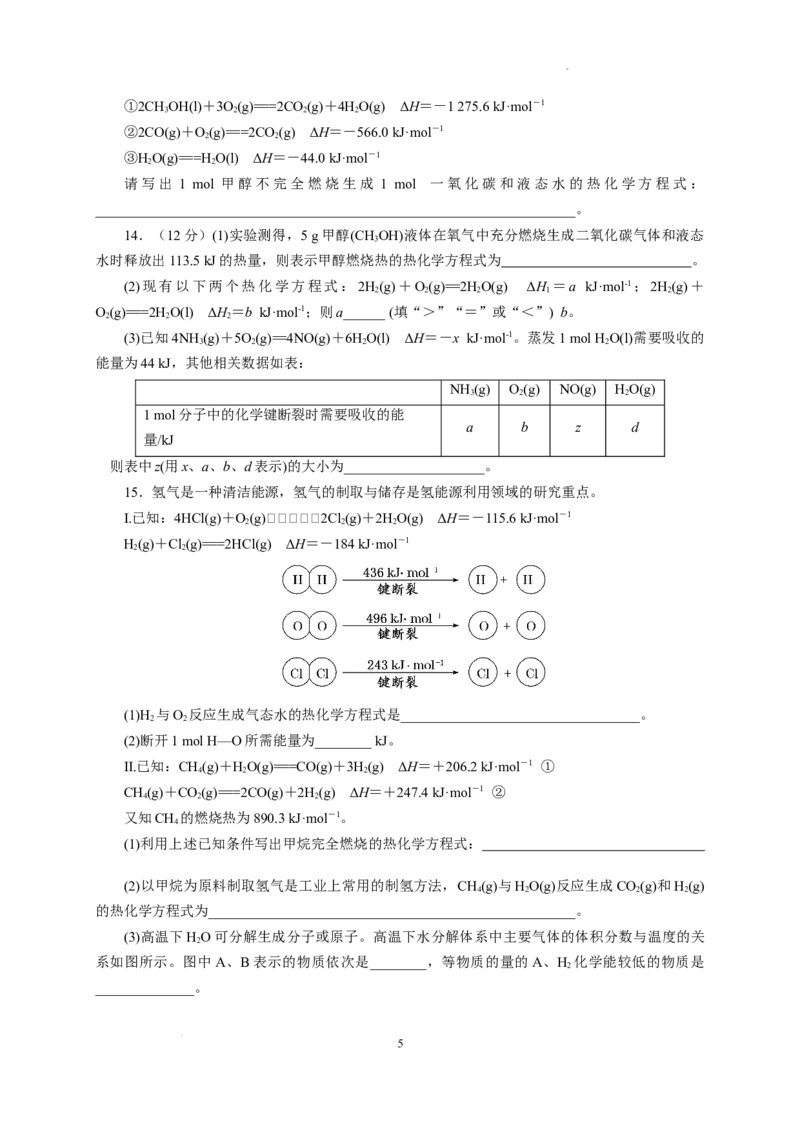
10.如图是金属镁和卤素单质(X )反应的能量变化示意图。下列说法正确的是( )
2
A.热稳定性:MgF 0,A项
2 3
错误;物质含有的能量只与物质的始态与终态有关,与反应途径无关,根据物质转化关系可知,
6
学科网(北京)股份有限公司ΔH+ΔH+ΔH+ΔH+ΔH=ΔH,B、D两项错误;ΔH+ΔH+ΔH+ΔH+ΔH=ΔH,ΔH>0,
1 2 3 4 5 6 1 2 3 4 5 6 1
ΔH>0,ΔH>0,ΔH>0,所以ΔH>ΔH,C项正确。
2 3 4 6 5
7.答案 A
解析:过程②是NH 在催化剂作用下分解生成N 和H,根据盖斯定律,由反应Ⅰ-3×反应Ⅱ,得:
3 2 2
2NH (g) == N(g)+3H(g) ΔH=ΔH-3ΔH=(-32.9+3×41.8)kJ·mol-1=+92.5 kJ·mol-1,故过程②
3 2 2 1 2
是吸热反应,A错误;反应Ⅱ是放热反应,能量过程示意图正确,B正确;放热反应中,反应物的
化学键的键能之和小于生成物的化学键的键能之和,C正确;根据盖斯定律,由反应Ⅰ-2×反应Ⅱ,
得:NH(g) ==N(g)+2H(g) ΔH=+50.7 kJ·mol-1,D正确。
2 4 2 2
8.答案 D
解析 由图可知,总反应为水分解生成氢气和氧气,实现了光能向化学能的转化,反应的化学方程
式为2HO=====2H↑+O↑,故A正确;过程Ⅰ为2 mol H O分子变成2 mol氢原子和2 mol羟基的
2 2 2 2
过程,吸收的能量为463 kJ·mol-1×2 mol=926 kJ,故B正确;过程Ⅱ为
2 mol氢原子和2 mol羟基生成1 mol氢气和1 mol过氧化氢,放出的能量为436 kJ+138 kJ=574
kJ,故C正确;过程Ⅲ为1 mol过氧化氢生成1 mol氧气和1 mol氢气,吸收的能量为463 kJ×2+
138 kJ=1 064 kJ,放出的能量为496 kJ+436 kJ=932 kJ,吸收的能量大于放出的能量,该过程为吸
热反应,故D错误。
9.答案 A
解析:酸根离子对应的酸越弱,结合氢离子能力越强,E对应的是ClO,HClO 是最强的无机酸,
4
酸根离子结合氢离子能力最弱,错误;B项,据能量越低越稳定原理知,A最稳定,正确;C项,
ΔH=生成物的总能量-反应物的总能量=(64+60-2×100)kJ·mol-1=-76 kJ·mol-1,所以C―→B
+D反应的热化学方程式为2ClO(aq)===ClO(aq)+ClO-(aq) ΔH=-76 kJ·mol-1,正确;D项,
3ClO-(aq)===2Cl-(aq)+ClO(aq)的ΔH=(0+64-3×60)kJ·mol-1=-116 kJ·mol-1,所以反应物的键
能之和小于生成物的键能之和,D正确。
10.答案 D
解析 物质的能量越低,其稳定性越强,根据图示可知,物质的稳定性:MgF >MgCl >MgBr >
2 2 2
MgI ,A项错误;未指明气体所处的状态,无法计算F(g)的物质的量,因此不能计算反应放出的热
2 2
量,B项错误;工业上可由电解熔融MgCl 冶炼金属Mg,该过程需要吸收热量,C项错误;根据
2
图示可知①MgCl (s)===Mg(s)+Cl(g) ΔH=+641 kJ·mol-1,②MgBr (s)===Mg(s)+Br (g) ΔH=
2 2 2 2
+524 kJ·mol-1,由②-①可得MgBr (s)+Cl(g)===MgCl (s)+Br (g) ΔH=-117 kJ·mol-1,物质由
2 2 2 2
气态变为液态,会放出热量,所以MgBr (s)+Cl(g)===MgCl (s)+Br (l) ΔH<-117 kJ·mol-1,D项
2 2 2 2
正确。
11. 答案:(1)吸热反应 否
(2)2CO(g)+O(g)===2CO (g) ΔH=-566 kJ·mol-1 -283
2 2
(3)-394
解析:(1)反应Ⅰ的ΔH>0,故反应为吸热反应;通过反应Ⅰ只能判断反应物总能量低于生成物总能
1
量,不能判断某一反应物与某一生成物之间的能量的相对大小。
(2)由图可知2CO(g)+O(g)===2CO (g) ΔH=-566 kJ·mol-1,则CO的燃烧热ΔH=×(-566
2 2
7
学科网(北京)股份有限公司kJ·mol-1)=-283 kJ·mol-1。
(3)利用盖斯定律将反应Ⅱ减去反应Ⅰ可得目标热化学方程式,其ΔH=(-175.6-218.4)kJ·mol
-1=-394 kJ·mol-1。
12.答案:(1)SO +I+2HO===4H++2I-+SO
2 2 2
(2)2HI(g) ===I (g)+H(g) ΔH=+8.7 kJ·mol-1
2 2
(3)8H S=====8H+S
2 2 8
解析:(1)由图可知,“Bunsen反应”的反应物为SO 、I 、HO,生成物为HI和HSO ,离子方程
2 2 2 2 4
式为SO +I +2HO===4H++SO+2I-。(2)ΔH=反应物总键能-生成物总键能,故该反应的热化
2 2 2
学方程式为2HI(g)I (g)+H(g) ΔH=(298.7×2-152.7-436.0)kJ·mol-1=+8.7 kJ·mol-1。(3)由
2 2
图可知,反应物HS最终转化成了H 和S,则循环过程的总反应为8HS=====8H+S。
2 2 8 2 2 8
13.答案:(1)减小 不变 NO (g)+CO(g)===CO (g)+NO(g) ΔH=-234 kJ·mol-1
2 2
(2)CH OH(g)+O(g)===CO (g)+2HO(l) ΔH=-764.7 kJ·mol-1
3 2 2 2
(3)CH OH(l)+O(g)===CO(g)+2HO(l) ΔH=-442.8 kJ·mol-1
3 2 2
解析:(1)观察图像,E 为反应的活化能,加入催化剂降低反应的活化能,但是 ΔH不变;1 mol
1
NO (g)和1 mol CO(g)反应生成CO 和NO的反应热数值即反应物和生成物的能量差,因此该反应的
2 2
热化学方程式为NO (g)+CO(g)===CO (g)+NO(g) ΔH=-234 kJ·mol-1。
2 2
(2)观察热化学方程式,利用盖斯定律,将所给热化学方程式作如下运算:②×3-①×2+
③×2,即可求出甲醇蒸气燃烧的热化学方程式。
(3)根据盖斯定律,由(①-②+③×4)×得CHOH(l)+O(g)===CO(g)+2HO(l) ΔH=-442.8
3 2 2
kJ·mol-1。
14.答案: (1)CHOH(l)+O(g)===CO (g)+2HO(l) ΔH=-726.4 kJ·mol-1
3 2 2 2
(2)>
(3)
解析:(1)5 g液态CHOH在氧气中充分燃烧生成CO 气体和液态水时放出113.5 kJ热量,故32 g即
3 2
1 mol液态CHOH在氧气中充分燃烧生成CO 气体和液态水时放出×113.5 kJ=726.4 kJ热量,则表
3 2
示甲醇燃烧热的热化学方程式为CHOH(l)+O(g)===CO (g)+2HO(l) ΔH=-726.4 kJ·mol-1。
3 2 2 2
(2)将两个热化学方程式进行比较,由于HO由气态变成液态放出热量,故ΔH >ΔH ,则a
2 1 2
>b。
(3)根据题意可知蒸发1 mol H O(l)需要吸收的能量为44 kJ,因此6 mol H O(g)变成液态水需
2 2
要放出的能量为6×44 kJ。根据ΔH=反应物的总键能-生成物的总键能可知,在反应 4NH (g)+
3
5O(g)===4NO(g)+6HO(l) ΔH=-x kJ=4a kJ+5b kJ-4z kJ-6d kJ-6×44 kJ,解得z=。
2 2
15.答案:Ⅰ.(1)2H (g)+O(g)===2H O(g) ΔH=-483.6 kJ·mol-1(合理即可)
2 2 2
(2)462.9
Ⅱ.(1)CH(g)+2O(g)===CO (g)+2HO(l) ΔH=-890.3 kJ·mol-1
4 2 2 2
(2)CH (g)+2HO(g)===CO (g)+4H(g) ΔH=+165.0 kJ·mol-1
4 2 2 2
8
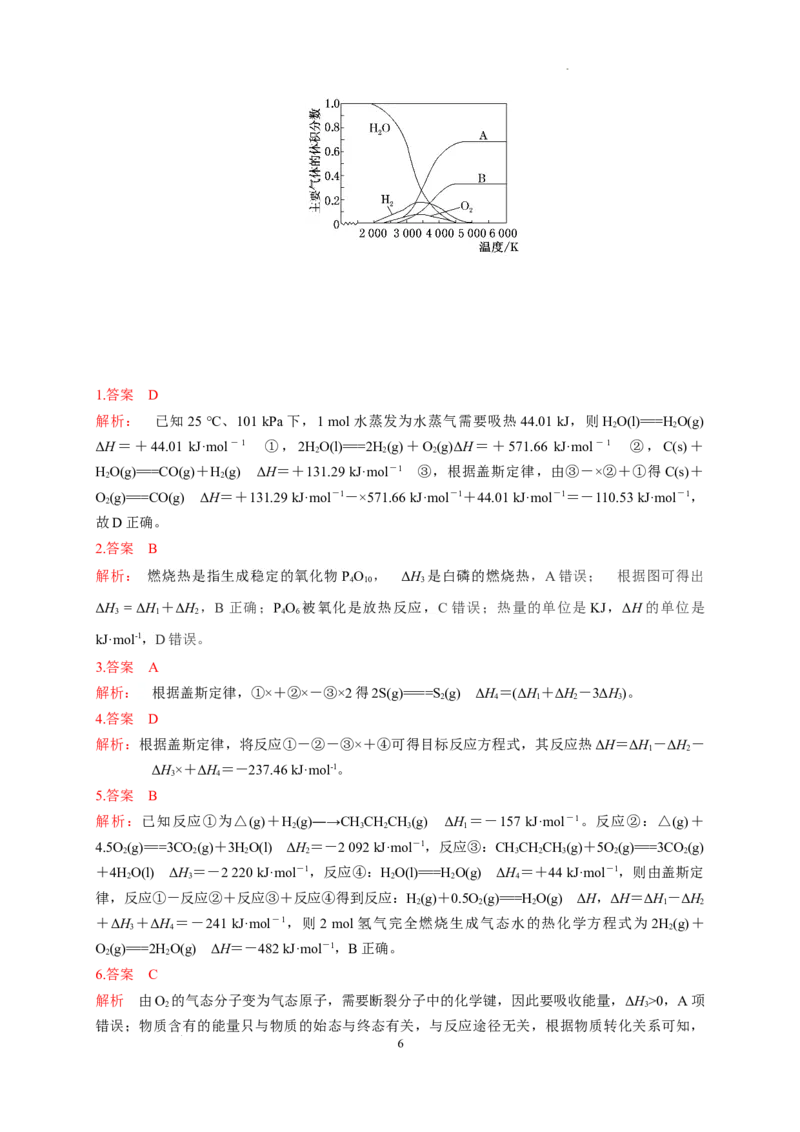
学科网(北京)股份有限公司(3)H、O(或氢原子、氧原子) H
2
解析:Ⅰ.(1)根据盖斯定律,由第一个热化学方程式+第二个热化学方程式×2 可得 2H(g)+
2
O(g)===2H O(g) ΔH=-115.6 kJ·mol-1-184 kJ·mol-1×2=-483.6 kJ·mol-1。(2)反应2H(g)+
2 2 2
O(g)===2H O(g)发生过程中断裂2 mol H—H和1 mol O===O,形成4 mol H—O,则2E(H—H)+
2 2
E(O===O)-4E(H—O)=-483.6 kJ·mol-1,则E(H—O)= kJ·mol-1=462.9 kJ·mol-1,即断开1 mol
H—O所需能量为462.9 kJ。
Ⅱ.(1)由 CH 的燃烧热为 890.3 kJ·mol-1可得甲烷完全燃烧的热化学方程式为 CH(g)+
4 4
2O(g)===CO (g)+2HO(l) ΔH=-890.3 kJ·mol-1。(2)根据盖斯定律,由①×2-②即可得到CH(g)
2 2 2 4
+2HO(g)===CO (g)+4H(g) ΔH=+165.0 kJ·mol-1。(3)观察图像信息知,高温时水先分解生成
2 2 2
H、O,然后两种单质分子可继续分解成氢原子、氧原子,由于氢原子比氧原子多,故A是氢原子,
2 2
B是氧原子。氢气分子分解成氢原子时需要吸收能量,故化学能较低的物质是氢气分子。
9
学科网(北京)股份有限公司10
学科网(北京)股份有限公司