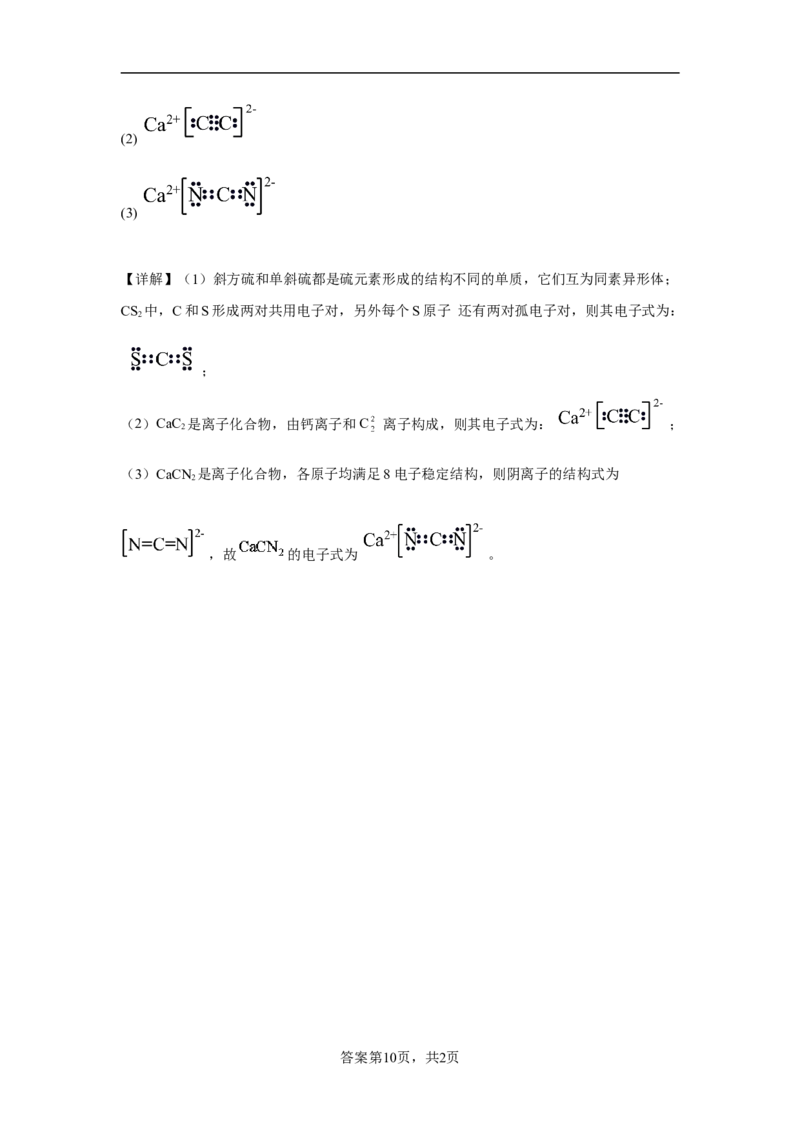文档内容
第七章第二节乙烯与有机高分子材料小题训练--人教版
(2019)必修第二册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
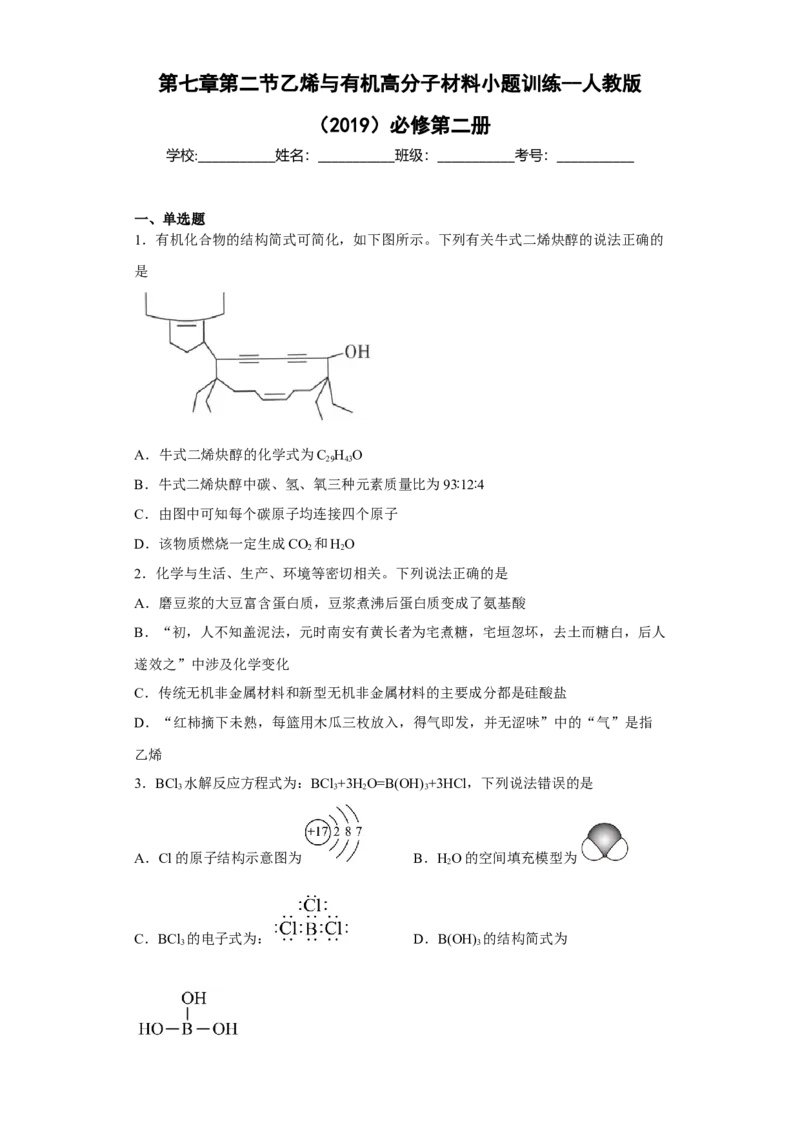
1.有机化合物的结构简式可简化,如下图所示。下列有关牛式二烯炔醇的说法正确的
是
A.牛式二烯炔醇的化学式为C H O
29 43
B.牛式二烯炔醇中碳、氢、氧三种元素质量比为93∶12∶4
C.由图中可知每个碳原子均连接四个原子
D.该物质燃烧一定生成CO 和HO
2 2
2.化学与生活、生产、环境等密切相关。下列说法正确的是
A.磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
B.“初,人不知盖泥法,元时南安有黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人
遂效之”中涉及化学变化
C.传统无机非金属材料和新型无机非金属材料的主要成分都是硅酸盐
D.“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”中的“气”是指
乙烯
3.BCl 水解反应方程式为:BCl +3H O=B(OH) +3HCl,下列说法错误的是
3 3 2 3
A.Cl的原子结构示意图为 B.HO的空间填充模型为
2
C.BCl 的电子式为: D.B(OH) 的结构简式为
3 34.2022年的诺贝尔化学奖颁给了K.Barry Sharpless等三位化学家,以表彰他们对“点
击化学”发展做出的贡献。如图为点击化学的经典反应机理。下列说法中正确的是
( 和 都是
烷基)
A.化合物C可发生加成反应 B.化合物B所有原子都在同一条直线上
C.反应中碳原子的杂化方式有2种 D.A、B、C的所有原子均满足8电子结
构
5.化学与生活、生产密切相关。下列说法错误的是
A.华为公司首创的液冷散热技术所用的石墨烯材料是有机高分子材料
B.晶体硅的导电性介于导体和绝缘体之间,常用于制造芯片
C.研发催化剂将 还原为甲醇是促进碳中和的有效途径
D.常用于医用滴眼液的聚乙烯醇易溶于水
6.化学与生活、科技、社会发展息息相关。下列说法正确的是
A.“歼-20”飞机上使用的碳纤维被誉为“新材料之王”,碳纤维属于无机非金属材料
B.用于3D打印材料的光敏树脂是高聚物,高聚物属于纯净物
C.量子通信材料螺旋碳纳米管与石墨互为同位素
D.2022年冬奥部分场馆建筑应用了新材料碲化镉发电玻璃,其中碲和镉均属于主族
元素
7.2022年北京冬奥会体现了绿色奥运、科技奥运的理念。下列说法错误的是
A.火炬“飞扬”使用纯氢做燃料,实现碳排放为零
B.冬奥场馆“冰丝带”使用CO 制冰,比氟利昂更环保
2
C.领奖礼服中的石墨烯发热材料属于有机高分子材料
D.火炬燃料出口处有钠盐涂层,能使火焰呈明亮黄色
8.下列化学用语错误的是
A. 和 互为同素异形体
B.氯化氢的分子结构模型:
试卷第2页,共3页C.由H和Cl形成HCl的过程:
D. 的分子结构式:O=C=O
9.下列化学用语表示错误的是
A.CO 分子的结构模型: B.S原子的结构示意图:
2
C.HO的结构式:H—O—H D.O 的电子式:
2 2
10.化学家已经合成了少量N,关于N 和N 说法正确的是
4 4 2
A.N 的电子式为
2
B.两者互为同素异形体
C.两者化学性质相同
D.N 和N 分子内含有的质子数相等
4 2
11.氯气与水的反应为Cl+H O=HCl+HClO。下列说法正确的是
2 2
A.Cl 的电子式: B.HO中含有非极性键
2 2
C.HCl的分子结构模型: D.HClO为共价化合物
12.乙烷气体中混有乙烯,欲除去乙烯得到纯净、干燥的乙烷,选用的试剂依次为
A.澄清石灰水,浓硫酸 B.酸性KMnO 溶液,浓硫酸
4
C.溴的四氯化碳溶液,碱石灰 D.水,浓硫酸
13.“逐梦苍穹之上,拥抱星辰大海”,航天科技的发展与化学密切相关。下列选项
正确的是
A.“北斗三号”导航卫星搭载计时铷原子钟,铷是第ⅠA族元素
B.“嫦娥五号”探测器配置砷化镓太阳能电池,太阳能电池将化学能直接转化为电能
C.“祝融号”火星车利用正十一烷储能,正十一烷属于不饱和烃
D.“神舟十三号”航天员使用塑料航天面窗,塑料属于无机非金属材料
14.使用化学用语使表述更准确。下列化学用语使用正确的是A. 的结构示意图:
B. 的电离方程式:
C. 的分子结构模型:
D.用电子式表示 的形成过程:
15.下列分子的结构式错误的是
A.Cl:Cl—Cl B.NH : C.CH: D.N:N=N
2 3 4 2
二、填空题
16.现有A、B、C、D、E、F六种短周期主族元素,其相关性质信息如下。
元 元
特征 特征
素 素
A D 在地壳中含量最多
简单氢化物的分子结构模型为
B 第三周期元素,原子最外层电子数为3 E 单质为黄绿色的有毒气体
该元素的某种原子不含中
C 在短周期主族元素中,原子半径最大 F
子
请回答下列问题:
(1)元素D在元素周期表中的位置为___________,其原子的结构示意图为___________。
(2)E和F形成的化合物的电子式为___________,该化合物含有的化学键类型是
___________。
(3)A的简单氢化物,1个分子中含有10个电子,则该氢化物的分子式为___________。
其稳定性___________(填“>”、“<”或“=”)D的简单氢化物的稳定性。
试卷第4页,共3页(4)B的单质与C的最高价氧化物对应的水化物反应的是离子方程式是___________。
(5)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(选填字
母编号)。A.酸性: B. 通入 溶液能产生黄色沉淀
C.氢化物稳定性: D.常温下,E的单质为气态,S的单质
为固态
17.高分子材料在生产、生活中的应用极为广泛,已知高分子材料的相关知识如下。
(1)高分子材料结构示意图:
(2)高分子材料的主要应用:
a、用于制备塑料薄膜
b、用于制备光学仪器
c、用于制备汽车轮胎
请从上述各项中选择出最恰当的选项,将其代号填入下表中。
项 硫化
目 橡胶
结
___________ ___________ ___________
构
用
___________ ___________ ___________
途
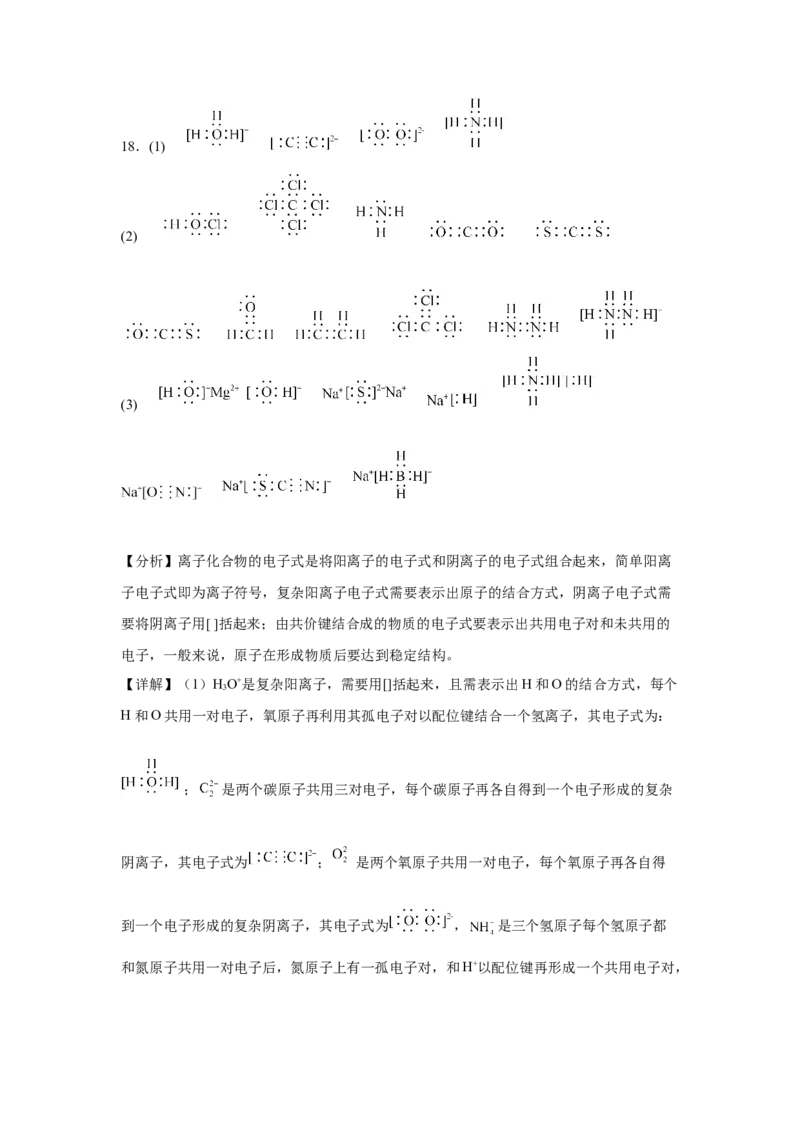
18.按要求书写下列微粒的电子式:
(1) _______, _______, _______, _______。
(2) _______, _______, _______, _______, _______,
_______, _______, _______, _______, _______,
_______。(3) _______, _______, _______, _______,
_______, _______, _______。
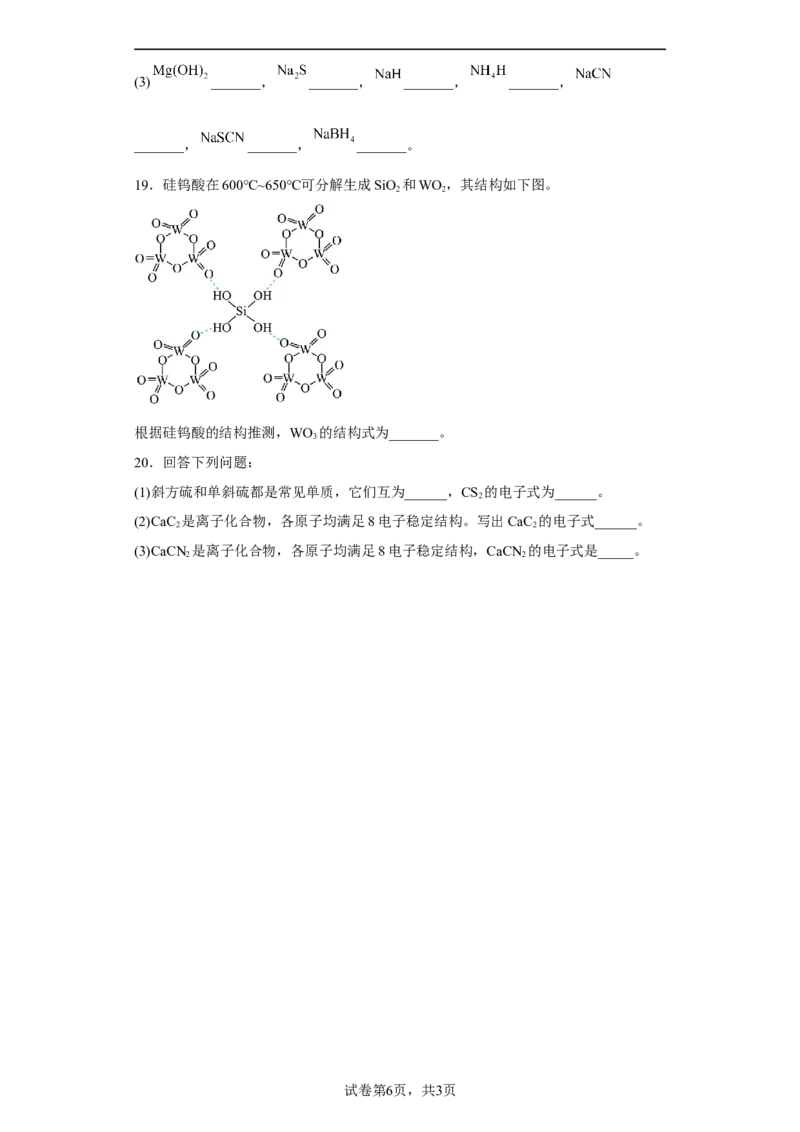
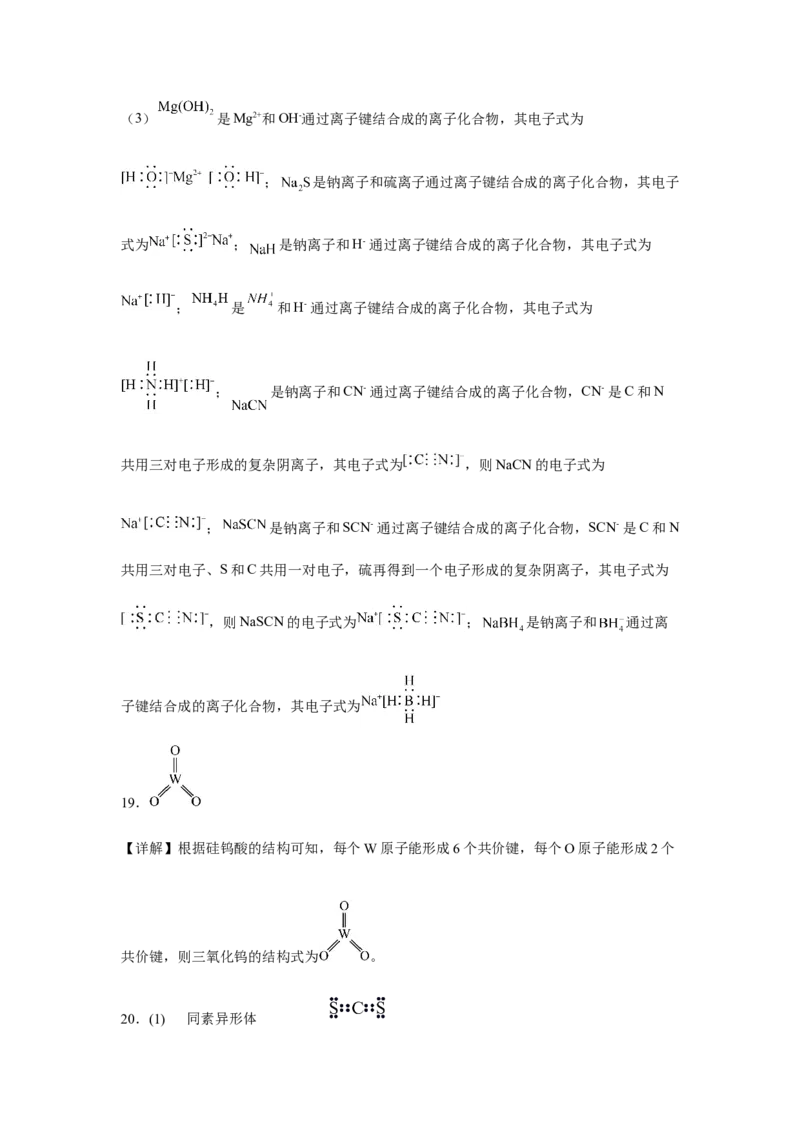
19.硅钨酸在600℃~650℃可分解生成SiO 和WO,其结构如下图。
2 2
根据硅钨酸的结构推测,WO 的结构式为_______。
3
20.回答下列问题:
(1)斜方硫和单斜硫都是常见单质,它们互为______,CS 的电子式为______。
2
(2)CaC 是离子化合物,各原子均满足8电子稳定结构。写出CaC 的电子式______。
2 2
(3)CaCN 是离子化合物,各原子均满足8电子稳定结构,CaCN 的电子式是_____。
2 2
试卷第6页,共3页参考答案:
1.B
【详解】A.该有机物的化学式为C H O,A错误;
31 48
B.该有机物的化学式为C H O,碳、氢、氧三种元素质量比为(12×31)∶48∶16=93∶12∶4,B
31 48
正确;
C.该物质含有碳碳双键和碳碳三键,则并非每个碳原子都连接四个原子,C错误;
D.该物质含碳量很高,燃烧除了生成CO 和HO,还可能生成CO,D错误;
2 2
故选B。
2.D
【详解】A.豆浆煮沸后蛋白质发生了变性,没有水解生成氨基酸,A错误;
B.蔗糖的分离提纯采用了黄泥除色,由此可见黄泥具有的性质是吸附性,该变化是物理
的吸附,属于物理变化,B错误;
C.无机非金属材料分为传统无机非金属材料和新型无机非金属材料两大类,传统无机非
金属材料的主要成分都是硅酸盐,如玻璃、水泥、陶瓷等,新型无机非金属材料是指一些
新型的具有特殊功能的非硅酸盐型材料,C错误;
D.乙烯能作水果的催熟剂,文中的“气”是指乙烯,D正确;
故选D。
3.C
【详解】A.Cl为荷电核数为17,原子结构示意图为 ,A项正确;
B. 分子为V形结构,且O原子的半径比H原子的半径大,B项正确;
C. 是缺电子化合物,B提供3个电子,与3个Cl分别共用1对电子,电子式应为
,C项错误;
D. 的结构简式为 ,D项正确;
答案选C。4.A
【详解】A.化合物C中含有碳碳双键,可以发生加成反应,故A正确;
B.化合物B中含有烷基,所有原子不可能都在同一条直线上,故B错误;
C.该反应中存在碳碳三键、碳碳双键和烷基,碳原子的杂化方式有sp2、sp3、sp共3种,
故C错误;
D.B、C中烷基中H原子满足2电子稳定结构,故D错误;
故选A。
5.A
【详解】A.石墨烯材料是无机非金属材料,A错误;
B.晶体硅的导电性介于导体和绝缘体之间,是良好的半导体,常用于制造芯片,B正确;
C.研发催化剂将 还原为甲醇可充分利用二氧化碳,是促进碳中和的有效途径,C正确;
D.医用滴眼液的聚乙烯醇具有良好水溶性,易溶于水,D正确;
故选A。
6.A
【详解】A.碳纤维由碳元素组成,碳属于非金属元素,“歼-20”飞机上使用的碳纤维属于
新型无机非金属材料,A正确;
B.高聚物中聚合度不确定,所以高聚物属于混合物,B错误;
C.量子通信材料螺旋碳纳米管、石墨均为碳组成的单质,互为同素异形体,C错误;
D.碲属于第五周期ⅥA族元素,镉属于第五周期ⅡB族元素,D错误;
故选A。
7.C
【详解】A. 火炬“飞扬”使用纯氢做燃料,生成物为水,实现碳排放为零,故A正确;
B. 二氧化碳跨临界制冰技术,与传统制冷剂氟利昂相比更加环保,减少了氟利昂对臭氧
层的破坏作用,故B正确;
C. 石墨烯是碳单质属于无机非金属材料,故C错误;
D. 钠的焰色反应为黄色,火炬燃料出口处有钠盐涂层,能使火焰呈明亮黄色,故D正确;
故选C。
8.A
【详解】A. 和 互为同位素,A项错误;
答案第2页,共2页B.物质分子的结构模型包括球棍模型和填充模型,图示为 分子的球棍模型,属于物
质分子的结构模型,B项正确;
C.氯化氢是共价化合物,由H和 形成 的过程: ,C项正确;
D.C原子最外层的4个单电子与2个O原子的最外层的4个单电子形成4对共用电子对,
从而使分子中各个原子都达到最外层8个电子的稳定结构,故 分子的结构式为
,D项正确;
故选A。
9.B
【详解】A.CO 分子中C原子与两个O原子分别形成双键,且C原子半径比O大,CO
2 2
分子的结构模型: ,A不符合;
B.S原子是第16号元素,最外层是6个电子,B符合;
C.HO中O原子与两个H原子形成单键,结构式:H—O—H,C不符合;
2
D.O 的电子式: , D不符合;
2
故B项符合题意。
10.B
【详解】A. 的电子式为 ,A错误;
B. 和 均是N元素的单质,二是互为同素异形体,B正确;
C. 和 的结构不同,化学性质不同,C错误;
D. 分子中含有28个质子, 分子中含有14个质子,D错误;
故选B。
11.D
【详解】A.Cl 的电子式: ,A错误;
2
B.HO中只含有极性键,B错误;
2
C.氢原子原子半径比氯原子小,所以HCl的分子结构模型中两个原子应该是一个半径大,一个半径小,C错误;
D.HClO中只含共价键,是共价化合物,D正确;
故选D。
12.C
【详解】A.常温常压下乙烷、乙烯与澄清石灰水均不反应,不能用于除杂,A错误;
B.乙烯能被酸性 溶液氧化生成 ,会引入新的杂质,B错误;
C.乙烯分子中含有碳碳双键,常温下能与 发生加成反应生成液态的1,2-二溴乙烷而
被除去,乙烷化学性质稳定,与强酸、强碱、强氧化剂均不反应,故可用碱石灰干燥,C
正确;
D.常温常压下乙烷、乙烯与水均不反应,不能用于除杂,D错误;
故选C。
13.A
【详解】A.铷是碱金属,位于第ⅠA族,故A正确;
B.太阳能电池是将太阳能转化为电能,故B错误;
C.正十一烷属于饱和烃,故C错误;
D.塑料属于有机合成材料,故D错误;
故选A。
14.C
【详解】A.S是16号元素,硫离子带有2个负电荷,其结构示意图为: ,
A错误;
B. 属于盐,可以电离出钾离子和氯酸根离子,其电离方程式为:
,B错误;
C. 为正四面体结构,其分子结构模型为: ,C正确;
答案第4页,共2页D. 为共价化合物,则用电子式表示 的形成过程为
,D错误;
故选C。
15.D
【详解】A.Cl 分子中两个氯原子形成了1个共价键,故氯气的结构式为:Cl—Cl,A正
2
确;
B.氨气分子中氮原子和3个氢原子形成了3个共价键,故氨气的结构式为: ,
B正确;
C.甲烷分子中碳原子和4个氢原子形成了4个共价键,故甲烷的结构式为: ,
C正确;
D.氮气分子中2个氮原子形成了3个共价键,故氮气的结构式为: ,D错误;
故本题选D。
16.(1) 第二周期第ⅥA族
(2) 共价键(极性共价键)
(3) <
(4)
(5)BC
【分析】根据A的简单氢化物的球棍模型,A为C;B为Al,C为Na,D为O,E为Cl,F
为H。【详解】(1)D为O,在元素周期表中的位置为:第二周期第ⅥA族,原子结构示意图为
;
(2)E为Cl,F为H ,E和F形成的化合物的电子式为: ,化学键类型为:共价键
(极性共价键);
(3)A为C ,A的简单氢化物,1个分子中含有10个电子,则该氢化物的分子式为:
CH;D为O,简单氢化物为HO,同周期从左往右非金属性增强,气态氢化物的稳定性增
4 2
强,故稳定性CHS。
A.非金属性越强,最高价氧化物的水化物的酸性越强,故酸性:HClO>H SO ,A错误;
4 2 4
B.非金属性越强,对应单质的氧化性越强,故氯气氧化性强于硫,氯气能将硫单质从HS
2
溶液中置换出来,B正确;
C.非金属性越强,简单气态氢化物的稳定性越强,故稳定性HCl>H S,C正确;
2
D.常温下物质的状态与非金属性无关,D错误;
故选BC。
17. Ⅲ Ⅰ Ⅱ c a b
【详解】硫化橡胶是立体网状结构,故对应图像Ⅲ,橡胶用于制备汽车轮胎;聚乙烯是线
型结构,故对应图像Ⅰ,聚乙烯通过加聚反应,可以制得塑料薄膜;
是支链型结构,故对应图像Ⅱ,有机玻璃可以用于制备光学仪器;
答案为:Ⅲ;Ⅰ;Ⅱ;c;a;b。
答案第6页,共2页18.(1)
(2)
(3)
【分析】离子化合物的电子式是将阳离子的电子式和阴离子的电子式组合起来,简单阳离
子电子式即为离子符号,复杂阳离子电子式需要表示出原子的结合方式,阴离子电子式需
要将阴离子用[ ]括起来;由共价键结合成的物质的电子式要表示出共用电子对和未共用的
电子,一般来说,原子在形成物质后要达到稳定结构。
【详解】(1)HO+是复杂阳离子,需要用[]括起来,且需表示出H和O的结合方式,每个
3
H和O共用一对电子,氧原子再利用其孤电子对以配位键结合一个氢离子,其电子式为:
; 是两个碳原子共用三对电子,每个碳原子再各自得到一个电子形成的复杂
阴离子,其电子式为 ; 是两个氧原子共用一对电子,每个氧原子再各自得
到一个电子形成的复杂阴离子,其电子式为 , 是三个氢原子每个氢原子都
和氮原子共用一对电子后,氮原子上有一孤电子对,和H+以配位键再形成一个共用电子对,其电子式为 ;
(2) 是氢原子、氯原子都和氧原子形成一个共用电子对,其电子式为 ;
是每个氯原子都和碳原子共用一对电子生成的共价化合物,其电子式为 ;
是氮原子利用其三个价电子和氢原子形成三个共价键,电子式为 ; 是每个
氧原子都和碳原子共用两对电子形成的,其电子式为 ;S和O是同主族元素,
CS 和CO 结构相似,其电子式为 ; 可以看做是CO 中的一个O被S替
2 2 2
换,其电子式为 ; 中H和O都和碳原子形成共价键,其电子式为
; 两个碳原子间共用两对电子,其电子式为 ; 是碳原子和
氧原子共用两对电子,和每个氯原子都共用一对电子,其电子式为 ; 是
每个氮原子都和另一个氮原子共用一对电子,和两个氢原子共用电子,其电子式为
; 是NH 中的一个氮原子利用其孤电子对和H+以配位键结合,电子式为
2 4
;
答案第8页,共2页(3) 是Mg2+和OH-通过离子键结合成的离子化合物,其电子式为
; 是钠离子和硫离子通过离子键结合成的离子化合物,其电子
式为 ; 是钠离子和H- 通过离子键结合成的离子化合物,其电子式为
; 是 和H- 通过离子键结合成的离子化合物,其电子式为
; 是钠离子和CN- 通过离子键结合成的离子化合物,CN- 是C和N
共用三对电子形成的复杂阴离子,其电子式为 ,则NaCN的电子式为
; 是钠离子和SCN- 通过离子键结合成的离子化合物,SCN- 是C和N
共用三对电子、S和C共用一对电子,硫再得到一个电子形成的复杂阴离子,其电子式为
,则NaSCN的电子式为 ; 是钠离子和 通过离
子键结合成的离子化合物,其电子式为
19.
【详解】根据硅钨酸的结构可知,每个W原子能形成6个共价键,每个O原子能形成2个
共价键,则三氧化钨的结构式为 。
20.(1) 同素异形体(2)
(3)
【详解】(1)斜方硫和单斜硫都是硫元素形成的结构不同的单质,它们互为同素异形体;
CS 中,C和S形成两对共用电子对,另外每个S原子 还有两对孤电子对,则其电子式为:
2
;
(2)CaC 是离子化合物,由钙离子和C 离子构成,则其电子式为: ;
2
(3)CaCN 是离子化合物,各原子均满足8电子稳定结构,则阴离子的结构式为
2
,故 的电子式为 。
答案第10页,共2页