文档内容
必修第一册 第三章 第一节 铁及其化合物 测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题4分,共40分)
1.我国清代《本草纲目拾遗》中叙述了“铁线粉”:“粤中洋行有舶上铁丝,……日久起销,用
刀刮其销,……,所刮下之销末,名铁线粉”。这里的“铁线粉”是指( )
A.Fe B.FeCl C.FeO D.Fe O
3 2 3
2.下列化合物中,不能由单质直接化合得到的是( )
A.FeCl B.FeS C.Fe O D.FeCl
2 3 4 3
3.等量的铁分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气
的体积比是( )
A.1∶1 B.3∶4 C.2∶3 D.4∶3
4.下列离子方程式正确的是( )
A.铁跟FeCl 溶液反应:Fe+Fe3+===2Fe2+
3
B.Fe跟稀盐酸反应:2Fe+6H+===2Fe3++3H
2
C.FeCl 溶液跟Cl 反应:Fe2++Cl===Fe3++2Cl-
2 2 2
D.Fe(OH) 跟盐酸反应:Fe(OH) +3H+===Fe3++3HO
3 3 2
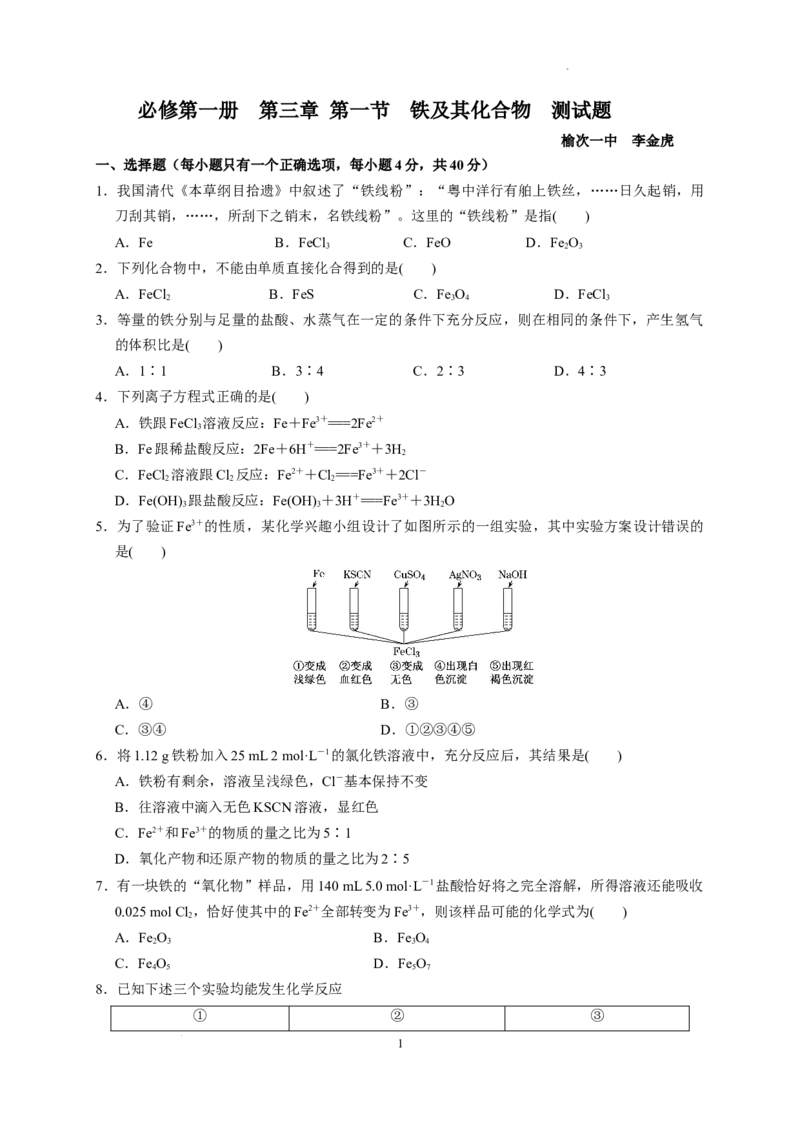
5.为了验证Fe3+的性质,某化学兴趣小组设计了如图所示的一组实验,其中实验方案设计错误的
是( )
A.④ B.③
C.③④ D.①②③④⑤
6.将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是( )
A.铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变
B.往溶液中滴入无色KSCN溶液,显红色
C.Fe2+和Fe3+的物质的量之比为5∶1
D.氧化产物和还原产物的物质的量之比为2∶5
7.有一块铁的“氧化物”样品,用140 mL 5.0 mol·L-1盐酸恰好将之完全溶解,所得溶液还能吸收
0.025 mol Cl ,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
2
A.Fe O B.Fe O
2 3 3 4
C.Fe O D.Fe O
4 5 5 7
8.已知下述三个实验均能发生化学反应
① ② ③
1
学科网(北京)股份有限公司将铁钉放入硫酸铜溶液中 向硫酸亚铁溶液中滴入几滴氯水 将铜丝放入氯化铁溶液中
下列判断正确的是( )
A.实验①中铁钉只作还原剂
B.实验②中Fe2+既显氧化性又显还原性
C.实验③中发生的是置换反应
D.上述实验证明氧化性:Fe3+>Fe2+>Cu2+
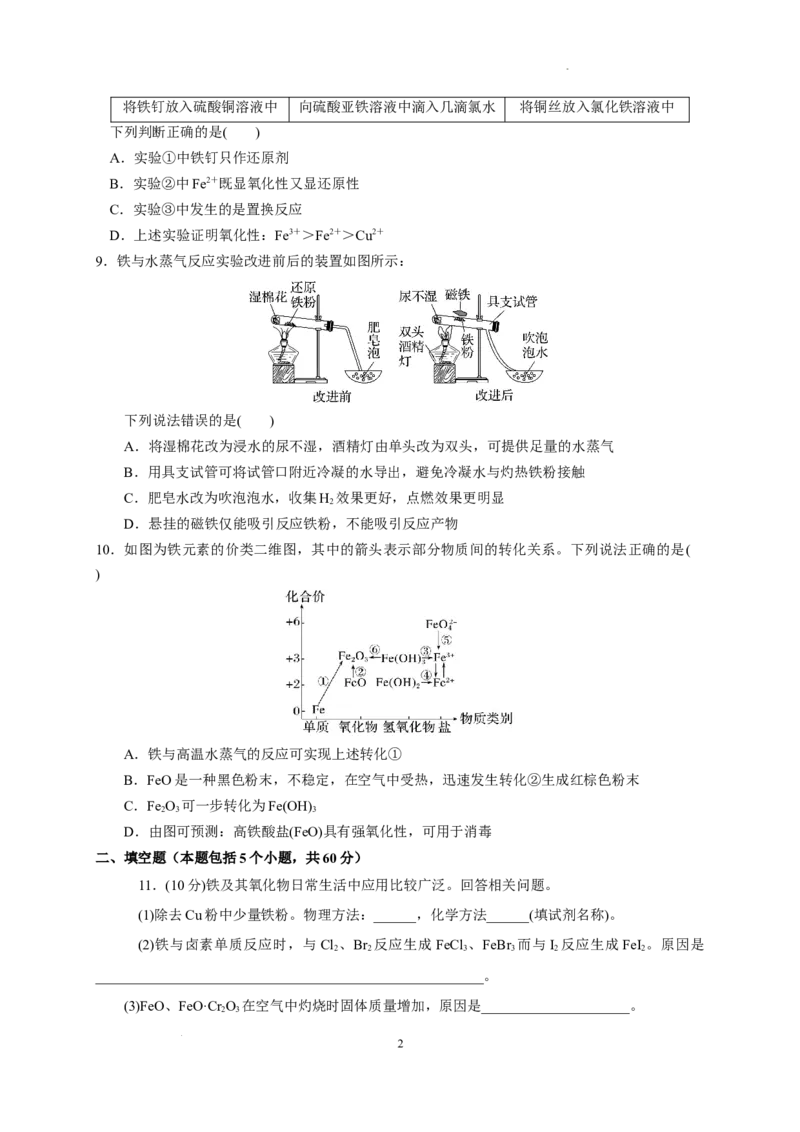
9.铁与水蒸气反应实验改进前后的装置如图所示:
下列说法错误的是( )
A.将湿棉花改为浸水的尿不湿,酒精灯由单头改为双头,可提供足量的水蒸气
B.用具支试管可将试管口附近冷凝的水导出,避免冷凝水与灼热铁粉接触
C.肥皂水改为吹泡泡水,收集H 效果更好,点燃效果更明显
2
D.悬挂的磁铁仅能吸引反应铁粉,不能吸引反应产物
10.如图为铁元素的价类二维图,其中的箭头表示部分物质间的转化关系。下列说法正确的是(
)
A.铁与高温水蒸气的反应可实现上述转化①
B.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②生成红棕色粉末
C.Fe O 可一步转化为Fe(OH)
2 3 3
D.由图可预测:高铁酸盐(FeO)具有强氧化性,可用于消毒
二、填空题(本题包括5个小题,共60分)
11.(10分)铁及其氧化物日常生活中应用比较广泛。回答相关问题。
(1)除去Cu粉中少量铁粉。物理方法:______,化学方法______(填试剂名称)。
(2)铁与卤素单质反应时,与Cl 、Br 反应生成FeCl 、FeBr 而与I 反应生成FeI 。原因是
2 2 3 3 2 2
_______________________________________________________。
(3)FeO、FeO·Cr O 在空气中灼烧时固体质量增加,原因是_____________________。
2 3
2
学科网(北京)股份有限公司(4)红珊瑚是一种贵重饰品,其颜色是因为含有一种铁的氧化物导致的,该氧化物的化学式为
________。
12.(12分)某班同学用如下实验探究Fe2+、Fe3+的性质。
回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成 0.1 mol·L-1的溶液。在FeCl 溶液中需加入
2
少量铁屑,其目的是____________________________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl
2 2
可将Fe2+氧化。FeCl 溶液与氯水反应的离子方程式为____________________________。
2
(3)乙组同学认为甲组的实验不够严谨,该组同学在2 mL FeCl 溶液中先加入0.5 mL煤油,再
2
于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作用是_____________________。
(4)丙组同学取10 mL 0.1 mol·L-1 KI溶液,加入6 mL 0.1 mol·L-1 FeCl 溶液混合。分别取2
3
mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1 mL CCl 充分振荡、静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K[Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍
含有________(填离子符号),由此可以证明该氧化还原反应为________。
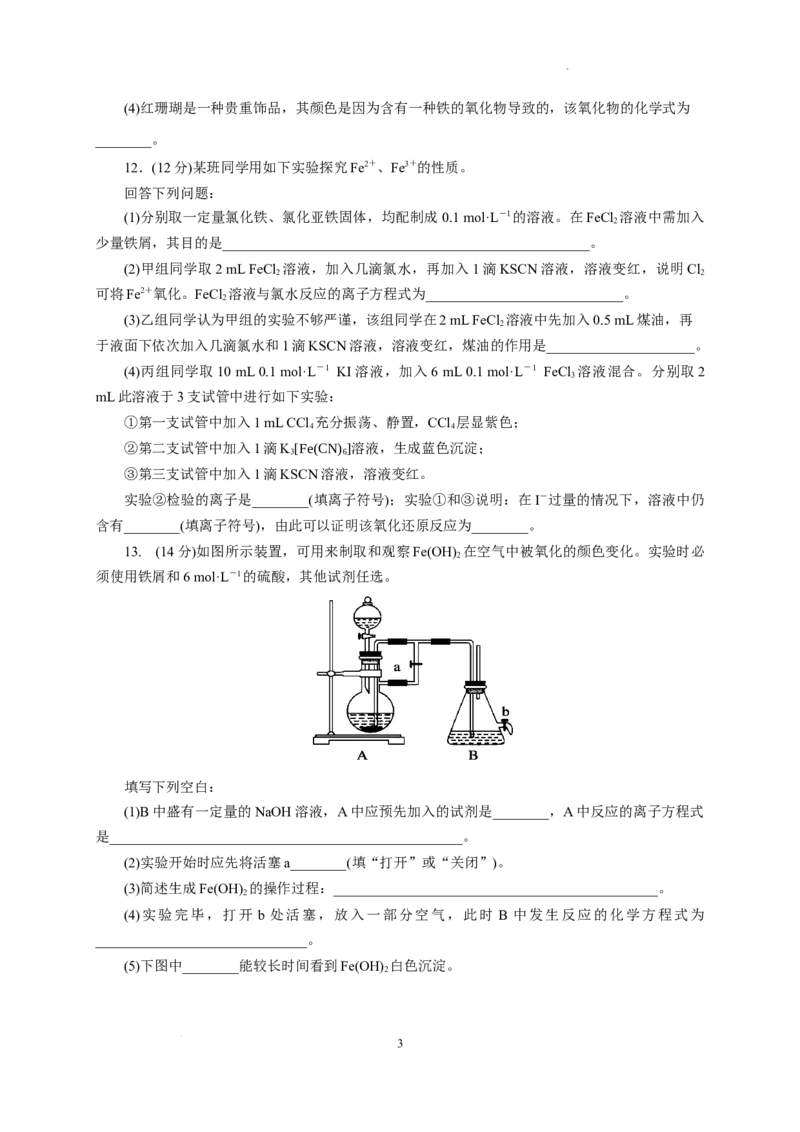
13. (14分)如图所示装置,可用来制取和观察Fe(OH) 在空气中被氧化的颜色变化。实验时必
2
须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。
填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是________,A中反应的离子方程式
是__________________________________________________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。
(3)简述生成Fe(OH) 的操作过程:______________________________________________。
2
(4)实验完毕,打开 b 处活塞,放入一部分空气,此时 B 中发生反应的化学方程式为
______________________________。
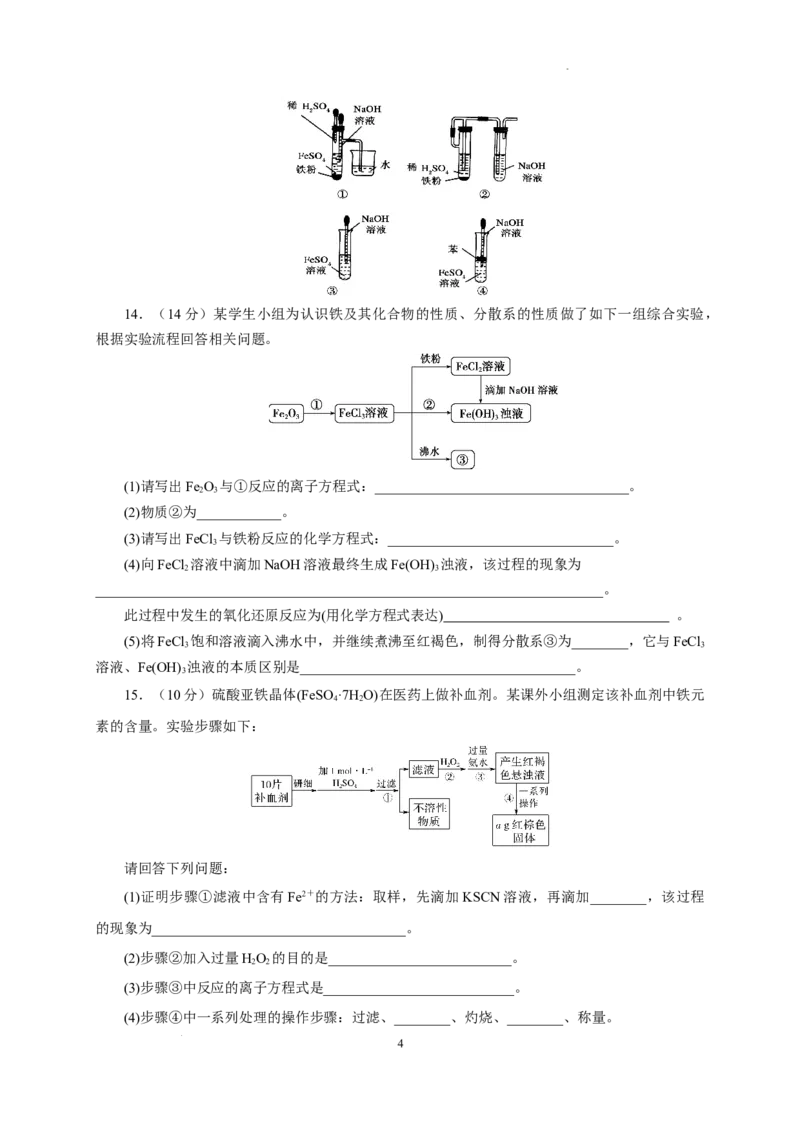
(5)下图中________能较长时间看到Fe(OH) 白色沉淀。
2
3
学科网(北京)股份有限公司14.(14分)某学生小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,
根据实验流程回答相关问题。
(1)请写出Fe O 与①反应的离子方程式:____________________________________。
2 3
(2)物质②为____________。
(3)请写出FeCl 与铁粉反应的化学方程式:________________________________。
3
(4)向FeCl 溶液中滴加NaOH溶液最终生成Fe(OH) 浊液,该过程的现象为
2 3
________________________________________________________________________。
此过程中发生的氧化还原反应为(用化学方程式表达) 。
(5)将FeCl 饱和溶液滴入沸水中,并继续煮沸至红褐色,制得分散系③为________,它与FeCl
3 3
溶液、Fe(OH) 浊液的本质区别是_______________________________________。
3
15.(10分)硫酸亚铁晶体(FeSO ·7H O)在医药上做补血剂。某课外小组测定该补血剂中铁元
4 2
素的含量。实验步骤如下:
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法:取样,先滴加KSCN溶液,再滴加________,该过程
的现象为____________________________________。
(2)步骤②加入过量HO 的目的是__________________________。
2 2
(3)步骤③中反应的离子方程式是___________________________。
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、________、称量。
4
学科网(北京)股份有限公司(5)若实验中铁无损耗,则每片补血剂中含铁元素的质量为________g。
【解析】
1.解析:D 铁在空气中容易发生吸氧腐蚀,根据题意“舶上铁丝,……日久起销”,说明销是
铁锈,铁锈的主要成分为Fe O,D项正确。
2 3
2.解析:A
3.解析:B 根据电子守恒分析:等量的铁与足量的盐酸和水蒸气反应失去的电子数比为2∶8/3,
即3∶4,则相同的条件下,产生氢气的体积比为3∶4。
4.解析:D
5.解析:C ③不反应,实验方案及现象均错误;④检验的是Cl-,与Fe3+的性质无关。
6.解析:B 1.12 g铁物质的量为=0.02 mol,25 mL 2 mol·L-1氯化铁溶液中Fe3+的物质的量为
0.025 L×2 mol·L-1=0.05 mol,发生的反应为Fe+2Fe3+===3Fe2+,根据比例关系可得,0.02 mol铁
完全反应,消耗0.04 mol Fe3+,生成0.06 mol Fe2+,所以Fe3+剩余0.01 mol,溶液中含有Fe3+的物
质的量为0.01 mol,Fe2+的物质的量为0.06 mol,没有金属铁剩余。铁没有剩余,溶液呈黄绿色,
Cl-基本保持不变,故A错误;溶液中有剩余的Fe3+,往溶液中滴入无色KSCN溶液,显红色,故
B正确;Fe2+和Fe3+的物质的量之比为0.06 mol∶0.01 mol=6∶1,故C错误;由反应离子方程式可
得,氧化产物和还原产物的物质的量之比为1∶2,故D错误。
7.解析:D 根据2Fe2++Cl===2Fe3++2Cl-,可知铁的“氧化物”样品用盐酸溶解后所得溶液中
2
n(Fe2+)=0.025 mol×2=0.05 mol,根据电荷守恒得2n(Fe2+)+3n(Fe3+)=n(Cl-),则n(Fe3+)=0.2
mol,故n(Fe2+)∶n(Fe3+)=0.05∶0.2=1∶4,故该氧化物可表示为FeO·2Fe O,即Fe O。
2 3 5 7
8.解析 A ①Cu2++Fe===Fe2++Cu,其中Fe作还原剂,氧化性Cu2+>Fe2+,A项正确,D项
错误;② 2Fe2++Cl===2Fe3++2Cl-,Fe2+作还原剂只表现还原性,B 项错误;③ 2Fe3++
2
Cu===2Fe2++Cu2+,Cu不如铁活泼,不可能置换出Fe单质,C项错误。
9. 解析 D 铁、四氧化三铁均可被磁铁吸引,则悬挂的磁体不仅能吸引铁粉,也能吸引反应产
物四氧化三铁,故D错误。
10. 解析 D 铁与高温水蒸气反应生成四氧化三铁和氢气,不能实现上述转化①,故A错误;
FeO是一种黑色粉末,不稳定,在空气中受热,部分被氧化生成 Fe O ,不能发生转化②,故B错
3 4
误;加热Fe(OH) 发生转化⑥分解生成氧化铁,氢氧化铁与酸反应可实现转化③,故C正确;高铁
3
酸盐中铁为+6价,具有强氧化性,可用于消毒。
11.答案: (1)用磁铁吸引 稀盐酸(稀硫酸)
(2)I 的氧化性弱 (3)吸收空气中的O (4)Fe O
2 2 2 3
12.答案:(1)Fe2+具有还原性,易被空气中的O 氧化为Fe3+,在FeCl 溶液中加入少量铁屑,可防
2 2
止Fe2+被氧化。
(2)Fe2+被氧化为Fe3+,Cl 被还原为Cl-,反应的离子方程式为2Fe2++Cl===2Fe3++2Cl-。
2 2
5
学科网(北京)股份有限公司(3)O 难溶于煤油,加入煤油能隔绝空气,排除O 对实验的影响。
2 2
(4)KI溶液与FeCl 溶液反应的离子方程式为2I-+2Fe3+===I +2Fe2+。K[Fe(CN) ]是检验Fe2+
3 2 3 6
的试剂。实验③溶液变红,说明溶液中仍存在Fe3+,由此可说明该氧化还原反应为可逆反应。
13答案:(1)铁屑 Fe+2H+===Fe2++H↑ (2)打开 (3)关闭活塞a,使FeSO 溶液被压入B中进
2 4
行反应 (4)4Fe(OH) +2HO+O===4Fe(OH) (5)①②③④
2 2 2 3
14. 答案: (1)Fe O+6H+===2Fe3++3HO
2 3 2
(2)NaOH溶液(其他合理答案也可)
(3)Fe+2FeCl ===3FeCl
3 2
(4)生成的白色沉淀迅速变成灰绿色,最终变成红褐色
4Fe(OH) +O+2HO===4Fe(OH)
2 2 2 3
(5)Fe(OH) 胶体 分散质粒子直径大小不同
3
15. 答案: (1)氯水(或双氧水、稀硝酸等合理氧化剂) 滴加KSCN无变化,滴加氯水后溶液由浅绿
色变为红色
(2)将Fe2+全部氧化为Fe3+
(3)Fe3++3NH ·H O===Fe(OH) ↓+3NH
3 2 3
(4)洗涤 冷却 (5)0.07a
解析 (2)由于HO 具有氧化性,加入过量HO 的目的是将Fe2+全部氧化为Fe3+。(3)步骤③的目的
2 2 2 2
是将 Fe3+全部转化为 Fe(OH) ,所以步骤③需加入过量的氨水,反应的离子方程式是 Fe3++
3
3NH ·H O===Fe(OH) ↓+3NH。(4)步骤④的目的是将产生的红褐色悬浊液分离,最终得到固体
3 2 3
Fe O ,所以步骤④的操作步骤是过滤、洗涤、灼烧、冷却、称量。(5)由于实验中铁无损耗,根据
2 3
铁元素守恒得,每片补血剂中m(Fe)=()÷10 g=0.07a g。
6
学科网(北京)股份有限公司7
学科网(北京)股份有限公司