文档内容
课时作业
A篇·知识对点训练
1.关于氮气的性质的说法中,错误的是( )
A.氮在自然界中既以游离态存在又以化合态存在
B.通常情况下,氮气性质很不活泼
C.可在氧气中燃烧生成一氧化氮
D.在反应3Mg+N =====Mg N 中N 作氧化剂
2 3 2 2
答案 C
解析 通常情况下氮气的性质很不活泼,不具有可燃性,在放电或高温条件
下,能跟氧气反应。
2.NO对于心脑血管系统功能的改善具有重要作用。下列关于NO的描述不
正确的是( )
A.不溶于水
B.可由氮气和氧气在放电条件下反应生成
C.常温下能与氧气化合
D.红棕色气体
答案 D
解析 NO为无色不溶于水的气体,D错误。
3.关于二氧化硫和二氧化氮叙述正确的是( )
A.两种气体都是无色有毒的气体,且都可用水吸收以消除对空气的污染
B.二氧化硫与过量的二氧化氮混合后通入水中能得到两种常用的强酸
C.两种气体都具有强氧化性,因此都能够使品红溶液褪色
D.两种气体溶于水都可以与水反应,且只生成相应的酸
答案 B
解析 A中二氧化氮为红棕色气体,二氧化氮与水反应生成的 NO也是大气
污染物之一;B中二氧化氮跟水反应,生成了硝酸,硝酸氧化亚硫酸生成硫酸,
能得到两种常用的强酸;C中二氧化硫的漂白原理不是利用强氧化性,二氧化硫也不具有强氧化性;D中二氧化氮跟水反应,还生成了一氧化氮。故B符合题意。
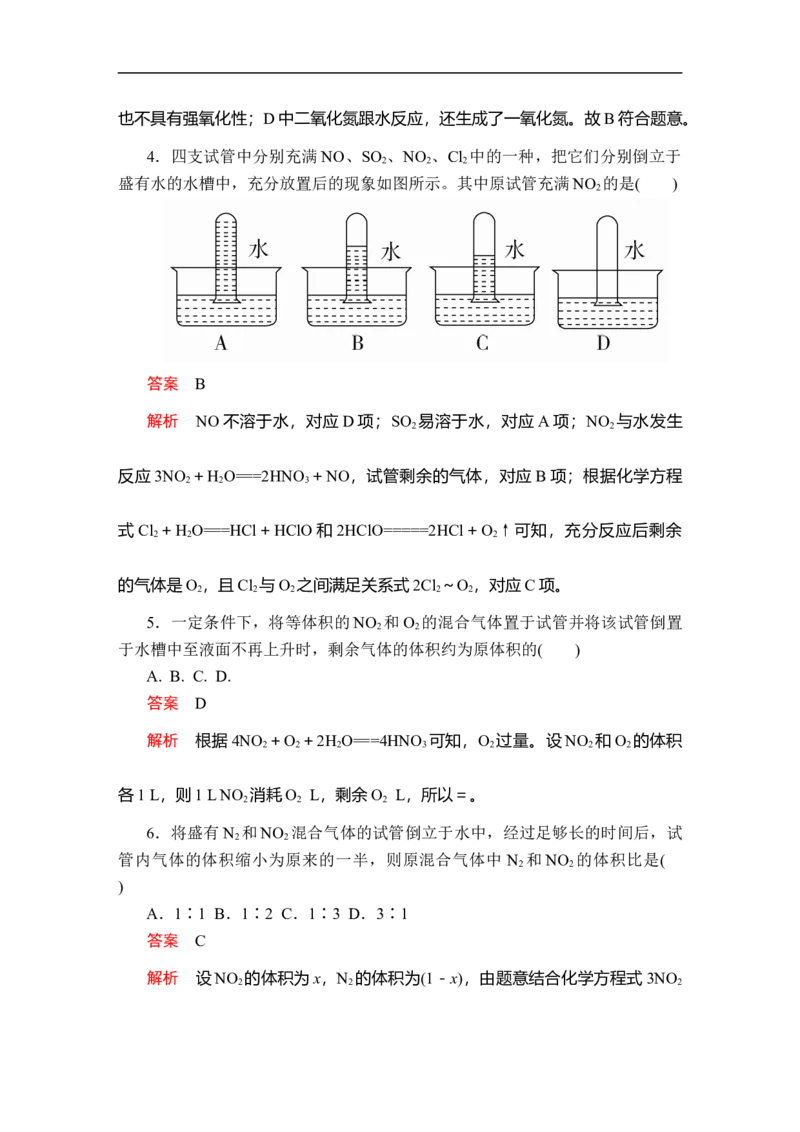
4.四支试管中分别充满 NO、SO 、NO 、Cl 中的一种,把它们分别倒立于
2 2 2
盛有水的水槽中,充分放置后的现象如图所示。其中原试管充满NO 的是( )
2
答案 B
解析 NO不溶于水,对应D项;SO 易溶于水,对应A项;NO 与水发生
2 2
反应3NO +H O===2HNO +NO,试管剩余的气体,对应B项;根据化学方程
2 2 3
式Cl +H O===HCl+HClO和2HClO=====2HCl+O ↑可知,充分反应后剩余
2 2 2
的气体是O ,且Cl 与O 之间满足关系式2Cl ~O ,对应C项。
2 2 2 2 2
5.一定条件下,将等体积的NO 和O 的混合气体置于试管并将该试管倒置
2 2
于水槽中至液面不再上升时,剩余气体的体积约为原体积的( )
A. B. C. D.
答案 D
解析 根据4NO +O +2H O===4HNO 可知,O 过量。设NO 和O 的体积
2 2 2 3 2 2 2
各1 L,则1 L NO 消耗O L,剩余O L,所以=。
2 2 2
6.将盛有N 和NO 混合气体的试管倒立于水中,经过足够长的时间后,试
2 2
管内气体的体积缩小为原来的一半,则原混合气体中 N 和NO 的体积比是(
2 2
)
A.1∶1 B.1∶2 C.1∶3 D.3∶1
答案 C
解析 设NO 的体积为x,N 的体积为(1-x),由题意结合化学方程式3NO
2 2 2+H O===2HNO +NO,可得x+(1-x)=,x=,1-x=,N 和NO 的体积比为
2 3 2 2
1∶3。
7.在容积为672 mL的烧瓶里充满NO、NO 的混合气体,将其倒立在水槽
2
里,去塞后再通入280 mL氧气,恰好完全反应,且水充满烧瓶(气体体积都折合
成标准状况下)。下列有关叙述中,正确的是( )
A.总反应可能为NO+NO +O +H O===2HNO
2 2 2 3
B.总反应可能为4NO+8NO +5O +6H O===
2 2 2
12HNO
3
C.生成HNO 的物质的量浓度接近0.03 mol·L-1
3
D.生成HNO 的物质的量浓度约为0.45 mol·L-1
3
答案 B
解析 根据得失电子守恒知:3n(NO)+n(NO )=4n(O ),解得 n(NO)=0.01
2 2
mol,n(NO )=0.02 mol,则总反应为 4NO+8NO +5O +6H O===12HNO 。
2 2 2 2 3
V(NO +NO)∶V(O )=12∶5,因烧瓶中的气体最终均生成了HNO ,故所得溶液
2 2 3
的体积与溶解的NO 、NO体积相等,故浓度为[V(NO +NO)÷22.4]÷V = mol·L
2 2 瓶
-1≈0.045 mol·L-1。
8.将盛有12 mL NO 和O 的混合气体的量筒倒立于水槽中,充分反应后,
2 2
还剩余2 mL无色气体,则原混合气体中O 的体积和剩余的2 mL气体可能分别
2
是( )
A.1.2 mL,NO B.2.4 mL,O
2
C.3.5 mL,O D.4 mL,NO
2
答案 A
解析 解题依据的化学反应原理为 4NO +O +2H O===4HNO 3NO +
2 2 2 3 2
H O===2HNO +NO
2 3
设O 的体积为x。剩余的气体有两种可能:①若剩O ,则V =x-(12 mL-
2 2 剩x)=2 mL,解得x=4 mL,B、C不正确。②若剩NO,则V =[(12 mL-x)-4x]
剩
=2 mL,解得x=1.2 mL,D不正确。
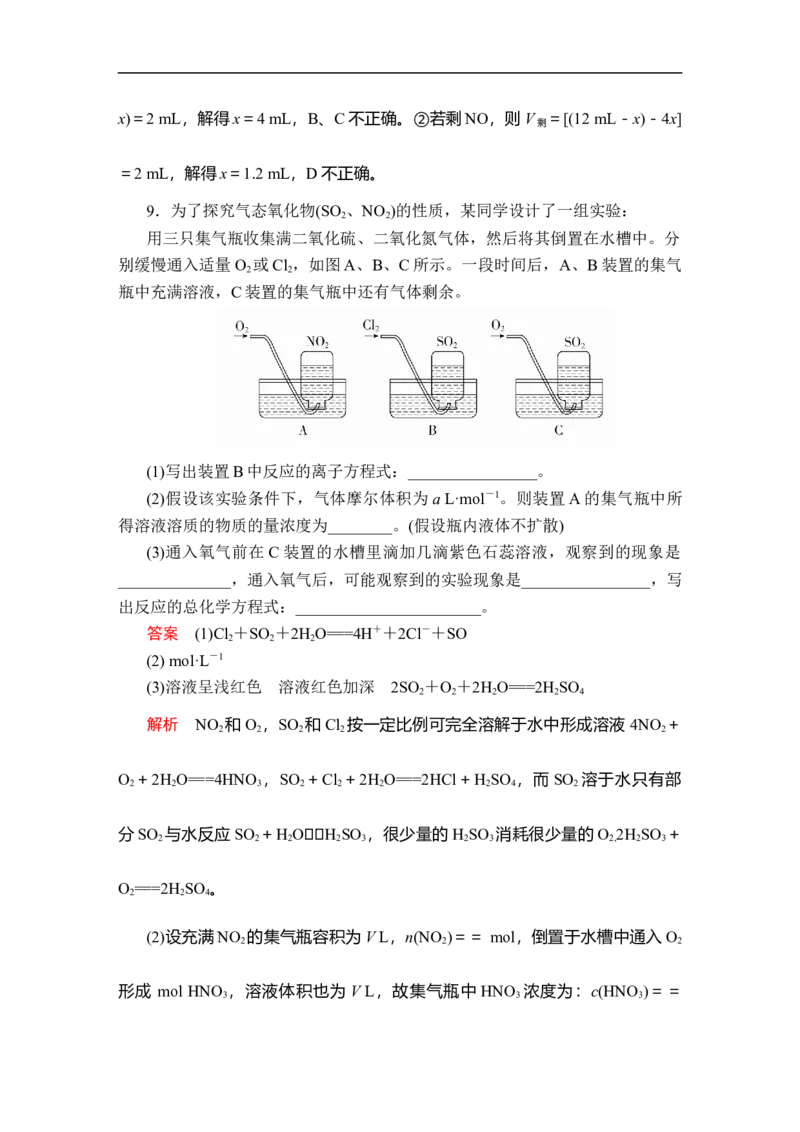
9.为了探究气态氧化物(SO 、NO )的性质,某同学设计了一组实验:
2 2
用三只集气瓶收集满二氧化硫、二氧化氮气体,然后将其倒置在水槽中。分
别缓慢通入适量O 或Cl ,如图A、B、C所示。一段时间后,A、B装置的集气
2 2
瓶中充满溶液,C装置的集气瓶中还有气体剩余。
(1)写出装置B中反应的离子方程式:________________。
(2)假设该实验条件下,气体摩尔体积为a L·mol-1。则装置A的集气瓶中所
得溶液溶质的物质的量浓度为________。(假设瓶内液体不扩散)
(3)通入氧气前在 C装置的水槽里滴加几滴紫色石蕊溶液,观察到的现象是
______________,通入氧气后,可能观察到的实验现象是________________,写
出反应的总化学方程式:_______________________。
答案 (1)Cl +SO +2H O===4H++2Cl-+SO
2 2 2
(2) mol·L-1
(3)溶液呈浅红色 溶液红色加深 2SO +O +2H O===2H SO
2 2 2 2 4
解析 NO 和O ,SO 和Cl 按一定比例可完全溶解于水中形成溶液 4NO +
2 2 2 2 2
O +2H O===4HNO ,SO +Cl +2H O===2HCl+H SO ,而 SO 溶于水只有部
2 2 3 2 2 2 2 4 2
分SO 与水反应SO +H OH SO ,很少量的H SO 消耗很少量的O 2H SO +
2 2 2 2 3 2 3 2, 2 3
O ===2H SO 。
2 2 4
(2)设充满NO 的集气瓶容积为V L,n(NO )== mol,倒置于水槽中通入O
2 2 2
形成 mol HNO ,溶液体积也为 V L,故集气瓶中 HNO 浓度为:c(HNO )==
3 3 3mol·L-1。
(3)H SO 是弱酸,滴加紫色石蕊溶液显浅红色,通入氧气后,H SO 被氧化
2 3 2 3
为 H SO ,酸性增强,石蕊溶液所显红色变深。总反应为 2SO +O +
2 4 2 2
2H O===2H SO 。
2 2 4
B篇·综合提升训练
10.不能实现下列物质间直接转化的元素是( )
→→→
A.碳 B.氮 C.硫 D.铝
答案 D
解析 A项,碳可以先生成一氧化碳,后生成二氧化碳,再和水反应生成酸,
正确;B项,氮气和氧气反应生成一氧化氮,后生成二氧化氮,和水反应时生成
硝酸,正确;C项,硫和氧气反应生成二氧化硫,后和氧气反应生成三氧化硫,
再和水反应生成硫酸,正确;D项,铝的氧化物只有氧化铝,错误。
11.硝酸工业尾气中含有高浓度的NO和NO ,它们都是大气的重要污染物。
2
已知某厂排放的尾气中NO、NO 的体积比为1∶1,该厂采用NaOH溶液来处理
2
该尾气,处理后所得溶液中只有一种含氮的钠盐。则该含氮的钠盐中,氮元素的
化合价为( )
A.-3 B.+1 C.+3 D.+5
答案 C
解析 设该含氮钠盐中氮元素的化合价为x价,NO、NO 在NaOH溶液中发
2
生氧化还原反应生成含氮元素的钠盐,根据得失电子守恒,推知 x-2=4-x,
解得x=3。
12.某混合气体中可能含有Cl 、O 、SO 、NO、NO 中的两种或多种。现
2 2 2 2
将此无色透明的混合气体通过品红溶液后,品红溶液褪色,把剩余气体排入空气中,很快变为红棕色。对于原混合气体成分的判断中正确的是( )
A.肯定有SO 和NO
2
B.肯定没有Cl 、O 和NO
2 2
C.可能有Cl 和O
2 2
D.肯定只有NO
答案 A
解析 由题意可知,混合气体无色,故无Cl (黄绿色)、NO (红棕色);能使
2 2
品红溶液褪色,说明有SO ;剩余气体排入空气中,很快变为红棕色,说明产生
2
了NO ,进而说明原混合气体中有NO,故无O 。
2 2
13.工业废气中氮氧化物是主要污染物,为了治理污染,常通入 NH ,发生
3
反应NO +NH ―→N +H O。现有NO、NO 的混合气体3 L,用同温同压下3.5
x 3 2 2 2
L NH 使其恰好完全转化为 N ,则混合气体中NO、NO 的物质的量之比为(
3 2 2
)
A.1∶1 B.1∶3 C.2∶1 D.1∶4
答案 B
解析 在相同条件下体积比等于物质的量之比,设混合气体中 NO、NO 的
2
物质的量分别是x mol和y mol,则x+y=3。根据得失电子守恒可知2x+4y=
3.5×3,解得x=0.75、y=2.25,因此混合气体中 NO、NO 的物质的量之比为
2
1∶3。
14.在一定条件下,将6体积的NO 和一定体积的NO置于试管中,并将试
2
管倒置于水中,当通入 4.5体积的O 充分反应后,剩余1.5体积气体,则原NO
2
体积可能为( )
①3体积 ②4体积 ③5体积 ④5.5体积
⑤2体积
A.③ B.⑤
C.④或⑤ D.②或⑤
答案 C解析 本题的关键在于理解剩余的 1.5体积气体,可能是一氧化氮,也有可
能是氧气。若是一氧化氮,则氧气全部反应,二氧化氮完全反应用掉了 1.5体积
氧气,剩余3体积应该被一氧化氮消耗,所以一氧化氮体积为 4体积+1.5体积
=5.5体积;若剩余的为氧气,则这过程中一氧化氮消耗的氧气为 1.5体积,所
以一氧化氮的体积是2体积。
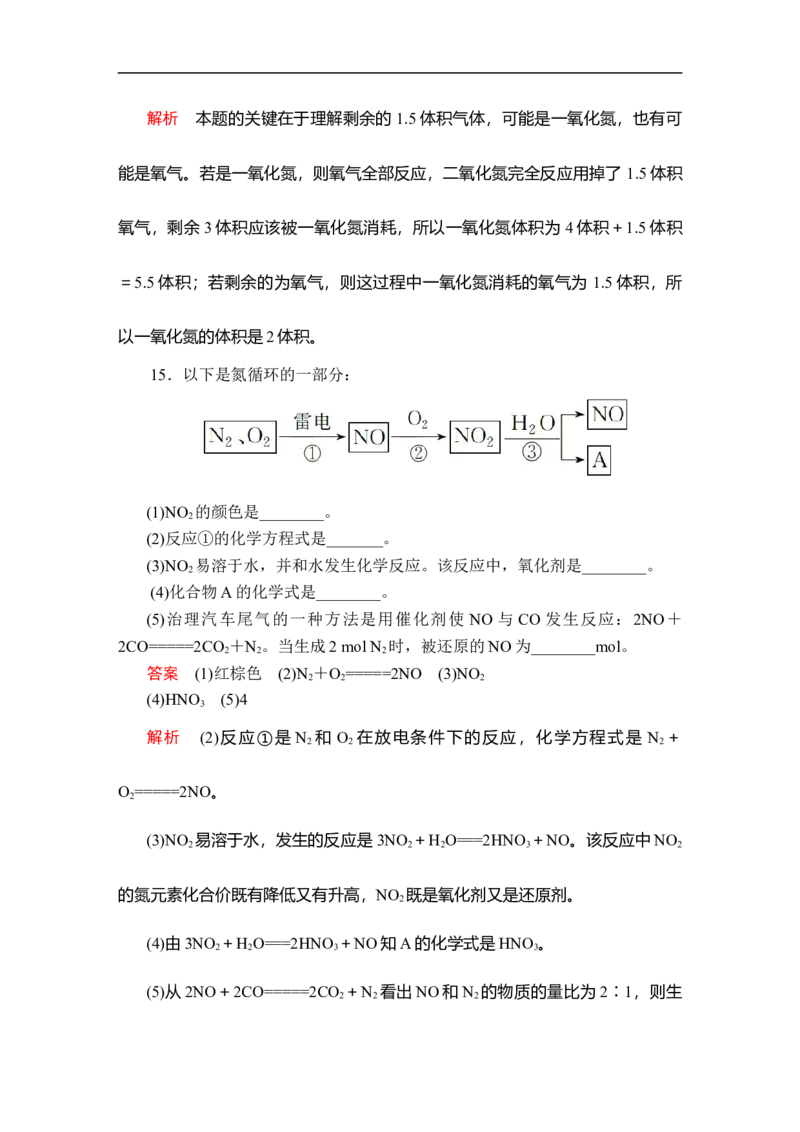
15.以下是氮循环的一部分:
(1)NO 的颜色是________。
2
(2)反应①的化学方程式是_______。
(3)NO 易溶于水,并和水发生化学反应。该反应中,氧化剂是________。
2
(4)化合物A的化学式是________。
(5)治理汽车尾气的一种方法是用催化剂使 NO 与 CO 发生反应:2NO+
2CO=====2CO +N 。当生成2 mol N 时,被还原的NO为________mol。
2 2 2
答案 (1)红棕色 (2)N +O =====2NO (3)NO
2 2 2
(4)HNO (5)4
3
解析 (2)反应①是 N 和 O 在放电条件下的反应,化学方程式是 N +
2 2 2
O =====2NO。
2
(3)NO 易溶于水,发生的反应是3NO +H O===2HNO +NO。该反应中NO
2 2 2 3 2
的氮元素化合价既有降低又有升高,NO 既是氧化剂又是还原剂。
2
(4)由3NO +H O===2HNO +NO知A的化学式是HNO 。
2 2 3 3
(5)从2NO+2CO=====2CO +N 看出NO和N 的物质的量比为2∶1,则生
2 2 2成2 mol N 时反应的NO为4 mol且全部作氧化剂被还原。
2
16.已知 NO 不溶于水,NO 易溶于水,且与水发生反应 3NO +
2 2
H O===2HNO +NO。把盛有48 mL NO和NO 混合气体的容器倒置于水中(保持
2 3 2
同温同压),待液面稳定后,容器内气体的体积变为24 mL,则:
(1)原混合气中,NO是________mL,NO 是________mL。
2
(2)若在剩余的24 mL气体中,通入6 mL O ,待液面稳定后,反应后容器内
2
剩余气体体积为________mL。
(3)若在剩余的24 mL气体中,通入24 mL O ,待液面稳定后,反应后容器
2
内剩余气体体积为________mL。
(4)若在原48 mL NO、NO 中,通入________mL O 再倒置于水中,气体会全
2 2
部被吸收。
答案 (1)12 36 (2)16 (3)6 (4)18
解析 (1)设NO 的体积为x,
2
3NO +H O===2HNO +NO 体积差
2 2 3
3 1 2
x (48-24) mL
x=36 mL
V(NO)=(48-36) mL=12 mL。
(2)由4NO+3O +2H O===4HNO
2 2 3
4 3
耗 8 mL 6 mL
容器内剩余气体为NO,体积为24 mL-8 mL=16 mL。
(3)由4NO~3O 知,24 mL NO只需消耗18 mL的O ,所以反应后容器内剩
2 2
余O 为24 mL-18 mL=6 mL。
2
(4)由4NO + 3O +2H O===4HNO
2 2 34 3
12 mL 9 mL
4NO +O +2H O===4HNO
2 2 2 3
4 1
36 mL 9 mL
可知,通入18 mL O ,可使容器内气体全部被H O吸收。
2 2