文档内容
浏阳市高三 12 月份联盟校联考
化学试卷
考试时间:75分钟,满分:100分
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-16 Cl-35.5 Fe-56 Cu-64
一、单选题:本题共14小题,每小题3分,共42分。
1.下列物质在生活中的用途与其化学性质对应正确的是( )
A.飞船返回舱使用耐高温的结构材料氮化硅,因为 是由共价键构成的分子晶体
B.利用废弃的秸秆生产生物质燃料乙醇,是由于纤维 3素 能4 发生水解反应生成乙醇
C.面包师用小苏打作发泡剂烘焙面包,是由于 是一种食用碱能与酸反应
D.离子液体作溶剂比传统有机溶剂难挥发,是 由 于2 阴 3阳离子间的作用力强于范德华力导致的
2.下列化学用语表示正确的是( )
A.基态 原子的价层电子的轨道表示式:
B. 分子的空间结构模型;
6
C. 形成的 键模型:
— −
D.用电子式表示 的形成过程:
2
3.下列事实可用勒夏特列原理解释的是( )
A. ℃比室温更有利于工业合成氨的反应
B.光50照0 新制氯水,一段时间后溶液 减小
C.由 和 组成的平衡体 系,加压后颜色变深
D.向 盛 有2双 氧水 2的 试4 管中加入少量 ,立即产生大量气泡
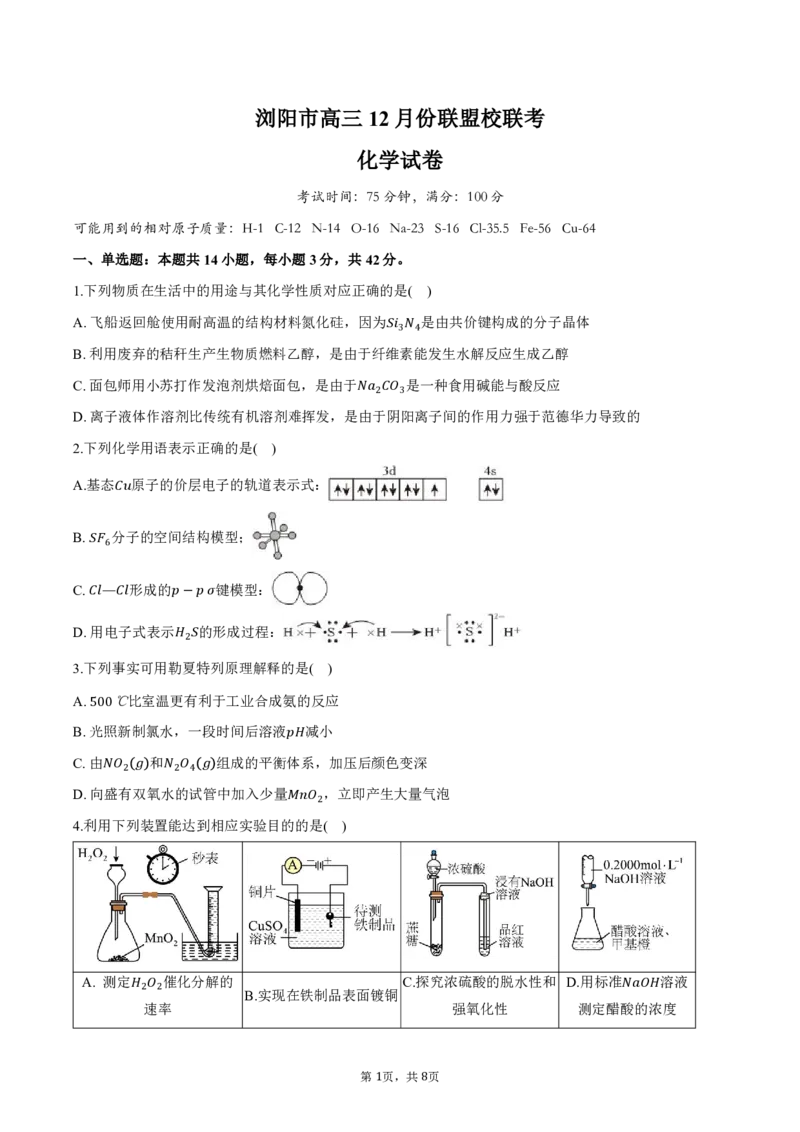
4.利用下列装置能达到相应实验目的 的 是2 ( )
A. 测定 催化分解的 C.探究浓硫酸的脱水性和 D.用标准 溶液
B.实现在铁制品表面镀铜
2速
2率 强氧化性 测定醋酸
的
浓
度
第 页,共 页
1 8
{#{QQABLQSEogCIAAIAARhCAwmwCgOQkgEAAagOBFAIsAIBSANABAA=}#}5.消毒剂需科学使用, 消毒液不能和医用酒精混用的原因是:
84 。下列说法不正确的是( ) 4 + 3 2 = 3+
A. 上 述 反 +应2中 +是 氧 化 +剂 2 B. mol 分子中含有 键数目为8N
A
C. 溶液 能 导 电 D.1 和3 2 含 有的化学键 类型相同
6.电 解 质 在 水溶液中的反应属于离子反应。下列离 子 方 程式 正 确 的是( )
A.浓盐酸与 反应制取少量氯气:
2+ −
B. 溶 液 中 2 加入过量的 溶 液 2 : +4 +2 2 + 2 ↑+2
+ + 2− 2+ −
( )2 4 4 4 + + 4 + +2 = 4 ↓+ 2 + 3⋅
C. 2 溶液中通入 气体:
−1 − + 3+
1 0.1 ⋅ [ ( )4] 0.28 5[ ( )4] +14 =2 ( )3 ↓+3 +
1D4. 2 通入 溶液中至 恰好完全反应:
2+ 2+ − 3+
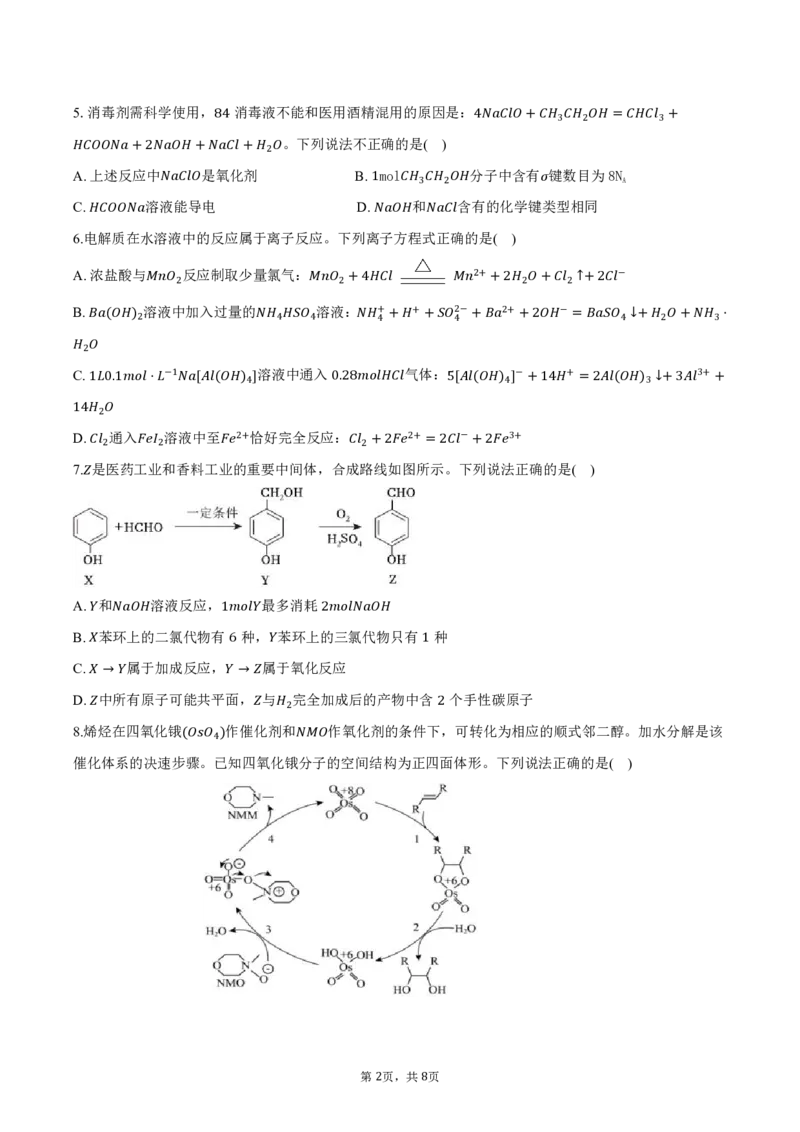
7. 是 2医药工 业 2和香料工业 的重要中间体,合成 路2+线2如 图所=示2。 下+列2说 法 正确的是( )
A. 和 溶液反应, 最多消耗
B. 苯环 上 的二氯代物有1 种 , 苯环上的2 三 氯 代 物 只有 种
C. 属于加成反应,6 属 于氧化反应 1
D. 中→所 有原子可能共平面 →, 与 完全加成后的产物中含 个手性碳原子
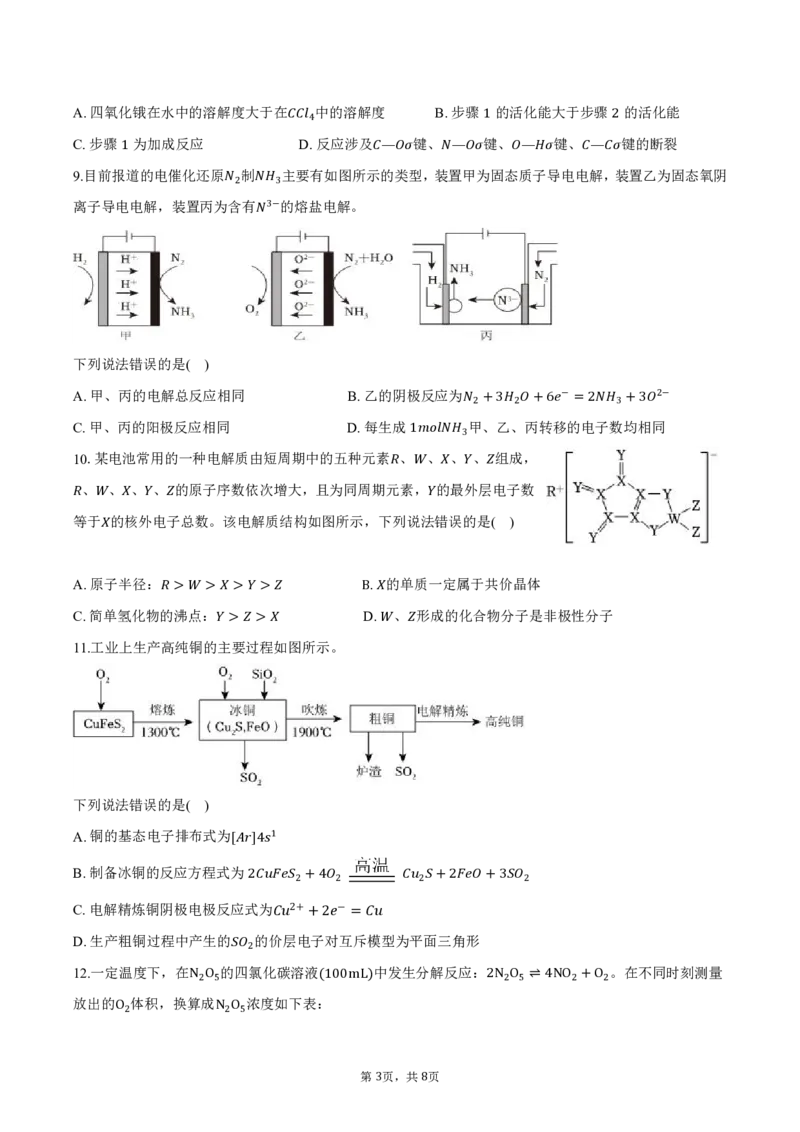
8.烯 烃在四氧化锇 作催 化剂 和2 作氧化剂的条件下2,可转化为相应的顺式邻二醇。加水分解是该
催化体系的决速步(骤 。 4已)知四氧化锇 分 子 的空间结构为正四面体形。下列说法正确的是( )
第 页,共 页
2 8
{#{QQABLQSEogCIAAIAARhCAwmwCgOQkgEAAagOBFAIsAIBSANABAA=}#}A.四氧化锇在水中的溶解度大于在 中的溶解度 B.步骤 的活化能大于步骤 的活化能
C.步骤 为加成反应 D 4 .反应涉及 键、 1键、 键、 2键的断裂
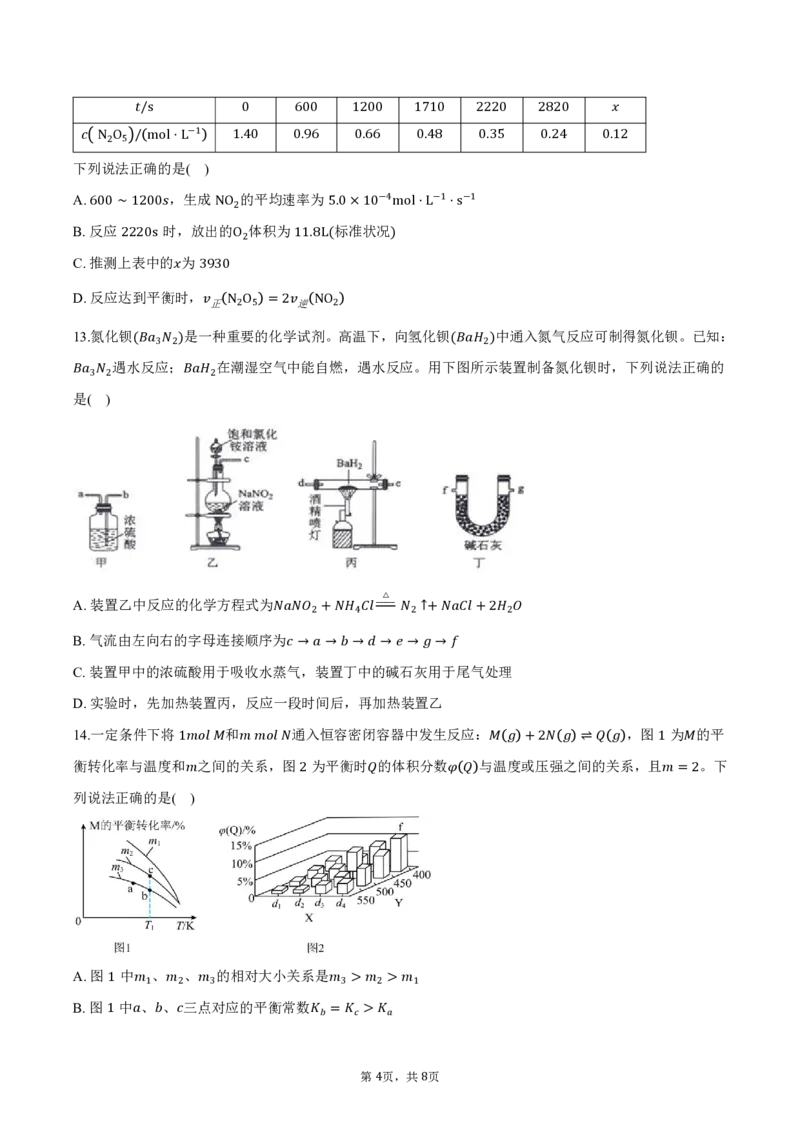
9.目前报1道的电催化还原 制 主要有如图所示 的—类 型,装 置—甲 为固态 质—子 导电电 解—, 装置乙为固态氧阴
离子导电电解,装置丙为 含2有 3的熔盐电解。
3−
下列说法错误的是( )
A.甲、丙的电解总反应相同 B.乙的阴极反应为
− 2−
C.甲、丙的阳极反应相同 D.每生成 甲2、+3乙 、2 丙+转6移 的=电2子 数3均+相3 同
10.某电池常用的一种电解质由短周期中的五种元素 、1 、 、 3 、 组成,
、 、 、 、 的原子序数依次增大,且为同周期元 素 , 的 最外 层 电子数
等于 的 核外 电 子总数。该电解质结构如图所示,下列说法 错误的是( )
A.原子半径: . 的单质一定属于共价晶体
C.简单氢化物的 >沸点 :> > > BD. 、 形成的化合物分子是非极性分子
11.工业上生产高纯铜的 主>要 过>程 如图所示。
下列说法错误的是( )
A.铜的基态电子排布式为
1
B.制备冰铜的反应方程式为[ ]4
2 2+4 2 2 +2 +3 2
C.电解精炼铜阴极电极反应式为
2+ −
D.生产粗铜过程中产生的 的价 层电+子2对 互=斥 模 型为平面三角形
12.一定温度下,在 的 四 2氯化碳溶液 中发生分解反应: 。在不同时刻测量
放出的 体积,换算N2成O5 浓度如下表:(100mL) 2N2O5 ⇌4NO2+O2
O2 N2O5
第 页,共 页
3 8
{#{QQABLQSEogCIAAIAARhCAwmwCgOQkgEAAagOBFAIsAIBSANABAA=}#}/s 0 600 1200 1710 2220 2820
−1
下 列N说 2O法 5 正/确m的ol是⋅L ( ) 1.40 0.96 0.66 0.48 0.35 0.24 0.12
A. ,生成 的平均速率为
−4 −1 −1
B.反60应0∼ 1200 时,放出N的O2 体积为 5标.0准×状10况mol⋅L ⋅s
C.推测上22表20中s的 为 O2 11.8L( )
D.反应达到平衡 时,3930
正 逆
N2O5 =2 NO2
13.氮化钡 是一种重要的化学试剂。高温下,向氢化钡 中通入氮气反应可制得氮化钡。已知:
遇水( 反 应3 ;2) 在潮湿空气中能自燃,遇水反应。用下( 图 所 2示)装置制备氮化钡时,下列说法正确的
是 ( 3 ) 2 2
A.装置乙中反应的化学方程式为
△
_____
B.气流由左向右的字母连接顺序为 2+ 4 2 ↑+ +2 2
C.装置甲中的浓硫酸用于吸收水蒸气 →, 装→置 丁→中 的→碱 石→灰 用→于 尾气处理
D.实验时,先加热装置丙,反应一段时间后,再加热装置乙
14.一定条件下将 和 通入恒容密闭容器中发生反应: ,图 为 的平
衡转化率与温度和1 之 间 的 关系 , 图 为平衡时 的体积分数 与 温度 或+压2 强 之间⇌的 关 系,且1 。下
列说法正确的是( ) 2 =2
A.图 中 、 、 的相对大小关系是
B.图 1中 、1 、 2三点 3对应的平衡常数 3 > 2 > 1
1 = >
第 页,共 页
4 8
{#{QQABLQSEogCIAAIAARhCAwmwCgOQkgEAAagOBFAIsAIBSANABAA=}#}C.图 中 表示压强, 点的数值比 点的大
D.若2点 的体积分数为 1 ,则该点 2 的平衡转化率为
二、非 选 择题:本题共41小0%题,共58分 。 25%
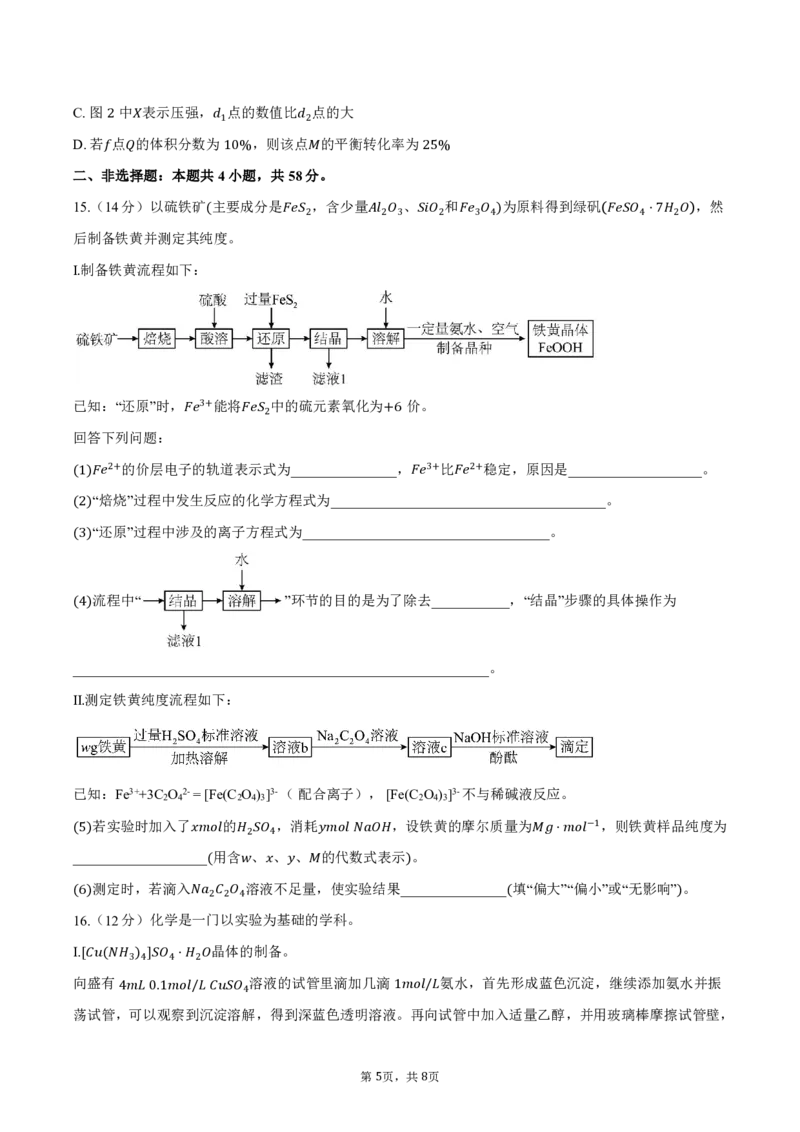
15.(14分)以硫铁矿 主要成分是 ,含少量 、 和 为原料得到绿矾 ,然
后制备铁黄并测定其纯(度。 2 2 3 2 3 4) 4⋅7 2
Ⅰ制备铁黄流程如下:
.
已知:“还原”时, 能将 中的硫元素氧化为 价。
3+
回答下列问题: 2 +6
的价层电子的轨道表示式为_______________, 比 稳定,原因是___________________。
2+ 3+ 2+
(1) “焙 烧”过程中发生反应的化学方程式为____________ _ _____ _ ____________________。
(2)“还原”过程中涉及的离子方程式为___________________________________。
(3)
流程中“ ”环节的目的是为了除去___________,“结晶”步骤的具体操作为
(4)
___________________________________________________________。
Ⅱ测定铁黄纯度流程如下:
.
已知:Fe3++3C O 2-=[Fe(C O ) ]3-(配合离子),[Fe(C O ) ]3-不与稀碱液反应。
2 4 2 4 3 2 4 3
若实验时加入了 的 ,消耗 ,设铁黄的摩尔质量为 ,则铁黄样品纯度为
−1
(_5_)_______________ _ _ 用 含 2、 4、 、 的 代 数 式 表 示 。 ⋅
测定时,若滴入 ( 溶液 不 足量 ,使实验结果_)______________ 填“偏大”“偏小”或“无影响” 。
(166).(12分)化学是 一 门2 以2 实4验为基础的学科。 ( )
I. 晶体的制备。
向[ 盛 有( 3)4] 4⋅ 2 溶液的试管里滴加几滴 氨水,首先形成蓝色沉淀,继续添加氨水并振
荡试管,4 可 以0观.1 察 到 / 沉 淀 溶 解4 ,得到深蓝色透明溶液1。 再 向/ 试管中加入适量乙醇,并用玻璃棒摩擦试管壁,
第 页,共 页
5 8
{#{QQABLQSEogCIAAIAARhCAwmwCgOQkgEAAagOBFAIsAIBSANABAA=}#}可以观察到有深蓝色的 晶体析出。回答下列问题:
写出蓝色沉淀溶解得[ 到 透( 明 溶3)4液] 的 4离⋅子 2方 程式:___________________________。
(1)加入适量乙醇有深蓝色的 晶体析出的原因:_________________________________。
(2)设计检验晶体中是否含有[ ( 的 实3)验4] 方 案4⋅: 2 _ _________________________________________。
2−
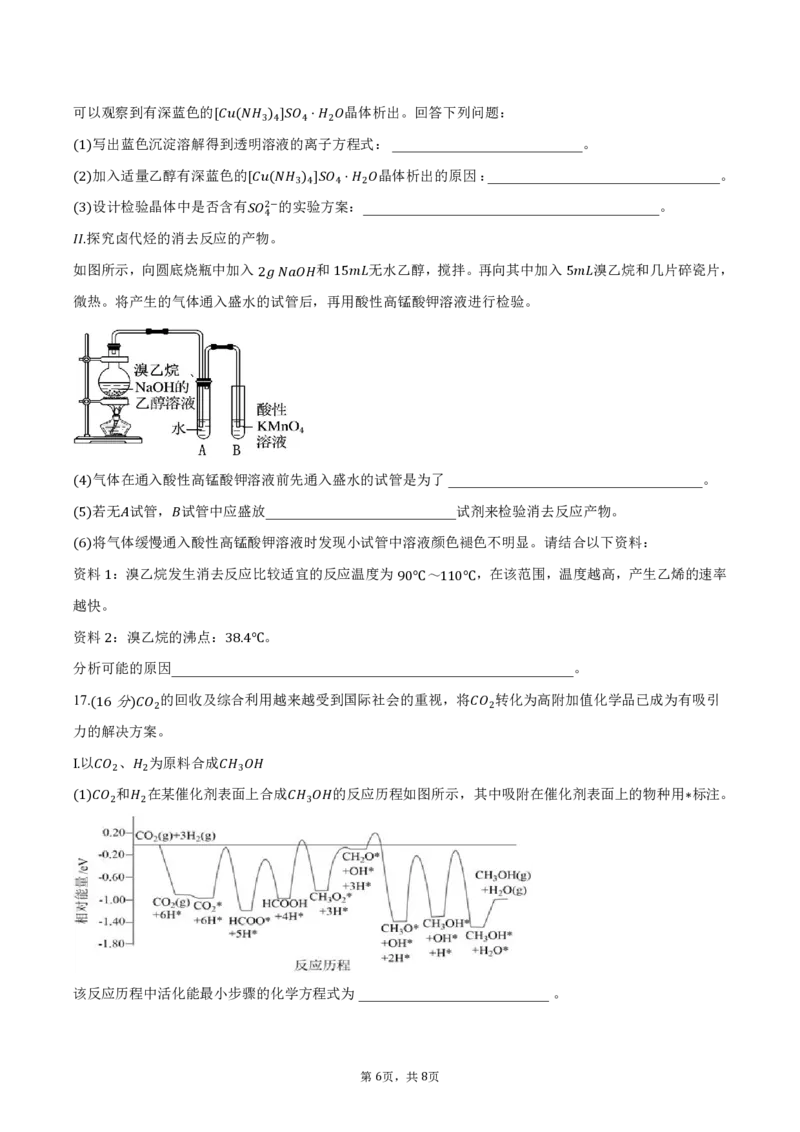
(3)探究卤代烃的消去反应的产 物4。
如 .图所示,向圆底烧瓶中加入 和 无水乙醇,搅拌。再向其中加入 溴乙烷和几片碎瓷片,
微热。将产生的气体通入盛水的2 试 管 后 ,再1用5 酸 性高锰酸钾溶液进行检验。 5
气体在通入酸性高锰酸钾溶液前先通入盛水的试管是为了____________________________________。
(4)若无 试管, 试管中应盛放___________________________试剂来检验消去反应产物。
(5)将气体 缓慢通 入酸性高锰酸钾溶液时发现小试管中溶液颜色褪色不明显。请结合以下资料:
(资6)料 :溴乙烷发生消去反应比较适宜的反应温度为 ~ ,在该范围,温度越高,产生乙烯的速率
越快。1 90℃ 110℃
资料 :溴乙烷的沸点: 。
分析可2能的原因________3_8_._4_℃_____________________________________________。
17. 分 的回收及综合利用越来越受到国际社会的重视,将 转化为高附加值化学品已成为有吸引
力的(1解6决方) 案 2。 2
Ⅰ以 、 为原料合成
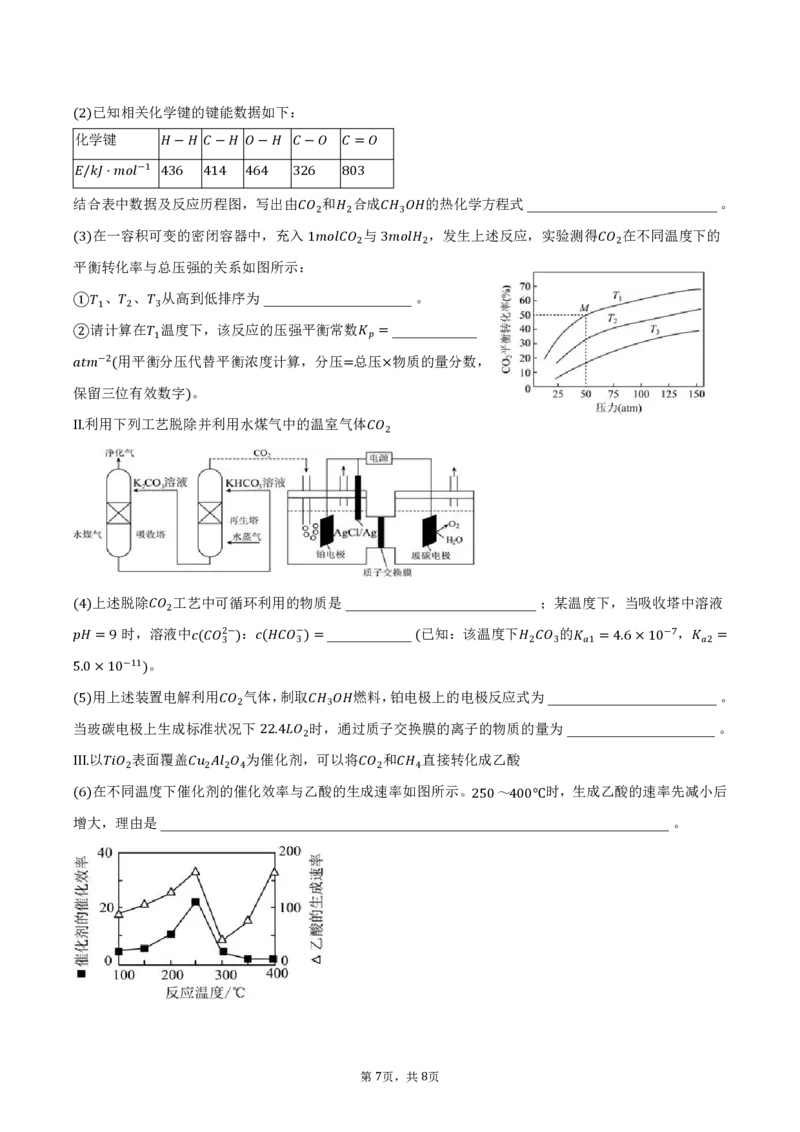
. 2和 2在某催化剂表 面3 上 合成 的反应历程如图所示,其中吸附在催化剂表面上的物种用 标注。
(1) 2 2 3 ∗
该反应历程中活化能最小步骤的化学方程式为___________________________。
第 页,共 页
6 8
{#{QQABLQSEogCIAAIAARhCAwmwCgOQkgEAAagOBFAIsAIBSANABAA=}#}已知相关化学键的键能数据如下:
化学键
(2)
− − − − =
−1
结 /合 表⋅ 中 数 据及43反6应历41程4图,46写4出由326 和 80合3成 的热化学方程式___________________________。
在一容积可变的密闭容器中,充入 2 2 与 3 ,发生上述反应,实验测得 在不同温度下的
(平3)衡转化率与总压强的关系如图所示:1 2 3 2 2
、 、 从高到低排序为_____________________。
① 请1计算 2在 3温度下,该反应的压强平衡常数 ____________
② 用平衡 1分压代替平衡浓度计算,分压 总 压 =物质的量分数,
−2
保 留三(位有效数字 。 = ×
Ⅱ利用下列工艺脱除) 并利用水煤气中的温室气体
. 2
上述脱除 工艺中可循环利用的物质是___________________________;某温度下,当吸收塔中溶液
(4) 时, 溶 液2 中 : ____________ 已知:该温度下 的 ,
2− − −7
=9 。 ( 3 ) ( 3)= ( 2 3 1 =4.6×10 2 =
−11
5.0用×上10述装)置电解利用 气体,制取 燃料,铂电极上的电极反应式为________________________。
(当5)玻碳电极上生成标准状 况2下 时 ,3 通 过质子交换膜的离子的物质的量为_____________________。
Ⅲ以 表面覆盖 为2催2化.4 剂 ,2 可以将 和 直接转化成乙酸
.在 不 同2温度下催 化 2剂 的 2 催4化效率与乙酸的生 成 速2 率 如 4图所示。 ~ 时,生成乙酸的速率先减小后
(增6)大,理由是_____________________________________________2_5_0___4_0_0_℃___________________。
第 页,共 页
7 8
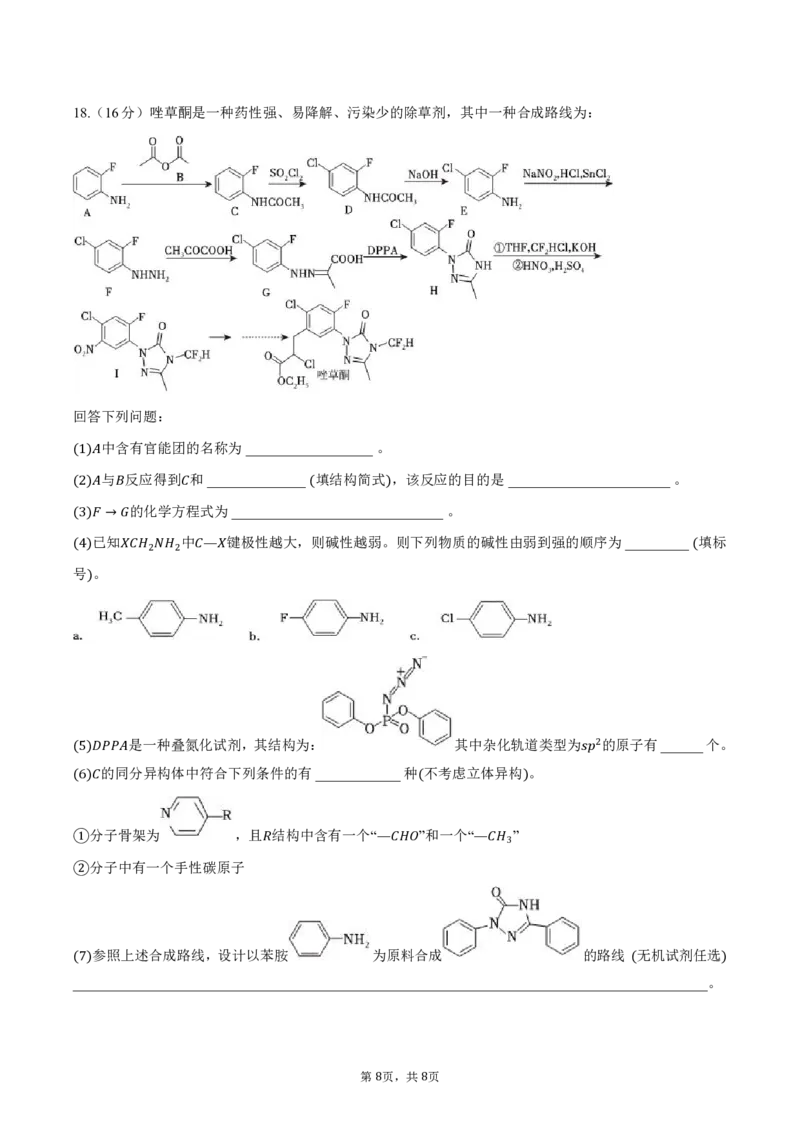
{#{QQABLQSEogCIAAIAARhCAwmwCgOQkgEAAagOBFAIsAIBSANABAA=}#}18.(16分)唑草酮是一种药性强、易降解、污染少的除草剂,其中一种合成路线为:
回答下列问题:
中含有官能团的名称为__________________。
(1) 与 反应得到 和______________ 填结构简式 ,该反应的目的是_______________________。
(2) 的化学方 程式为___________(___________)________。
(3) 已→知 中 键极性越大,则碱性越弱。则下列物质的碱性由弱到强的顺序为_________ 填标
(号4)。 2 2 — (
)
是一种叠氮化试剂,其结构为: 其中杂化轨道类型为 的原子有______个。
2
(5)
的
同
分异构体中符合下列条件的有____________种 不考虑立体异构 。
(6) ( )
分子骨架为 ,且 结构中含有一个“ ”和一个“ ”
①分子中有一个手性碳原子 — — 3
②
参照上述合成路线,设计以苯胺 为原料合成 的路线 无机试剂任选
(_7_)______________________________________________________________________________(__________。
)
第 页,共 页
8 8
{#{QQABLQSEogCIAAIAARhCAwmwCgOQkgEAAagOBFAIsAIBSANABAA=}#}