文档内容
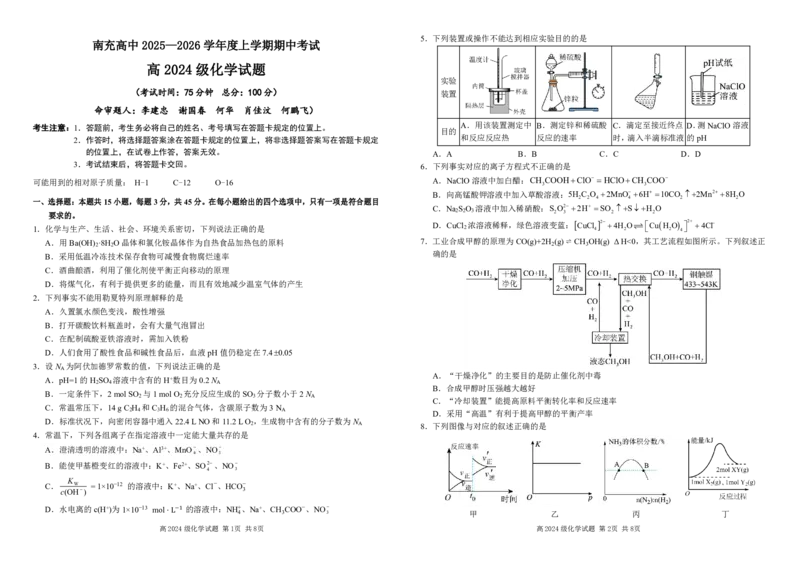
5.下列装置或操作不能达到相应实验目的的是
南充高中 2025—2026 学年度上学期期中考试
高 2024 级化学试题
实验
(考试时间:75分钟 总分:100分) 装置
命审题人:李建忠 谢国春 何华 肖佳汶 何鹏飞)
考生注意:1.答题前,考生务必将自己的姓名、考号填写在答题卡规定的位置上。
A.用该装置测定中 B.测定锌和稀硫酸 C.滴定至接近终点 D.测NaClO溶液
目的
2.作答时,将选择题答案涂在答题卡规定的位置上,将非选择题答案写在答题卡规定 和反应反应热 反应的速率 时,滴入半滴标准液的pH
的位置上,在试卷上作答,答案无效。 A.A B.B C.C D.D
3.考试结束后,将答题卡交回。 6.下列事实对应的离子方程式不正确的是
可能用到的相对原子质量: H-1 C-12 O-16 A.NaClO溶液中加白醋:CH
3
COOHClO HClOCH
3
COO
B.向高锰酸钾溶液中加入草酸溶液:5H C O 2MnO6H 10CO 2Mn28H O
一、选择题:本题共15小题,每题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目 2 2 4 4 2 2
C.Na S O 溶液中加入稀硝酸:S O2 2H SO SH O
要求的。 2 2 3 2 3 2 2
1.化学与生产、生活、社会、环境关系密切,下列说法正确的是
D.CuCl
2
浓溶液稀释,绿色溶液变蓝:CuCl
4
24H
2
O
CuH
2
O
4
2 4Cl
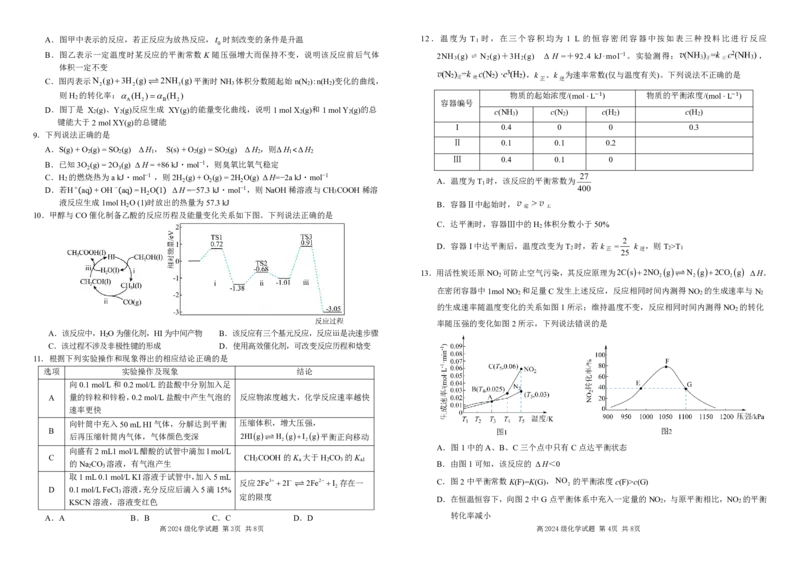
A.用Ba(OH) 2 ·8H 2 O晶体和氯化铵晶体作为自热食品加热包的原料 7.工业合成甲醇的原理为CO(g)+2H 2 (g)⇌ CH 3 OH(g) ΔH<0,其工艺流程如图所示。下列叙述正
确的是
B.采用低温冷冻技术保存食物可减慢食物腐烂速率
C.酒曲酿酒,利用了催化剂使平衡正向移动的原理
D.将煤气化,有利于提供更多的能量,而且有效地减少温室气体的产生
2.下列事实不能用勒夏特列原理解释的是
A.久置氯水颜色变浅,酸性增强
B.打开碳酸饮料瓶盖时,会有大量气泡冒出
C.在配制硫酸亚铁溶液时,需加入铁粉
D.人们食用了酸性食品和碱性食品后,血液pH值仍稳定在7.40.05
3.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.“干燥净化”的主要目的是防止催化剂中毒
A.pH=1的H SO 溶液中含有的H+数目为0.2N
2 4 A
B.合成甲醇时压强越大越好
B.一定条件下,2molSO 与1molO 充分反应生成的SO 分子数小于2N
2 2 3 A
C.“冷却装置”能提高原料平衡转化率和反应速率
C.常温常压下,14gC H 和C H 的混合气体,含碳原子数为3N
2 4 3 6 A D.采用“高温”有利于提高甲醇的平衡产率
D.标准状况下,向密闭容器中通入22.4LNO和11.2LO ,生成物中含有的分子数为N
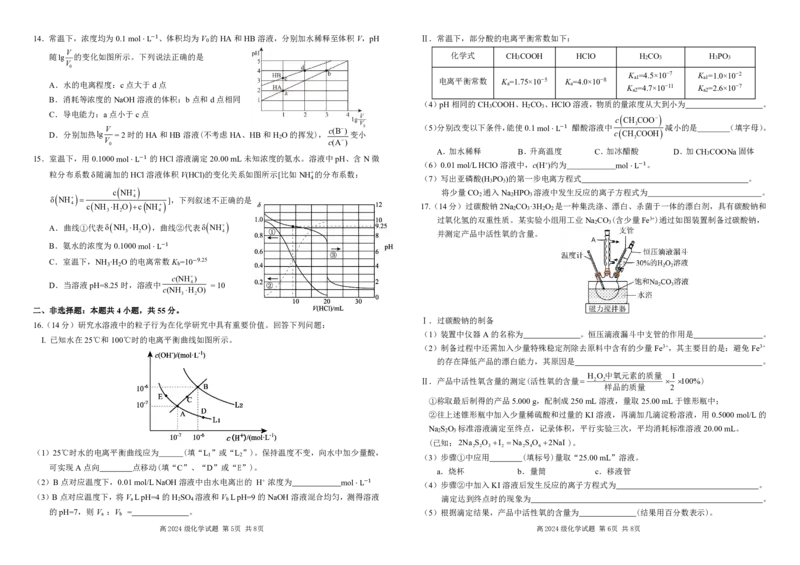
2 A 8.下列图像与对应的叙述正确的是
4.常温下,下列各组离子在指定溶液中一定能大量共存的是
能量/kJ
A.澄清透明的溶液中:Na+、Al3+、MnO、NO 反应速率
4 3
B.能使甲基橙变红的溶液中:K+、Fe2+、SO2、NO
4 3
K
C. W =1×10−12 的溶液中:K+、Na+、Cl-、HCO−
c(OH) 3
D.水电离的c(H+)为1×10−13 mol 的溶液中:NH+、Na+、CH COO−、NO
4 3 3 甲 乙 丙 丁
−1
高⋅2L024级化学试题 第1页 共8页 高2024级化学试题 第2页 共8页A.图甲中表示的反应,若正反应为放热反应,t 时刻改变的条件是升温 12.温度为 T
1
时,在三个容积均为 1 L 的恒容密闭容器中按如表三种投料比进行反应
0
B.图乙表示一定温度时某反应的平衡常数K 随压强增大而保持不变,说明该反应前后气体 2NH (g) ⇌ N (g)+3H (g) Δ H =+92.4 kJ·mol−1。实验测得: ,
3 2 2
体积一定不变
,k 、k 为速率常数(仅与温度有关)。下列说法不正确的是
C.图丙表示N (g)3H (g)2NH (g)平衡时NH 体积分数随起始n(N ):n(H )变化的曲线, 正 逆
2 2 3 3 2 2
则H 的转化率: (H ) (H ) 物质的起始浓度/(mol ) 物质的平衡浓度/(mol )
2 A 2 B 2 容器编号
D.图丁是 X 2 (g)、Y 2 (g)反应生成 XY(g)的能量变化曲线,说明1molX 2 (g)和1molY 2 (g)的总 c(NH 3 ) c(N 2 ) ⋅L −1 c(H 2 ) c(H 2 ) ⋅L −1
键能大于2molXY(g)的总键能
I 0.4 0 0 0.3
9.下列说法正确的是
Ⅱ 0.1 0.1 0.2
A.S(g)+O (g)=SO (g) ΔH , S(s)+O (g)=SO (g) ΔH ,则ΔH <ΔH
2 2 1 2 2 2 1 2
Ⅲ 0.4 0.1 0
B.已知3O (g)=2O (g) ∆H=+86kJ·mol−1,则臭氧比氧气稳定
2 3
C.H 2 的燃烧热为akJ·mol−1 ,则2H 2 (g)+O 2 (g)=2H 2 O(g) ΔH=−2akJ·mol−1 A.温度为T 时,该反应的平衡常数为 27
1
D.若H+ aq +OH− aq =H O 1 ΔH=−57.3kJ·mol−1,则NaOH稀溶液与CH COOH稀溶 400
2 3
液反应生成1molH
2
O(1)时放出的热量为57.3kJ B.容器Ⅱ中起始时,
10.甲醇与CO催化制备乙酸的反应历程及能量变化关系如下图。下列说法正确的是
C.达平衡时,容器Ⅲ中的H 体积分数小于50%
2
2
D.容器I中达平衡后,温度改变为T 时,若k = k ,则T >T
2 正 逆 2 1
25
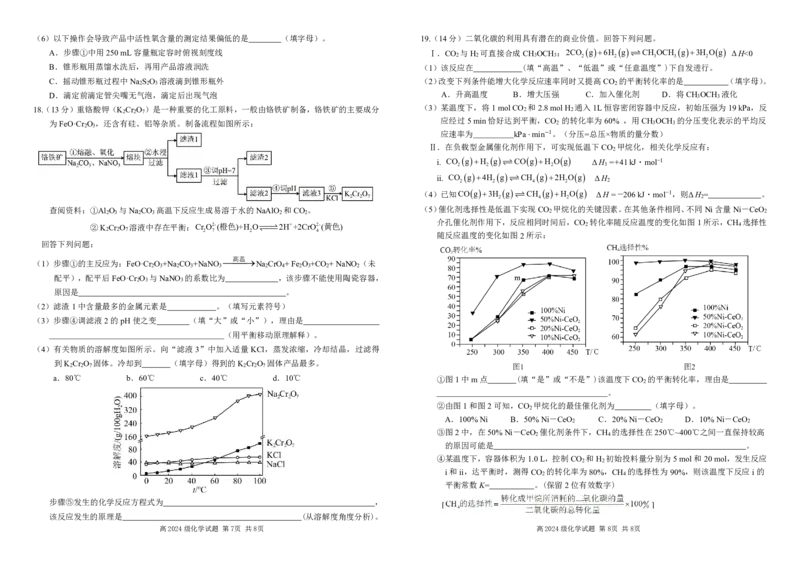
13.用活性炭还原NO 可防止空气污染,其反应原理为2Cs2NO g N g2CO g ΔH。
2 2 2 2
在密闭容器中1molNO 和足量C发生上述反应,反应相同时间内测得NO 的生成速率与N
2 2 2
的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内测得NO 的转化
2
率随压强的变化如图2所示,下列说法错误的是
A.该反应中,HO为催化剂,HI为中间产物 B.该反应有三个基元反应,反应ⅲ是决速步骤
2
C.该过程不涉及非极性键的形成 D.使用高效催化剂,可改变反应历程和焓变
11.根据下列实验操作和现象得出的相应结论正确的是
选项 实验操作及现象 结论
向0.1mol/L和0.2mol/L的盐酸中分别加入足
A 量的锌粒和锌粉,0.2mol/L盐酸中产生气泡的 反应物浓度越大,化学反应速率越快
速率更快
向针筒中充入50mLHI气体,分解达到平衡 压缩体积,增大压强,
B
后再压缩针筒内气体,气体颜色变深 2HIg H gI g平衡正向移动
2 2
向盛有2mL1mol/L醋酸的试管中滴加lmol/L
A.图1中的A、B、C三个点中只有C点达平衡状态
C CH COOH的K 大于H CO 的K
3 a 2 3 a1
的Na CO 溶液,有气泡产生 B.由图1可知,该反应的 ΔH<0
2 3
取1mL0.1mol/LKI溶液于试管中,加入5mL
反应2Fe3 2I 2Fe2I 存在一 C.图2中平衡常数K(F)=K(G),NO
2
的平衡浓度c(F)>c(G)
D 0.1mol/LFeCl 溶液,充分反应后滴入5滴15% 2
3
KSCN溶液,溶液变红色
定的限度 D.在恒温恒容下,向图2中G点平衡体系中充入一定量的NO
2
,与原平衡相比,NO
2
的平衡
A.A B.B C.C D.D 转化率减小
高2024级化学试题 第3页 共8页 高2024级化学试题 第4页 共8页14.常温下,浓度均为0.1mol 、体积均为V 的HA和HB溶液,分别加水稀释至体积V,pH Ⅱ.常温下,部分酸的电离平衡常数如下:
0
−1
随lg V 的变化如图所示。下⋅L列说法正确的是 化学式 CH
3
COOH HClO H
2
CO
3
H
3
PO
3
V
0
A.水的电离程度:c点大于d点 电离平衡常数 K a =1.75×10−5 K a =4.0×10−8
K
K a1
=
=
4
4
.
.
7
5
×
×
1
1
0
0
−
−
1
7
1
K
K
a1 =
=
1
2
.
.
0
6
×
×
1
1
0
0
−
−
2
7
a2 a2
B.消耗等浓度的NaOH溶液的体积:b点和d点相同
(4)pH相同的CH COOH、H CO 、HClO溶液,物质的量浓度从大到小为 。
3 2 3
C.导电能力:a点小于c点
c
CH
COO
D.分别加热lg
V
=2时的HA和HB溶液(不考虑HA、HB和H O的挥发),
c(B)
变小
(5)分别改变以下条件,能使0.1mol 醋酸溶液中 cCH 3 COOH 减小的是 (填字母)。
V
0
2 c(A)
⋅L
−1 3
A.加水稀释 B.升高温度 C.加冰醋酸 D.加CH COONa固体
3
15.室温下,用0.1000mol 的HCl溶液滴定20.00mL未知浓度的氨水。溶液中pH、含N微
(6)0.01mol/LHClO溶液中,c(H+)约为 mol 。
−1
粒分布系数δ随滴加的H⋅LCl溶液体积V(HCl)的变化关系如图所示[比如NH
4
+的分布系数:
(7)写出亚磷酸(H PO )的第一步电离方程式 −1 。
3 3 ⋅L
c
NH
将少量CO 通入Na HPO 溶液中发生反应的离子方程式为 。
δ NH 4 ],下列叙述不正确的是 2 2 3
4 cNH H Oc NH 17.(14分)过碳酸钠2Na CO ·3H O 是一种集洗涤、漂白、杀菌于一体的漂白剂,具有碳酸钠和
3 2 4 2 3 2 2
过氧化氢的双重性质。某实验小组用工业Na CO (含少量Fe3+)通过如图装置制备过碳酸钠,
A.曲线①代表δNH H O,曲线②代表δ NH 2 3
3 2 4 并测定产品中活性氧的含量。
B.氨水的浓度为0.1000mol
−1
C.室温下,NH 3 ∙H 2 O的电离 ⋅ 常 L 数K b =10 9.25
−
c(NH)
D.当溶液pH=8.25时,溶液中 4 =10
c(NH H O)
3 2
二、非选择题:本题共4小题,共55分。
Ⅰ.过碳酸钠的制备
16.(14分)研究水溶液中的粒子行为在化学研究中具有重要价值。回答下列问题:
(1)装置中仪器A的名称为 。恒压滴液漏斗中支管的作用是 。
I. 已知水在25℃和100℃时的电离平衡曲线如图所示。
(2)制备过程中还需加入少量特殊稳定剂除去原料中含有的少量Fe3+,其主要目的是:避免Fe3+
的存在降低产品的漂白能力,其原因是 。
H O中氧元素的质量 1
Ⅱ.产品中活性氧含量的测定(活性氧的含量 2 2 100%)
样品的质量 2
①称取最后制得的产品5.000g,配制成250mL溶液,量取25.00mL于锥形瓶中;
②往上述锥形瓶中加入少量稀硫酸和过量的KI溶液,再滴加几滴淀粉溶液,用0.5000mol/L的
Na S O 标准溶液滴定至终点,记录体积,平行实验三次,平均消耗标准溶液20.00mL。
2 2 3
(已知:2Na S O I Na S O 2NaI )。
2 2 3 2 2 4 6
(1)25℃时水的电离平衡曲线应为 (填“L ”或“L ”)。保持温度不变,向水中加少量酸,
1 2 (3)步骤①中应用 (填标号)量取“25.00mL”溶液。
可实现A点向 点移动(填“C”、“D”或“E”)。
a.烧杯 b.量筒 c.移液管
(2)B点对应温度下,0.01mol/LNaOH溶液中由水电离出的 H+ 浓度为 mol (4)步骤②中加入KI溶液后发生反应的离子方程式为 。
(3)B点对应温度下,将V a LpH=4的H 2 SO 4 溶液和V b LpH=9的NaOH溶液混合均匀,测得 ⋅L 溶−1液 滴定达到终点时的现象为 。
的pH=7,则V
a
:V
b
= 。 (5)根据滴定结果,产品中活性氧的含量为 (结果用百分数表示)。
高2024级化学试题 第5页 共8页 高2024级化学试题 第6页 共8页(6)以下操作会导致产品中活性氧含量的测定结果偏低的是 (填字母)。 19.(14分)二氧化碳的利用具有潜在的商业价值。回答下列问题。
A.步骤①中用250mL容量瓶定容时俯视刻度线 Ⅰ.CO 与H 可直接合成CH OCH :2CO g6H g CH OCH g3H Og ΔH<0
2 2 3 3 2 2 3 3 2
B.锥形瓶用蒸馏水洗后,再用产品溶液润洗 (1)该反应在 (填“高温”、“低温”或“任意温度”)下自发进行。
C.摇动锥形瓶过程中Na S O 溶液滴到锥形瓶外 (2)改变下列条件能增大化学反应速率同时又提高CO 的平衡转化率的是 (填字母)。
2 2 3 2
D.滴定前滴定管尖嘴无气泡,滴定后出现气泡 A.升高温度 B.增大压强 C.加入催化剂 D.将CH
3
OCH
3
液化
18.(13分)重铬酸钾(K 2 Cr 2 O 7 )是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分 (3)某温度下,将1molCO 2 和2.8molH 2 通入1L恒容密闭容器中反应,初始压强为19kPa,反
为FeO·Cr O ,还含有硅、铝等杂质。制备流程如图所示: 应经过5min恰好达到平衡,CO 2 的转化率为60% ,用CH 3 OCH 3 的分压变化表示的平均反
2 3
应速率为 kPa min 1。(分压=总压×物质的量分数)
Ⅱ.在负载型金属催化剂作用下,−可实现低温下CO 甲烷化,相关化学反应有:
⋅ 2
i. CO gH g COgH Og ΔH =+41kJ·mol−1
2 2 2 1
ii. CO g4H g CH g2H Og ΔH
2 2 4 2 2
(4)已知COg3H g CH gH Og ΔH=-206kJ·mol−1,则ΔH = 。
2 4 2 2
查阅资料:①Al 2 O 3 与Na 2 CO 3 高温下反应生成易溶于水的NaAlO 2 和CO 2 。 (5)催化剂选择性是低温下实现CO 2 甲烷化的关键因素。在其他条件相同、不同Ni含量Ni-CeO 2
介孔催化剂作用下,反应相同时间后,CO 转化率随反应温度的变化如图1所示,CH 选择性
②K
2
Cr
2
O
7
溶液中存在平衡:Cr
2
O
7
2-(橙色)+H
2
O2H++2CrO2
4
-(黄色) 2 4
随反应温度的变化如图2所示:
回答下列问题:
(1)步骤①的主反应为:FeO·Cr O +Na CO +NaNO
高温
Na CrO +Fe O +CO +NaNO (未
2 3 2 3 3 2 4 2 3 2 2
配平),配平后FeO·Cr O 与NaNO 的系数比为 ,该步骤不能使用陶瓷容器,
2 3 3
原因是 。
(2)滤渣1中含量最多的金属元素是 。(填写元素符号)
(3)步骤④调滤液2的pH使之变 (填“大”或“小”),理由是
(用平衡移动原理解释)。
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得
到K Cr O 固体。冷却到 (填字母)得到的K Cr O 固体产品最多。
2 2 7 2 2 7
a.80℃ b.60℃ c.40℃ d.10℃ ①图1中m点 (填“是”或“不是”)该温度下CO 的平衡转化率,理由是
2
。
②由图1和图2可知,CO 甲烷化的最佳催化剂为 (填字母)。
2
A.100%Ni B.50%Ni-CeO C.20%Ni-CeO D.10%Ni-CeO
2 2 2
③图2中,在50%Ni-CeO 催化剂条件下,CH 的选择性在250℃~400℃之间一直保持较高
2 4
的原因可能是 。
④某温度下,容器体积为1.0L,控制CO 和H 初始投料量分别为5mol和20mol,发生反应
2 2
i和ii,达平衡时,测得CO 的转化率为80%,CH 的选择性为90%,则该温度下反应i的
2 4
平衡常数K= 。(保留2位有效数字)
步骤⑤发生的化学反应方程式为 ,
该反应发生的原理是 (从溶解度角度分析)。
高2024级化学试题 第7页 共8页 高2024级化学试题 第8页 共8页