文档内容
玉溪一中2025-2026学年上学期高二年级月考一
化学试题
考试时间:75分钟 试卷满分:100分 命题人:段翠红 肖虎 审题人:段翠红 肖虎
可能用到的相对原子质量:H-1 C-12 O-16 S-32 Cl-35.5 Fe-56 Cu-64
一、单选题:本题共14小题,每题3分,共42分。
1.中国传统文化中蕴含着许多化学知识,下列说法错误的是( )
A.“火树银花合,星桥铁锁开”诗词中所涉及的焰色试验,属于化学变化
B.“绿蚁新醅酒,红泥小火炉”,制成火炉的“红泥”中含氧化铁
C.《淮南万毕术》中记载,“曾青得铁则化为铜”,这种湿法炼铜属于置换反应
D.“古人以剂钢为刃,柔铁为茎干,不尔则多断折”里的“剂钢”的硬度比纯铁的大
2.下列化学用语正确的是( )
A.丙烷的结构式:CHCHCH
3 2 3
B.用电子式表示KS的形成过程:
2
C.CCl 的空间填充模型: D.CO 的电子式为
4 2
3.下列有关热化学方程式的说法正确的是( )
A.稀盐酸和稀NaOH溶液的反应热 ,则稀硝酸溶解 在相同条件
下的热化学方程式为
B.甲醇的燃烧热的热化学反应方程式:2CHOH(l)+3O (g)=2CO (g)+4HO(l) ΔH=
3 2 2 2
-726KJ·mol-1
C.已知C(石墨,s) = C(金刚石,s) △H>0 ,则石墨比金刚石稳定
D.将2mol SO (g)和1mol O(g)置于密闭的容器中充分反应生成 SO (g),放出热量 ,
2 2 3
4.设N 为阿伏伽德罗常数的值,下列说法正确的是( )
A
A.氢氧燃料电池正极消耗22.4 L气体时,负极消耗的气体分子数目为2N
A
B.用惰性电极电解饱和食盐水,若阴极产生35.5g气体,则线路中通过N 个电子
A
化学试题第1页(共8页)C.电解精炼铜时,若阴极得到电子数为2N 个,则阳极质量减少64g
A
D.用惰性电极电解稀硫酸的过程中,溶液的质量每减少3.6g转移电子数为0.4N
A
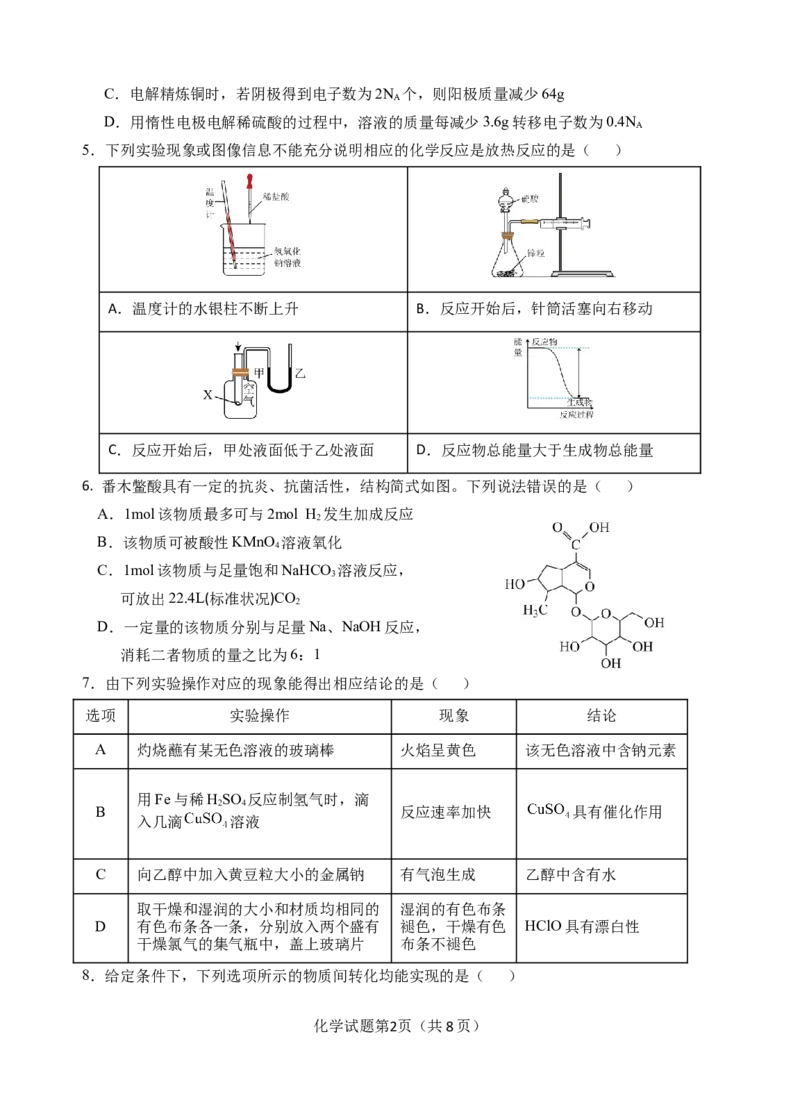
5.下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是( )
A.温度计的水银柱不断上升 B.反应开始后,针筒活塞向右移动
C.反应开始后,甲处液面低于乙处液面 D.反应物总能量大于生成物总能量
6. 番木鳖酸具有一定的抗炎、抗菌活性,结构简式如图。下列说法错误的是( )
A.1mol该物质最多可与2mol H 发生加成反应
2
B.该物质可被酸性KMnO 溶液氧化
4
C.1mol该物质与足量饱和NaHCO 溶液反应,
3
可放出22.4L(标准状况)CO
2
D.一定量的该物质分别与足量Na、NaOH反应,
消耗二者物质的量之比为6:1
7.由下列实验操作对应的现象能得出相应结论的是( )
选项 实验操作 现象 结论
A 灼烧蘸有某无色溶液的玻璃棒 火焰呈黄色 该无色溶液中含钠元素
用Fe与稀HSO 反应制氢气时,滴
2 4
B 反应速率加快 具有催化作用
入几滴 溶液
C 向乙醇中加入黄豆粒大小的金属钠 有气泡生成 乙醇中含有水
取干燥和湿润的大小和材质均相同的 湿润的有色布条
D 有色布条各一条,分别放入两个盛有 褪色,干燥有色 HClO具有漂白性
干燥氯气的集气瓶中,盖上玻璃片 布条不褪色
8.给定条件下,下列选项所示的物质间转化均能实现的是( )
化学试题第2页(共8页)A. B.
C. D.
9.X、Y、Z、M四种主族元素,原子序数依次增大,分别位于三个不同短周期,Z与M同主
族,Y与Z核电荷数相差1,M原子的电子总数是其最外层电子数的3倍。下列说法正确的是
( )
A.原子半径:Z>Y B.简单氢化物的还原性:Z>M
C.最高价氧化物对应水化物的酸性:Z>M D.X、Y能组成电子数为8的分子
10. 铜-铈氧化物(xCuO·yCeO ,Ce是活泼金属)催化氧化可除去H 中少量CO,总反应为
2 2
2CO+O=2CO ,其反应过程与能量关系及可能机理如下图所示。下列说法正确的是( )
2 2
A.(i)中只有一种元素化合价发生变化
B.步骤(iii)中既有共价键的断裂,也有共价键的生成
C.反应过程中催化剂未参与反应
D.总反应过程中形成化学键释放的总能量低于断裂化学键吸收的总能量
11. 根据能量变化示意图,下列说法不正确的是( )
A.相同质量的NO (g)和NO(g),前者具有的能量较高
2 2 4
B.ΔH=ΔH +ΔH+ΔH+ΔH
5 1 2 3 4
C.2HO(l)=2H(g)+O(g) ΔH=-ΔH >0
2 2 2 6 5
D.NH(l)+NO (g)= N(g)+2HO(l) ΔH ,则ΔH>ΔH
2 4 2 2 2 4
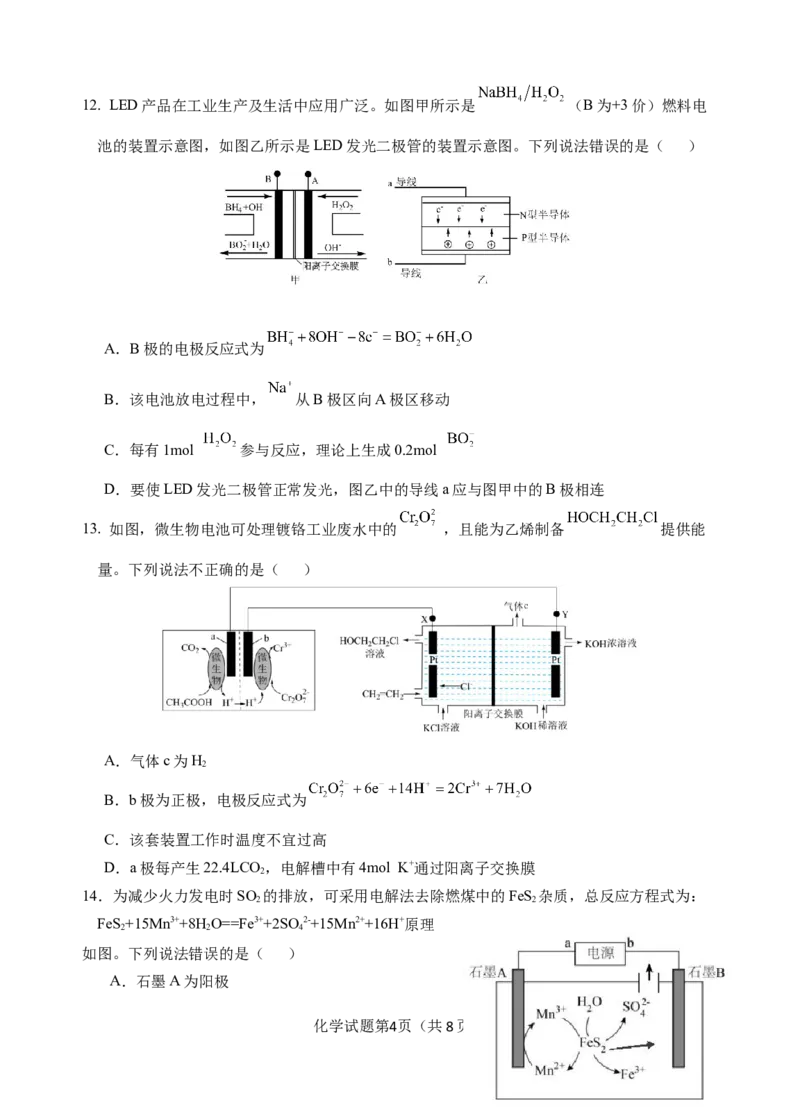
化学试题第3页(共8页)12. LED产品在工业生产及生活中应用广泛。如图甲所示是 (B为+3价)燃料电
池的装置示意图,如图乙所示是LED发光二极管的装置示意图。下列说法错误的是( )
A.B极的电极反应式为
B.该电池放电过程中, 从B极区向A极区移动
C.每有1mol 参与反应,理论上生成0.2mol
D.要使LED发光二极管正常发光,图乙中的导线a应与图甲中的B极相连
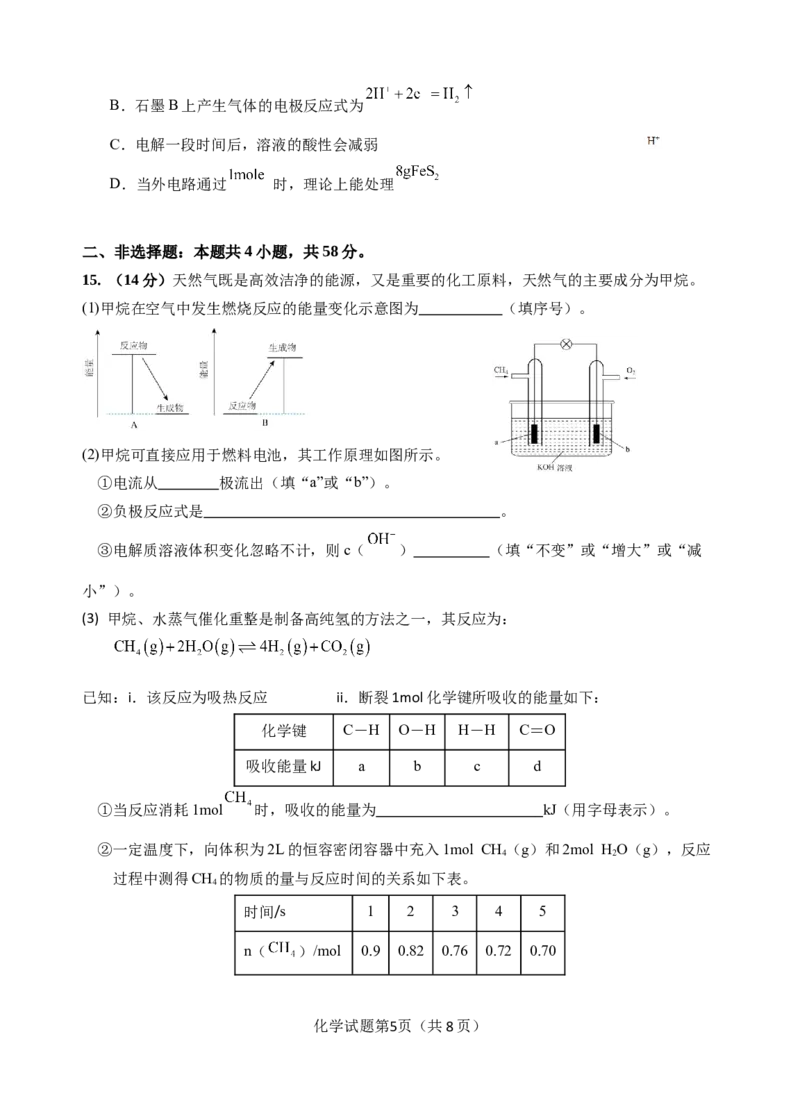
13. 如图,微生物电池可处理镀铬工业废水中的 ,且能为乙烯制备 提供能
量。下列说法不正确的是( )
A.气体c为H
2
B.b极为正极,电极反应式为
C.该套装置工作时温度不宜过高
D.a极每产生22.4LCO ,电解槽中有4mol K+通过阳离子交换膜
2
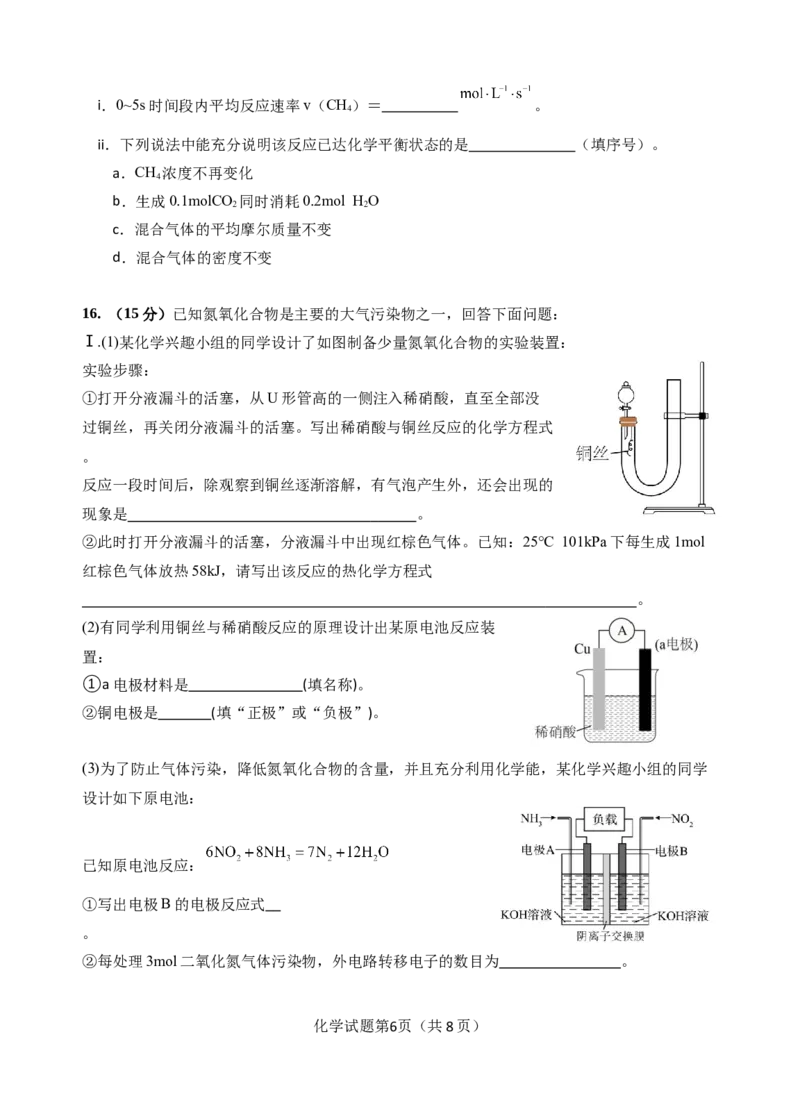
14.为减少火力发电时SO 的排放,可采用电解法去除燃煤中的FeS 杂质,总反应方程式为:
2 2
FeS+15Mn3++8H O==Fe3++2SO2-+15Mn2++16H+原理
2 2 4
如图。下列说法错误的是( )
A.石墨A为阳极
化学试题第4页(共8页)B.石墨B上产生气体的电极反应式为
C.电解一段时间后,溶液的酸性会减弱
D.当外电路通过 时,理论上能处理
二、非选择题:本题共4小题,共58分。
15. (14分)天然气既是高效洁净的能源,又是重要的化工原料,天然气的主要成分为甲烷。
(1)甲烷在空气中发生燃烧反应的能量变化示意图为 (填序号)。
(2)甲烷可直接应用于燃料电池,其工作原理如图所示。
①电流从 极流出(填“a”或“b”)。
②负极反应式是 。
③电解质溶液体积变化忽略不计,则c( ) (填“不变”或“增大”或“减
小”)。
(3) 甲烷、水蒸气催化重整是制备高纯氢的方法之一,其反应为:
已知:i.该反应为吸热反应 ii.断裂1mol化学键所吸收的能量如下:
化学键 C-H O-H H-H C=O
吸收能量kJ a b c d
①当反应消耗1mol 时,吸收的能量为 kJ(用字母表示)。
②一定温度下,向体积为2L的恒容密闭容器中充入1mol CH(g)和2mol HO(g),反应
4 2
过程中测得CH 的物质的量与反应时间的关系如下表。
4
时间/s 1 2 3 4 5
n( )/mol 0.9 0.82 0.76 0.72 0.70
化学试题第5页(共8页)i.0~5s时间段内平均反应速率v(CH)= 。
4
ii.下列说法中能充分说明该反应已达化学平衡状态的是 (填序号)。
a.CH 浓度不再变化
4
b.生成0.1molCO 同时消耗0.2mol HO
2 2
c.混合气体的平均摩尔质量不变
d.混合气体的密度不变
16. (15分)已知氮氧化合物是主要的大气污染物之一,回答下面问题:
Ⅰ.(1)某化学兴趣小组的同学设计了如图制备少量氮氧化合物的实验装置:
实验步骤:
①打开分液漏斗的活塞,从U形管高的一侧注入稀硝酸,直至全部没
过铜丝,再关闭分液漏斗的活塞。写出稀硝酸与铜丝反应的化学方程式
。
反应一段时间后,除观察到铜丝逐渐溶解,有气泡产生外,还会出现的
现象是 。
②此时打开分液漏斗的活塞,分液漏斗中出现红棕色气体。已知:25℃ 101kPa下每生成1mol
红棕色气体放热58kJ,请写出该反应的热化学方程式
。
(2)有同学利用铜丝与稀硝酸反应的原理设计出某原电池反应装
置:
①a电极材料是 (填名称)。
②铜电极是 (填“正极”或“负极”)。
(3)为了防止气体污染,降低氮氧化合物的含量,并且充分利用化学能,某化学兴趣小组的同学
设计如下原电池:
已知原电池反应:
①写出电极B的电极反应式
。
②每处理3mol二氧化氮气体污染物,外电路转移电子的数目为 。
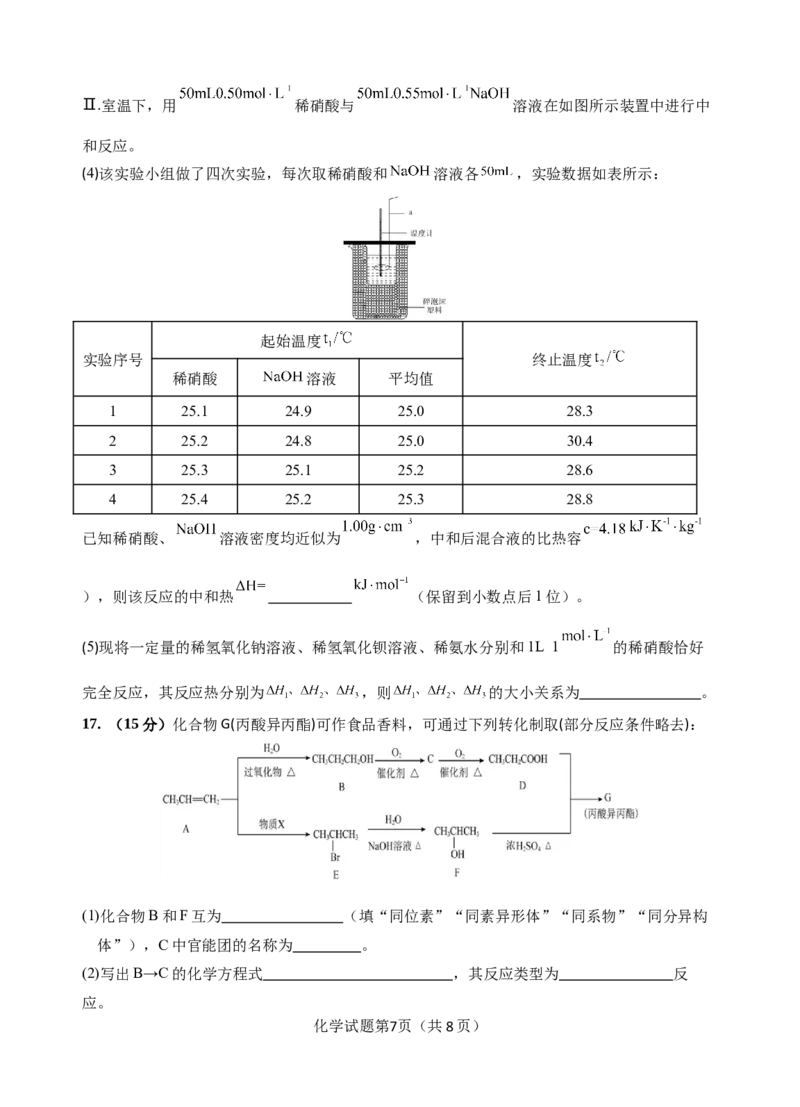
化学试题第6页(共8页)Ⅱ.室温下,用 稀硝酸与 溶液在如图所示装置中进行中
和反应。
(4)该实验小组做了四次实验,每次取稀硝酸和 溶液各 ,实验数据如表所示:
起始温度
实验序号 终止温度
稀硝酸 溶液 平均值
1 25.1 24.9 25.0 28.3
2 25.2 24.8 25.0 30.4
3 25.3 25.1 25.2 28.6
4 25.4 25.2 25.3 28.8
已知稀硝酸、 溶液密度均近似为 ,中和后混合液的比热容
),则该反应的中和热 (保留到小数点后1位)。
(5)现将一定量的稀氢氧化钠溶液、稀氢氧化钡溶液、稀氨水分别和1L 1 的稀硝酸恰好
完全反应,其反应热分别为 ,则 的大小关系为 。
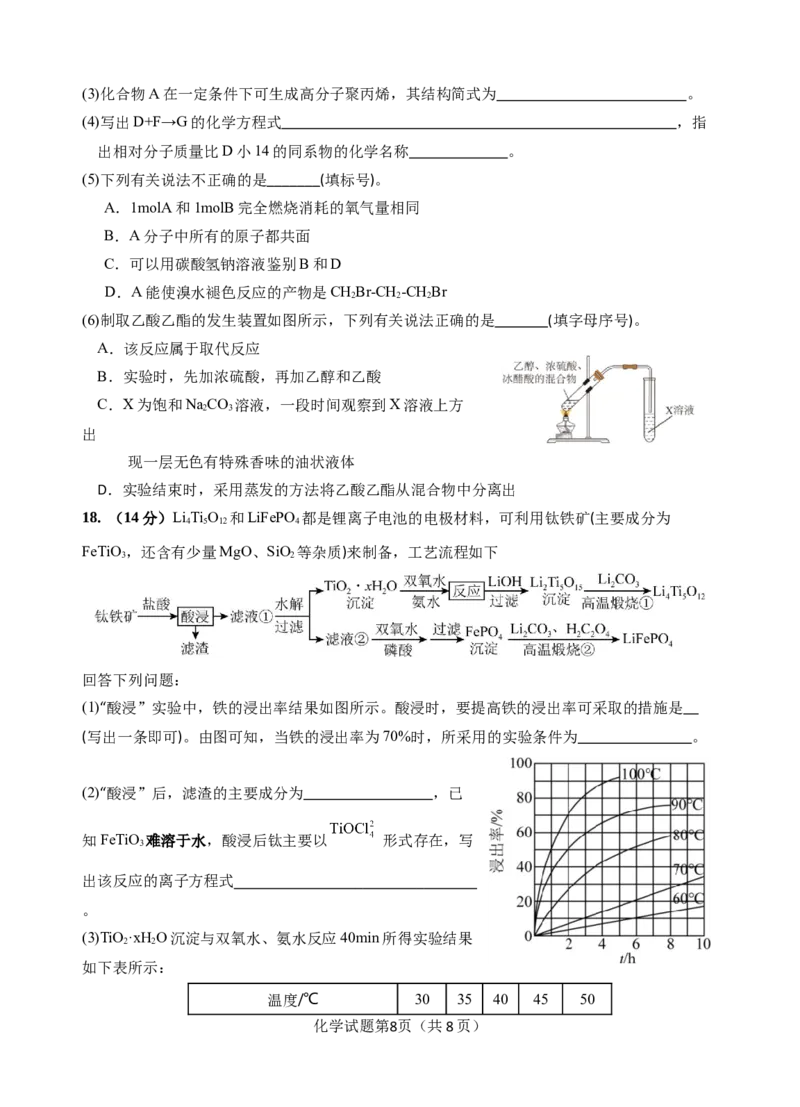
17. (15分)化合物G(丙酸异丙酯)可作食品香料,可通过下列转化制取(部分反应条件略去):
(1)化合物B和F互为 (填“同位素”“同素异形体”“同系物”“同分异构
体”),C中官能团的名称为 。
(2)写出B→C的化学方程式 ,其反应类型为 反
应。
化学试题第7页(共8页)(3)化合物A在一定条件下可生成高分子聚丙烯,其结构简式为 。
(4)写出D+F→G的化学方程式 ,指
出相对分子质量比D小14的同系物的化学名称 。
(5)下列有关说法不正确的是_______(填标号)。
A.1molA和1molB完全燃烧消耗的氧气量相同
B.A分子中所有的原子都共面
C.可以用碳酸氢钠溶液鉴别B和D
D.A能使溴水褪色反应的产物是CHBr-CH -CHBr
2 2 2
(6)制取乙酸乙酯的发生装置如图所示,下列有关说法正确的是 (填字母序号)。
A.该反应属于取代反应
B.实验时,先加浓硫酸,再加乙醇和乙酸
C.X为饱和NaCO 溶液,一段时间观察到X溶液上方
2 3
出
现一层无色有特殊香味的油状液体
D.实验结束时,采用蒸发的方法将乙酸乙酯从混合物中分离出
18. (14分)LiTi O 和LiFePO 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为
4 5 12 4
FeTiO,还含有少量MgO、SiO 等杂质)来制备,工艺流程如下
3 2
回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如图所示。酸浸时,要提高铁的浸出率可采取的措施是
(写出一条即可)。由图可知,当铁的浸出率为70%时,所采用的实验条件为 。
(2)“酸浸”后,滤渣的主要成分为 ,已
知FeTiO 难溶于水,酸浸后钛主要以 形式存在,写
3
出该反应的离子方程式
。
(3)TiO·xH O沉淀与双氧水、氨水反应40min所得实验结果
2 2
如下表所示:
温度/℃ 30 35 40 45 50
化学试题第8页(共8页)TiO·xH O转化率% 92 95 97 93 88
2 2
分析40℃时TiO·xH O转化率最高的原因 。
2 2
(4)Li Ti O 中Ti的化合价为+4,其中过氧键(过氧化合物中氧和氧之间的连接方式为过氧键)
2 5 15
的数目为 。某可充电的锂离子电池以LiTi O 为正极,嵌入锂的碳材料为负极,含
4 5 12
Li+导电固体为电解质。放电时的电池反应为 ,则充电时
阴极电极反应式为 。
(5)写出“高温煅烧②”中由FePO 制备LiFePO 的化学方程式 。
4 4
化学试题第9页(共8页)