文档内容
B.硫酸工业中,在接触室安装热交换器是为了利用SO 转化为H SO 时放出的热量
2007年天津市高考化学试卷 3 2 4
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl 进入阳极室
2
一、选择题(共7小题,每小题6分,满分42分)
D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
1.(6分)2007年3月21日,我国公布了111号元素Rg的中文名称.该元素名称及所在周期是( )
7.(6 分)天津是我国研发和生产锂离子电池的重要基地.锂离子电池正极材料是含锂的二氧化钴
A.錀 第七周期 B.镭 第七周期
(LiCoO ),充电时LiCoO 中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C )中,以LiC 表示.
2 2 6 6
C.铼 第六周期 D.氡 第六周期
2.(6分)为达到预期的实验目的,下列操作正确的是( )
电池反应为LiCoO +C CoO +LiC ,下列说法正确的是( )
2 6 2 6
A.欲配制质量分数为10%的ZnSO 溶液,将10gZnSO •7H 0溶解在90g水中
4 4 2
B.欲制备Fe(OH) 胶体,向盛有沸水的烧杯中滴加FeCl 饱和溶液并长时间煮沸
3 3
A.充电时,电池的负极反应为LiC ﹣e﹣=Li++C
6 6
C.为鉴别KCl、AlCl 和MgCl 溶液,分别向三种溶液中滴加NaOH溶液至过量
3 2
B.放电时,电池的正极反应为CoO +Li++e﹣=LiCoO
2 2
D.为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用
C.羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质
3.(6分)下列关于粒子结构的描述不正确的是( )
D.锂离子电池的比能量(单位质量释放的能量)低
A.H S和NH 均是价电子总数为8的极性分子
2 3
二、非选择题(共4小题,满分66分)
B.HS﹣和HCl均是含一个极性键的18电子粒子
8.(14分)U、V、W、X、Y、Z是原子序数依次增大的六种常见元素.Y的单质在W 中燃烧的产物可使品
2
C.CH Cl 和CCl 均是四面体构型的非极性分子
2 2 4
红溶液褪色.Z和W元素形成的化合物Z W 具有磁性.U的单质在W 中燃烧可生成UW和UW 两种气体.
3 4 2 2
D.1 mol D 16O中含中子、质子、电子各10 N (N 代表阿伏加德罗常数的值)
2 A A
X的单质是一种金属,该金属在UW 中剧烈燃烧生成黑、白两种固体.
2
4.(6分)草酸是二元中强酸,草酸氢钠溶液显酸性.常温下,向 10mL 0.01mol•L﹣1NaHC O 溶液中滴加
2 4
请回答下列问题:
0.01mol•L﹣1NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是( )
(1)V的单质分子的结构式为 ;XW的电子式为 ;Z元素在周期表中的位置是 .
A.V(NaOH)=0时,c(H+)=1×10﹣2mol•L﹣1
(2)U元素形成的同素异形体的晶体类型可能是(填序号) .
B.V(NaOH)<10mL时,不可能存在c(Na+)=2c(C O 2﹣)+c(HC O ﹣ )
2 4 2 4
原子晶体 离子晶体 分子晶体 金属晶体
C.V(NaOH)=10 mL时,c(H+)=1×10﹣7mol•L﹣1
①(3)U、V、W②形成的10电子氢③化物中,U、V的④氢化物沸点较低的是(写化学式) ;V、W的氢
D.V(NaOH)>10 mL时,c(Na+)>c(C O 2﹣)>c(HC O ﹣ )
2 4 2 4 化物分子结合H+能力较强的是(写化学式) ,用一个离子方程式加以证明 .
5.(6分)25℃时,水的电离达到平衡:H O H++OH﹣△H>0,下列叙述正确的是( )
2 (4)YW 气体通入BaCl 和HNO 的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为
2 2 3
A.向水中加入氨水,平衡逆向移动,c(O⇌H﹣)降低
,由此可知VW和YW 还原性较强的是(写化学式) .
2
B.向水中加入少量固体硫酸氢钠,c(H+)增大,K 不变
W
9.(19分)奶油中有一种只含C、H、O的化合物A.A可用作香料,其相对分子质量为88,分子中C、H、O
C.向水中加入少量固体CH COONa,平衡逆向移动,c(H+)降低
3
原子个数比为2:4:1.
D.将水加热,K 增大,pH不变
W
(1)A的分子式为 .
6.(6分)下列有关工业生产的叙述正确的是( )
(2)写出与A分子式相同的所有酯的结构简式: .
A.合成氨生产过程中将NH 液化分离,可加快正反应速率,提高N 、H 的转化率
3 2 2已知:
A中含有碳氧双键,与A相关的反应如下:
(1)图中气体发生和尾气处理装置不够完善,请你提出改进意见 .
利用改进后的正确装置进行实验,请回答下列问题:
(2)B中反应的离子方程式: ;E中反应的化学方程式: .
(3)写出A→E、E→F的反应类型:A→E 、E→F .
(3)C、D中的试剂分别是 、 .
(4)写出A、C、F的结构简式:A 、C 、F .
(4)仪器A、B的名称分别是 、 ,F的作用是 .
(5)写出B→D反应的化学方程式: .
(5)如果在加热E时温度过高,对实验结果的影响是 ,在F中可能出现的现象是 .
(6)在空气中长时间搅拌奶油,A可转化为相对分子质量为86的化合物G,G的一氯代物只有一种,写出
(6)S Cl 粗品中可能混有的杂质是(填写两种) 、 ,为了提高S Cl 的纯度,关键的操作是
2 2 2 2
G的结构简式: .A→G的反应类型为 .
控制好温度和 .
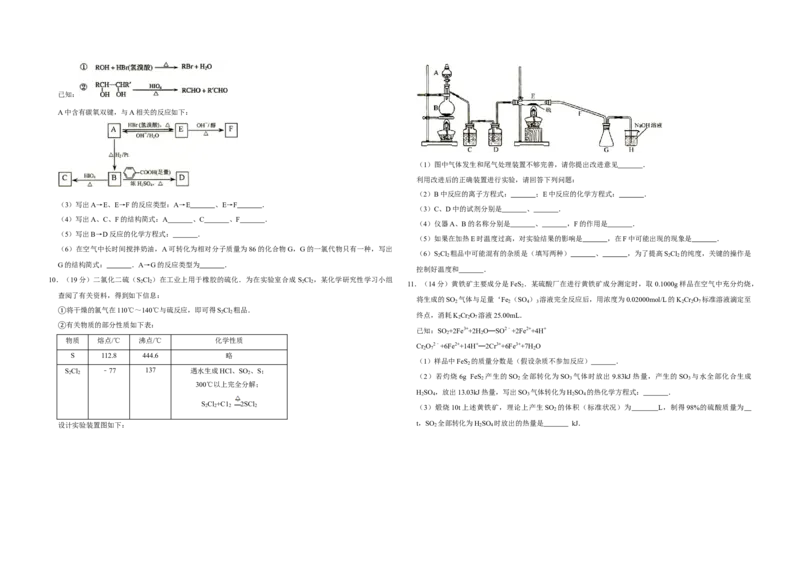
10.(19分)二氯化二硫(S Cl )在工业上用于橡胶的硫化.为在实验室合成 S Cl ,某化学研究性学习小组
2 2 2 2 11.(14分)黄铁矿主要成分是FeS .某硫酸厂在进行黄铁矿成分测定时,取0.1000g样品在空气中充分灼烧,
2
查阅了有关资料,得到如下信息:
将生成的SO 气体与足量‘Fe (SO ) 溶液完全反应后,用浓度为0.02000mol/L的K Cr O 标准溶液滴定至
2 2 4 3 2 2 7
将干燥的氯气在110℃~140℃与硫反应,即可得S Cl 粗品.
2 2
终点,消耗K Cr O 溶液25.00mL.
2 2 7
①有关物质的部分性质如下表:
已知:SO +2Fe3++2H O═SO2﹣+2Fe2++4H+
2 2
②物质 熔点/℃ 沸点/℃ 化学性质
Cr O 2﹣+6Fe2++14H+═2Cr3++6Fe3++7H O
2 7 2
S 112.8 444.6 略
(1)样品中FeS 的质量分数是(假设杂质不参加反应) .
2
S Cl ﹣77 137 遇水生成HCl、SO 、S;
2 2 2
(2)若灼烧6g FeS 产生的SO 全部转化为SO 气体时放出9.83kJ热量,产生的SO 与水全部化合生成
2 2 3 3
300℃以上完全分解;
H SO ,放出13.03kJ热量,写出SO 气体转化为H SO 的热化学方程式: .
2 4 3 2 4
S Cl +C1 2SCl
2 2 2 2 (3)煅烧10t上述黄铁矿,理论上产生SO 的体积(标准状况)为 L,制得98%的硫酸质量为
2
设计实验装置图如下: t,SO 2 全部转化为H 2 SO 4 时放出的热量是 kJ.