文档内容
高考化学试卷(2013 四川)
一、选择题共42分
1.(6分)(2013•四川)化学与生活密切相关,下列说法不正确的是( )
A 二氧化硫可广泛用于食品的增白
.
B.葡萄糖可用于补钙药物的合成
C.聚乙烯塑料制品可用于食品的包装
D 次氯酸钠溶液可用于环境的消毒杀菌
.
2.(6分)(2013•四川)下列物质分类正确的是( )
A SO 、SiO 、CO均为酸性氧化物
2 2
.
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D 福尔马林、水玻璃、氨水均为混合物
.
3.(6分)(2013•四川)下列离子方程式正确的是( )
A Cl 通入水中:Cl +H O═2H++Cl﹣+ClO﹣
2 2 2
.
B.双氧水中加入稀硫酸和KI溶液:H O +2H++2I﹣═I +2H O
2 2 2 2
C.
用铜作电极电解CuSO 溶液:2Cu2++2H O 2Cu+O ↑+4H+
4 2 2
D Na S O 溶液中加入稀硫酸:2S O 2﹣+4H+═SO 2﹣+3S↓+2H O
2 2 3 2 3 4 2
.
4.(6分)(2013•四川)短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原
子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是(
)
A W、Y、Z的电负性大小顺序一定是Z>Y>W
.
B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C.Y、Z形成的分子空间构型可能是正四面体
D WY 分子中δ键与π键的数目之比是2:1
2
.
5.(6分)(2013•四川)室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体
积变化),实验数据如下表:
实验编号 起始浓度/(mol•L﹣1) 反应后溶液的pH
c(HA) c
(KOH
)
① 0.1 0.1 9
② x 0.2 7
下列判断不正确的是( )
A 实验①反应后的溶液中:c(K+)>c(A﹣)>c(OH﹣)>c(H+)
.
B.
实验①反应后的溶液中:c(OH﹣)=c(K+)﹣c(A﹣)= mol/L
C.实验②反应后的溶液中:c(A﹣)+c(HA)>0.1 mol/L
D 实验②反应后的溶液中:c(K+)=c(A﹣)>c(OH﹣)=c(H+)
.6.(6分)(2013•四川)在一定温度下,将气体X和气体Y 各0.16mol充入10L恒容
密闭容器中,发生反应X(g)+Y(g) ⇌2Z(g)△H<0,一段时间后达到平衡.反应过
程中测定的数据如下表,下列说法正确的是( )
t/min 2 4 7 9
n(Y)/mol 0.12 0.11 0.10 0.10
A 反应前2min的平均速率v(Z)=2.0×10﹣3 mol/(L•min)
.
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
.
7.(6分)(2013•四川)1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL、质量分数为
63%的浓硝酸中,得到NO 和N O 的混合气体1120mL(标准状况),向反应后的溶液中
2 2 4
加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的
是( )
A 该合金中铜与镁的物质的量之比是2:1
.
B.该浓硝酸中HNO 的物质的量浓度是14.0 mol/L
3
C.NO 和N O 的混合气体中,NO 的体积分数是80%
2 2 4 2
D 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
.
二、非选择题(共58分)
8.(11分)(2013•四川)X、Y、Z、R为前四周期元素且原子序数依次增大.X的单质
与氢气可化合生成气体G,其水溶液pH>7;Y的单质是一种黄色晶体;R基态原子3d轨
道的电子数是4s轨道电子数的3倍.Y、Z分别与钠元素可形成化合物Q和J,J的水溶液
与AgNO 溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应
3
生成M.
请回答下列问题:
(1)M固体的晶体类型是 .
(2)Y基态原子的核外电子排布式是 ;G分子中X原
子的杂化轨道类型是 .
(3)L的悬浊液中加入Q的溶液,白色沉淀转化为黑色沉淀,其原因是
(4)R的一种含氧酸根RO 2﹣具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,
4
并有无色气体产生,该反应的离子方程式是9.(15分)(2013•四川)为了探究AgNO 的氧化性和热稳定性,某化学兴趣小组设计了
3
如下实验.
Ⅰ.AgNO 的氧化性
3
将光亮的铁丝伸入AgNO 溶液中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,
3
将溶液中的Ag+ 除尽后,进行了如下实验.可选用的试剂:KSCN溶液、K [Fe(CN)
3 6
溶液、氯水.
]
(1)请完成下表:
操作 现象 结论
取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 存在Fe3+
取少量除尽Ag+后的溶液于试管中,加入 存在Fe2+
,振荡
【实验结论】Fe的氧化产物为Fe2+和Fe2+.
Ⅱ.AgNO 的热稳定性
3
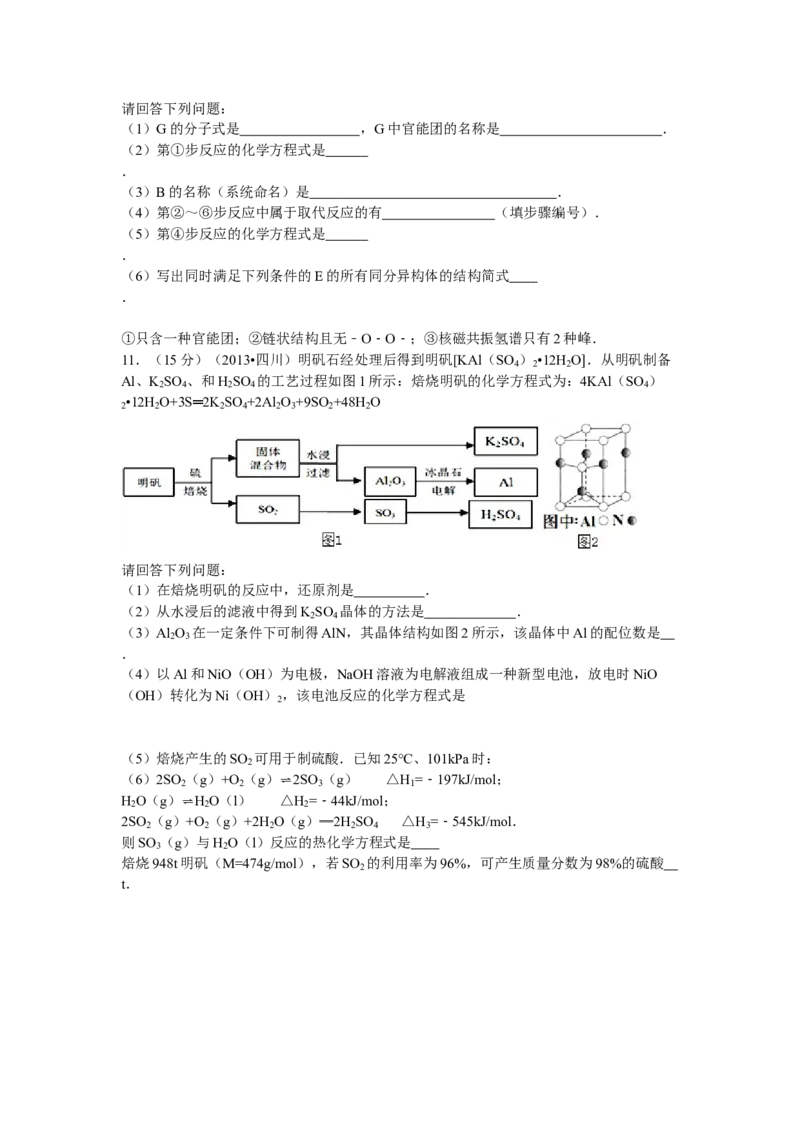
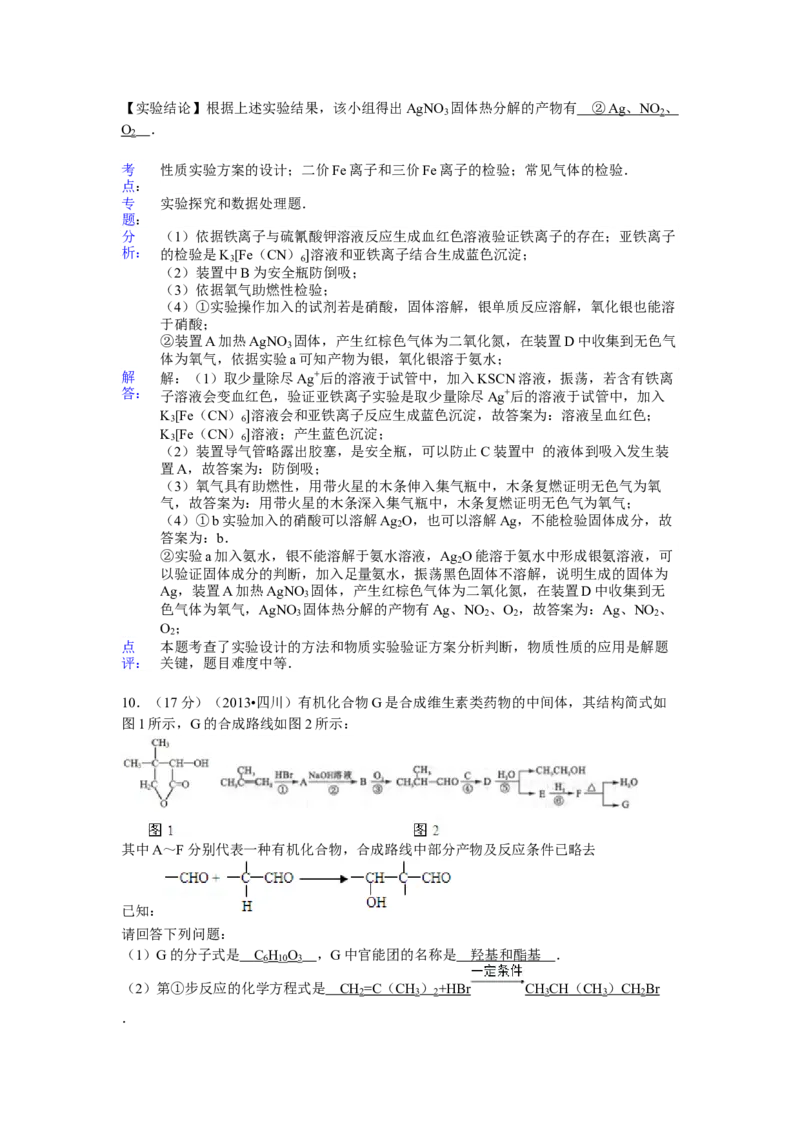
用如图所示的实验装置A加热AgNO 固体,产生红棕色气体,在装置D中收集到无色气
3
体.当反应结束后,试管中残留固体为黑色.
(2)装置B的作用是 .
(3)经小组讨论并验证该无色气体为O ,其验证方法是
2
.
(4)【查阅资料】Ag O和粉末状的Ag均为黑色; Ag O可溶于氨水.
2 2
【提出设想】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag O;ⅲ.Ag和Ag O.
2 2
【实验验证】该小组为验证上述猜想,分别取少量黑色固体放入试管中,进行了如下实验.
实验编号 操作 现象
a 加入足量氨水,振荡 黑色固体不溶解
b 加入足量稀硝酸,振荡 黑色固体溶解,并有气体产生
【实验评价】根据上述实验,不能确定固体产物成分的实验是 (填实验编
号).
【实验结论】根据上述实验结果,该小组得出AgNO 固体热分解的产物有
3
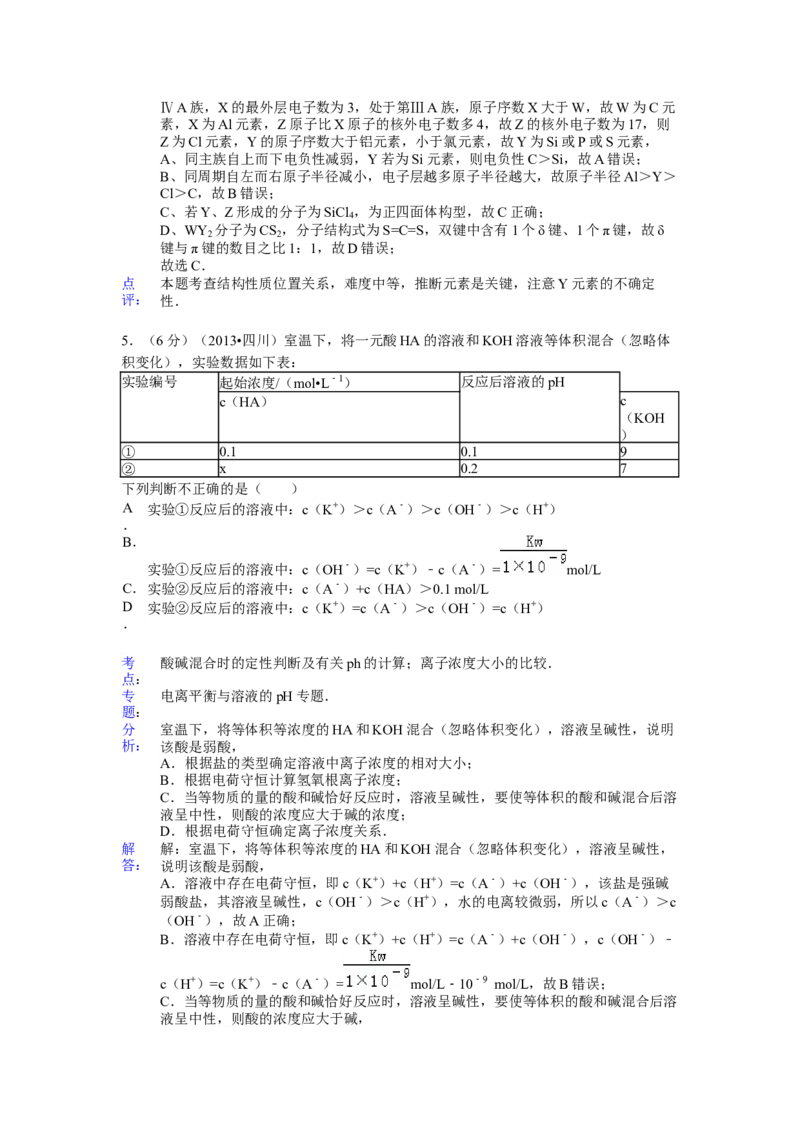
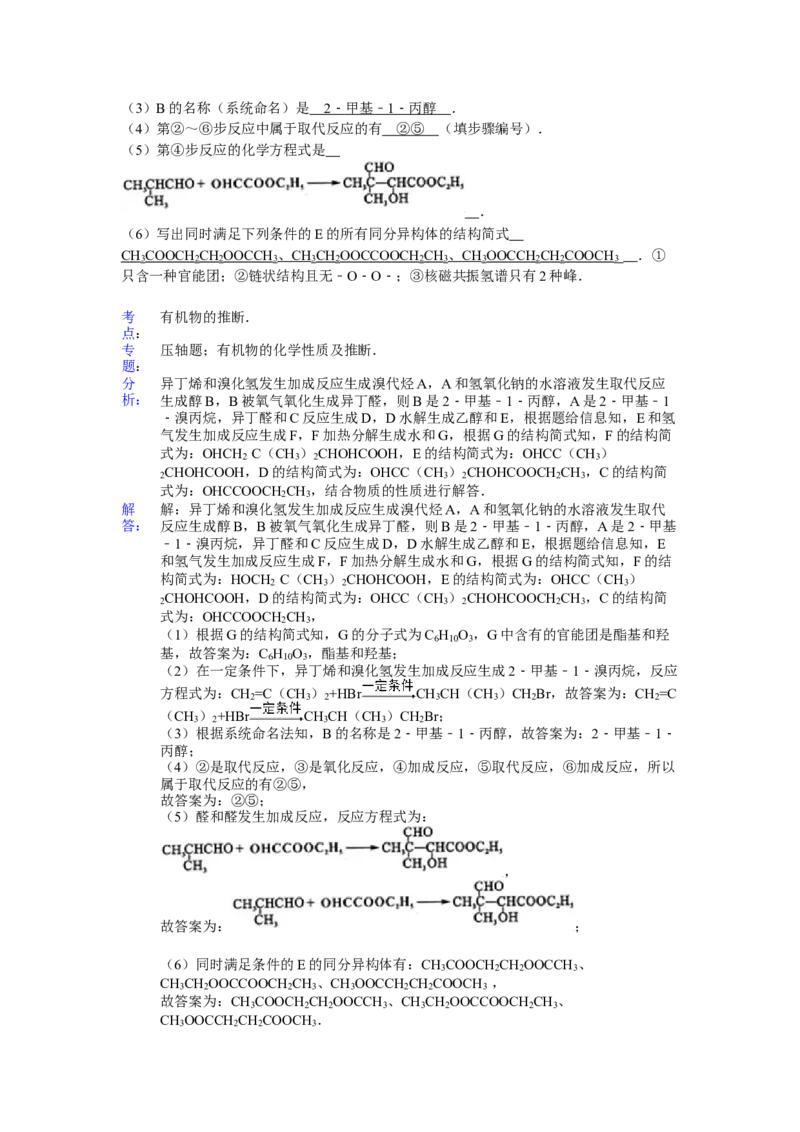
10.(17分)(2013•四川)有机化合物G是合成维生素类药物的中间体,其结构简式如
图1所示,G的合成路线如图2所示:
其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知:请回答下列问题:
(1)G的分子式是 ,G中官能团的名称是 .
(2)第①步反应的化学方程式是
.
(3)B的名称(系统命名)是 .
(4)第②~⑥步反应中属于取代反应的有 (填步骤编号).
(5)第④步反应的化学方程式是
.
(6)写出同时满足下列条件的E的所有同分异构体的结构简式
.
①只含一种官能团;②链状结构且无﹣O﹣O﹣;③核磁共振氢谱只有2种峰.
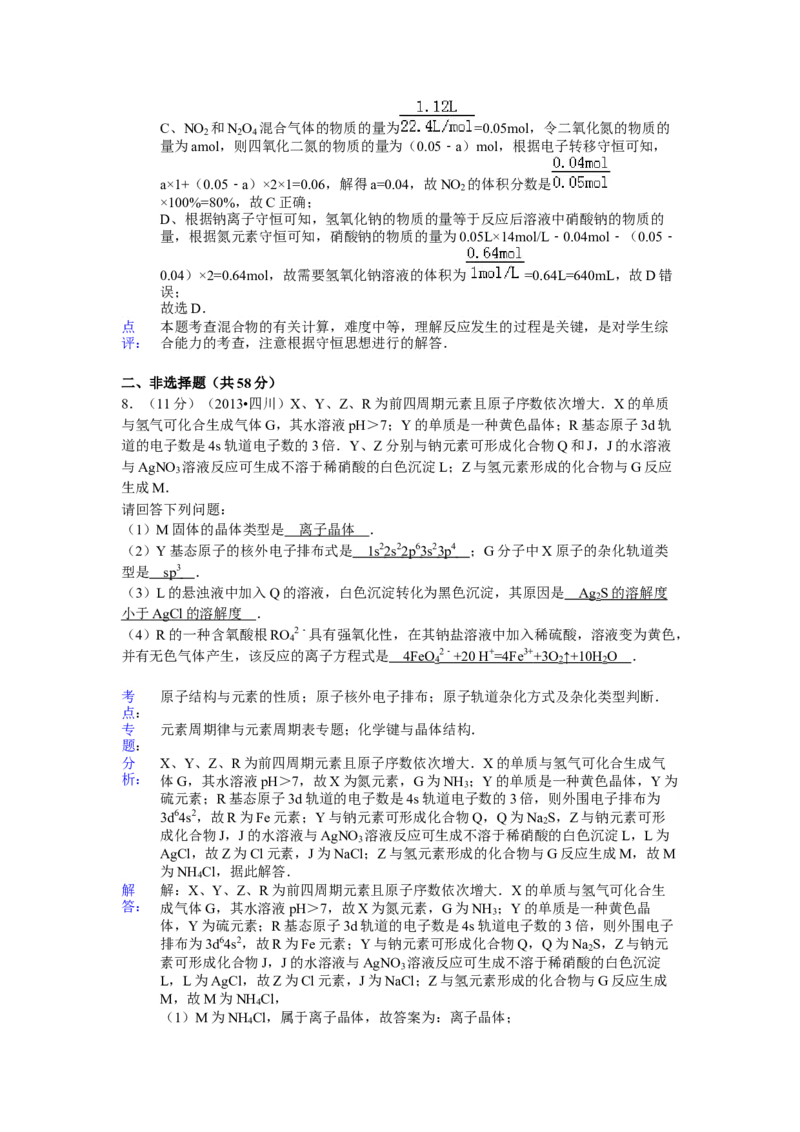
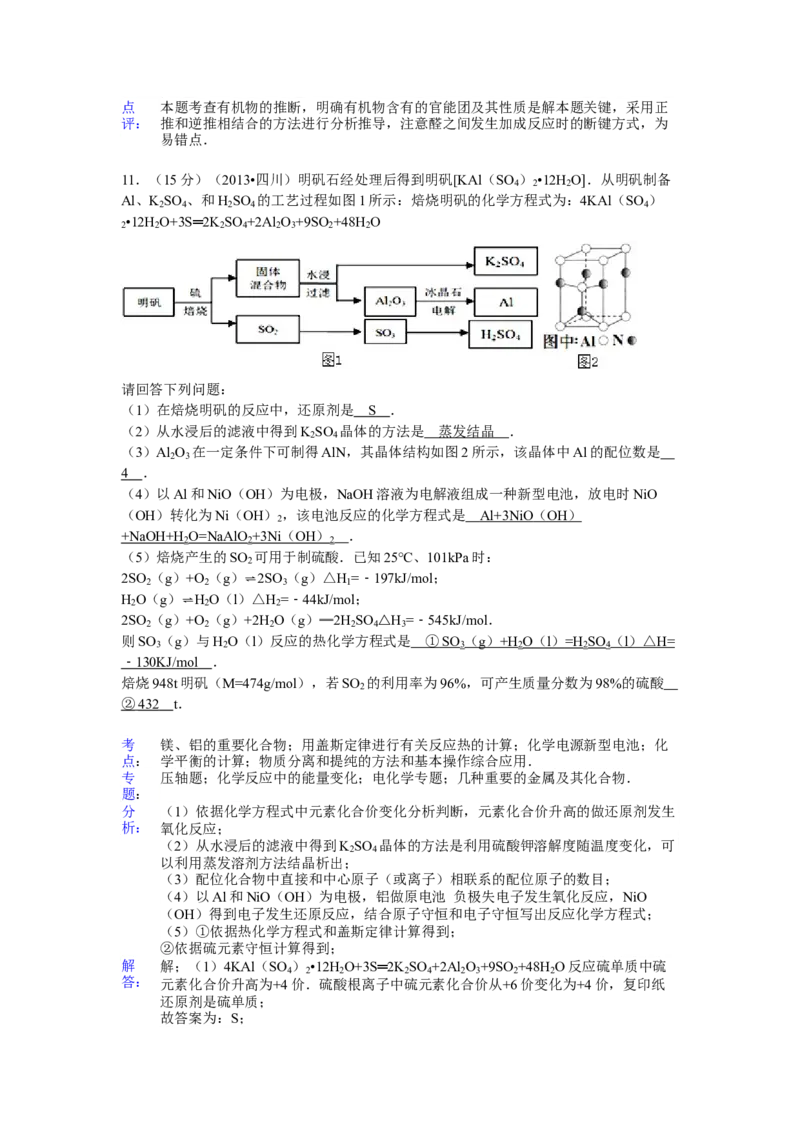
11.(15分)(2013•四川)明矾石经处理后得到明矾[KAl(SO ) •12H O .从明矾制备
4 2 2
Al、K SO 、和H SO 的工艺过程如图1所示:焙烧明矾的化学方程式为:4KAl(SO )
2 4 2 4 4
]
•12H O+3S═2K SO +2Al O +9SO +48H O
2 2 2 4 2 3 2 2
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 .
(2)从水浸后的滤液中得到K SO 晶体的方法是 .
2 4
(3)Al O 在一定条件下可制得AlN,其晶体结构如图2所示,该晶体中Al的配位数是
2 3
.
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO
(OH)转化为Ni(OH) ,该电池反应的化学方程式是
2
(5)焙烧产生的SO 可用于制硫酸.已知25℃、101kPa时:
2
(6)2SO
2
(g)+O
2
(g) ⇌2SO
3
(g) △H
1
=﹣197kJ/mol;
H
2
O(g) ⇌H
2
O(l) △H
2
=﹣44kJ/mol;
2SO
2
(g)+O
2
(g)+2H
2
O(g)═2H
2
SO
4
△H
3
=﹣545kJ/mol.
则SO (g)与H O(l)反应的热化学方程式是
3 2
焙烧948t明矾(M=474g/mol),若SO 的利用率为96%,可产生质量分数为98%的硫酸
2
t.一、选择题共42分
1.(6分)(2013•四川)化学与生活密切相关,下列说法不正确的是( )
A 二氧化硫可广泛用于食品的增白
.
B.葡萄糖可用于补钙药物的合成
C.聚乙烯塑料制品可用于食品的包装
D 次氯酸钠溶液可用于环境的消毒杀菌
.
考 药物的主要成分和疗效;氯、溴、碘及其化合物的综合应用;二氧化硫的化学性
点: 质;常用合成高分子材料的化学成分及其性能.
菁优网版权所有
专 化学应用.
题:
分 A.二氧化硫有一定毒性;
析: B.葡萄糖可用于合成葡萄糖酸钙;
C.聚乙烯无毒;
D.次氯酸钠有强氧化性.
解 解:A.二氧化硫有一定毒性,不能用于食物漂白,故A错误;
答: B.葡萄糖酸钙常被用做补钙剂,故B正确;
C.聚乙烯可做食品的包装,而聚氯乙烯不可,故C正确;
D.“84”消毒液的有效成分就是NaClO,可用于环境消毒,故D正确;
故选A.
点 本题考查化学在生活中的应用,难度不大,注意聚乙烯无毒,聚氯乙烯有毒.
评:
2.(6分)(2013•四川)下列物质分类正确的是( )
A SO 、SiO 、CO均为酸性氧化物
2 2
.
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D 福尔马林、水玻璃、氨水均为混合物
.
考 酸、碱、盐、氧化物的概念及其相互联系;混合物和纯净物;分散系、胶体与溶液
点: 的概念及关系;电解质与非电解质.
菁优网版权所有
专 物质的分类专题.
题:
分 A、酸性氧化物是指和碱反应生成盐和水的氧化物,一氧化碳是不成盐氧化物;
析: B、胶体是分散质直径在1﹣100nm的分散系,硅酸是沉淀,氯化铁溶液不是胶体;
C、电解质是水溶液中或熔融状态能导电的化合物,四氯化碳是非电解质;
D、不同物质组成的物质为混合物;
解 解:A、SO 、SiO 和碱反应生成盐和水,均为酸性氧化物,CO不能和碱反应生成
2 2
答: 盐和水是不成盐氧化物,故A错误;
B、稀豆浆属于胶体、硅酸是难溶的沉淀、氯化铁溶液不是胶体,分散质微粒直径不
同是分散系的本质区别,故B错误;
C、烧碱是氢氧化钠水溶液中完全电离是强电解质、冰醋酸水溶液中部分电离是弱电
解质、四氯化碳水溶液中或熔融状态都不导电属于非电解质,故C错误;
D、福尔马林是甲醛水溶液属于混合物、水玻璃是硅酸钠水溶液,属于混合物、氨水
氨气溶于水形成的溶液属于混合物,所以均为混合物,故D正确;
故选D.
点 本题考查了氧化物分类,分散系的区分,电解质的判断,混合物的物质组成,题目
评: 较简单.3.(6分)(2013•四川)下列离子方程式正确的是( )
A Cl 通入水中:Cl +H O═2H++Cl﹣+ClO﹣
2 2 2
.
B.双氧水中加入稀硫酸和KI溶液:H O +2H++2I﹣═I +2H O
2 2 2 2
C.
用铜作电极电解CuSO 溶液:2Cu2++2H O 2Cu+O ↑+4H+
4 2 2
D Na S O 溶液中加入稀硫酸:2S O 2﹣+4H+═SO 2﹣+3S↓+2H O
2 2 3 2 3 4 2
.
考 离子方程式的书写.
菁优网版权所有
点:
专 离子反应专题.
题:
分 A.HClO为弱酸,在离子反应中保留化学式;
析: B.发生氧化还原反应生成硫酸钾、碘、水;
C.铜作电解,阳极Cu失去电子,实质为电镀;
D.发生氧化还原反应生成S、SO 、H O.
2 2
解 解:A.Cl 通入水中的离子反应为Cl +H O H++Cl﹣+HClO,故A错误;
2 2 2
答: B.双氧水中加入稀硫酸和KI溶液的离子反应为H O +2H++2I﹣═I +2H O,故B正
2 2 2 2
确; ⇌
C.用铜作电极电解CuSO 溶液,实质为电镀,阳极Cu失去电子,阴极铜离子得电
4
子,故C错误;
D.Na S O 溶液中加入稀硫酸的离子反应为S O 2﹣+2H+═SO ↑+S↓+H O,故D错
2 2 3 2 3 2 2
误;
故选B.
点 本题考查离子反应的书写,明确发生的化学反应是解答本题的关键,注意发生的氧
评: 化还原反应为解答的难点,题目难度中等.
4.(6分)(2013•四川)短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原
子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是(
)
A W、Y、Z的电负性大小顺序一定是Z>Y>W
.
B.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
C.Y、Z形成的分子空间构型可能是正四面体
D WY 分子中δ键与π键的数目之比是2:1
2
.
考 原子结构与元素的性质.
菁优网版权所有
点:
专 元素周期律与元素周期表专题.
题:
分 短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之
析: 比为4:3,由于最外层电子数不超过8,故W的最外层电子数为4,处于第ⅣA
族,X的最外层电子数为3,处于第ⅢA族,原子序数X大于W,故W为C元素,
X为Al元素,Z原子比X原子的核外电子数多4,故Z的核外电子数为17,则Z为
Cl元素,Y的原子序数大于铝元素,小于氯元素,故Y为Si或P或S元素,据此解
答.
解 解:短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子
答: 数之比为4:3,由于最外层电子数不超过8,故W的最外层电子数为4,处于第ⅣA族,X的最外层电子数为3,处于第ⅢA族,原子序数X大于W,故W为C元
素,X为Al元素,Z原子比X原子的核外电子数多4,故Z的核外电子数为17,则
Z为Cl元素,Y的原子序数大于铝元素,小于氯元素,故Y为Si或P或S元素,
A、同主族自上而下电负性减弱,Y若为Si元素,则电负性C>Si,故A错误;
B、同周期自左而右原子半径减小,电子层越多原子半径越大,故原子半径Al>Y>
Cl>C,故B错误;
C、若Y、Z形成的分子为SiCl ,为正四面体构型,故C正确;
4
D、WY 分子为CS ,分子结构式为S=C=S,双键中含有1个δ键、1个π键,故δ
2 2
键与π键的数目之比1:1,故D错误;
故选C.
点 本题考查结构性质位置关系,难度中等,推断元素是关键,注意Y元素的不确定
评: 性.
5.(6分)(2013•四川)室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体
积变化),实验数据如下表:
实验编号 起始浓度/(mol•L﹣1) 反应后溶液的pH
c(HA) c
(KOH
)
① 0.1 0.1 9
② x 0.2 7
下列判断不正确的是( )
A 实验①反应后的溶液中:c(K+)>c(A﹣)>c(OH﹣)>c(H+)
.
B.
实验①反应后的溶液中:c(OH﹣)=c(K+)﹣c(A﹣)= mol/L
C.实验②反应后的溶液中:c(A﹣)+c(HA)>0.1 mol/L
D 实验②反应后的溶液中:c(K+)=c(A﹣)>c(OH﹣)=c(H+)
.
考 酸碱混合时的定性判断及有关ph的计算;离子浓度大小的比较.
菁优网版权所有
点:
专 电离平衡与溶液的pH专题.
题:
分 室温下,将等体积等浓度的HA和KOH混合(忽略体积变化),溶液呈碱性,说明
析: 该酸是弱酸,
A.根据盐的类型确定溶液中离子浓度的相对大小;
B.根据电荷守恒计算氢氧根离子浓度;
C.当等物质的量的酸和碱恰好反应时,溶液呈碱性,要使等体积的酸和碱混合后溶
液呈中性,则酸的浓度应大于碱的浓度;
D.根据电荷守恒确定离子浓度关系.
解 解:室温下,将等体积等浓度的HA和KOH混合(忽略体积变化),溶液呈碱性,
答: 说明该酸是弱酸,
A.溶液中存在电荷守恒,即c(K+)+c(H+)=c(A﹣)+c(OH﹣),该盐是强碱
弱酸盐,其溶液呈碱性,c(OH﹣)>c(H+),水的电离较微弱,所以c(A﹣)>c
(OH﹣),故A正确;
B.溶液中存在电荷守恒,即c(K+)+c(H+)=c(A﹣)+c(OH﹣),c(OH﹣)﹣
c(H+)=c(K+)﹣c(A﹣)= mol/L﹣10﹣9 mol/L,故B错误;
C.当等物质的量的酸和碱恰好反应时,溶液呈碱性,要使等体积的酸和碱混合后溶
液呈中性,则酸的浓度应大于碱,根据物料守恒得c(A﹣)+c(HA)>0.1 mol/L,故C正确;
D.溶液中存在电荷守恒,即c(K+)+c(H+)=c(A﹣)+c(OH﹣),溶液呈中
性,即c(OH﹣)=c(H+),则c(K+)=c(A﹣),中性溶液中水的电离较微弱,
所以c(A﹣)>c(OH﹣),故D正确;
故选B.
点 本题考查离子浓度大小的比较,根据电荷守恒和微粒守恒来分析解答即可,易错选
评: 项是C,难度较大.
6.(6分)(2013•四川)在一定温度下,将气体X和气体Y 各0.16mol充入10L恒容密
闭容器中,发生反应X(g)+Y(g) ⇌2Z(g)△H<0,一段时间后达到平衡.反应过程
中测定的数据如下表,下列说法正确的是( )
t/min 2 4 7 9
n(Y)/mol 0.12 0.11 0.10 0.10
A 反应前2min的平均速率v(Z)=2.0×10﹣3 mol/(L•min)
.
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
.
考 化学平衡的计算;化学平衡的影响因素.
菁优网版权所有
点:
专 压轴题;化学平衡专题.
题:
分
析:
A、2min内Y物质的量变化为0.16mol﹣0.12mol=0.04mol,根据v= 计算v
(Y),在利用速率之比等于化学计量数之比计算v(Z);
B、该反应正反应是放热反应,降低温度平衡向正反应移动,反应达到新平衡前v
(逆)<v(正);
C、由表中数据可知7min时,反应到达平衡,根据平衡时Y的物质的量,利用三段
式计算平衡时其它组分的物质的量,由于反应前后气体的化学计量数相等,用物质
的量代替浓度代入平衡常数表达式计算;
D、再通入0.2 mol Z,等效为在原平衡基础上增大压强,反应前后气体的体积不
变,平衡不移动.
解 解:A、2min内Y物质的量变化为0.16mol﹣0.12mol=0.04mol,故v(Y)=
答:
=0.002mol/(L•min),速率之比等于化学计量数之比,故v(Z)=2v
(Y)=2×0.002mol/(L•min)=0.004mol/(L•min),故A错误;
B、该反应正反应是放热反应,降低温度平衡向正反应移动,反应达到新平衡前v
(逆)<v(正),故B错误;
C、由表中数据可知7min时,反应到达平衡,平衡时Y的物质的量为0.10mol,
则:
X(g)+Y(g) ⇌2Z(g)
开始(mol):0.16 0.16 0
变化(mol):0.06 0.06 0.12
平衡(mol):0.1 0.1 0.12
由于反应前后气体的化学计量数相等,用物质的量代替浓度进行计算,故化学平衡常数k= =1.44,故C正确;
D、再通入0.2 mol Z,等效为在原平衡基础上增大压强,反应前后气体的体积不
变,平衡不移动,X的体积分数不变,故D错误;
故选C.
点 本题考查化学反应速率、化学平衡常数、化学平衡的影响因素等,难度中等,注意
评: C选项中对化学平衡常数的理解.
7.(6分)(2013•四川)1.52g 铜镁合金完全溶解于50mL 密度为1.40g/mL、质量分数为
63%的浓硝酸中,得到NO 和N O 的混合气体1120mL(标准状况),向反应后的溶液中
2 2 4
加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的
是( )
A 该合金中铜与镁的物质的量之比是2:1
.
B.该浓硝酸中HNO 的物质的量浓度是14.0 mol/L
3
C.NO 和N O 的混合气体中,NO 的体积分数是80%
2 2 4 2
D 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
.
考 有关混合物反应的计算;硝酸的化学性质.
菁优网版权所有
点:
专 压轴题;守恒法.
题:
分 A、金属离子全部沉淀时,得到2.54g沉淀为氢氧化铜、氢氧化镁,故沉淀中氢氧根
析:
的质量为2.54g﹣1.52g=1.02g,根据n= 计算氢氧根的物质的量,根据电荷守恒可
知,金属提供的电子物质的量等于氢氧根的物质的量,令铜、镁合金中Cu、Mg的
物质的量分别为xmol、ymol,根据提供的电子物质的量与二者质量之和列方程计算
x、y的值,据此解答;
B、根据c= 计算该浓硝酸的物质的量浓度;
C、根据n= 计算NO 和N O 混合气体的物质的量,令二氧化氮的物质的量为
2 2 4
amol,根据电子转移列放出计算,进而计算二氧化氮的体积分数;
D、根据钠离子守恒可知,氢氧化钠的物质的量等于反应后溶液中硝酸钠的物质的
量,根据氮元素守恒计算硝酸钠的物质的量,再根据V= 计算需要氢氧化钠溶液的
体积.
解 解:A、金属离子全部沉淀时,得到2.54g沉淀为氢氧化铜、氢氧化镁,故沉淀中氢
答:
氧根的质量为2.54g﹣1.52g=1.02g,氢氧根的物质的量为 =0.06mol,根据电
荷守恒可知,金属提供的电子物质的量等于氢氧根的物质的量,令铜、镁合金中
Cu、Mg的物质的量分别为xmol、ymol,则: ,解得x=0.02,
y=0.01,故合金中铜与镁的物质的量之比是0.02mol:0.01mol=2:1,故A正确;
B、该浓硝酸密度为1.40g/mL、质量分数为63%,故该浓硝酸的物质的量浓度为
mol/L=14mol/L,故B正确;C、NO 和N O 混合气体的物质的量为 =0.05mol,令二氧化氮的物质的
2 2 4
量为amol,则四氧化二氮的物质的量为(0.05﹣a)mol,根据电子转移守恒可知,
a×1+(0.05﹣a)×2×1=0.06,解得a=0.04,故NO 的体积分数是
2
×100%=80%,故C正确;
D、根据钠离子守恒可知,氢氧化钠的物质的量等于反应后溶液中硝酸钠的物质的
量,根据氮元素守恒可知,硝酸钠的物质的量为0.05L×14mol/L﹣0.04mol﹣(0.05﹣
0.04)×2=0.64mol,故需要氢氧化钠溶液的体积为 =0.64L=640mL,故D错
误;
故选D.
点 本题考查混合物的有关计算,难度中等,理解反应发生的过程是关键,是对学生综
评: 合能力的考查,注意根据守恒思想进行的解答.
二、非选择题(共58分)
8.(11分)(2013•四川)X、Y、Z、R为前四周期元素且原子序数依次增大.X的单质
与氢气可化合生成气体G,其水溶液pH>7;Y的单质是一种黄色晶体;R基态原子3d轨
道的电子数是4s轨道电子数的3倍.Y、Z分别与钠元素可形成化合物Q和J,J的水溶液
与AgNO 溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应
3
生成M.
请回答下列问题:
(1)M固体的晶体类型是 离子晶体 .
(2)Y基态原子的核外电子排布式是 1 s 2 2 s 2 2 p 6 3 s 2 3 p 4 ;G分子中X原子的杂化轨道类
型是 s p 3 .
(3)L的悬浊液中加入Q的溶液,白色沉淀转化为黑色沉淀,其原因是 A g S 的溶解度
2
小于 AgC l 的溶解度 .
(4)R的一种含氧酸根RO 2﹣具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,
4
并有无色气体产生,该反应的离子方程式是 4FeO 2﹣ +20 H + =4Fe 3+ +3O ↑+10H O .
4 2 2
考 原子结构与元素的性质;原子核外电子排布;原子轨道杂化方式及杂化类型判断.
菁优网版权所有
点:
专 元素周期律与元素周期表专题;化学键与晶体结构.
题:
分 X、Y、Z、R为前四周期元素且原子序数依次增大.X的单质与氢气可化合生成气
析: 体G,其水溶液pH>7,故X为氮元素,G为NH ;Y的单质是一种黄色晶体,Y为
3
硫元素;R基态原子3d轨道的电子数是4s轨道电子数的3倍,则外围电子排布为
3d64s2,故R为Fe元素;Y与钠元素可形成化合物Q,Q为Na S,Z与钠元素可形
2
成化合物J,J的水溶液与AgNO 溶液反应可生成不溶于稀硝酸的白色沉淀L,L为
3
AgCl,故Z为Cl元素,J为NaCl;Z与氢元素形成的化合物与G反应生成M,故M
为NH Cl,据此解答.
4
解 解:X、Y、Z、R为前四周期元素且原子序数依次增大.X的单质与氢气可化合生
答: 成气体G,其水溶液pH>7,故X为氮元素,G为NH ;Y的单质是一种黄色晶
3
体,Y为硫元素;R基态原子3d轨道的电子数是4s轨道电子数的3倍,则外围电子
排布为3d64s2,故R为Fe元素;Y与钠元素可形成化合物Q,Q为Na S,Z与钠元
2
素可形成化合物J,J的水溶液与AgNO 溶液反应可生成不溶于稀硝酸的白色沉淀
3
L,L为AgCl,故Z为Cl元素,J为NaCl;Z与氢元素形成的化合物与G反应生成
M,故M为NH Cl,
4
(1)M为NH Cl,属于离子晶体,故答案为:离子晶体;
4(2)Y为硫元素,基态原子的核外电子排布式是1s22s22p63s23p4;G为NH ,分子
3
中N原子成3个N﹣H键,含有1对孤对电子,杂化轨道数目为4,故采取sp3杂
化,
故答案为:1s22s22p63s23p4;sp3;
(3)L为AgCl,Q为Na S,AgCl的悬浊液中加入Na S的溶液,由于Ag S的溶解
2 2 2
度小于AgCl的溶解度,故白色沉淀转化为黑色沉淀,故答案为:Ag S的溶解度小
2
于AgCl的溶解度;
(4)R为Fe元素,含氧酸根FeO 2﹣具有强氧化性,在其钠盐溶液中加入稀硫酸,
4
溶液变为黄色,有Fe3+生成,并有无色气体产生,结合电子转移守恒可知,只有氧
元素被氧化,故该无色气体为O ,反应离子方程式为:4FeO 2﹣+20 H+=4Fe3+
2 4
+3O ↑+10H O,故答案为:4FeO 2﹣+20 H+=4Fe3++3O ↑+10H O.
2 2 4 2 2
点 本题考查结构性质位置关系、无机物的推断、核外电子排布规律、杂化理论、沉淀
评: 转化、氧化还原反应等,难度中等,(4)中注意根据氧化还原反应知识判断生成的
气体是氧气,是易错点与难点.
9.(15分)(2013•四川)为了探究AgNO 的氧化性和热稳定性,某化学兴趣小组设计了
3
如下实验.
Ⅰ.AgNO 的氧化性
3
将光亮的铁丝伸入AgNO 溶液中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,
3
将溶液中的Ag+ 除尽后,进行了如下实验.可选用的试剂:KSCN溶液、K [Fe(CN)
3 6
溶液、氯水.
]
(1)请完成下表:
操作 现象 结论
取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 ①溶液呈血 存在Fe3+
红色
取少量除尽Ag+后的溶液于试管中,加入 ② K [Fe ( CN ) ③产生蓝色 存在Fe2+
3 6
溶液 ,振荡 沉淀
【实验结论】Fe的氧化产物为Fe2+和Fe2+. ]
Ⅱ.AgNO 的热稳定性
3
用如图所示的实验装置A加热AgNO 固体,产生红棕色气体,在装置D中收集到无色气
3
体.当反应结束后,试管中残留固体为黑色.
(2)装置B的作用是 防倒吸 .
(3)经小组讨论并验证该无色气体为O ,其验证方法是 用带火星的木条深入集气瓶中 ,
2
木条复燃证明无色气为氧气 .
(4)【查阅资料】Ag O和粉末状的Ag均为黑色; Ag O可溶于氨水.
2 2
【提出设想】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag O;ⅲ.Ag和Ag O.
2 2
【实验验证】该小组为验证上述猜想,分别取少量黑色固体放入试管中,进行了如下实验.
实验编号 操作 现象
a 加入足量氨水,振荡 黑色固体不溶解
b 加入足量稀硝酸,振荡 黑色固体溶解,并有气体产生
【实验评价】根据上述实验,不能确定固体产物成分的实验是 ① b (填实验编号).【实验结论】根据上述实验结果,该小组得出AgNO 固体热分解的产物有 ② A g 、 NO 、
3 2
O .
2
考 性质实验方案的设计;二价Fe离子和三价Fe离子的检验;常见气体的检验.
菁优网版权所有
点:
专 实验探究和数据处理题.
题:
分 (1)依据铁离子与硫氰酸钾溶液反应生成血红色溶液验证铁离子的存在;亚铁离子
析: 的检验是K [Fe(CN) 溶液和亚铁离子结合生成蓝色沉淀;
3 6
(2)装置中B为安全瓶防倒吸;
(3)依据氧气助燃性检]验;
(4)①实验操作加入的试剂若是硝酸,固体溶解,银单质反应溶解,氧化银也能溶
于硝酸;
②装置A加热AgNO 固体,产生红棕色气体为二氧化氮,在装置D中收集到无色气
3
体为氧气,依据实验a可知产物为银,氧化银溶于氨水;
解 解:(1)取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡,若含有铁离
答: 子溶液会变血红色,验证亚铁离子实验是取少量除尽Ag+后的溶液于试管中,加入
K [Fe(CN) 溶液会和亚铁离子反应生成蓝色沉淀,故答案为:溶液呈血红色;
3 6
K [Fe(CN) 溶液;产生蓝色沉淀;
3 6
(2)装置导气]管略露出胶塞,是安全瓶,可以防止C装置中 的液体到吸入发生装
置A,故答案为] :防倒吸;
(3)氧气具有助燃性,用带火星的木条伸入集气瓶中,木条复燃证明无色气为氧
气,故答案为:用带火星的木条深入集气瓶中,木条复燃证明无色气为氧气;
(4)①b实验加入的硝酸可以溶解Ag O,也可以溶解Ag,不能检验固体成分,故
2
答案为:b.
②实验a加入氨水,银不能溶解于氨水溶液,Ag O能溶于氨水中形成银氨溶液,可
2
以验证固体成分的判断,加入足量氨水,振荡黑色固体不溶解,说明生成的固体为
Ag,装置A加热AgNO 固体,产生红棕色气体为二氧化氮,在装置D中收集到无
3
色气体为氧气,AgNO 固体热分解的产物有Ag、NO 、O ,故答案为:Ag、NO 、
3 2 2 2
O ;
2
点 本题考查了实验设计的方法和物质实验验证方案分析判断,物质性质的应用是解题
评: 关键,题目难度中等.
10.(17分)(2013•四川)有机化合物G是合成维生素类药物的中间体,其结构简式如
图1所示,G的合成路线如图2所示:
其中A~F分别代表一种有机化合物,合成路线中部分产物及反应条件已略去
已知:
请回答下列问题:
(1)G的分子式是 C H O ,G中官能团的名称是 羟基和酯基 .
6 10 3
(2)第①步反应的化学方程式是 CH =C ( CH ) +HBr CH CH ( CH ) CH Br
2 3 2 3 3 2
.(3)B的名称(系统命名)是 2﹣ 甲基﹣ 1﹣ 丙醇 .
(4)第②~⑥步反应中属于取代反应的有 ②⑤ (填步骤编号).
(5)第④步反应的化学方程式是
.
(6)写出同时满足下列条件的E的所有同分异构体的结构简式
CH COOCH CH OOCCH 、 CH CH OOCCOOCH CH 、 CH OOCCH CH COOCH .①
3 2 2 3 3 2 2 3 3 2 2 3
只含一种官能团;②链状结构且无﹣O﹣O﹣;③核磁共振氢谱只有2种峰.
考 有机物的推断.
菁优网版权所有
点:
专 压轴题;有机物的化学性质及推断.
题:
分 异丁烯和溴化氢发生加成反应生成溴代烃A,A和氢氧化钠的水溶液发生取代反应
析: 生成醇B,B被氧气氧化生成异丁醛,则B是2﹣甲基﹣1﹣丙醇,A是2﹣甲基﹣1
﹣溴丙烷,异丁醛和C反应生成D,D水解生成乙醇和E,根据题给信息知,E和氢
气发生加成反应生成F,F加热分解生成水和G,根据G的结构简式知,F的结构简
式为:OHCH C(CH ) CHOHCOOH,E的结构简式为:OHCC(CH )
2 3 2 3
CHOHCOOH,D的结构简式为:OHCC(CH ) CHOHCOOCH CH ,C的结构简
2 3 2 2 3
式为:OHCCOOCH CH ,结合物质的性质进行解答.
2 3
解 解:异丁烯和溴化氢发生加成反应生成溴代烃A,A和氢氧化钠的水溶液发生取代
答: 反应生成醇B,B被氧气氧化生成异丁醛,则B是2﹣甲基﹣1﹣丙醇,A是2﹣甲基
﹣1﹣溴丙烷,异丁醛和C反应生成D,D水解生成乙醇和E,根据题给信息知,E
和氢气发生加成反应生成F,F加热分解生成水和G,根据G的结构简式知,F的结
构简式为:HOCH C(CH ) CHOHCOOH,E的结构简式为:OHCC(CH )
2 3 2 3
CHOHCOOH,D的结构简式为:OHCC(CH ) CHOHCOOCH CH ,C的结构简
2 3 2 2 3
式为:OHCCOOCH CH ,
2 3
(1)根据G的结构简式知,G的分子式为C H O ,G中含有的官能团是酯基和羟
6 10 3
基,故答案为:C H O ,酯基和羟基;
6 10 3
(2)在一定条件下,异丁烯和溴化氢发生加成反应生成2﹣甲基﹣1﹣溴丙烷,反应
方程式为:CH =C(CH ) +HBr CH CH(CH )CH Br,故答案为:CH =C
2 3 2 3 3 2 2
(CH ) +HBr CH CH(CH )CH Br;
3 2 3 3 2
(3)根据系统命名法知,B的名称是2﹣甲基﹣1﹣丙醇,故答案为:2﹣甲基﹣1﹣
丙醇;
(4)②是取代反应,③是氧化反应,④加成反应,⑤取代反应,⑥加成反应,所以
属于取代反应的有②⑤,
故答案为:②⑤;
(5)醛和醛发生加成反应,反应方程式为:
,
故答案为: ;
(6)同时满足条件的E的同分异构体有:CH COOCH CH OOCCH 、
3 2 2 3
CH CH OOCCOOCH CH 、CH OOCCH CH COOCH ,
3 2 2 3 3 2 2 3
故答案为:CH COOCH CH OOCCH 、CH CH OOCCOOCH CH 、
3 2 2 3 3 2 2 3
CH OOCCH CH COOCH .
3 2 2 3点 本题考查有机物的推断,明确有机物含有的官能团及其性质是解本题关键,采用正
评: 推和逆推相结合的方法进行分析推导,注意醛之间发生加成反应时的断键方式,为
易错点.
11.(15分)(2013•四川)明矾石经处理后得到明矾[KAl(SO ) •12H O .从明矾制备
4 2 2
Al、K SO 、和H SO 的工艺过程如图1所示:焙烧明矾的化学方程式为:4KAl(SO )
2 4 2 4 4
]
•12H O+3S═2K SO +2Al O +9SO +48H O
2 2 2 4 2 3 2 2
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是 S .
(2)从水浸后的滤液中得到K SO 晶体的方法是 蒸发结晶 .
2 4
(3)Al O 在一定条件下可制得AlN,其晶体结构如图2所示,该晶体中Al的配位数是
2 3
4 .
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO
(OH)转化为Ni(OH) ,该电池反应的化学方程式是 Al+3NiO ( OH )
2
+NaOH+H O=NaAlO +3Ni ( OH ) .
2 2 2
(5)焙烧产生的SO 可用于制硫酸.已知25℃、101kPa时:
2
2SO
2
(g)+O
2
(g) ⇌2SO
3
(g)△H
1
=﹣197kJ/mol;
H
2
O(g) ⇌H
2
O(l)△H
2
=﹣44kJ/mol;
2SO
2
(g)+O
2
(g)+2H
2
O(g)═2H
2
SO 4△H
3
=﹣545kJ/mol.
则SO (g)与H O(l)反应的热化学方程式是 ① SO ( g ) +H O ( l ) =H SO ( l )△ H=
3 2 3 2 2 4
﹣130KJ/mol .
焙烧948t明矾(M=474g/mol),若SO 的利用率为96%,可产生质量分数为98%的硫酸
2
② 43 2 t.
考 镁、铝的重要化合物;用盖斯定律进行有关反应热的计算;化学电源新型电池;化
点: 学平衡的计算;物质分离和提纯的方法和基本操作综合应用.
菁优网版权所有
专 压轴题;化学反应中的能量变化;电化学专题;几种重要的金属及其化合物.
题:
分 (1)依据化学方程式中元素化合价变化分析判断,元素化合价升高的做还原剂发生
析: 氧化反应;
(2)从水浸后的滤液中得到K SO 晶体的方法是利用硫酸钾溶解度随温度变化,可
2 4
以利用蒸发溶剂方法结晶析出;
(3)配位化合物中直接和中心原子(或离子)相联系的配位原子的数目;
(4)以Al和NiO(OH)为电极,铝做原电池 负极失电子发生氧化反应,NiO
(OH)得到电子发生还原反应,结合原子守恒和电子守恒写出反应化学方程式;
(5)①依据热化学方程式和盖斯定律计算得到;
②依据硫元素守恒计算得到;
解 解;(1)4KAl(SO ) •12H O+3S═2K SO +2Al O +9SO +48H O反应硫单质中硫
4 2 2 2 4 2 3 2 2
答: 元素化合价升高为+4价.硫酸根离子中硫元素化合价从+6价变化为+4价,复印纸
还原剂是硫单质;
故答案为:S;(2)从水浸后的滤液中得到K SO 晶体的方法是利用硫酸钾溶解度随温度变化不
2 4
大,可以利用蒸发溶剂方法结晶析出晶体;
故答案为:蒸发结晶;
(3)依据晶体晶胞结构分析,结合配位数含义可知,每个铝原子和四个单原子相
连,所以铝原子的配位数为4;
故答案为:4;
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时
NiO(OH)转化为Ni(OH) ,铝做负极失电子在氢氧化钠溶液中生成偏铝酸钠,
2
反应的化学方程式为:
Al+3NiO(OH)+NaOH+H O=NaAlO +3Ni(OH) ;
2 2 2
故答案为:Al+3NiO(OH)+NaOH+H O=NaAlO +3Ni(OH) ;
2 2 2
(5)①2SO
2
(g)+O
2
(g) ⇌2SO
3
(g)△H
1
=﹣197kJ/mol;Ⅰ
H
2
O(g) ⇌H
2
O(l)△H
2
=﹣44kJ/mol;Ⅱ
2SO (g)+O (g)+2H O(g)═2H SO (l)△H =﹣545kJ/mol.Ⅲ
2 2 2 2 4 3
依据盖斯定律Ⅲ﹣Ⅰ﹣2×Ⅱ得到:2SO (g)+2H O(l)=2H SO (l)△H=﹣
3 2 2 4
260KJ/mol;
即反应的热化学方程式为:SO (g)+H O(l)=H SO (l)△H=﹣130KJ/mol;
3 2 2 4
故答案为:SO (g)+H O(l)=H SO (l)△H=﹣130KJ/mol;
3 2 2 4
②948 t明矾生成SO
2
物质的量为4500mol 故生成硫酸的质量
m=4500×0.96×98÷0.98=432000Kg=432t.
故答案为:432t;
点 本题考查了氧化还原反应概念分析判断,晶体结构的理解分析,原电池反应的实质
评: 应用,热化学方程式和盖斯定律的计算,元素守恒的计算应用,题目难度中等.