文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题三 物质的组成与结构
(试题分值:100分 测试时间:60分钟)
一、选择题(本题包括15小题,每小题3分,共45分.每小题只有一个正确答案)
1.【新考法】结合新科技----水105度“结冰”
2024年12月26日,中国的两款第六代战斗机试飞成功,我国成为首个试飞六代机的国家,标志着我
国航空事业取得重大突破,科学家利用碳纳米管实现了水温加到105度“结冰”,该项技术在航空航
天工业有着极大的应用价值。下列说法正确的是
A.可燃冰和冰都是由水分子构成 B.碳纳米管中的水分子不再运动
C.氢氧两种元素只能组成水 D.水蒸气冷凝成水,分子间隔减小
【答案】D
【详解】A、可燃冰主要成分是甲烷水合物,由甲烷和水分子构成,并非全部由水分子构成;冰是固态
的水,是由水分子构成,故A错误;
B、分子总是在不断运动着,碳纳米管中的水分子也在不停运动,故B错误;
C、氢氧两种元素组成的物质除了水(HO),还有过氧化氢(HO),故C错误;
2 2 2
D、水蒸气冷凝成水,水分子间隔减小,故D正确。
故选D。
2.【新考法】结合新材料----芳香性环型碳近日,同济大学科研团队首次精准合成两种全新的碳分子材料
——芳香性环型碳 和 (如图所示),下列关于 和 的描述中正确的是
A.是两种新型的化合物
B.其结构与金刚石均不同
C.在氧气中燃烧时都生成二氧化碳
D.碳原子是决定其化学性质的最小微粒
【答案】B
【详解】A、C 和C 都是只含碳元素一种元素的纯净物,都是碳的单质,故A错误;
10 14
B、C 和C 是环状结构,金刚石是立体网状结构,其结构与金刚石均不同,故B正确;
10 14
C、C 和C 是碳的单质,它们的化学性质相似,在氧气中充分燃烧时都生成二氧化碳,故C错误;
10 14
D、由分子构成的物质,分子是保持物质化学性质的最小粒子。对于C 和C 来说,它们的化学性质是
10 14
由C 分子和C 分子分别保持的,而不是由单个的碳原子保持的,故D错误。
10 14
故选B。
3.华南理工大学研究团队利用动态“局域柔性”框架材料,实现了在室温下对重水和普通水的有效分
离。一个重水分子(2HO)中含有的质子个数为
2
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.3 B.10 C.12 D.20
【答案】B
【详解】由于2HO中的氢原子的质子数和中子数分别为1,所以称为重水,则一个重水分子(2HO)
2 2
中含有的质子个数=1×2+8=10。故选B。
4.【新考法】结合理论研究 “大爆炸理论”指出:200 亿年以前,宇宙中所有物质都包含在一个密度无
限大,温度无限高的原始核中,由于某种原因它发生了爆炸,首先产生了中子、质子和电子,随后就
产生了元素。你由此可知最先产生的元素是
A.H B.C C.O D.Si
【答案】A
【详解】元素是具有相同质子数(或核电荷数)的一类原子的总称。原始核中发生爆炸,首先产生了
中子、质子和电子,随后就产生了元素。氢原子由1个质子和一个电子构成,因此最先产生的原子是
氢原子,则最先产生的元素是氢元素。
故选:A。
5.下列物质由原子直接构成的是
A.氯化钠 B.过氧化氢 C.汞 D.C
60
【答案】C
【分析】由原子直接构成的物质有金属单质、部分非金属固态单质、稀有气体。
【详解】A、氯化钠是由钠离子和氯离子构成的,故A不符合题意;
B、过氧化氢是由过氧化氢分子构成的,故B不符合题意;
C、汞是金属,是由汞原子直接构成的,故C符合题意;
D、C 是由C 分子构成的,故D不符合题意。
60 60
故选:C。
6.下列为四种粒子的结构示意图,有关说法正确的是
A.①表示的是阳离子 B.②表示的元素在化合物中通常显+2价
C.②③表示的是同一种元素 D.④属于一种非金属元素
【答案】C
【详解】A、原子的质子数等于核外电子数,原子结构示意图左侧圆圈内的数字表示质子数,①的质子
数和核外电子数都是8,表示的是原子,A选项错误;
B、②的最外层电子数为6,大于4且没有排满,容易得到2个电子形成稳定结构,则②表示的元素在
化合物中通常显-2价,B选项错误;
C、元素是具有相同质子数(或核电荷数)的一类原子的总称,②③的质子数都是16,表示的是同一种
元素,C选项正确;
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
D、④的质子数为13,属于铝元素,铝元素是金属元素,D选项错误。
故选:C。
7.下列关于Al、Al3+两种粒子的判断中,正确的是:
①核电荷数相同 ②核外电子数相等 ③电子层数相同
④质量几乎相等 ⑤化学性质Al3+比Al稳定
A.①④⑤ B.①②④⑤ C.①③⑤ D.①③④⑤
【答案】A
【详解】①铝原子失去最外层的3个电子形成铝离子,故它们的核外电子数不同,但核电荷数相同,
故正确;
②铝原子失去最外层的3个电子形成铝离子,故它们的核外电子数不同,故错误;
③铝原子失去最外层的3个电子形成铝离子,电子层数不同,故错误;
④铝原子失去最外层的3个电子形成铝离子,电子的质量很小,可以忽略不计,所以二者的质量几乎
相等,故正确;
⑤铝原子失去最外层的3个电子形成铝离子,铝离子最外层电子数为8,所以化学性质Al3+比Al稳定,
故正确;
所以正确的是①④⑤;
故选:A。
8.【新考法】传统文化——古籍记载中的化学腊月二十六,炖猪肉。《本草备要》指出,“猪肉,其味
隽永,食之润肠胃,生津液,丰肌体,泽皮肤,固其所也。”猪肉汤含有丰富的蛋白质、脂肪、碳水
化合物、钙、磷、铁等成分。下列有关磷元素的说法错误的是
A.质子数为15 B.反应中容易得到电子
C.原子质量为30.97 D.属于非金属元素
【答案】C
【详解】A、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为15;
原子中原子序数=核电荷数=质子数=核外电子数,则该元素原子的质子数为15,说法正确,不符合题
意;
B、根据元素周期表中的一格可知,左上角的数字为15,表示原子序数为15;原子中原子序数=核电荷
数=质子数=核外电子数,则该元素的原子核外电子数为15,核外有3个电子层,第一层上有2个电
子、第二层上有8个电子,最外层上有5个电子,多于4,在化学反应中易得到3个电子而形成带3个
单位负电荷的阴离子,说法正确,不符合题意;
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为
30.97,而不是原子质量为30.97,说法正确,不符合题意;D、磷元素名称中带“石”字旁,属于固态
非金属元素,说法正确,不符合题意。
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
故选C。
9.元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分,X、Y、Z、M分别代表四种
不同的元素。下列说法正确的是
A.M原子最外层电子数是2 B.X和Z处于同一周期
C.原子序数: D.最外层电子数:
【答案】D
【详解】A、根据元素周期表中的位置,则M为10号元素氖元素,氖原子质子数=核外电子数=原子序
数=10,氖原子核外电子排布依次为2、8,则M原子最外层电子数为8,故选项说法不正确;
B、由图示可知,He是第一周期的元素,则X位于第二周期,Z位于第三周期,因此X和Z位于不同
周期,故选项说法不正确;
C、元素周期表中,同一周期从左往右,原子序数依次增大,另外,周期数较大的元素的原子序数一定
大于周期数较小的元素的原子序数。图中X、M位于第二周期,且M位于X右侧,Y、Z位于第三周
期,且Z位于Y右侧,可知X、M、Y、Z的原子序数大小关系为:Z>Y>M>X,故选项说法不正
确;
D、X、Z处于同一主族,则最外层电子数:X=Z,故选项说法正确;
故选D。
10.【新考法】结合新材料如图是“奥林匹克烯”(olympicene)单分子图像,化学式为 ,堪称世界上
最小的五环标志。下列说法不正确的是
A.1个“奥林匹克烯”分子由31个原子构成
B.“奥林匹克烯”的相对分子质量为240
C.“奥林匹克烯”中碳元素的质量分数为95%
D.“奥林匹克烯”由碳元素和氢元素质量比为19:12
【答案】D
【详解】A、1个“奥林匹克烯”分子包含19个碳原子和12个氢原子,总计19+12=31个原子,A正
确;
B、“奥林匹克烯”的相对分子质量为19×12+12×1=240,B正确;
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
C、“奥林匹克烯”中碳元素的质量分数为 ,C正确;
D、“奥林匹克烯”由碳元素和氢元素质量比为(19×12):(1×12)=19:1,D错误。
故选D。
11.【新考法】新型价类图铁元素的价类图如图,同一条射线上的物质类别相同,同一圆圈上的物质中铁
元素化合价相同。下列说法正确的是
A.a点对应物质的溶液呈浅绿色
B.转化FeO→Fe,一定属于置换反应
C.转化c→a→Fe(OH),均可通过复分解反应实现
3
D.b在潮湿空气中被氧化为Fe(OH) 的化学方程式为
3
【答案】C
【详解】A、由题可知,同一圆圈上的物质中铁元素化合价相同。a点对应的盐中铁元素的化合价与
Fe(OH) 中铁元素的化合价相同,为+3价,含+3价铁离子的盐溶液呈黄色,故A错误;
3
B、CO具有还原性,可以与FeO反应生成Fe和CO,反应物中没有单质,不属于置换反应,即转化
2
FeO→Fe,不一定属于置换反应,故B错误;
C、c对应的物质为氧化铁,氧化铁与盐酸反应可以转化成铁盐a和水,a与氢氧化钠反应可以转化成
Fe(OH) ,涉及到的反应均满足复分解反应的条件,均属于复分解反应,故C正确;
3
D、由图可知,b为氢氧化亚铁,氢氧化亚铁在潮湿空气中被氧化为Fe(OH) 的化学方程式为
3
,故D错误。
故选C。
12.食醋是生活中常用的调味剂,其主要成分乙酸的结构模型图如下所示。下列说法不正确的是
A.乙酸的化学式为CHCOOH
3
B.乙酸中碳元素和氢元素的质量比为6∶1
C.乙酸由2个碳原子、4个氢原子和2个氧原子构成
D.乙酸中氧元素的质量分数最大
【答案】C
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
【详解】A.根据图示分析,乙酸的化学式为CHCOOH;正确;
3
B.乙酸中碳、氢元素的质量比为(12×2):(1×4)=6:1;正确;
C.乙酸是由分子构成的,一个乙酸分子由2个碳原子、4个氢原子和2个氧原子构成;错误;
D.乙酸中碳、氢、氧元素的质量比为(12×2):(1×4):(16×2)=6:1:8,可见其中氧元素的
质量分数最大;正确;
故选:C。
13.对于下列几种化学符号,有关说法正确的是
①H ②Na ③SO ④Na+ ⑤HgO
2
A.能表示一个分子的是①③ B.表示物质化学式的只有③⑤
C.②④的质子数相同,化学性质不同 D.③中的数字“2”表示2个氧原子
【答案】C
【详解】A、分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应
的数字。能表示一个分子的是③SO (1个二氧化硫分子),而①H表示1个氢原子、氢元素,故A
2
错误;
B、表示物质化学式的有②Na(钠)、③SO (二氧化硫)、⑤HgO(氧化汞),故B错误;
2
C、②Na、④Na+,钠离子是钠原子失去最外层的1个电子形成的,钠原子和钠离子的质子数相同,
最外层电子数不同,化学性质不同,故C正确;
D、标在化学式中元素符号右下角的数字表示一个分子中含有该原子的数目,则③中的数字“2”表示1
个二氧化硫分子中含有2个氧原子,故D错误。
故选:C。
14.碘元素是甲状腺激素的重要成分,人体缺碘或碘过量都会引起甲状腺肿大。市售加碘盐是在食盐中加入
一定量的碘酸钾 碘酸钾中碘元素的化合价是
A.-1 B.+1 C.+3 D.+5
【答案】D
【详解】碘酸钾中钾元素显+1价,氧元素显-2价,设碘元素的化合价为x,根据化合物中,正、负化
合价的代数和为零,可得: ,x=+5。
故选D。
15.某赤铁矿石样品中,铁元素的质量分数为56%,则该矿石样品中氧化铁的质量分数为
A.95% B.85% C.70% D.80%
【答案】D
【详解】根据题意可知,铁元素全部来源于氧化铁,所以该矿石中氧化铁的质量分数为:
故选:D。
二、填空题(本题6小题,除标注外,其余每空1分,共45分)
16.(4分)化学用语是国际通用的化学语言。试用化学用语填空。
(1)3个磷原子 ;
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(2)氩气 ;
(3)过氧化氢 ;
(4)标出氧化铝中氧元素的化合价 。
【答案】(1)3P
(2)Ar
(3)H O
2 2
(4)
【详解】(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号
前加上相应的数字,3个磷原子表示为3P。
(2)稀有气体的化学式用元素符号表示,氩气属于稀有气体,其化学式为Ar。
(3)过氧化氢由过氧化氢分子构成,一个过氧化氢分子由两个氢原子、两个氧原子构成,过氧化氢
的化学式为HO。
2 2
(4)化合价标在元素符号的正上方,正负号在前,价数在后。氧化铝中氧元素的化合价表示为
。
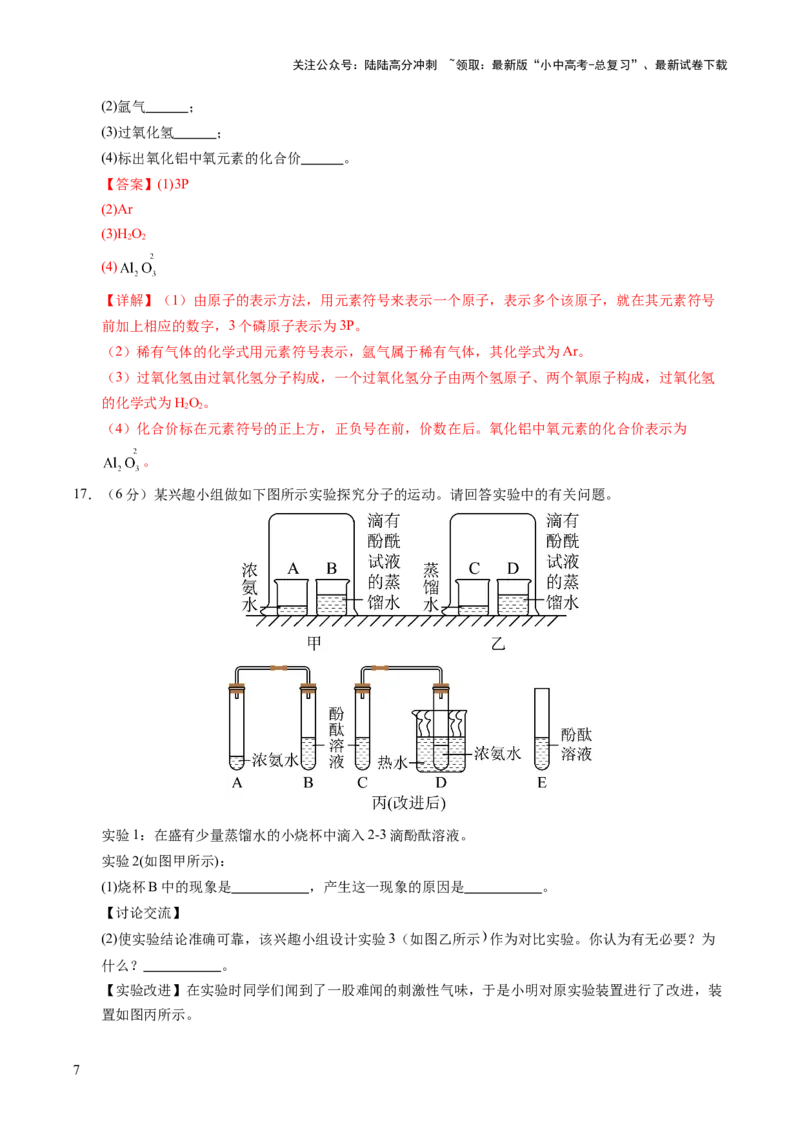
17.(6分)某兴趣小组做如下图所示实验探究分子的运动。请回答实验中的有关问题。
实验1:在盛有少量蒸馏水的小烧杯中滴入2-3滴酚酞溶液。
实验2(如图甲所示):
(1)烧杯B中的现象是 ,产生这一现象的原因是 。
【讨论交流】
(2)使实验结论准确可靠,该兴趣小组设计实验3(如图乙所示 作为对比实验。你认为有无必要?为
什么? 。
【实验改进】在实验时同学们闻到了一股难闻的刺激性气味,于是小明对原实验装置进行了改进,装
置如图丙所示。
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
a向B、C、E三支试管中分别加入 的蒸馏水,各滴入1-2滴无色酚酞溶液,振荡,观察溶液颜
色。
b在A、D试管中分别加入 浓氨水,立即用带橡胶塞的导管按图丙连接好,并将D试管放置在盛
有热水的烧杯中,观察几分钟。
【交流讨论】
(3)①E试管放有酚酞溶液的目的是 。
进行操作丙时观察到的现象是 。
对比改进前的实验,改进后实验的优点是 。
【答案】(1) 溶液变红 氨分子不断地运动扩散到烧杯中
(2)没有,在实验1中已经证明了蒸馏水不能使酚酞变红
(3) 验证空气中的物质不能使酚酞试液变红 试管中的溶液变红速率比试管快 节约药
品、环保、能获得更多的实验结论(答案合理即可)
【详解】(1) 实验如图甲所示:氨分子运动到烧杯中形成氨水,观察到溶液变红,说明氨分子不断
地运动扩散到烧杯中去;
(2)由于图甲中滴有酚酞试液的B烧杯中溶液没有变红,说明蒸馏水不能使酚酞试液变红,故没有
必要再设计实验3;
(3)①试管中液体与空气接触,所以设置试管放有酚酞溶液的目的是验证空气中的物质不能使酚酞
试液变红;
②操作丙将浓氨水的试管放入热水中,温度升高,分子运动加快,所以观察到试管中的溶液变红速率
比试管快;
③改进后实验的优点是节约药品、环保、能获得更多的实验结论。
18.(6分)如图是五种粒子的结构示意图,根据图形回答问题
(1)图1中共有 种元素。
(2)图1中b粒子所表示元素处于周期表的第 周期。
(3)图1中表示阴离子的是 。
(4)与图1中a粒子化学性质相似的原子有 (填一种原子的名称)。
(5)从原子结构解释a粒子和d粒子构成物质的过程 。
(6)从图2中你能获得的信息是 (写一条)。
【答案】(1)4/四
(2)三
(3)e
(4)氟原子
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(5)a粒子得到一个电子形成氯离子,d粒子失去一个电子形成钠离子,氯离子和钠离子带相反电荷,
相互吸引结合
(6)相对原子质量40.08
【详解】(1)不同元素本质区别是质子数不同,图1中质子数分别为17、12、18、11、17,共四种
元素,故填:4或四。
(2)b粒子表示镁离子,属于第三周期,故填:三。
(3)阴离子核电荷数小于核外电子数,故e为阴离子,故填:e。
(4)最外层电子数相同,化学性质相识,与图1中a粒子化学性质相似的原子还有氟原子等,故填:
氟原子。
(5)多电子层原子,最外层8电子属于稳定结构,最外层电子数大于4,容易得电子,最外层电子数
小于4,容易失电子,故a粒子容易得到一个电子形成氯离子,d粒子容易失去一个电子形成钠离子,
氯离子和钠离子带相反电荷,相互吸引结合构成氯化钠,故填:a粒子得到一个电子形成氯离子,d粒
子失去一个电子形成钠离子,氯离子和钠离子带相反电荷,相互吸引结合。
(6)元素周期表小方格最下方表示相对原子质量,故填:相对原子质量40.08。
19.(8分)元素化合价和物质类别是学习物质性质的两个基本内容,如图是硫元素的价类关系图。
(1)图中A点对应物质的物质类别X是 。
(2)H S中硫元素的化合价为 。
2
(3)煤燃烧产生的SO 排放到空气中会形成酸雨,SO 对应图中的 点(填字母),它可与水发生化合
2 2
反应生成亚硫酸(H SO ),请写出该反应的化学方程式 。(2分)该反应过程中硫元素的化合价
2 3
(填“升高”“不变”或“降低”)。
(4)Na SO 在工业上具有广泛的用途,请标出NaSO 中硫元素的化合价: ,它对应图中的
2 4 2 4
点(填字母)。
【答案】(1)单质
(2)-2
(3) C 不变
(4) D
【详解】(1)A点中硫元素化合价为0价,物质是硫,化学式为S,属于单质,故填:单质;
(2)HS中氢元素显+1价,设硫元素的化合价为x,根据化合物中正负化合价代数和为零,得
2
,即硫元素的化合价为-2,故填:-2;
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(3)SO 是硫的氧化物,其中硫元素的化合价为+4价,则对应图中的C点;二氧化硫与水反应生成
2
亚硫酸,反应的化学方程式为 ,该反应过程中硫元素的化合价不变,均为+4价,
故填:C; ;不变;
(4)NaSO 中钠元素显+1价,氧元素显-2价,设硫元素的化合价为 ,根据化合物中正负化合价代
2 4
数和为零,得 ,元素化合价的表示方法:确定出化合物中所要标出的元
素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,则NaSO
2 4
中硫元素的化合价表示为 ,它对应图中的D点,故填: ;D。
20.(11分)下面是元素周期表中1~18号元素原子核外电子排布图,我们对它进行研究:
(1)第16号元素的化学名称为 ,它在化学反应中容易 (填“得”或“失”)电子,形成的粒子
为 (填符号)。
(2)通过上表可推知,19号元素应该属于第 周期,最外层电子数为 ,该元素应属于 (填
“金属”或“非金属”)元素。
(3)在同一族中,各元素原子的结构呈现的规律有 (任写一点)。
(4)S、Cl、F三种非金属元素的原子得电子能力逐渐增强,我能根据这三种非金属元素的原子结构推
测:非金属元素的原子得电子能力的强弱主要与 、 有关。
(5)居里夫妇在1934年发现了金属镭(Ra),它的原子核内有88个质子、138个中子,最外层电子数为
2,则镭元素的原子序数是 ,它与1~18号元素中的 (填元素符号)元素具有相似的化学性
质。
【答案】(1) 硫 得
(2) 四/4 1 金属
(3)在同一族中,各元素的原子最外层电子数相等(答案合理即可)
(4) 最外层电子数 电子层数
(5) 88 Mg、Be
【详解】(1)由图可知,16号元素的元素符号是S,故名称是硫;硫原子的最外层电子数为6,大于
4,在化学反应中,容易得到2个电子,从而带上2个单位的负电荷,形成硫离子,离子符号为:S2-;
(2)由图可知,第三周期的元素为第11号-第18号元素,故19号元素应该属于第四周期;19号元素
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
的原子核外应有4个电子层,在原子中,质子数=原子序数=核外电子数,故19号元素的原子核外电
子排布为2、8、8、1,最外层电子数为1;19号元素是钾元素,由“金”字旁可知,钾元素属于金属
元素;
(3)由图可知,在同一族中,各元素原子的结构呈现的规律有:在同一族中,各元素的原子最外层
电子数相等,从上到下,电子层数依次递增(合理即可);
(4)氟原子有2个电子层,最外层有7个电子,氯原子和硫原子都有3个电子层,而氯原子最外层电
子为7,硫原子最外层电子数为6,三种非金属元素的原子得电子能力逐渐减弱,与最外层电子数或
电子层数有关;
(5)原子序数等于质子数,镭(Ra)的原子核内有88个质子,即原子序数为88;镭(Ra)原子的最
外层有2个电子,铍和镁原子的最外层有2个电子,在化学反应中都易失去2个电子,化学性质相
似;元素符号表示为Mg或Be。
21.(10分)建立宏观与微观的联系是化学特有的思维方式
(1)科学技术的进步,证明了物质是由分子、 和离子等微粒构成的。
(2)氧气可压缩储存于钢瓶中,这是因为 。
某化学兴趣小组设计了探究分子性质的两个实验
实验一:借助氧气传感器探究分子运动的特点
【操作与分析】
(3)按图1连接好实验装置,打开氧气传感器,测得前3分钟曲线为图2中AB段,请从分子的性质角
度回答氧气体积分数下降的原因是 。
(4)用双手给塑料瓶加热2分钟,测得曲线为BC段,对比曲线AB和BC可知:温度升高,分子
。
(5)松开双手并将塑料瓶的瓶口朝下,测得曲线为CD段,对比AB段,请分析CD段氧气体积分数下
降更快的原因是 。
实验二:通过化学反应探究分子数目与压强的关系
【操作与记录】如图所示连接好实验装置,并确保其气密性良好。
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
操作1:将5mL水一次性注入到充满二氧化碳气体的吸滤瓶内,轻轻振荡,发现95℃热水无明显变
化。
操作2:若将操作1中注入的水改成相同体积的氢氧化钠溶液,进行相同实验,观察到95℃热水立即
沸腾。
【分析与结论】回答下列问题
(6)设计操作1的目的是 。
(7)二氧化碳与氢氧化钠反应的化学方程式是 。(2分)
(8)95℃热水立即沸腾的合理解释是 。(2分)
【答案】(1)原子
(2)分子间有间隔
(3)分子在不断地运动,部分氧分子运动到瓶外
(4)分子之间间隔变大,导致部分气体膨胀逸出
(5) 密度大于空气
(6)排除水的干扰
(7)
(8) 与 反应,瓶内压强变小
【详解】(1)科学技术的进步,证明了物质是由分子、原子和离子等微粒构成的,如水由水分子构
成,铁由铁原子构成,氯化钠由钠离子和氯离子构成,故填:原子;
(2)氧气可压缩储存于钢瓶中,这是因为分子之间有间隔,气体分子间间隔较大,容易压缩。故
填:分子间有间隔;
(3)按图1连接好实验装置,打开氧气传感器,测得前3分钟曲线为图2中 AB 段,敞口放置,氧
气体积分数不断减小,原因是分子在不断地运动,部分氧分子运动到瓶外,故填:分子在不断地运
动,部分氧分子运动到瓶外;
(4)用双手给塑料瓶加热2分钟,测得曲线为 BC 段,对比曲线 AB 和 BC 可知,温度升高,分
子之间间隔变大,导致部分气体膨胀逸出,故填:分子之间间隔变大,导致部分气体膨胀逸出;
(5)松开双手并将塑料瓶的瓶口朝下,测得曲线为 CD 段,对比 AB 段, CD 段氧气体积分数下
降更快,原因是氧气的密度比空气大,氧分子更快更多地从瓶口向下逸出,故填:O 密度大于空
2
气;
(6)将5mL水一次性注入到充满二氧化碳气体的吸滤瓶内,轻轻振荡,发现95° C 热水无明显变
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
化,设计操作1的目的是作对照组,排除水的干扰,故填:排除水的干扰;
(7)二氧化碳与氢氧化钠反应生成碳酸钠和水,反应的化学方程式为
,故填: ;
(8)CO 与NaOH反应,瓶内压强变小,水的沸点降低,所以95℃热水立即沸腾,故填:CO 与
2 2
NaOH反应,瓶内压强变小。
三、计算题(本题2小题,除标注外每空1分,共10分)
22.(4分)(2024·天津·中考真题)蛋白质由甘氨酸(C HON)等多种氨基酸构成。计算:
2 5 2
(1)甘氨酸由 种元素组成(写数值)。
(2)一个甘氨酸分子中含有 个原子。
(3) 75g甘氨酸中含有氮元素的质量为 g。(2分)
【答案】(1)4
(2)10
(3)14
【详解】(1)甘氨酸由C、H、O、N 4种元素组成;
(2)化学式中右下角的数字表示1个分子中原子的个数,则一个甘氨酸分子中含有2+5+1+2=10个原
子;
(3)75g甘氨酸中含有氮元素的质量为 g。
23.(6分)钠元素摄入过量或钾元素摄入不足都是导致高血压的风险因素。日常生活中选择食用低钠盐
能实现减钠补钾。某生产厂家为改善“低钠盐”口味还加入少量的食用硫酸镁。如图为该品牌低钠盐
的标签,请回答以下问题。
XX 品牌 低钠盐
产品标准号……
配料及含量:氯化钠(NaCl)70% 氯化钾(KCl)25%
硫酸镁( )5%
生产日期……
保质期……
(1)该品牌低钠盐中含有的非金属元素有 (填元素符号)。
(2)硫酸镁的相对原子质量为 ,硫酸镁中硫元素的化合价为 。
(3)人体每天摄入钠元素的质量不宜超过2.3g。如果人体所需的钠元素全部来自该品牌低钠盐,那么一
个人每天摄入该品牌低钠盐的质量不宜超过多少克?(结果保留一位小数)(3分)
【答案】(1)Cl、S、O
(2) 120 +6
(3)解:设一个人每天摄入该品牌低钠盐的最低质量为x,由题意可知:
解得
13关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
答:一个人每天摄入该品牌低钠盐的质量不宜超过8.4g。
【详解】(1)由配料表可知,该低钠盐中含有钠元素、氯元素、钾元素、镁元素、硫元素和氧元
素,故该品牌低钠盐中含有的非金属元素有氯元素、硫元素和氧元素,元素符号为Cl、S、O;
(2)镁原子的相对原子质量为24,硫原子的相对原子质量为32,氧原子的相对原子质量为16,故硫
酸镁的相对原子质量=24+32+16×4=120;在硫酸镁中镁元素为+2价,氧元素为-2价,设硫元素化合价
为x,根据化合物中各元素化合价代数和为零,可知 ,解得x=+6,故硫酸镁中硫
元素的化合价为+6;
(3)见答案。
14