文档内容
单元检测三 物质的量
一、选择题(本题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.气体体积的大小,跟下列因素几乎无关的是( )
A.分子个数 B.分子直径
C.压强 D.温度
2.假设把C的相对原子质量定为24,且以0.024 kg 12C所含的原子数为阿伏加德罗常数的
值,下列数值肯定不变的是( )
A.气体摩尔体积(标准状况)
B.标准状况下,16 g O 所占的体积
2
C.O 的式量
2
D.一定条件下,跟2 g H 相化合的O 的物质的量
2 2
3.在一定温度和压强下,1体积X 气体与3体积Y 气体化合生成2体积气体化合物,则
2 2
该化合物的化学式为( )
A.XY B.XY
3
C.XY D.XY
3 2 3
5.选择性催化还原技术(SCR)是针对柴油车尾气排放中,NO 的一项处理工艺,即在催化
x
剂的作用下,喷入32.5%的尿素水溶液(密度1.1 g·cm-3),尿素在高温下发生水解和热解反
应后生成NH ,NH 把尾气中的NO 还原成N 和HO,从而达到既节能、又减排的目的。
3 3 x 2 2
下列说法不正确的是( )
A.柴油车尾气排放中,NO是汽缸内的N 与O 在放电作用下产生的
2 2
B.32.5%的尿素水溶液浓度6 mol·L-1
C.NO、NO 、NH 按物质的量之比1∶1∶2反应时可完全转化为无毒物质
2 3
D.SCR技术既能提高发动机功率又能减少污染物排放
6.下列叙述正确的是( )
①一定温度和压强下,气体体积主要由其分子的大小决定
②一定温度和压强下,气体体积主要由其分子的物质的量决定
③气体摩尔体积是指单位物质的量气体所占的体积,其单位是L
④不同的气体,若体积不相等,则它们所含的分子数一定不相等
⑤在同温同体积时,气体的物质的量越大,则压强越大
A.②⑤ B.①③
C.②③⑤ D.②④⑤
7.配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是( )
A.容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液B.配制一定物质的量浓度的稀盐酸时,用量筒量取9.82 mL浓盐酸
C.配制1 L 0.1 mol·L-1的NaCl溶液时,用托盘天平称量5.85 g NaCl固体
D.定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁
8.氮氧化物的排放易造成环境污染,可用氢氧化钠溶液吸收氮氧化物,其反应为 2NO +
2
2NaOH===NaNO +NaNO +HO,设N 为阿伏加德罗常数的值。下列说法正确的是( )
3 2 2 A
A.9 g HO中含有的中子数为5N
2 A
B.每消耗11.2 L NO ,转移的电子数为0.5N
2 A
C.1 L 0.1 mol·L-1 NaOH溶液中含有的氧原子总数为0.1N
A
D.将1 mol NO 溶于足量的NaOH溶液,得溶液中NO和NO数目之和小于N
2 A
9.10月23日为“摩尔日”,N 代表阿伏加德罗常数的值,下列说法正确的是( )
A
A.标准状况下,22.4 L SO 的分子数为N
3 A
B.58.5 g氯化钠中的Na+数为N
A
C.1 L 0.1 mol·L-1的醋酸溶液中H+数为0.1N
A
D.5.6 g Fe和足量S反应转移的电子数为0.3N
A
10.全氮阴离子盐是一种新型超高能含能材料,全氮阴离子的化学式为 N,某种全氮阴离
子盐结构如图。下列有关说法正确的是( )
A.该全氮阴离子盐属于有机物
B.N的摩尔质量为71 g·mol-1
C.每个N含有26个电子
D.该全氮阴离子盐既含共价键又含离子键
11.中国科学家孙予罕等发现,以泡沫镍[3NiO/Ni(3表示 NiO在泡沫镍中的质量百分数)]
作为基材上的催化剂可实现将烷烃直接电催化转化为醇类(转化示意图如图所示)。下列说
法正确的是( )
A.22.4 L A中质子数为10 mol
B.1 mol C中共价键数目为4N
A
C.生成1 mol Ni可还原出1 mol B
D.11.8 g泡沫镍含Ni单质0.194 mol
12.N 为阿伏加德罗常数的值,下列说法正确的是( )
AA.12 g C所含的原子数为阿伏加德罗常数
B.O 的相对分子质量为32,所以O 的摩尔质量也为32
2 2
C.标准状况下,1 mol NO与11.2 L O 充分反应后分子总数为N
2 A
D.P 为正四面体形分子,则1 mol P 分子中含有6N 个共价键
4 4 A
13.N 表示阿伏加德罗常数的值,下列叙述正确的是( )
A
A.125 g CuSO ·5H O晶体中含有Cu2+数目一定小于0.5N
4 2 A
B.常温下,pH=3的醋酸溶液中,CHCOOH分子的数目一定大于10-3N
3 A
C.由S、S、S 组成的硫蒸气为6.4 g,其中所含硫原子数目一定为0.2N
2 4 8 A
D.3.6 g C与3.36 L O 一定条件下恰好完全反应,生成CO的分子数一定为0.3N
2 A
14.在t ℃时,将a g NH 完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·mL-
3
1,质量分数为ω,其中含有NH的物质的量是b mol,下列叙述正确的是( )
A.溶质的质量分数ω=×100%
B.溶质的物质的量浓度c= mol·L-1
C.溶液中c(OH-)= mol·L-1+c(H+)
D.向上述溶液中加入V mL水,所得溶液的溶质质量分数大于0.5ω
15.一个密闭容器,中间有可自由滑动的隔板(厚度不计)将容器分成两部分, 当左边充入
1 mol N ,右边充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法正确的
2
是( )
A.右边与左边分子数之比为4∶1
B.右侧CO的质量为5.6 g
C.右侧气体密度是相同条件下氢气密度的14倍
D.若改变右边CO的充入量而使隔板处于容器正中间保持温度不变,则应充入0.2 mol CO
二、非选择题(本题包括5小题,共55分)
16.(11分)在花瓶中加入“鲜花保鲜剂”可延长鲜花的寿命。下表是1 L“鲜花保鲜剂”的
成分,阅读后并回答下列问题:
成分 质量/g 摩尔质量/(g·mol-1)
蔗糖 50.00 342
硫酸钾 0.50 174
阿司匹林 0.35 180
高锰酸钾 0.50 158
硝酸银 0.04 170
(1)“鲜花保鲜剂”中物质的量浓度最大的成分是______________(填写名称)。(2)“鲜花保鲜剂”中K+的物质的量浓度为(阿司匹林中不含K+)__________________(只要
求写表达式,不需计算)mol·L-1。
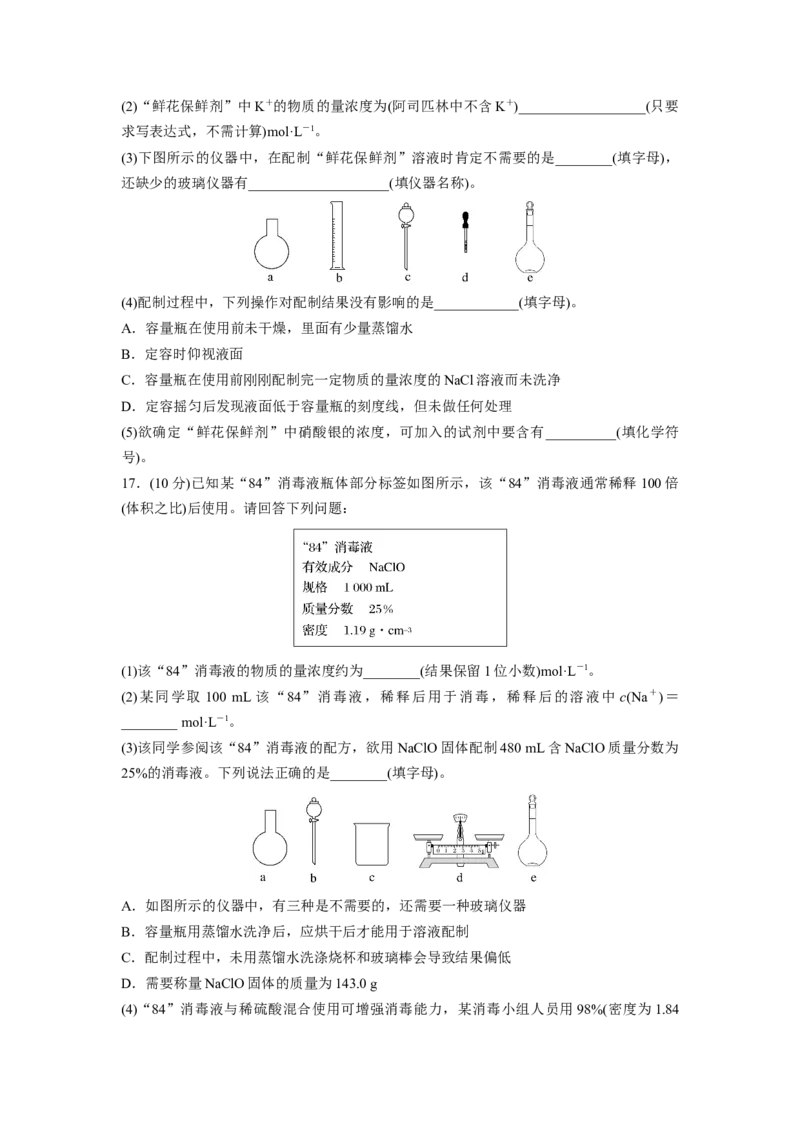
(3)下图所示的仪器中,在配制“鲜花保鲜剂”溶液时肯定不需要的是________(填字母),
还缺少的玻璃仪器有____________________(填仪器名称)。
(4)配制过程中,下列操作对配制结果没有影响的是____________(填字母)。
A.容量瓶在使用前未干燥,里面有少量蒸馏水
B.定容时仰视液面
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)欲确定“鲜花保鲜剂”中硝酸银的浓度,可加入的试剂中要含有__________(填化学符
号)。
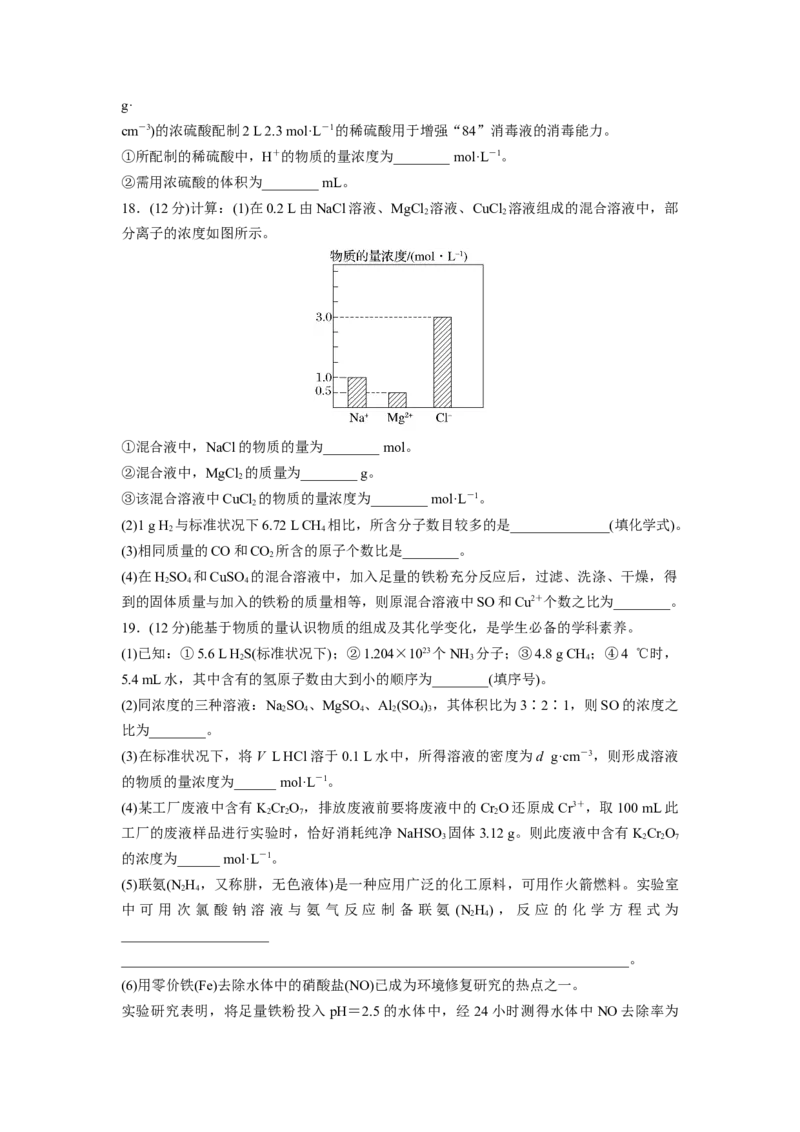
17.(10分)已知某“84”消毒液瓶体部分标签如图所示,该“84”消毒液通常稀释100倍
(体积之比)后使用。请回答下列问题:
(1)该“84”消毒液的物质的量浓度约为________(结果保留1位小数)mol·L-1。
(2)某同学取 100 mL 该“84”消毒液,稀释后用于消毒,稀释后的溶液中 c(Na+)=
________ mol·L-1。
(3)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480 mL含NaClO质量分数为
25%的消毒液。下列说法正确的是________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒会导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(4)“84”消毒液与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84g·
cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84”消毒液的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________ mol·L-1。
②需用浓硫酸的体积为________ mL。
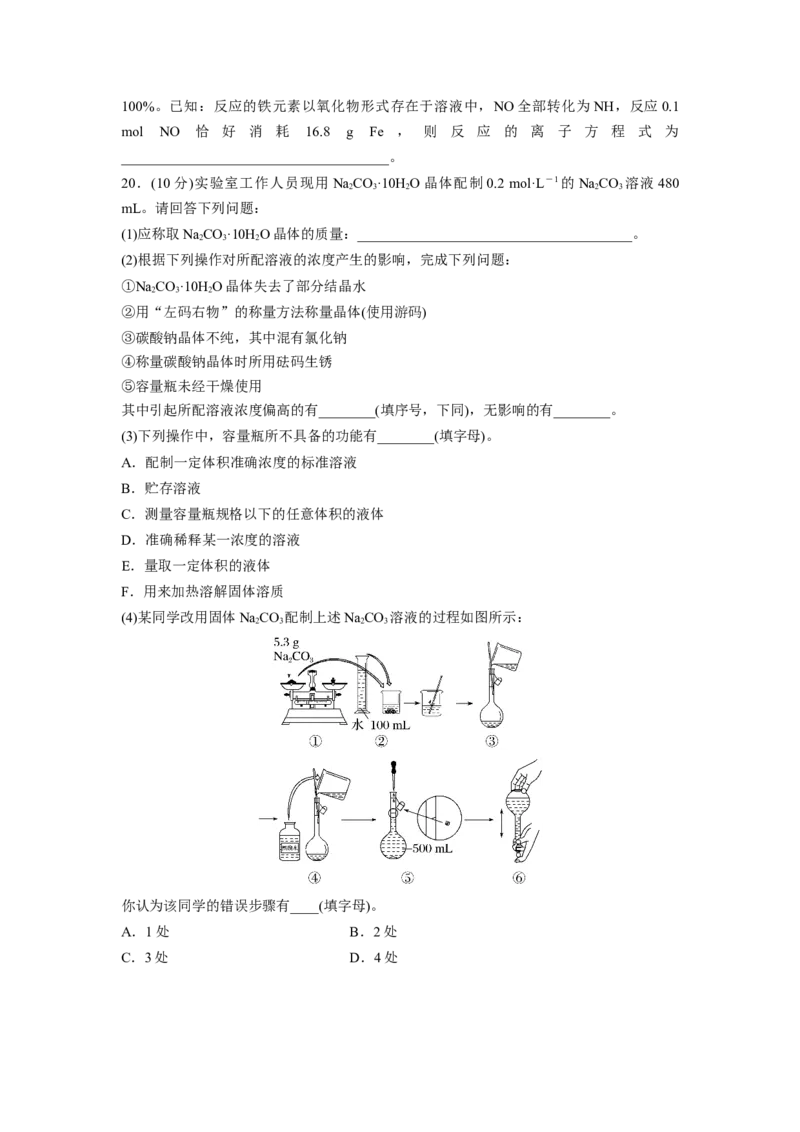
18.(12分)计算:(1)在0.2 L由NaCl溶液、MgCl 溶液、CuCl 溶液组成的混合溶液中,部
2 2
分离子的浓度如图所示。
①混合液中,NaCl的物质的量为________ mol。
②混合液中,MgCl 的质量为________ g。
2
③该混合溶液中CuCl 的物质的量浓度为________ mol·L-1。
2
(2)1 g H 与标准状况下6.72 L CH 相比,所含分子数目较多的是______________(填化学式)。
2 4
(3)相同质量的CO和CO 所含的原子个数比是________。
2
(4)在HSO 和CuSO 的混合溶液中,加入足量的铁粉充分反应后,过滤、洗涤、干燥,得
2 4 4
到的固体质量与加入的铁粉的质量相等,则原混合溶液中SO和Cu2+个数之比为________。
19.(12分)能基于物质的量认识物质的组成及其化学变化,是学生必备的学科素养。
(1)已知:①5.6 L H S(标准状况下);②1.204×1023个NH 分子;③4.8 g CH ;④4 ℃时,
2 3 4
5.4 mL水,其中含有的氢原子数由大到小的顺序为________(填序号)。
(2)同浓度的三种溶液:NaSO 、MgSO 、Al (SO ) ,其体积比为3∶2∶1,则SO的浓度之
2 4 4 2 4 3
比为________。
(3)在标准状况下,将V L HCl溶于0.1 L水中,所得溶液的密度为d g·cm-3,则形成溶液
的物质的量浓度为______ mol·L-1。
(4)某工厂废液中含有KCr O ,排放废液前要将废液中的Cr O还原成Cr3+,取100 mL此
2 2 7 2
工厂的废液样品进行实验时,恰好消耗纯净 NaHSO 固体3.12 g。则此废液中含有KCr O
3 2 2 7
的浓度为______ mol·L-1。
(5)联氨(N H ,又称肼,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。实验室
2 4
中 可 用 次 氯 酸 钠 溶 液 与 氨 气 反 应 制 备 联 氨 (N H) , 反 应 的 化 学 方 程 式 为
2 4
_____________________
________________________________________________________________________。
(6)用零价铁(Fe)去除水体中的硝酸盐(NO)已成为环境修复研究的热点之一。
实验研究表明,将足量铁粉投入pH=2.5的水体中,经24小时测得水体中NO去除率为100%。已知:反应的铁元素以氧化物形式存在于溶液中,NO全部转化为NH,反应0.1
mol NO 恰 好 消 耗 16.8 g Fe , 则 反 应 的 离 子 方 程 式 为
______________________________________。
20.(10分)实验室工作人员现用NaCO·10H O晶体配制0.2 mol·L-1的NaCO 溶液480
2 3 2 2 3
mL。请回答下列问题:
(1)应称取NaCO·10H O晶体的质量:_______________________________________。
2 3 2
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列问题:
①NaCO·10H O晶体失去了部分结晶水
2 3 2
②用“左码右物”的称量方法称量晶体(使用游码)
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有________(填序号,下同),无影响的有________。
(3)下列操作中,容量瓶所不具备的功能有________(填字母)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.量取一定体积的液体
F.用来加热溶解固体溶质
(4)某同学改用固体NaCO 配制上述NaCO 溶液的过程如图所示:
2 3 2 3
你认为该同学的错误步骤有____(填字母)。
A.1处 B.2处
C.3处 D.4处单元检测三 物质的量
1.答案 B
解析 影响物质体积的因素有微粒数目、分子本身大小以及分子间的距离等因素,温度、
压强决定气体分子间距,对于气体来说,气体分子间的距离远大于分子本身的大小,分子
本身可以忽略不计,所以气体体积的大小,跟分子直径几乎无关。
2.答案 B
解析 以0.024 kg 12C所含的原子数为阿伏加德罗常数的值,则阿伏加德罗常数的值变为
原来的2倍,每摩气体所含分子数为原来的2倍,气体摩尔体积(标准状况)肯定变化,故A
不选;气体的质量一定,温度压强也被规定,则体积必然一定,故 B选;由于12C的相对
原子质量由12变为24,显然相对单位质量减为原来的,那么其他原子或分子的相对质量
都将变为原来的2倍,故C不选;由C可知,分子的相对质量改变,质量一定时,物质的
量显然要改变,故D不选。
3.答案 A
解析 假设生成的气体化合物为Z,根据体积之比等于物质的量之比得到反应的化学方程
式为X + 3Y===2Z,根据原子守恒,Z的化学式为XY ,故A符合题意。
2 2 3
4.答案 B
5.答案 A
解析 柴油车尾气排放中NO是汽缸内的N 与O 在高温环境下反应产生的,而不是放电条
2 2
件下反应产生的,A错误;32.5%的尿素水溶液浓度c= mol·L-1≈6 mol·
L-1,B正确;若NO、NO 、NH 按物质的量之比1∶1∶2,则会发生反应:NO+NO +
2 3 2
2NH ===2N +3HO,恰好反应转化为无毒物质N 、HO,C正确;选择性催化还原技术
3 2 2 2 2
(SCR)能够将NO 还原为无毒气体,达到节能、减排的目的,提高了能量利用率,从而提
x
高了发动机功率,D正确。
6.答案 A
解析 一定温度和压强下,气体分子间的距离相等,气体体积主要由其分子个数决定,即
由其分子的物质的量决定,①错误,②正确;气体摩尔体积是指单位物质的量气体所占的
体积,其单位是L·mol-1,③错误;不同的气体,若体积不相等,则它们所含的分子数也
可能相等,④错误;依据阿伏加德罗定律及其推论可知,在同温同体积时,气体的物质的
量越大,则压强越大,⑤正确。
7.答案 A
解析 容量瓶用蒸馏水洗净后,不需要干燥,因定容时还需要加水,故A正确;量筒的精
确度为0.1 mL,无法量取9.82 mL浓盐酸,故B错误;托盘天平的精确度为0.1 g,无法称
量5.85 g NaCl固体,故C错误;定容时,胶头滴管要悬空正放,不能紧贴容量瓶内壁,故D错误。
8.答案 D
解析 1个HO中含有8个中子,9 g H O的物质的量为=0.5 mol,故9 g H O中含有的中
2 2 2
子数为4N ,故A项错误;不是标准状况,无法计算气体的物质的量,故B错误;1 L 0.1
A
mol·L-1 NaOH溶液中NaOH的物质的量为0.1 mol,其中氧原子总数为0.1N ,但是溶剂水
A
中还含有氧原子,故C错误;亚硝酸是弱酸,NO会水解,会消耗一部分NO,故溶液中
NO和NO数目之和小于N ,故D项正确。
A
9.答案 B
解析 标准状况下三氧化硫是固体,无法计算其体积,A错误;氯化钠是由钠离子和氯离
子组成的,58.5 g氯化钠的物质的量为1 mol,故Na+的物质的量为1 mol,数目为N ,B
A
正确;醋酸是弱电解质,故1 L 0.1 mol·L-1的醋酸溶液中H+数小于0.1N ,C错误;S的氧
A
化性较弱,铁和S反应生成二价铁,故5.6 g Fe和足量S反应转移的电子数为0.2N ,D错
A
误。
10.答案 D
解析 该全氮阴离子盐不含碳元素,属于无机物,故A错误;N的摩尔质量为70 g·mol-
1,故B错误;每个N含有36个电子,故C错误;该全氮阴离子盐中,N、Cl-、NH之间
存在离子键,N内存在N—N、NH内存在N—H,所以既含共价键又含离子键,故D正确。
11.答案 D
解析 由A的球棍模型可知A为甲烷,未说明为标况下,不能利用气体摩尔体积计算甲烷
的物质的量及其中的质子数,故A错误;由C的球棍模型可知C为甲醇,1 mol C中共价
键数目为5N ,故B错误;由总反应方程式:3CH +3NiO===3Ni+CHOH+CHCHOH+
A 4 3 3 2
HO可知,生成1 mol Ni可得到 mol B,故C错误;11.8 g泡沫镍含Ni单质=0.194 mol,
2
故D正确。
12.答案 D
解析 12 g C中所含的碳原子数称为阿伏加德罗常数,A错误;O 的摩尔质量为32 g·mol-
2
1,B 错误;由反应 2NO+O===2NO 知,1 mol NO 与 0.5 mol O 恰好反应生成 1 mol
2 2 2
NO ,但由于反应2NO NO 的存在,导致反应后气体分子数小于1 mol,C错误;白磷
2 2 2 4
分子为正四面体结构,P原子位于4个顶点,故1个P 分子中含有6个P—P共价键,即1
4
mol P 分子中含有6 mol P—P共价键,D正确。
4
13.答案 C
解析 125 g CuSO ·5H O的物质的量为0.5 mol,因为是晶体,所以Cu2+数目等于0.5N ,
4 2 A
若将其溶于水,铜离子水解会导致铜离子的数目小于 0.5N ,A项错误;没有指明pH=3
A
的醋酸溶液的体积,无法计算CHCOOH的物质的量,B项错误;S、S、S 均由硫原子组
3 2 4 8
成,所以6.4 g硫蒸气含有的硫原子的物质的量为=0.2 mol,硫原子的个数为0.2N ,
AC项正确;3.36 L O 没有说明气体所处的温度和压强,无法确定O 的物质的量,从而也无
2 2
法计算生成的CO的量,D项错误。
14.答案 C
解析 溶质的质量分数 ω=×100%,A错误;在计算时氨水中的溶质是 NH ,而不是
3
NH ·H O,a g NH 的物质的量为= mol,溶液体积为V mL则溶质的物质的量浓度为c=
3 2 3
mol·L-1=mol·L-1,B错误;氨水中含有的阳离子为H+和NH,含有的阴离子只有OH-,
根据电荷守恒可知C正确;由于氨水的密度小于水的密度,与水等体积混合所得稀氨水的
质量大于原氨水质量的2倍,故其质量分数小于0.5ω,D错误。
15.答案 C
解析 气体的分子数与物质的量成正比,则右边与左边分子数之比为1∶4,A错误;右侧
CO的质量为28 g·mol-1×0.25 mol=7 g,B错误;相同条件下气体密度之比等于气体摩尔
质量之比,所以右侧CO气体的密度是相同条件下氢气密度的=14倍,C正确;相同条件
下气体体积与物质的量成正比,隔板处于容器正中间时,左右两侧气体的物质的量相等,
则需要充入的CO的物质的量为1 mol-0.25 mol=0.75 mol,D错误。
16.答案 (1)蔗糖 (2)2×+ (3)ac 玻璃棒、烧杯 (4)AD (5)Cl-(或Br-)
解析 (1)同一溶液,体积相等,则物质的量越大其物质的量浓度越大,蔗糖的物质的量为
≈0.146 mol;硫酸钾的物质的量为≈0.002 87 mol;阿司匹林的物质的量为≈0.001 94 mol;
高锰酸钾的物质的量为≈0.003 2 mol;硝酸银的物质的量为≈0.000 24 mol;所以蔗糖的物
质的量最大,溶液中蔗糖的物质的量浓度最大。(2)依据c=,V=1 L,溶液中钾离子的物
质的量浓度为=(2×+) mol·L-1。(3)配制一定物质的量浓度溶液的一般步骤:计算、称量、
溶解、移液、洗涤、定容等,用到的仪器:托盘天平、烧杯、玻璃棒、药匙、1 000 mL容
量瓶、胶头滴管;用不到烧瓶和分液漏斗,还缺少的仪器:玻璃棒、烧杯。(4)容量瓶在使
用前未干燥,里面有少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度
不变,故A选;定容时仰视液面,导致溶液体积偏大,溶液浓度偏小,故B不选;容量瓶
在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净,容量瓶中沾有氯化钠,氯化
钠能够消耗银离子,导致溶液中银离子浓度偏小,故 C不选;定容摇匀后发现液面低于容
量瓶的刻度线,但未做任何处理,属于正确操作,溶液浓度不变,故D选。(5)银离子能够
与氯离子反应生成氯化银白色沉淀,向待测液中加入少量氯化钠,若产生白色沉淀即可证
明溶液中含有银离子。
17.答案 (1)4.0 (2)0.04 (3)C
(4)①4.6 ②250.0
解析 (1)由c=得,c(NaClO)= mol·L-1≈4.0 mol·L-1。(2)稀释前后溶液中NaClO的物质
的量不变,则有100×10-3 L×4.0 mol·L-1=100×10-3 L×c(NaClO)
×100,解得稀释后c(NaClO)=0.04 mol·L-1,c(Na+)=c(NaClO)=0.04 mol·L-1。(3)图示中的a、b不需要,但还需要玻璃棒和胶头滴管,故A错误;配制过程中需要加水,所以洗涤
干净后的容量瓶不必烘干,且容量瓶也不能烘干,故 B错误;未洗涤烧杯和玻璃棒将导致
配制的溶液中溶质的物质的量减小,结果偏低,故C正确;因实验室无480 mL规格的容
量瓶,应选取500 mL的容量瓶进行配制,然后取出480 mL即可,所以需要NaClO的质量
为m(NaClO)=0.5 L×4.0 mol·L-1×74.5 g·mol-1=149.0 g,故D错误。(4)①因为稀硫酸的浓
度为2.3 mol·L-1,由HSO 的组成可知,溶液中c(H+)=2c(H SO )=2×2.3 mol·L-1=4.6
2 4 2 4
mol·L-1。②2 L 2.3 mol·
L-1的稀硫酸中溶质的物质的量为2 L×2.3 mol·L-1=4.6 mol,设需要98%(密度为1.84 g·cm-
3)的浓硫酸的体积为V mL,则有=4.6 mol,解得V=250.0。
18.答案 (1)①0.2 ②9.5 ③0.5 (2)H
2
(3)22∶21 (4)8∶7
解析 (1)①根据公式n=cV,所以钠离子的物质的量为n=0.2 L×1.0 mol·L-1=0.2 mol,
n(NaCl)=n(Na+),所以 NaCl的物质的量为 0.2 mol。②根据公式 n=cV,n(Mg2+)=0.2
L×0.5 mol·
L-1=0.1 mol,根据n=,所以m(MgCl )=0.1 mol×95 g·mol-1=9.5 g。③根据电荷守恒有:
2
c(Na+)+2c(Mg2+)+2c(Cu2+)=c(Cl-),所以根据已知条件,1.0 mol·L-1+2×0.5 mol·L-1+
2×c(Cu2+)=3.0 mol·L-1,解得c(Cu2+)=0.5 mol·L-1,c(Cu2+)=c(CuCl )= 0.5 mol·L-1。
2
(2)根据公式n=,所以n(H )=0.5 mol,标准状况下的气体n=,所以n(CH)=0.3 mol,根
2 4
据分子数目之比等于物质的量之比可知,所含分子数目较多的是 H 。(3)根据公式n=,假
2
设质量都为m g,所以n(CO)= mol,原子个数为N ,n(CO)= mol,原子个数为N ,所
A 2 A
以相同质量的CO和CO 所含的原子个数比是∶=22∶21。(4)设HSO 的物质的量为x
2 2 4
mol,CuSO 的物质的量为y mol,根据反应Fe+HSO ===FeSO +H↑,消耗的金属铁的
4 2 4 4 2
物质的量为x mol,质量为56x g,Fe+CuSO ===FeSO +Cu,消耗的金属铁的物质的量为
4 4
y mol,质量为56y g,生成Cu的质量为64y g,所以根据已知条件56x+56y=64y,解得y
=7x,所以原混合溶液中SO和Cu2+个数之比为8∶7。
19.答案 (1)③>②=④>① (2)1∶1∶3 (3) (4)0.1 (5)NaClO+2NH ===NH+NaCl+
3 2 4
HO (6)3Fe+NO+2H++HO===Fe O+NH
2 2 3 4
解析 (1)标准状况下,5.6 L H S为0.25 mol,含有0.25N ×2=0.5N 个H原子;1.204×1023
2 A A
个NH 含有0.2N ×3=0.6N 个H原子;4.8 g CH 为0.3 mol,含有0.3N ×4=1.2N 个H原
3 A A 4 A A
子;4 ℃时,5.4 mL水为5.4 g,其物质的量为0.3 mol,含有0.3N ×2=0.6N 个H原子,
A A
综上,氢原子数由大到小的顺序为③>②=④>①。(2)假设三种溶液的浓度均为1 mol·L-
1,则NaSO 、MgSO 、Al (SO ) 溶液中SO的浓度分别为 1 mol·L-1×1=1 mol·L-1、1
2 4 4 2 4 3
mol·L-1×1=1 mol·L-1、1 mol·L-1×3=3 mol·L-1,即浓度之比为1∶1∶3。(3)标准状况下,
V L HCl的物质的量为 mol,质量是 g,所以溶液的质量是(100+) g,因此溶液的体积是=×10-3 L。根据c=可知,溶液的浓度是c= mol·
L-1= mol·L-1。(4)亚硫酸氢钠与重铬酸钾反应的离子方程式为Cr O+3HSO+5H+===2Cr3
2
++3SO+4HO,此时每消耗3 mol亚硫酸氢根离子可以处理1 mol重铬酸根离子,当工厂
2
处理废水消耗了3.12 g亚硫酸氢钠固体,即0.03 mol亚硫酸氢钠时,可以处理0.01 mol重铬
酸根离子,此时溶液中重铬酸钾的浓度c==0.1 mol·L-1。(6)0.1 mol硝酸根离子完全反应生
成铵根离子共转移0.8 mol电子,此时共消耗Fe 16.8 g,即0.3 mol,说明有0.3 mol Fe失去
0.8 mol电子,此时生成的Fe的氧化物应为Fe O,故硝酸根离子和Fe反应的离子方程式为
3 4
3Fe+NO+2H++HO===Fe O+NH。
2 3 4
20.答案 (1)28.6 g (2)①④ ⑤
(3)BCF (4)B
解析 (1)配制题给溶液时应选择500 mL的容量瓶,所以应称取NaCO·10H O晶体的质量:
2 3 2
0.2 mol·L-1×0.5 L×286 g·mol-1=28.6 g。(2)①Na CO·10H O晶体失去部分结晶水,则溶
2 3 2
质的物质的量偏大,所配溶液的浓度偏高;②用“左码右物”的称量方法称量晶体(使用游
码),则所称取溶质的质量偏小,所配溶液的浓度偏低;③碳酸钠晶体不纯,其中混有氯化
钠,则所称取溶质的质量偏小,所配溶液的浓度偏低;④称量碳酸钠晶体时所用砝码生锈
则所称取溶质的质量偏大,所配溶液的浓度偏高;⑤容量瓶未经干燥使用,对溶质的物质
的量、溶液的体积都不产生影响,所配溶液的浓度不变。(3)A项,使用容量瓶,可以将一
定物质的量的溶质溶解在一定量的溶剂中,配成一定体积准确浓度的标准溶液;B项,容
量瓶不能用于贮存溶液,尤其是碱性溶液;C项,容量瓶只有一个刻度线,所以只能配制
确定体积的液体;D项,利用容量瓶,可以将一定物质的量的溶液加水稀释配成准确浓度
的溶液;E项,容量瓶只能量取与容量瓶规格相同的液体;F项,容量瓶是不耐热的仪器,
不能用来加热溶解固体溶质。(4)改用固体NaCO 配制上述NaCO 溶液,所需NaCO 的质
2 3 2 3 2 3
量为0.2 mol·L-1×
0.5 L×106 g·mol-1=10.6 g,①不正确;定容时,视线与凹液面最低处相水平,⑤不正确。