文档内容
第 50 讲 沉淀溶解平衡图像的分析
复习目标 1.能正确分析沉淀溶解平衡图像。2.利用沉淀溶解平衡原理,分析图像中离子浓
度的关系、K 的计算等。
sp
类型一 有关沉淀溶解平衡 K 曲线的分析
sp
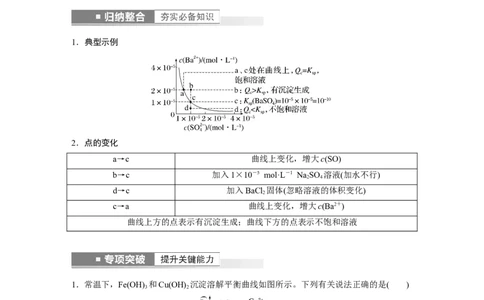
1.典型示例
2.点的变化
a→c 曲线上变化,增大c(SO)
b→c 加入1×10-5 mol·L-1 Na SO 溶液(加水不行)
2 4
d→c 加入BaCl 固体(忽略溶液的体积变化)
2
c→a 曲线上变化,增大c(Ba2+)
曲线上方的点表示有沉淀生成;曲线下方的点表示不饱和溶液
1.常温下,Fe(OH) 和Cu(OH) 沉淀溶解平衡曲线如图所示。下列有关说法正确的是( )
3 2
A.K [Fe(OH) ]>K [Cu(OH) ]
sp 3 sp 2
B.a、b、c、d四点的K 不同
w
C.在Fe(OH) 饱和溶液中加入适量硝酸钾晶体可使a点变到b点
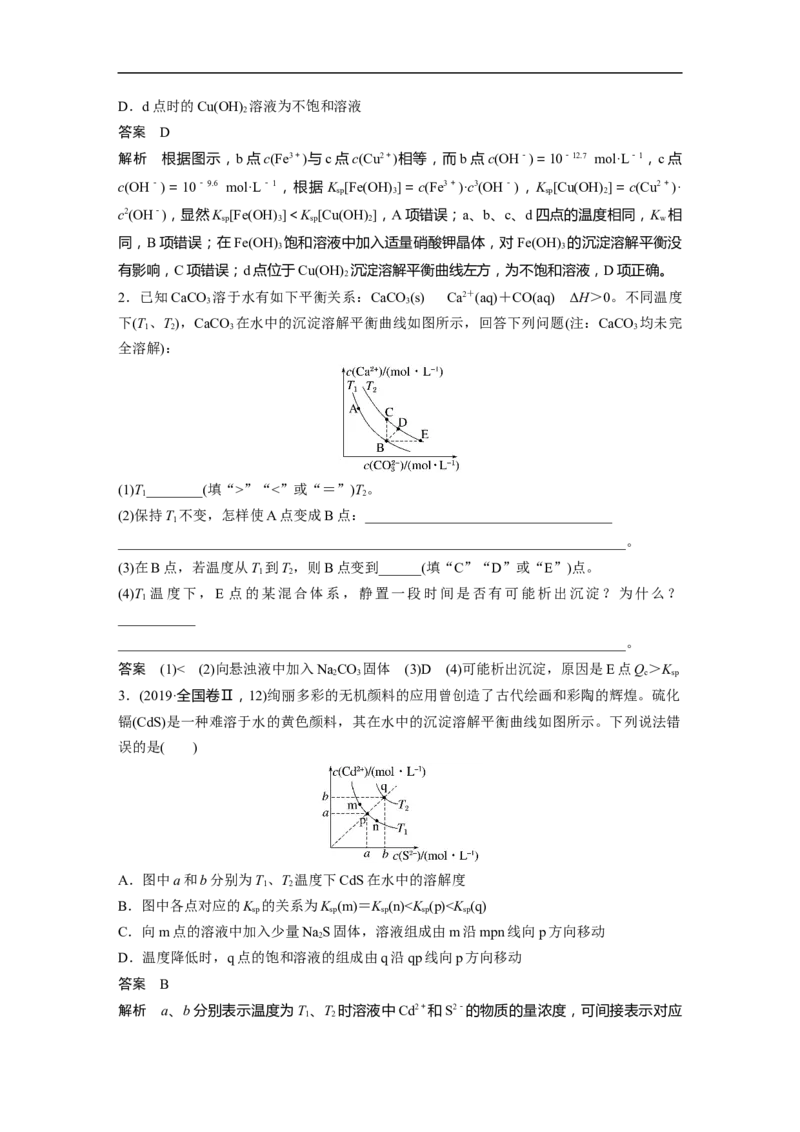
3D.d点时的Cu(OH) 溶液为不饱和溶液
2
答案 D
解析 根据图示,b点c(Fe3+)与c点c(Cu2+)相等,而b点c(OH-)=10-12.7 mol·L-1,c点
c(OH-)=10-9.6 mol·L-1,根据 K [Fe(OH) ]=c(Fe3+)·c3(OH-),K [Cu(OH) ]=c(Cu2+)·
sp 3 sp 2
c2(OH-),显然K [Fe(OH) ]<K [Cu(OH) ],A项错误;a、b、c、d四点的温度相同,K 相
sp 3 sp 2 w
同,B项错误;在Fe(OH) 饱和溶液中加入适量硝酸钾晶体,对Fe(OH) 的沉淀溶解平衡没
3 3
有影响,C项错误;d点位于Cu(OH) 沉淀溶解平衡曲线左方,为不饱和溶液,D项正确。
2
2.已知CaCO 溶于水有如下平衡关系:CaCO (s)Ca2+(aq)+CO(aq) ΔH>0。不同温度
3 3
下(T 、T),CaCO 在水中的沉淀溶解平衡曲线如图所示,回答下列问题(注:CaCO 均未完
1 2 3 3
全溶解):
(1)T________(填“>”“<”或“=”)T。
1 2
(2)保持T 不变,怎样使A点变成B点:___________________________________
1
________________________________________________________________________。
(3)在B点,若温度从T 到T,则B点变到______(填“C”“D”或“E”)点。
1 2
(4)T 温度下,E 点的某混合体系,静置一段时间是否有可能析出沉淀?为什么?
1
___________
________________________________________________________________________。
答案 (1)< (2)向悬浊液中加入NaCO 固体 (3)D (4)可能析出沉淀,原因是E点Q>K
2 3 c sp
3.(2019·全国卷Ⅱ,12)绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化
镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错
误的是( )
A.图中a和b分别为T、T 温度下CdS在水中的溶解度
1 2
B.图中各点对应的K 的关系为K (m)=K (n)c(K+)>c(Ag+)>c(H+)>c(OH-)
C.该温度下,K (Ag CrO)=4.0×10-12
sp 2 4
D.相同实验条件下,若改为0.05 mol·L-1的KCl和KCrO 溶液,则曲线L 中N点移到Q
2 4 2
点
答案 D
解析 KCl和硝酸银反应的化学方程式为KCl+AgNO===AgCl↓+KNO,铬酸钾和硝酸银
3 3
反应的化学方程式为KCrO +2AgNO===Ag CrO↓+2KNO ,根据反应化学方程式可知在
2 4 3 2 4 3
相同浓度的KCl和KCrO 溶液中加入相同浓度的硝酸银溶液,氯离子浓度减小的更快,所
2 4
以L 代表的是-lg c(Cl-)与V(AgNO)的变化关系,故 A正确;M点加入的硝酸银溶液体
1 3
积是15 mL,根据反应的化学方程式可知,生成0.001 mol硝酸钾和0.001 mol氯化银,剩余
0.000 5 mol硝酸银,则c(NO)>c(K+)>c(Ag+),银离子水解使溶液显酸性,则c(H+)>c(OH
-),所以M点溶液中,离子浓度大小顺序为 c(NO)>c(K+)>c(Ag+)>c(H+)>c(OH-),故 B正
确;N点纵坐标的数值是4.0,则Ag CrO 在沉淀溶解平衡中c(CrO)=10-4 mol·L-1,c(Ag+)
2 4
=2×10-4mol·L-1,K (Ag CrO)=c(CrO)·c2(Ag+)=10-4×(2×10-4)2=4.0×10-12 ,故C正
sp 2 4
确。
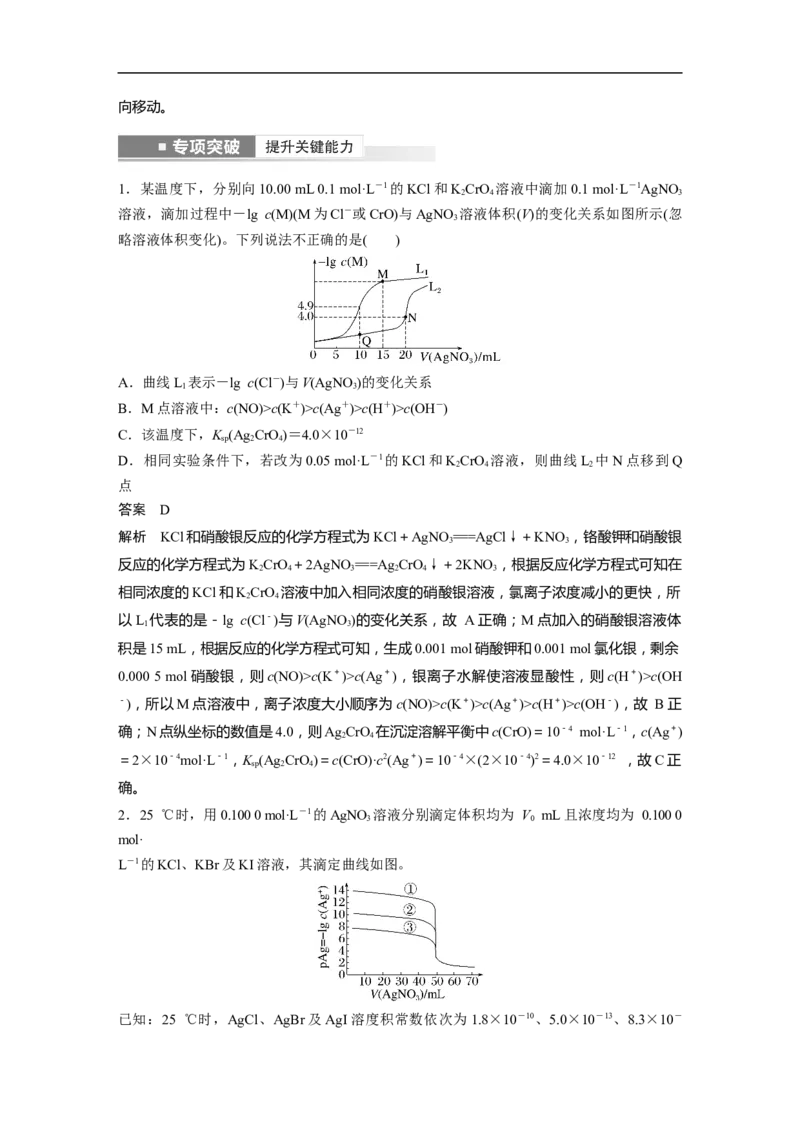
2.25 ℃时,用0.100 0 mol·L-1的AgNO 溶液分别滴定体积均为 V mL且浓度均为 0.100 0
3 0
mol·
L-1的KCl、KBr及KI溶液,其滴定曲线如图。
已知:25 ℃时,AgCl、AgBr及AgI溶度积常数依次为1.8×10-10、5.0×10-13、8.3×10-17,下列说法正确的是( )
A.V=45.00
0
B.滴定曲线①表示KCl的滴定曲线
C.滴定KCl时,可加入少量的KI作指示剂
D.当AgNO 溶液滴定至60.00 mL时,溶液中c(I-)<c(Br-)<c(Cl-)
3
答案 D
解析 由25 ℃时AgCl、AgBr及AgI的溶度积及图像可知,V =50.00;c(Ag+)由大到小依
0
次是AgCl、AgBr、AgI,所以-lg c(Ag+)从小到大依次为AgCl、AgBr、AgI,所以曲线③、
②、①依次为KCl、KBr及KI溶液的滴定曲线;在滴定KCl时,不能用KI作指示剂,因为
AgI溶度积更小,更容易沉淀;同理,当 AgNO 溶液滴定至60.00 mL时,AgNO 溶液过量
3 3
10.00 mL,溶液中的c(Ag+)相同,所以溶液中c(I-)<c(Br-)<c(Cl-)。
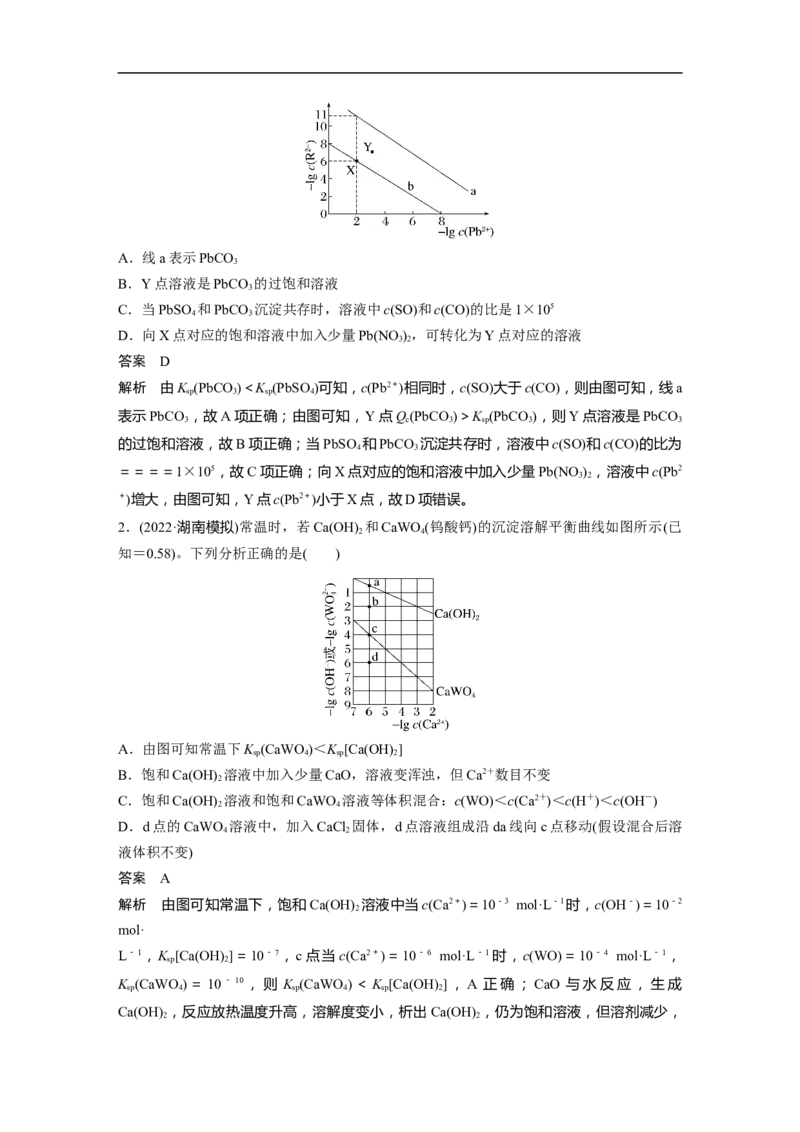
1.(2021·全国甲卷,12)已知相同温度下,K (BaSO)<K (BaCO)。某温度下,饱和溶液中
sp 4 sp 3
-lg [c(SO)]、-lg[c(CO)]与-lg[c(Ba2+)]的关系如图所示。下列说法正确的是( )
A.曲线①代表BaCO 的沉淀溶解曲线
3
B.该温度下BaSO 的K (BaSO)值为1.0×10-10
4 sp 4
C.加适量BaCl 固体可使溶液由a点变到b点
2
D.c(Ba2+)=10-5.1时两溶液中=
答案 B
解析 由题可知,曲线上的点均为饱和溶液中微粒浓度关系,由题及图像分析可知,曲线①
为BaSO 的沉淀溶解曲线,选项A错误;曲线①为BaSO 溶液中-lg[c(Ba2+)]与-lg[c(SO)]
4 4
的关系,由图可知,当溶液中-lg[c(Ba2+)]=3时,-lg[c(SO)]=7,则-lg[K (BaSO)]=7+
sp 4
3=10,因此K (BaSO)=1.0×10-10,选项B正确;向饱和BaCO 溶液中加入适量BaCl 固
sp 4 3 2
体后,溶液中c(Ba2+)增大,根据温度不变则K (BaCO)不变可知,溶液中c(CO)将减小,因
sp 3
此a点将沿曲线②向左上方移动,选项C错误;由图可知,当溶液中c(Ba2+)=10-5.1 mol·L-1时,两溶液中= = ,选项D错误。
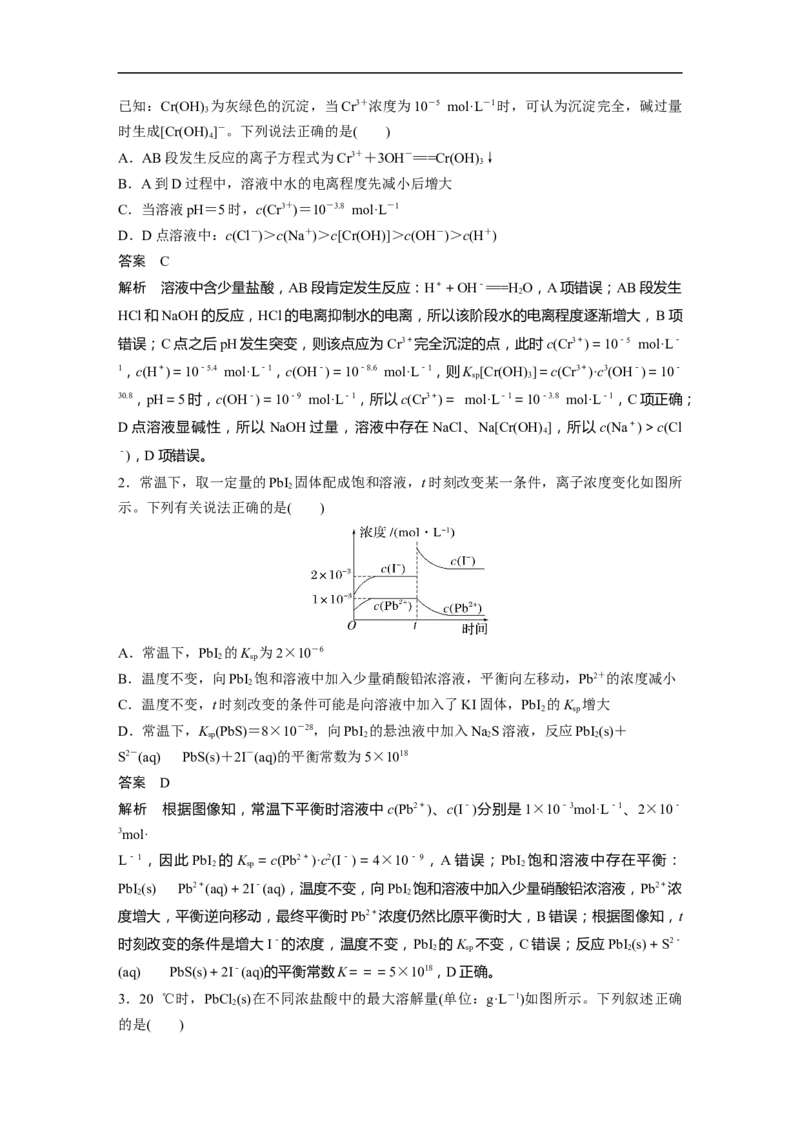
2.(2021·全国乙卷,13)HA是一元弱酸,难溶盐MA的饱和溶液中c(M+)随c(H+)而变化,
M+不发生水解。实验发现,298 K时c2(M+)~c(H+)为线性关系,如图中实线所示。
下列叙述错误的是( )
A.溶液pH=4时,c(M+)<3.0×10-4mol·L-1
B.MA的溶度积K (MA)=5.0×10-8
sp
C.溶液pH=7时,c(M+)+c(H+)=c(A-)+c(OH-)
D.HA的电离常数K(HA)=2.0×10-4
a
答案 C
解析 由图可知pH=4,即c(H+)=10×10-5mol·L-1时,c2(M+)=7.5×10-8 mol2·L-2,c(M
+)=mol·L-1=×10-4mol·L-1<3.0×10-4mol·L-1,A正确;由图可知,c(H+)=0时,可看作
溶液中有较大浓度的 OH-,此时 A-的水解极大地被抑制,溶液中 c(M+)=c(A-),则
K (MA)=c(M+)·c(A-)=c2(M+)=5.0×10-8,B正确;MA饱和溶液中,M+不发生水解,A
sp
-水解使溶液呈碱性,若使pH=7,需加入酸,会引入其他阴离子,此时c(M+)+c(H+)≠
c(A-)+c(OH-),C错误;K(HA)=,当c(A-)=c(HA)时,由物料守恒知c(A-)+c(HA)=
a
c(M+),则c(A-)=,K (MA)=c(M+)·c(A-)==5.0×10-8,则c2(M+)=10×10-8 mol2·L-
sp
2,对应图得此时溶液中c(H+)=2.0×10-4mol·L-1,K(HA)==2.0×10-4,D正确。
a
课时精练
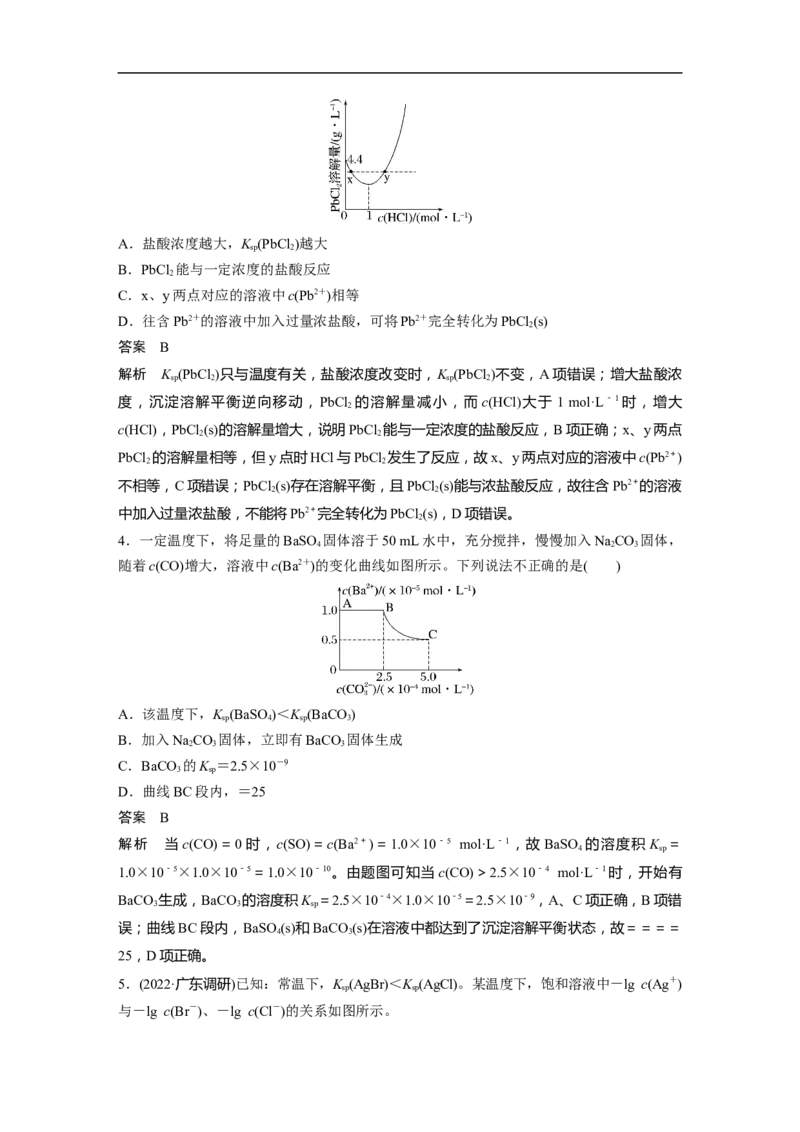
1.(2022·山东潍坊模拟)常温下,向含少量盐酸的 0.1 mol·L-1的CrCl 溶液中逐滴滴加
3
NaOH溶液,所加NaOH溶液的体积与溶液pH变化如图所示。已知:Cr(OH) 为灰绿色的沉淀,当Cr3+浓度为10-5 mol·L-1时,可认为沉淀完全,碱过量
3
时生成[Cr(OH) ]-。下列说法正确的是( )
4
A.AB段发生反应的离子方程式为Cr3++3OH-===Cr(OH) ↓
3
B.A到D过程中,溶液中水的电离程度先减小后增大
C.当溶液pH=5时,c(Cr3+)=10-3.8 mol·L-1
D.D点溶液中:c(Cl-)>c(Na+)>c[Cr(OH)]>c(OH-)>c(H+)
答案 C
解析 溶液中含少量盐酸,AB段肯定发生反应:H++OH-===HO,A项错误;AB段发生
2
HCl和NaOH的反应,HCl的电离抑制水的电离,所以该阶段水的电离程度逐渐增大,B项
错误;C点之后pH发生突变,则该点应为Cr3+完全沉淀的点,此时c(Cr3+)=10-5 mol·L-
1,c(H+)=10-5.4 mol·L-1,c(OH-)=10-8.6 mol·L-1,则K [Cr(OH) ]=c(Cr3+)·c3(OH-)=10-
sp 3
30.8,pH=5时,c(OH-)=10-9 mol·L-1,所以c(Cr3+)= mol·L-1=10-3.8 mol·L-1,C项正确;
D点溶液显碱性,所以 NaOH过量,溶液中存在 NaCl、Na[Cr(OH)],所以c(Na+)>c(Cl
4
-),D项错误。
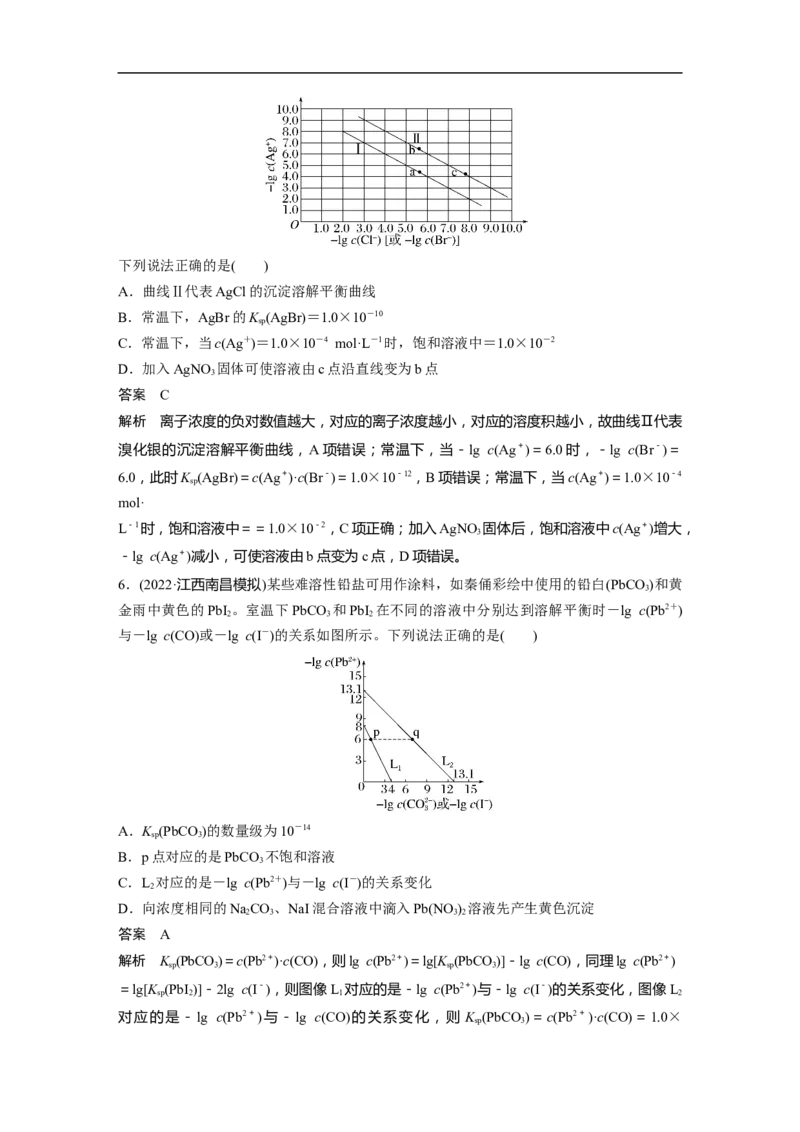
2.常温下,取一定量的PbI 固体配成饱和溶液,t时刻改变某一条件,离子浓度变化如图所
2
示。下列有关说法正确的是( )
A.常温下,PbI 的K 为2×10-6
2 sp
B.温度不变,向PbI 饱和溶液中加入少量硝酸铅浓溶液,平衡向左移动,Pb2+的浓度减小
2
C.温度不变,t时刻改变的条件可能是向溶液中加入了KI固体,PbI 的K 增大
2 sp
D.常温下,K (PbS)=8×10-28,向PbI 的悬浊液中加入NaS溶液,反应PbI (s)+
sp 2 2 2
S2-(aq)PbS(s)+2I-(aq)的平衡常数为5×1018
答案 D
解析 根据图像知,常温下平衡时溶液中 c(Pb2+)、c(I-)分别是1×10-3mol·L-1、2×10-
3mol·
L-1,因此 PbI 的 K =c(Pb2+)·c2(I-)=4×10-9,A 错误;PbI 饱和溶液中存在平衡:
2 sp 2
PbI (s)Pb2+(aq)+2I-(aq),温度不变,向PbI 饱和溶液中加入少量硝酸铅浓溶液,Pb2+浓
2 2
度增大,平衡逆向移动,最终平衡时Pb2+浓度仍然比原平衡时大,B错误;根据图像知,t
时刻改变的条件是增大I-的浓度,温度不变,PbI 的K 不变,C错误;反应PbI (s)+S2-
2 sp 2
(aq) PbS(s)+2I-(aq)的平衡常数K===5×1018,D正确。
3.20 ℃时,PbCl (s)在不同浓盐酸中的最大溶解量(单位:g·L-1)如图所示。下列叙述正确
2
的是( )A.盐酸浓度越大,K (PbCl )越大
sp 2
B.PbCl 能与一定浓度的盐酸反应
2
C.x、y两点对应的溶液中c(Pb2+)相等
D.往含Pb2+的溶液中加入过量浓盐酸,可将Pb2+完全转化为PbCl (s)
2
答案 B
解析 K (PbCl )只与温度有关,盐酸浓度改变时,K (PbCl )不变,A项错误;增大盐酸浓
sp 2 sp 2
度,沉淀溶解平衡逆向移动,PbCl 的溶解量减小,而 c(HCl)大于 1 mol·L-1时,增大
2
c(HCl),PbCl (s)的溶解量增大,说明PbCl 能与一定浓度的盐酸反应,B项正确;x、y两点
2 2
PbCl 的溶解量相等,但y点时HCl与PbCl 发生了反应,故x、y两点对应的溶液中c(Pb2+)
2 2
不相等,C项错误;PbCl (s)存在溶解平衡,且PbCl (s)能与浓盐酸反应,故往含Pb2+的溶液
2 2
中加入过量浓盐酸,不能将Pb2+完全转化为PbCl (s),D项错误。
2
4.一定温度下,将足量的BaSO 固体溶于50 mL水中,充分搅拌,慢慢加入NaCO 固体,
4 2 3
随着c(CO)增大,溶液中c(Ba2+)的变化曲线如图所示。下列说法不正确的是( )
A.该温度下,K (BaSO)<K (BaCO)
sp 4 sp 3
B.加入NaCO 固体,立即有BaCO 固体生成
2 3 3
C.BaCO 的K =2.5×10-9
3 sp
D.曲线BC段内,=25
答案 B
解析 当 c(CO)=0 时,c(SO)=c(Ba2+)=1.0×10-5 mol·L-1,故 BaSO 的溶度积 K =
4 sp
1.0×10-5×1.0×10-5=1.0×10-10。由题图可知当c(CO)>2.5×10-4 mol·L-1时,开始有
BaCO 生成,BaCO 的溶度积K =2.5×10-4×1.0×10-5=2.5×10-9,A、C项正确,B项错
3 3 sp
误;曲线BC段内,BaSO(s)和BaCO (s)在溶液中都达到了沉淀溶解平衡状态,故====
4 3
25,D项正确。
5.(2022·广东调研)已知:常温下,K (AgBr)<K (AgCl)。某温度下,饱和溶液中-lg c(Ag+)
sp sp
与-lg c(Br-)、-lg c(Cl-)的关系如图所示。下列说法正确的是( )
A.曲线Ⅱ代表AgCl的沉淀溶解平衡曲线
B.常温下,AgBr的K (AgBr)=1.0×10-10
sp
C.常温下,当c(Ag+)=1.0×10-4 mol·L-1时,饱和溶液中=1.0×10-2
D.加入AgNO 固体可使溶液由c点沿直线变为b点
3
答案 C
解析 离子浓度的负对数值越大,对应的离子浓度越小,对应的溶度积越小,故曲线Ⅱ代表
溴化银的沉淀溶解平衡曲线,A项错误;常温下,当-lg c(Ag+)=6.0时,-lg c(Br-)=
6.0,此时K (AgBr)=c(Ag+)·c(Br-)=1.0×10-12,B项错误;常温下,当c(Ag+)=1.0×10-4
sp
mol·
L-1时,饱和溶液中==1.0×10-2,C项正确;加入AgNO 固体后,饱和溶液中c(Ag+)增大,
3
-lg c(Ag+)减小,可使溶液由b点变为c点,D项错误。
6.(2022·江西南昌模拟)某些难溶性铅盐可用作涂料,如秦俑彩绘中使用的铅白(PbCO )和黄
3
金雨中黄色的PbI 。室温下PbCO 和PbI 在不同的溶液中分别达到溶解平衡时-lg c(Pb2+)
2 3 2
与-lg c(CO)或-lg c(I-)的关系如图所示。下列说法正确的是( )
A.K (PbCO )的数量级为10-14
sp 3
B.p点对应的是PbCO 不饱和溶液
3
C.L 对应的是-lg c(Pb2+)与-lg c(I-)的关系变化
2
D.向浓度相同的NaCO、NaI混合溶液中滴入Pb(NO ) 溶液先产生黄色沉淀
2 3 3 2
答案 A
解析 K (PbCO )=c(Pb2+)·c(CO),则lg c(Pb2+)=lg[K (PbCO )]-lg c(CO),同理lg c(Pb2+)
sp 3 sp 3
=lg[K (PbI )]-2lg c(I-),则图像L 对应的是-lg c(Pb2+)与-lg c(I-)的关系变化,图像L
sp 2 1 2
对应的是-lg c(Pb2+)与-lg c(CO)的关系变化,则 K (PbCO )=c(Pb2+)·c(CO)=1.0×
sp 310-13.1,数量级为10-14,故A项正确,C项错误;离子浓度的负对数值越小,则离子浓度越
大,p点位于L 的左下方,则对应PbCO 溶液为过饱和溶液,故B项错误;K (PbCO )=
2 3 sp 3
1.0×
10-13.1,K (PbI )=c(Pb2+)·c2(I-)=1.0×10-8,假设c(CO)和c(I-)均为1 mol·L-1,形成PbCO
sp 2 3
饱和溶液时,c(Pb2+)= mol·L-1=10-13.1 mol·L-1,形成 PbI 饱和溶液时,c(Pb2+)=
2
10-8 mol·L-1,则生成PbCO 沉淀需要的Pb2+的浓度更小,先生成白色沉淀,故D项错误。
3
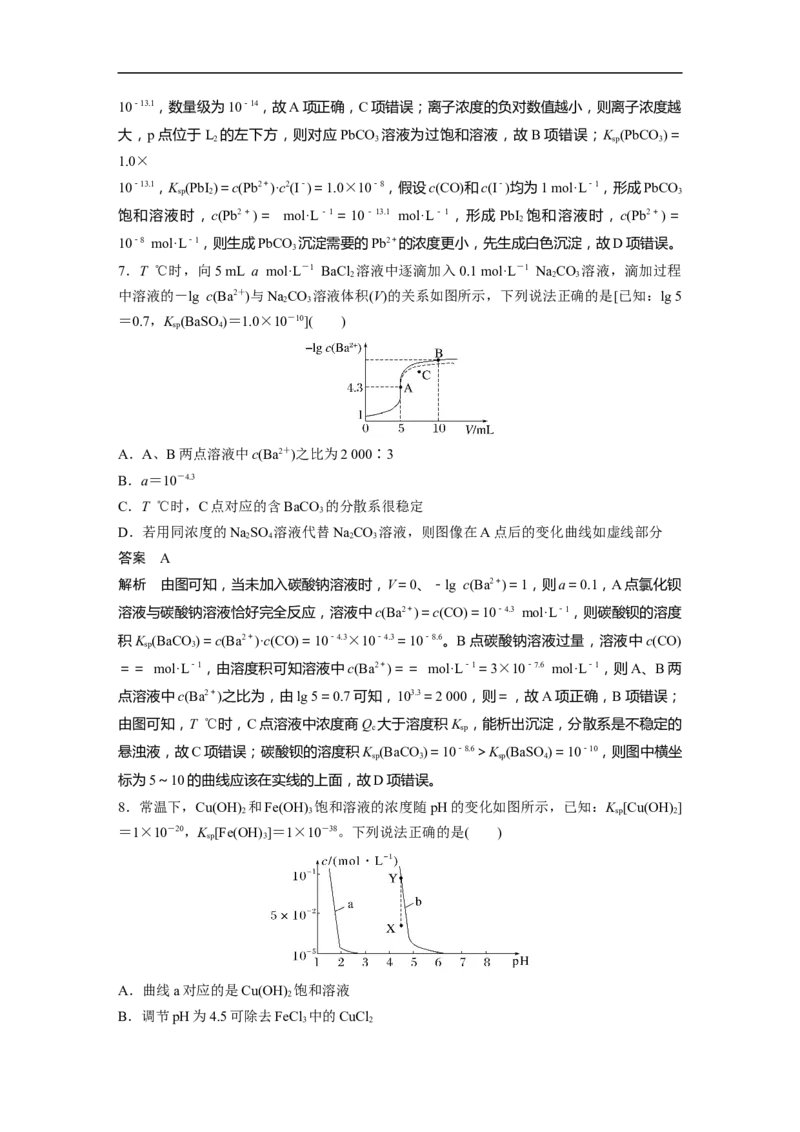
7.T ℃时,向5 mL a mol·L-1 BaCl 溶液中逐滴加入0.1 mol·L-1 Na CO 溶液,滴加过程
2 2 3
中溶液的-lg c(Ba2+)与NaCO 溶液体积(V)的关系如图所示,下列说法正确的是[已知:lg 5
2 3
=0.7,K (BaSO)=1.0×10-10]( )
sp 4
A.A、B两点溶液中c(Ba2+)之比为2 000∶3
B.a=10-4.3
C.T ℃时,C点对应的含BaCO 的分散系很稳定
3
D.若用同浓度的NaSO 溶液代替NaCO 溶液,则图像在A点后的变化曲线如虚线部分
2 4 2 3
答案 A
解析 由图可知,当未加入碳酸钠溶液时,V=0、-lg c(Ba2+)=1,则a=0.1,A点氯化钡
溶液与碳酸钠溶液恰好完全反应,溶液中c(Ba2+)=c(CO)=10-4.3 mol·L-1,则碳酸钡的溶度
积K (BaCO)=c(Ba2+)·c(CO)=10-4.3×10-4.3=10-8.6。B点碳酸钠溶液过量,溶液中c(CO)
sp 3
== mol·L-1,由溶度积可知溶液中c(Ba2+)== mol·L-1=3×10-7.6 mol·L-1,则A、B两
点溶液中c(Ba2+)之比为,由lg 5=0.7可知,103.3=2 000,则=,故A项正确,B项错误;
由图可知,T ℃时,C点溶液中浓度商Q 大于溶度积K ,能析出沉淀,分散系是不稳定的
c sp
悬浊液,故C项错误;碳酸钡的溶度积K (BaCO)=10-8.6>K (BaSO)=10-10,则图中横坐
sp 3 sp 4
标为5~10的曲线应该在实线的上面,故D项错误。
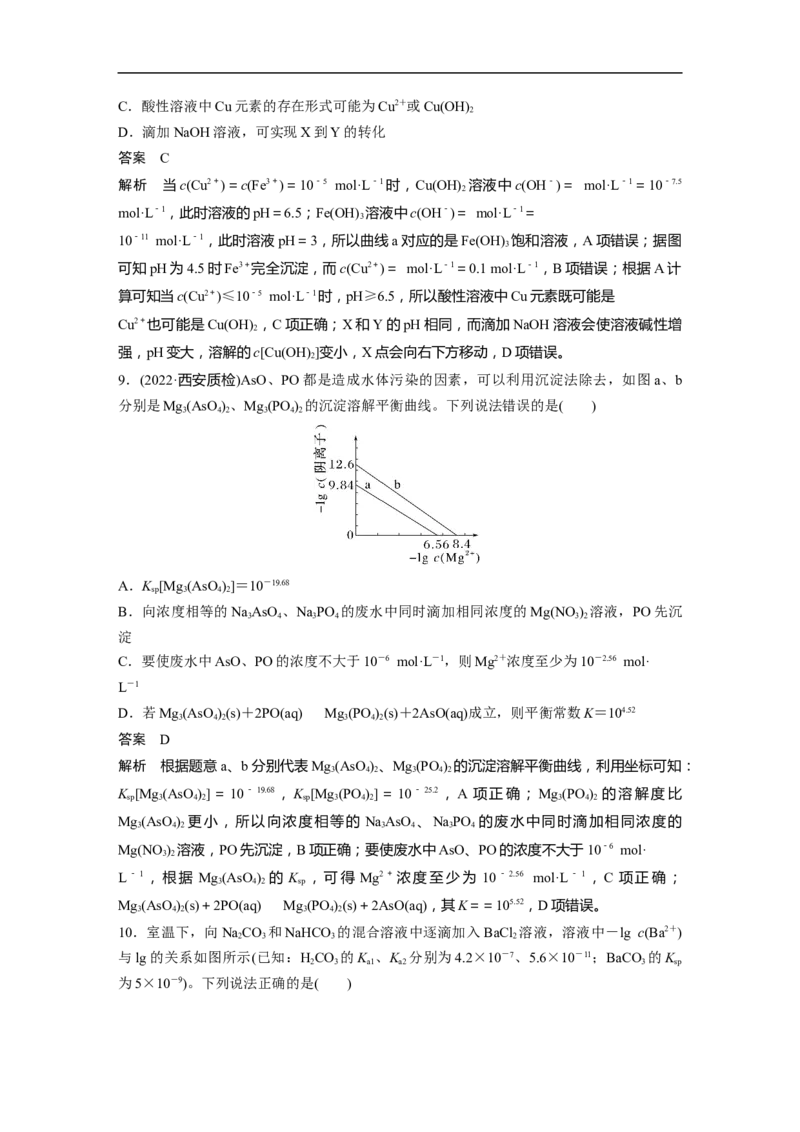
8.常温下,Cu(OH) 和Fe(OH) 饱和溶液的浓度随pH的变化如图所示,已知:K [Cu(OH) ]
2 3 sp 2
=1×10-20,K [Fe(OH) ]=1×10-38。下列说法正确的是( )
sp 3
A.曲线a对应的是Cu(OH) 饱和溶液
2
B.调节pH为4.5可除去FeCl 中的CuCl
3 2C.酸性溶液中Cu元素的存在形式可能为Cu2+或Cu(OH)
2
D.滴加NaOH溶液,可实现X到Y的转化
答案 C
解析 当c(Cu2+)=c(Fe3+)=10-5 mol·L-1时,Cu(OH) 溶液中c(OH-)= mol·L-1=10-7.5
2
mol·L-1,此时溶液的pH=6.5;Fe(OH) 溶液中c(OH-)= mol·L-1=
3
10-11 mol·L-1,此时溶液pH=3,所以曲线a对应的是Fe(OH) 饱和溶液,A项错误;据图
3
可知pH为4.5时Fe3+完全沉淀,而c(Cu2+)= mol·L-1=0.1 mol·L-1,B项错误;根据A计
算可知当c(Cu2+)≤10-5 mol·L-1时,pH≥6.5,所以酸性溶液中Cu元素既可能是
Cu2+也可能是Cu(OH) ,C项正确;X和Y的pH相同,而滴加NaOH溶液会使溶液碱性增
2
强,pH变大,溶解的c[Cu(OH) ]变小,X点会向右下方移动,D项错误。
2
9.(2022·西安质检)AsO、PO都是造成水体污染的因素,可以利用沉淀法除去,如图a、b
分别是Mg(AsO)、Mg(PO ) 的沉淀溶解平衡曲线。下列说法错误的是( )
3 4 2 3 4 2
A.K [Mg (AsO)]=10-19.68
sp 3 4 2
B.向浓度相等的NaAsO 、NaPO 的废水中同时滴加相同浓度的Mg(NO) 溶液,PO先沉
3 4 3 4 3 2
淀
C.要使废水中AsO、PO的浓度不大于10-6 mol·L-1,则Mg2+浓度至少为10-2.56 mol·
L-1
D.若Mg(AsO)(s)+2PO(aq)Mg(PO )(s)+2AsO(aq)成立,则平衡常数K=104.52
3 4 2 3 4 2
答案 D
解析 根据题意a、b分别代表Mg(AsO) 、Mg(PO ) 的沉淀溶解平衡曲线,利用坐标可知:
3 4 2 3 4 2
K [Mg (AsO)]=10-19.68,K [Mg (PO )]=10-25.2,A 项正确;Mg(PO ) 的溶解度比
sp 3 4 2 sp 3 4 2 3 4 2
Mg(AsO) 更小,所以向浓度相等的 NaAsO 、NaPO 的废水中同时滴加相同浓度的
3 4 2 3 4 3 4
Mg(NO) 溶液,PO先沉淀,B项正确;要使废水中AsO、PO的浓度不大于10-6 mol·
3 2
L-1,根据 Mg(AsO) 的 K ,可得 Mg2+浓度至少为 10-2.56 mol·L-1,C 项正确;
3 4 2 sp
Mg(AsO)(s)+2PO(aq)Mg(PO )(s)+2AsO(aq),其K==105.52,D项错误。
3 4 2 3 4 2
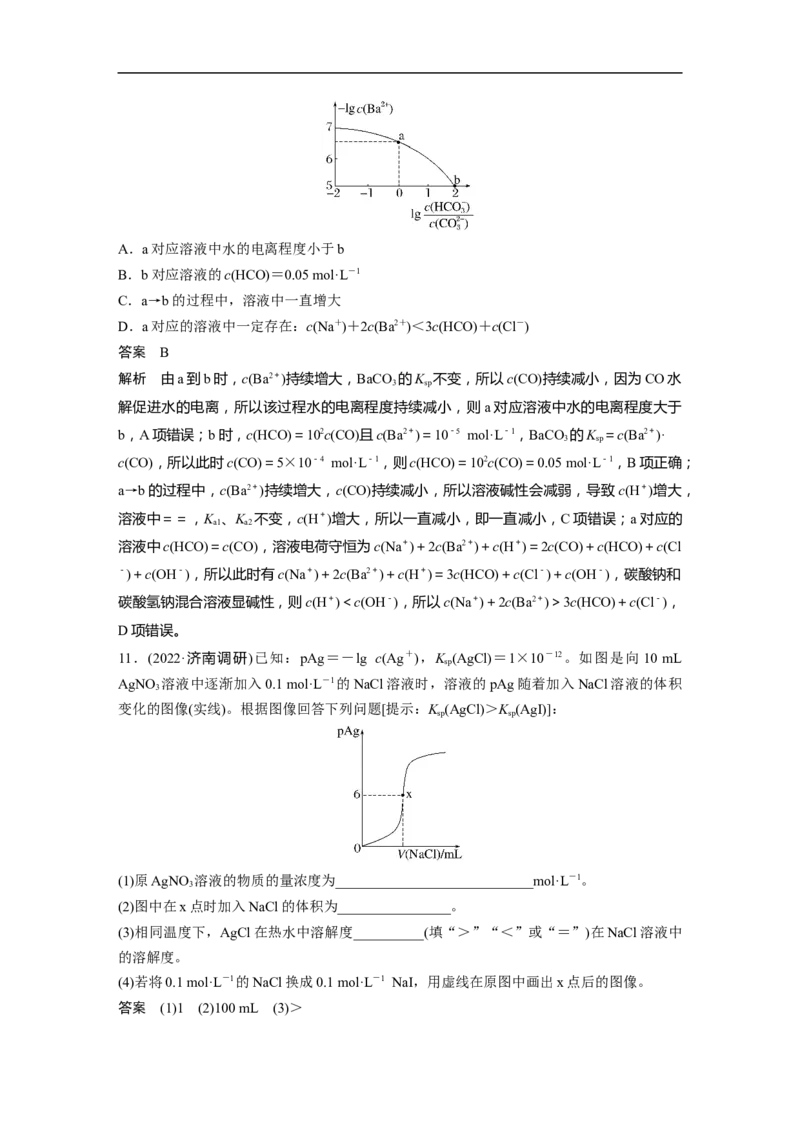
10.室温下,向NaCO 和NaHCO 的混合溶液中逐滴加入BaCl 溶液,溶液中-lg c(Ba2+)
2 3 3 2
与lg 的关系如图所示(已知:HCO 的K 、K 分别为4.2×10-7、5.6×10-11;BaCO 的K
2 3 a1 a2 3 sp
为5×10-9)。下列说法正确的是( )A.a对应溶液中水的电离程度小于b
B.b对应溶液的c(HCO)=0.05 mol·L-1
C.a→b的过程中,溶液中一直增大
D.a对应的溶液中一定存在:c(Na+)+2c(Ba2+)<3c(HCO)+c(Cl-)
答案 B
解析 由a到b时,c(Ba2+)持续增大,BaCO 的K 不变,所以c(CO)持续减小,因为CO水
3 sp
解促进水的电离,所以该过程水的电离程度持续减小,则a对应溶液中水的电离程度大于
b,A项错误;b时,c(HCO)=102c(CO)且c(Ba2+)=10-5 mol·L-1,BaCO 的K =c(Ba2+)·
3 sp
c(CO),所以此时c(CO)=5×10-4 mol·L-1,则c(HCO)=102c(CO)=0.05 mol·L-1,B项正确;
a→b的过程中,c(Ba2+)持续增大,c(CO)持续减小,所以溶液碱性会减弱,导致 c(H+)增大,
溶液中==,K 、K 不变,c(H+)增大,所以一直减小,即一直减小,C项错误;a对应的
a1 a2
溶液中c(HCO)=c(CO),溶液电荷守恒为c(Na+)+2c(Ba2+)+c(H+)=2c(CO)+c(HCO)+c(Cl
-)+c(OH-),所以此时有c(Na+)+2c(Ba2+)+c(H+)=3c(HCO)+c(Cl-)+c(OH-),碳酸钠和
碳酸氢钠混合溶液显碱性,则c(H+)<c(OH-),所以c(Na+)+2c(Ba2+)>3c(HCO)+c(Cl-),
D项错误。
11.(2022·济南调研)已知:pAg=-lg c(Ag+),K (AgCl)=1×10-12。如图是向 10 mL
sp
AgNO 溶液中逐渐加入0.1 mol·L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积
3
变化的图像(实线)。根据图像回答下列问题[提示:K (AgCl)>K (AgI)]:
sp sp
(1)原AgNO 溶液的物质的量浓度为____________________________mol·L-1。
3
(2)图中在x点时加入NaCl的体积为________________。
(3)相同温度下,AgCl在热水中溶解度__________(填“>”“<”或“=”)在NaCl溶液中
的溶解度。
(4)若将0.1 mol·L-1的NaCl换成0.1 mol·L-1 NaI,用虚线在原图中画出x点后的图像。
答案 (1)1 (2)100 mL (3)>(4)
解析 (1)加入NaCl之前,pAg=0,所以c(AgNO)=1 mol·L-1。
3
(2)由于c(Ag+)=10-6 mol·L-1,所以Ag+沉淀完全,n(NaCl)=n(AgNO)=0.01 L×1 mol·L-
3
1=0.01 mol,所以V(NaCl)=100 mL。
(3)AgCl在水中存在溶解平衡:AgCl(s)Ag+(aq)+Cl-(aq),相同温度下,c(Cl-)增大,平
衡逆向移动,溶解度减小,温度升高,平衡右移,溶解度增大。
(4)若把NaCl换成NaI,由于K (AgI)更小,所以c(Ag+)更小,pAg更大。
sp