文档内容
2025届高三化学一轮专题复习讲义(09)
专题三 基本理论
3-2 原电池原理及应用(1课时)
【复习目标】
1.了解原电池及常见化学电源的工作原理。
2.通过生活中实例,认识化学能与电能相互转化的实际意义及其重要应用。
【重点突破】
1.原电池的工作原理。
2.常见化学电源在实际生产和生活中的应用。
【真题再现】
例题1.(2023·江苏高考)下列物质结构与性质或物质性质与用途具有对应关系的是
A.H 具有还原性,可作为氢氧燃料电池的燃料
2
B.氨极易溶于水,液氨可用作制冷剂
C.HO分子之间形成氢键,HO(g)的热稳定性比HS(g)的高
2 2 2
D.NH 中的N原子与H+形成配位键,NH 具有还原性
2 4 2 4
解析:A项,燃料电池负极物质失电子,具有还原性,故A正确;B项,制冷剂是因为氨气易液化,
气化时需要吸热,B错误;C项,热稳定性是化学性质范畴,与化学键有关与氢键无关,氢键
只是影响物质的物理性质,C错误;D项,NH 是共价分子,构成微粒是原子,原子间通过形
2 4
成共用电子对,D错误。
答案:A
例题2.(2022·江苏高考)周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热
(890.3 kJ·mol-1 ),是常见燃料;Si、Ge是重要的半导体材料,硅晶体表面SiO 能与氢氟酸
2
(HF,弱酸)反应生成HSiF(H SiF 在水中完全电离为H+和SiF);1885年德国化学家将硫化锗
2 6 2 6
(GeS )与H 共热制得了门捷列夫预言的类硅—锗;下列化学反应表示正确的是
2 2
A. SiO 与HF溶液反应:SiO+6HF===2H++SiF+2H O
2 2 2
B. 高温下H 还原GeS :GeS +H ===Ge+2H S
2 2 2 2 2
C. 铅蓄电池放电时的正极反应:Pb-2e-+SO===PbSO
4
D. 甲烷的燃烧:CH(g)+2O(g) ===CO(g)+2HO(g) △H=890.3kJ·mol-1
4 2 2 2
解析:A项,由题意可知,二氧化硅与氢氟酸溶液反应生成强酸HSiF 和水,反应的离子方程式为
2 6
SiO+6HF===2H++SiF+2H O,正确;B项,硫化锗与氢气共热反应时,氢气与硫化锗反应生成
2 2
锗和硫化氢,硫化氢高温下分解生成硫和氢气,则反应的总方程式为GeS======Ge+2S,故
2
B错误;C项,铅蓄电池放电时,二氧化铅为正极,酸性条件下在硫酸根离子作用下二氧化铅
得到电子发生还原反应生成硫酸铅和水,电极反应式为正极反应PbO+2e-
2
+SO+4H+===PbSO +2HO,错误;D项,由题意可知,1mol甲烷完全燃烧生成二氧化碳和液态
4 2
水放出热量为890.3kJ,热化学方程式为CH(g)+2O(g) ===CO(g)+2HO(g)
4 2 2 2
△H=-890.3kJ·mol-1,错误。
答案:A。
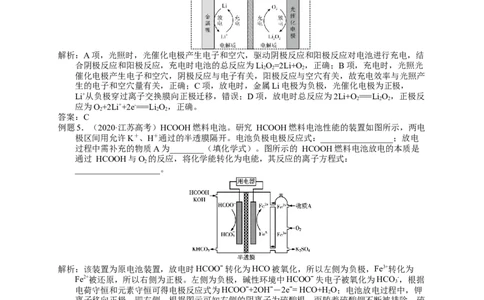
例题3.(2022·全国高考真题)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示[KOH溶液
2
中,Zn2+以Zn(OH)存在]。电池放电时,下列叙述错误的是
A.Ⅱ区的K+通过隔膜向Ⅲ区迁移
B.Ⅰ区的SO 通过隔膜向Ⅱ区迁移
C.MnO 电极反应:MnO +2e-+4H+===Mn2++2H O
2 2 2
D.电池总反应:Zn+4OH-+MnO+4H+===Zn(OH) +Mn2++2H O
2 2
解析:A项,根据分析,Ⅱ区的K+只能向Ⅰ区移动,错误;B项,根据分析,Ⅰ区的SO 向Ⅱ区移动,B正确;C项,MnO 电极的电极反应式为MnO +2e-+4H+=Mn2++2H O,C正确;D项,
2 2 2
电池的总反应为Zn+4OH-+MnO+4H+=Zn(OH)+Mn2++2H O,正确。
2 2
答案:A
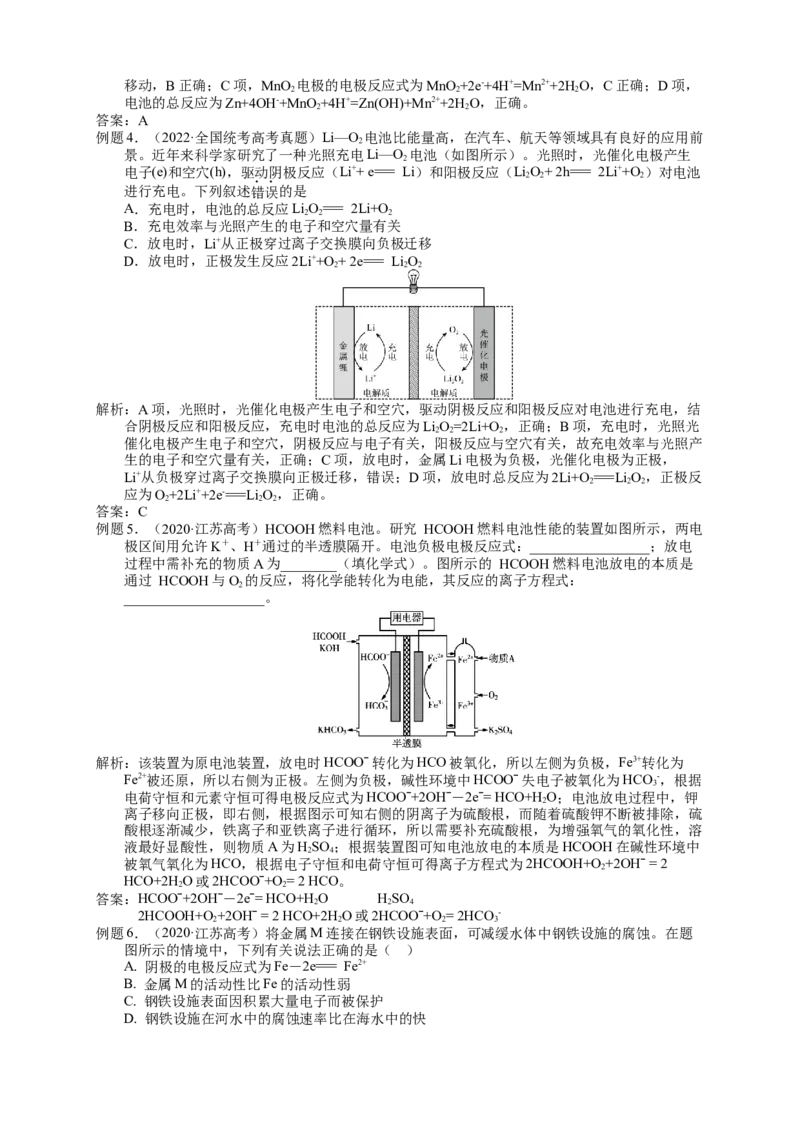
例题4.(2022·全国统考高考真题)Li—O 电池比能量高,在汽车、航天等领域具有良好的应用前
2
景。近年来科学家研究了一种光照充电Li—O 电池(如图所示)。光照时,光催化电极产生
2
电子(e)和空穴(h),驱动阴极反应(Li++ e=== Li)和阳极反应(LiO+ 2h=== 2Li++O )对电池
2 2 2
进行充电。下列叙述错误的是
A.充电时,电池的总反应LiO=== 2Li+O
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应2Li++O + 2e=== LiO
2 2 2
解析:A项,光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结
合阴极反应和阳极反应,充电时电池的总反应为LiO=2Li+O ,正确;B项,充电时,光照光
2 2 2
催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率与光照产
生的电子和空穴量有关,正确;C项,放电时,金属Li电极为负极,光催化电极为正极,
Li+从负极穿过离子交换膜向正极迁移,错误;D项,放电时总反应为2Li+O===LiO,正极反
2 2 2
应为O+2Li++2e-===LiO,正确。
2 2 2
答案:C
例题5.(2020·江苏高考)HCOOH燃料电池。研究 HCOOH燃料电池性能的装置如图所示,两电
极区间用允许K+、H+通过的半透膜隔开。电池负极电极反应式:_________________;放电
过程中需补充的物质A为________(填化学式)。图所示的 HCOOH燃料电池放电的本质是
通过 HCOOH与O 的反应,将化学能转化为电能,其反应的离子方程式:
2
____________________。
解析:该装置为原电池装置,放电时HCOOˉ转化为HCO被氧化,所以左侧为负极,Fe3+转化为
Fe2+被还原,所以右侧为正极。左侧为负极,碱性环境中HCOOˉ失电子被氧化为HCO -,根据
3
电荷守恒和元素守恒可得电极反应式为HCOOˉ+2OHˉ-2eˉ= HCO+H O;电池放电过程中,钾
2
离子移向正极,即右侧,根据图示可知右侧的阴离子为硫酸根,而随着硫酸钾不断被排除,硫
酸根逐渐减少,铁离子和亚铁离子进行循环,所以需要补充硫酸根,为增强氧气的氧化性,溶
液最好显酸性,则物质A为HSO ;根据装置图可知电池放电的本质是HCOOH在碱性环境中
2 4
被氧气氧化为HCO,根据电子守恒和电荷守恒可得离子方程式为2HCOOH+O +2OHˉ = 2
2
HCO+2H O或2HCOOˉ+O = 2 HCO。
2 2
答案:HCOOˉ+2OHˉ-2eˉ= HCO+H O H SO
2 2 4
2HCOOH+O +2OHˉ = 2 HCO+2H O或2HCOOˉ+O = 2HCO -
2 2 2 3
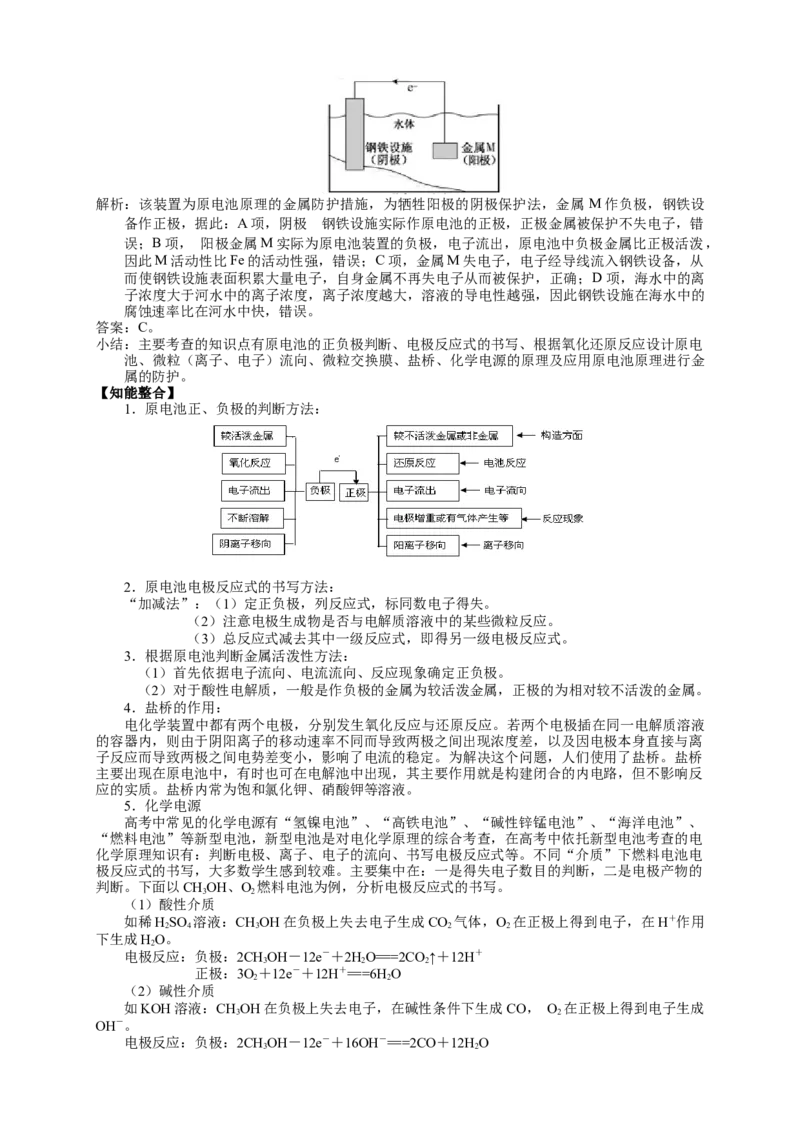
例题6.(2020·江苏高考)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题
图所示的情境中,下列有关说法正确的是( )
A. 阴极的电极反应式为Fe-2e=== Fe2+
B. 金属M的活动性比Fe的活动性弱
C. 钢铁设施表面因积累大量电子而被保护
D. 钢铁设施在河水中的腐蚀速率比在海水中的快解析:该装置为原电池原理的金属防护措施,为牺牲阳极的阴极保护法,金属 M作负极,钢铁设
备作正极,据此:A项,阴极 钢的铁设施实际作原电池的正极,正极金属被保护不失电子,错
误;B项, 阳极金属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,
因此M活动性比Fe的活动性强,错误;C项,金属M失电子,电子经导线流入钢铁设备,从
而使钢铁设施表面积累大量电子,自身金属不再失电子从而被保护,正确;D项,海水中的离
子浓度大于河水中的离子浓度,离子浓度越大,溶液的导电性越强,因此钢铁设施在海水中的
腐蚀速率比在河水中快,错误。
答案:C。
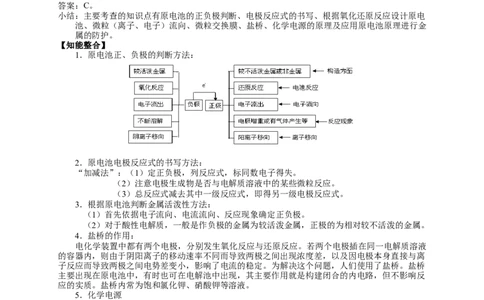
小结:主要考查的知识点有原电池的正负极判断、电极反应式的书写、根据氧化还原反应设计原电
池、微粒(离子、电子)流向、微粒交换膜、盐桥、化学电源的原理及应用原电池原理进行金
属的防护。
【知能整合】
1.原电池正、负极的判断方法:
2.原电池电极反应式的书写方法:
“加减法”:(1)定正负极,列反应式,标同数电子得失。
(2)注意电极生成物是否与电解质溶液中的某些微粒反应。
(3)总反应式减去其中一级反应式,即得另一级电极反应式。
3.根据原电池判断金属活泼性方法:
(1)首先依据电子流向、电流流向、反应现象确定正负极。
(2)对于酸性电解质,一般是作负极的金属为较活泼金属,正极的为相对较不活泼的金属。
4.盐桥的作用:
电化学装置中都有两个电极,分别发生氧化反应与还原反应。若两个电极插在同一电解质溶液
的容器内,则由于阴阳离子的移动速率不同而导致两极之间出现浓度差,以及因电极本身直接与离
子反应而导致两极之间电势差变小,影响了电流的稳定。为解决这个问题,人们使用了盐桥。盐桥
主要出现在原电池中,有时也可在电解池中出现,其主要作用就是构建闭合的内电路,但不影响反
应的实质。盐桥内常为饱和氯化钾、硝酸钾等溶液。
5.化学电源
高考中常见的化学电源有“氢镍电池”、“高铁电池”、“碱性锌锰电池”、“海洋电池”、
“燃料电池”等新型电池,新型电池是对电化学原理的综合考查,在高考中依托新型电池考查的电
化学原理知识有:判断电极、离子、电子的流向、书写电极反应式等。不同“介质”下燃料电池电
极反应式的书写,大多数学生感到较难。主要集中在:一是得失电子数目的判断,二是电极产物的
判断。下面以CHOH、O 燃料电池为例,分析电极反应式的书写。
3 2
(1)酸性介质
如稀HSO 溶液:CHOH在负极上失去电子生成CO 气体,O 在正极上得到电子,在H+作用
2 4 3 2 2
下生成HO。
2
电极反应:负极:2CHOH-12e-+2HO===2CO ↑+12H+
3 2 2
正极:3O+12e-+12H+===6H O
2 2
(2)碱性介质
如KOH溶液:CHOH在负极上失去电子,在碱性条件下生成CO, O 在正极上得到电子生成
3 2
OH-。
电极反应:负极:2CHOH-12e-+16OH-===2CO+12HO
3 2正极:3O+12e-+6HO===12OH-
2 2
(3)熔融盐介质
如KCO :在电池工作时,CO移向负极。CHOH在负极上失去电子,在CO的作用下生成
2 3 3
CO 气体,O 在正极上得到电子,在CO 的作用下生成CO。
2 2 2
电极反应:负极:2CHOH-12e-+6CO===8CO ↑+4HO
3 2 2
正极:3O+12e-+6CO===6CO
2 2
(4)其它介质
如掺杂YO 的ZrO 固体作电解质,在高温下能传导正极生成的O2-。根据O2-移向负极,在负
2 3 3
极上CHOH失电子生成CO 气体,而O 在正极上得电子生成O2-。
3 2 2
电极反应:负极:2CHOH-12e-+6O2-===2CO ↑+4HO
3 2 2
正极:3O+12e-===6O2-
2
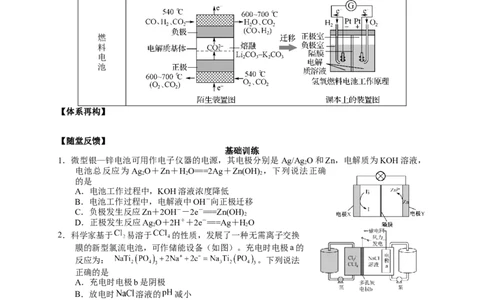
6.思维方式:知识迁移
由陌生装置图迁移到课本熟悉的装置图
燃
料
电
池
【体系再构】
【随堂反馈】
基础训练
1.微型银—锌电池可用作电子仪器的电源,其电极分别是 Ag/Ag O和Zn,电解质为KOH溶液,
2
电池总反应为 Ag O+Zn+HO===2Ag+Zn(OH) ,下列说法正确
2 2 2
的是
A.电池工作过程中,KOH溶液浓度降低
B.电池工作过程中,电解液中OH-向正极迁移
C.负极发生反应Zn+2OH--2e-===Zn(OH)
2
D.正极发生反应Ag O+2H++2e-===Ag+HO
2 2
2.科学家基于 易溶于 的性质,发展了一种无需离子交换
膜的新型氯流电池,可作储能设备(如图)。充电时电极a的
反应为: 。下列说法
正确的是
A.充电时电极b是阴极
B.放电时 溶液的 减小
C.放电时 溶液的浓度增大
D.每生成 ,电极a质量理论上增加
3.利用生物燃料电池原理研究室温下氨的合成,电池工作时 MV2+/MV+在电极与酶之间传递电子,
示意图如下所示。下列说法错误的是题3图 题4图
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应H+2MV2+===2H++2MV+
2
C.正极区,固氮酶为催化剂,N 发生还原反应生成NH
2 3
D.电池工作时质子通过交换膜由负极区向正极区移动
4.海水电池在海洋能源领域备受关注,一种锂-海水电池构造如示意题4图。下列说法错误的是
A.海水起电解质溶液作用
B.N极仅发生的电极反应:
C.玻璃陶瓷具有传导离子和防水的功能
D.该锂-海水电池属于一次电池
拓展训练
5.镍镉电池是二次电池,其工作原理示意图如题5图(L为小灯泡,K、K 为开关,a、b为直流
1 2
电源的两极)。下列说法不正确的是
A.断开K、合上K,镍镉电池能量转化形式:化学能→电能
2 1
B.断开K、合上K,电极A为阴极,发生还原反应
1 2
C.电极B发生氧化反应过程中,溶液中KOH浓度不变
D.镍镉二次电池的总反应式:Cd+ 2NiOOH+2H O Cd(OH) +2Ni(OH)
2 2 2
题5 题6
6.某全固态薄膜锂离子电池截面结构如题6图所示,电极A为非晶硅薄膜,充电时Li+得电子成为
Li嵌入该薄膜材料中;电极B为LiCoO 薄膜;集流体起导电作用。下列说法不正确的是
2
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过amol电子时,LiPON薄膜电解质损失amolLi+
C.放电时,电极B为正极,反应可表示为
D.电池总反应可表示为
7.一种以 和 为电极、 水溶液为电解质的电池,其示意图如下所示。放电时,
可插入 层间形成 。下列说法错误的是A.放电时VO 为正极
2 5
B.放电时Zn2+由负极向正极迁移
C.充电总反应:
D.充电阳极反应:
8. 科学家近年发明了一种新型Zn−CO 水介质电池。电池示意图如图,电极为金属锌和选择性催化
2
材料,放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新
2
途径。下列说法错误的是
A.放电时,负极反应为
B.放电时,1 mol CO 转化为HCOOH,转移的电子数为2 mol
2
C.充电时,电池总反应为
D.充电时,正极溶液中OH−浓度升高
【随堂反馈】答案:
1.C 2.C 3.B 4.B 5.C 6 .B 7.C 8. D
【课后作业】
1.如图是一种电解质溶液可以循环流动的新型电池。下列说法正确的是
A.Cu电极为正极
B.PbO 电极反应式:PbO +2e-+4H+===Pb2++2HO
2 2 2
C.放电后循环液中HSO 与CuSO 物质的量之比变小
2 4 4
D.若将Cu换成Pb,则电路中电子转移方向改变
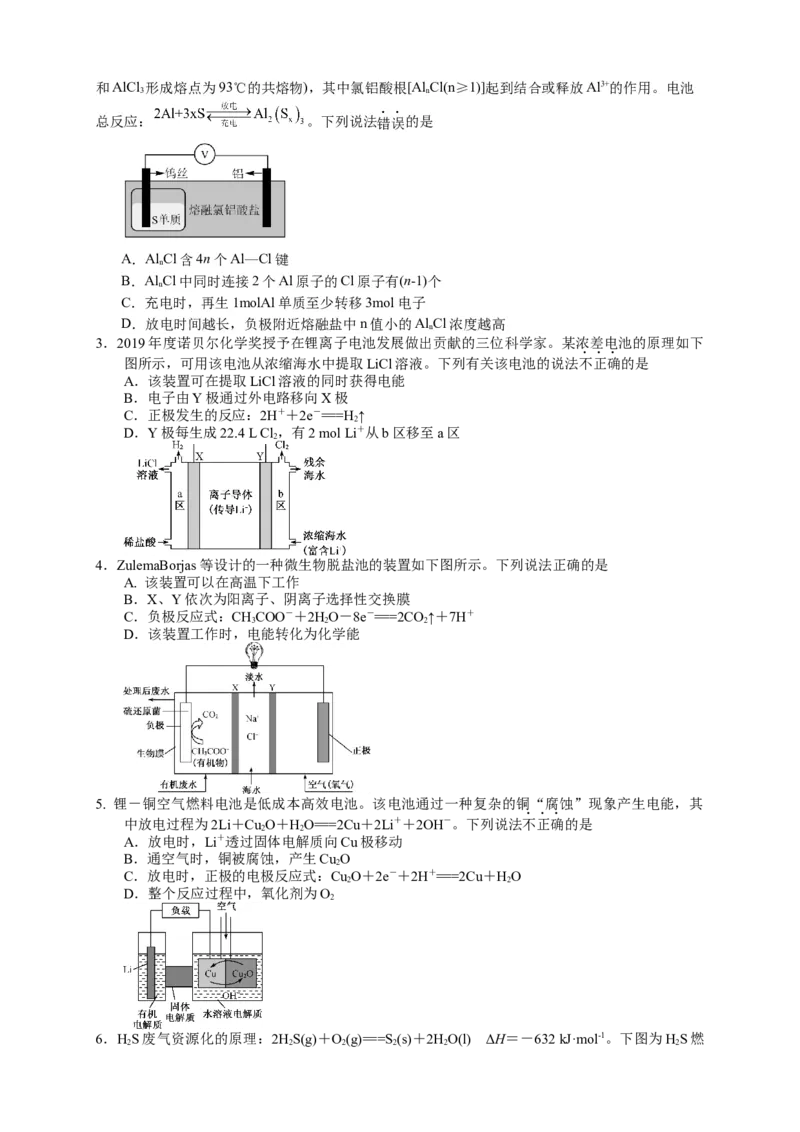
2.一种可在较高温下安全快充的铝-硫电池的工作原理如图,电解质为熔融氯铝酸盐(由NaCl、KCl和AlCl 形成熔点为93℃的共熔物),其中氯铝酸根[AlCl(n≥1)]起到结合或释放Al3+的作用。电池
3 n
总反应: 。下列说法错误的是
A.AlCl含4n个Al—Cl键
n
B.AlCl中同时连接2个Al原子的Cl原子有(n-1)个
n
C.充电时,再生1molAl单质至少转移3mol电子
D.放电时间越长,负极附近熔融盐中n值小的AlCl浓度越高
n
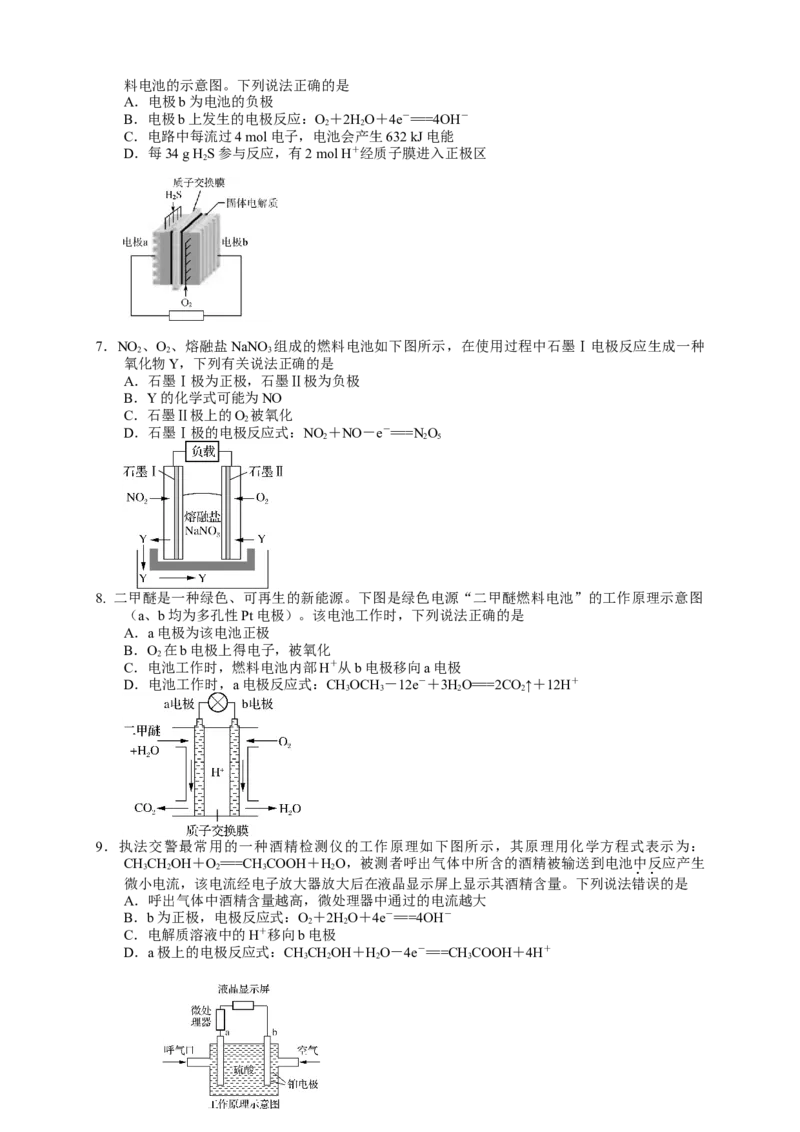
3.2019年度诺贝尔化学奖授予在锂离子电池发展做出贡献的三位科学家。某浓差电池的原理如下
图所示,可用该电池从浓缩海水中提取LiCl溶液。下列有关该电池的说法不正确的是
A.该装置可在提取LiCl溶液的同时获得电能
B.电子由Y极通过外电路移向X极
C.正极发生的反应:2H++2e-===H ↑
2
D.Y极每生成22.4 L Cl ,有2 mol Li+从b区移至a区
2
4.ZulemaBorjas等设计的一种微生物脱盐池的装置如下图所示。下列说法正确的是
A. 该装置可以在高温下工作
B.X、Y依次为阳离子、阴离子选择性交换膜
C.负极反应式:CHCOO-+2HO-8e-===2CO ↑+7H+
3 2 2
D.该装置工作时,电能转化为化学能
5. 锂-铜空气燃料电池是低成本高效电池。该电池通过一种复杂的铜“腐蚀”现象产生电能,其
中放电过程为2Li+Cu O+HO===2Cu+2Li++2OH-。下列说法不正确的是
2 2
A.放电时,Li+透过固体电解质向Cu极移动
B.通空气时,铜被腐蚀,产生Cu O
2
C.放电时,正极的电极反应式:Cu O+2e-+2H+===2Cu+HO
2 2
D.整个反应过程中,氧化剂为O
2
6.HS废气资源化的原理:2HS(g)+O(g)===S (s)+2HO(l) ΔH=-632 kJ·mol-1。下图为HS燃
2 2 2 2 2 2料电池的示意图。下列说法正确的是
A.电极b为电池的负极
B.电极b上发生的电极反应:O+2HO+4e-===4OH-
2 2
C.电路中每流过4 mol电子,电池会产生632 kJ电能
D.每34 g HS参与反应,有2 mol H+经质子膜进入正极区
2
7.NO 、O 、熔融盐NaNO 组成的燃料电池如下图所示,在使用过程中石墨Ⅰ电极反应生成一种
2 2 3
氧化物Y,下列有关说法正确的是
A.石墨Ⅰ极为正极,石墨Ⅱ极为负极
B.Y的化学式可能为NO
C.石墨Ⅱ极上的O 被氧化
2
D.石墨Ⅰ极的电极反应式:NO +NO-e-===N O
2 2 5
8. 二甲醚是一种绿色、可再生的新能源。下图是绿色电源“二甲醚燃料电池”的工作原理示意图
(a、b均为多孔性Pt电极)。该电池工作时,下列说法正确的是
A.a电极为该电池正极
B.O 在b电极上得电子,被氧化
2
C.电池工作时,燃料电池内部H+从b电极移向a电极
D.电池工作时,a电极反应式:CHOCH -12e-+3HO===2CO ↑+12H+
3 3 2 2
9.执法交警最常用的一种酒精检测仪的工作原理如下图所示,其原理用化学方程式表示为:
CHCHOH+O===CH COOH+HO,被测者呼出气体中所含的酒精被输送到电池中反应产生
3 2 2 3 2
微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法错误的是
A.呼出气体中酒精含量越高,微处理器中通过的电流越大
B.b为正极,电极反应式:O+2HO+4e-===4OH-
2 2
C.电解质溶液中的H+移向b电极
D.a极上的电极反应式:CHCHOH+HO-4e-===CH COOH+4H+
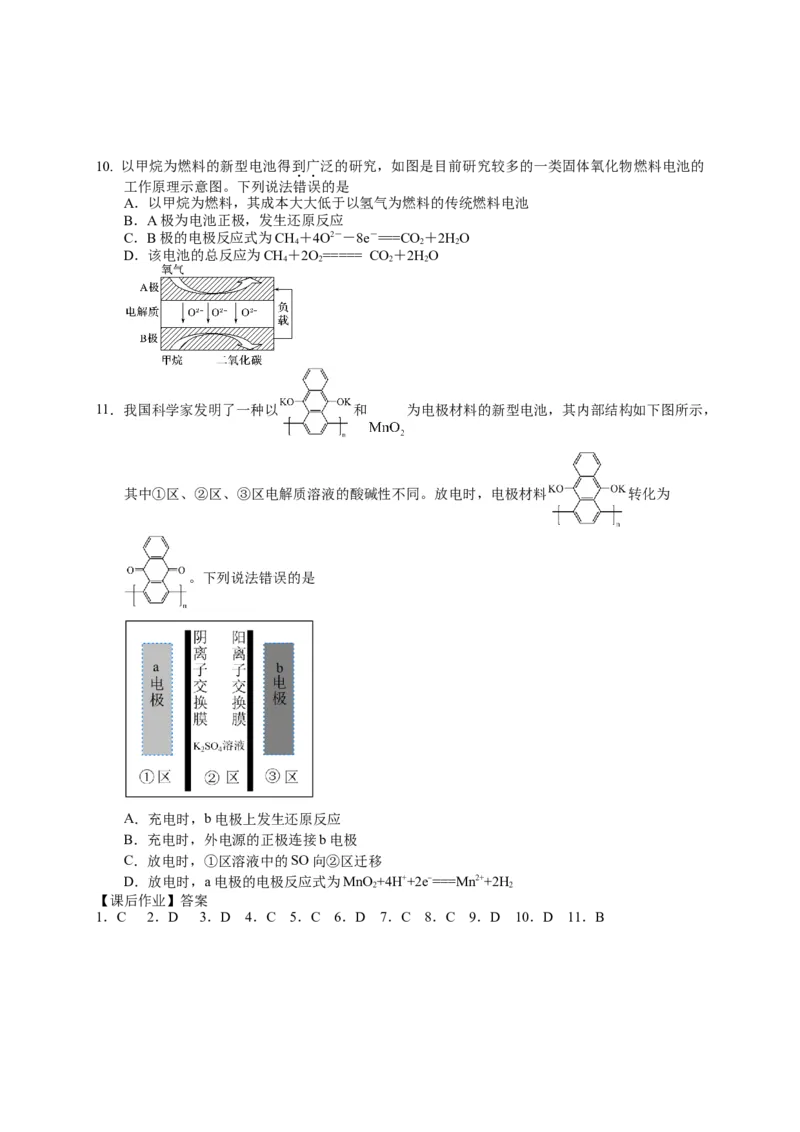
3 2 2 310. 以甲烷为燃料的新型电池得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池的
工作原理示意图。下列说法错误的是
A.以甲烷为燃料,其成本大大低于以氢气为燃料的传统燃料电池
B.A极为电池正极,发生还原反应
C.B极的电极反应式为CH+4O2--8e-===CO +2HO
4 2 2
D.该电池的总反应为CH+2O===== CO+2HO
4 2 2 2
11.我国科学家发明了一种以 和 为电极材料的新型电池,其内部结构如下图所示,
其中①区、②区、③区电解质溶液的酸碱性不同。放电时,电极材料 转化为
。下列说法错误的是
A.充电时,b电极上发生还原反应
B.充电时,外电源的正极连接b电极
C.放电时,①区溶液中的SO向②区迁移
D.放电时,a电极的电极反应式为MnO+4H++2e-===Mn2++2H
2 2
【课后作业】答案
1.C 2.D 3.D 4.C 5.C 6.D 7.C 8.C 9.D 10.D 11.B