文档内容
2025届高三化学一轮专题复习讲义(10)
专题三 基本理论
3-3 电解原理及应用(1课时)
【复习目标】
1.理解电解池的能量转化、工作原理,能写出简单电极反应和电池反应式。
2.认识电解在实际生活中的具体应用。
3.能利用电化学原理解释金属腐蚀现象,选择并设计防腐措施。
【重点突破】
1.能分析、解释电解池的工作原理。
2.掌握电解原理的工业应用。
【真题再现】
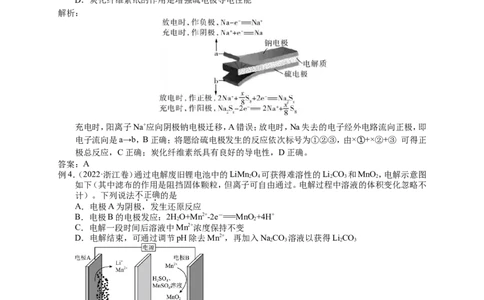
例1.(2023·全国甲卷)用可再生能源电还原CO 时,采用高浓度的K+ 抑制酸性电解液中的析氢反应
2
可提高多碳产物(乙烯、乙醇等)的生成率,装置如图所示。下列说法正确的是
A.析氢反应发生在IrO -Ti电极上
x
B.Cl-从Cu 电极迁移到IrO -Ti电极
x
C.阴极发生的反应有:2CO+12H++12e-===C H+4H O
2 2 4 2
D.每转移1mol 电子,阳极生成11.2L气体(标准状况)
解析:IrO -Ti 电极接电源正极,为阳极,发生失电子的氧化反应,故电极反应为2HO-4e-===4H+
x 2
+O ↑,A 错误;质子交换膜只允许H+ 通过,故左室H+ 从IrO -Ti 电极向Cu 电极迁移,B 错误;
2 x
Cu电极接电源负极,为阴极,发生得电子的还原反应,根据图中物质转化关系知CO 可发生反应
2
2CO+12H++12e-===C H+4H O,C正确;由A可知每转移1mol电子,阳极生成0.25mol即5.6L
2 2 4 2
(标准状况)O,D错误。
2
答案:C
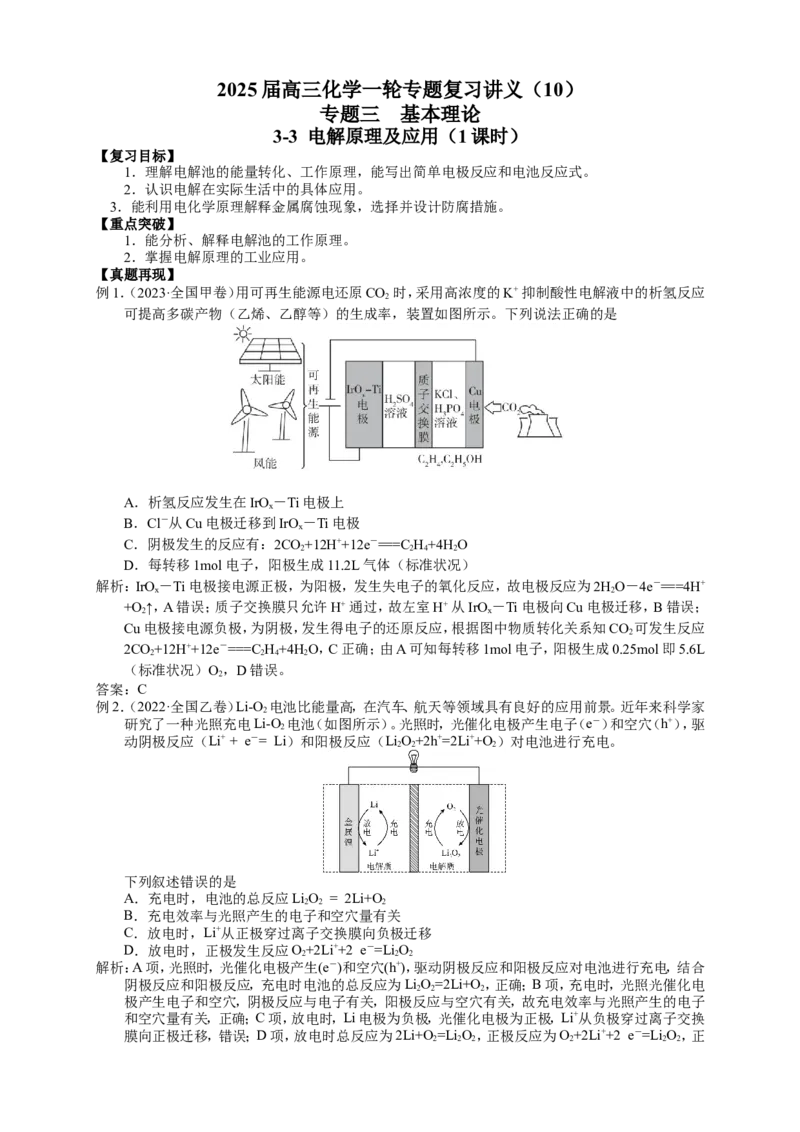
例2.(2022·全国乙卷)Li-O 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家
2
研究了一种光照充电Li-O 电池(如图所示)。光照时,光催化电极产生电子(e-)和空穴(h+),驱
2
动阴极反应(Li+ + e-= Li)和阳极反应(LiO+2h+=2Li++O )对电池进行充电。
2 2 2
下列叙述错误的是
A.充电时,电池的总反应LiO = 2Li+O
2 2 2
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应O+2Li++2 e-=Li O
2 2 2
解析:A项,光照时,光催化电极产生(e-)和空穴(h+),驱动阴极反应和阳极反应对电池进行充电,结合
阴极反应和阳极反应,充电时电池的总反应为LiO=2Li+O ,正确;B项,充电时,光照光催化电
2 2 2
极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率与光照产生的电子
和空穴量有关,正确;C项,放电时,Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换
膜向正极迁移,错误;D项,放电时总反应为2Li+O=Li O,正极反应为O+2Li++2 e-=Li O,正
2 2 2 2 2 2确。
答案:C
【知能整合】
根据课程标准,纵观近几年江苏及全国高考试卷,在高考中涉及电解方面重点考查:
(1)电解产物的判断及电池反应式的书写、离子移动方向的判定、电子、电流的流向等。
(2)以可充电电池为载体考查电极反应式的书写、离子移动方向的判定等。
(3)以金属的腐蚀与防护为背景进行考查。
高考中考查形式:电化学是氧化还原反应知识的应用和延伸,高考中一是以选择题的形式呈
现,二是在非选择题中电化学知识与工业生产、环境保护、新科技、新能源知识相结合进行
命制。
解决“电解原理”问题的方法思路:
1.电解池的电极反应及其放电顺序
(1)阳离子在阴极上的放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>…Fe2+>Zn2+>H+(水)> …
(2)阴离子在阳极上的放电顺序:S2->I->Br->Cl->OH->…
2.判断电解池阴、阳极的方法
(1)根据所连接的外加电源判断:与直流电源正极相连的为阳极,与直流电源负极相连的为阴
极。
(2)根据电子流动方向判断:电子从电源负极流向阴极,从阳极流向电源正极。
(3)根据电解池电解质溶液中离子的移动方向判断:阳离子向阴极移动,阴离子向阳极移动。
(4)根据电解池两极产物判断,一般情况下:
①阴极上的现象是:析出金属(质量增加)或有无色气体(H)放出;
2
②阳极上的现象是:有非金属单质生成,呈气态的有Cl、O 或电极质量减小(活性电极作
2 2
阳极)。
3.电解池中电极反应式的书写步骤
4.理解充、放电,准确剖析电化学原理
对于可充电电池,放电时为原电池,符合原电池工作原理,负极发生氧
根据原电池
化反应,正极发生还原反应;外电路中电子由负极流向正极,内电路中
原理分析
阳离子向正极移动,阴离子向负极移动。
可充电电池充电时为电解池,阳极发生氧化反应,阴极发生还原反应;
根据电解池
充电时电池的“+”极与外接直流电源的正极相连,电池的“-”极
原理分析
与外接直流电源的负极相连。
【技巧点拨】 可充电电池(二次电池)的工作原理如下图所示
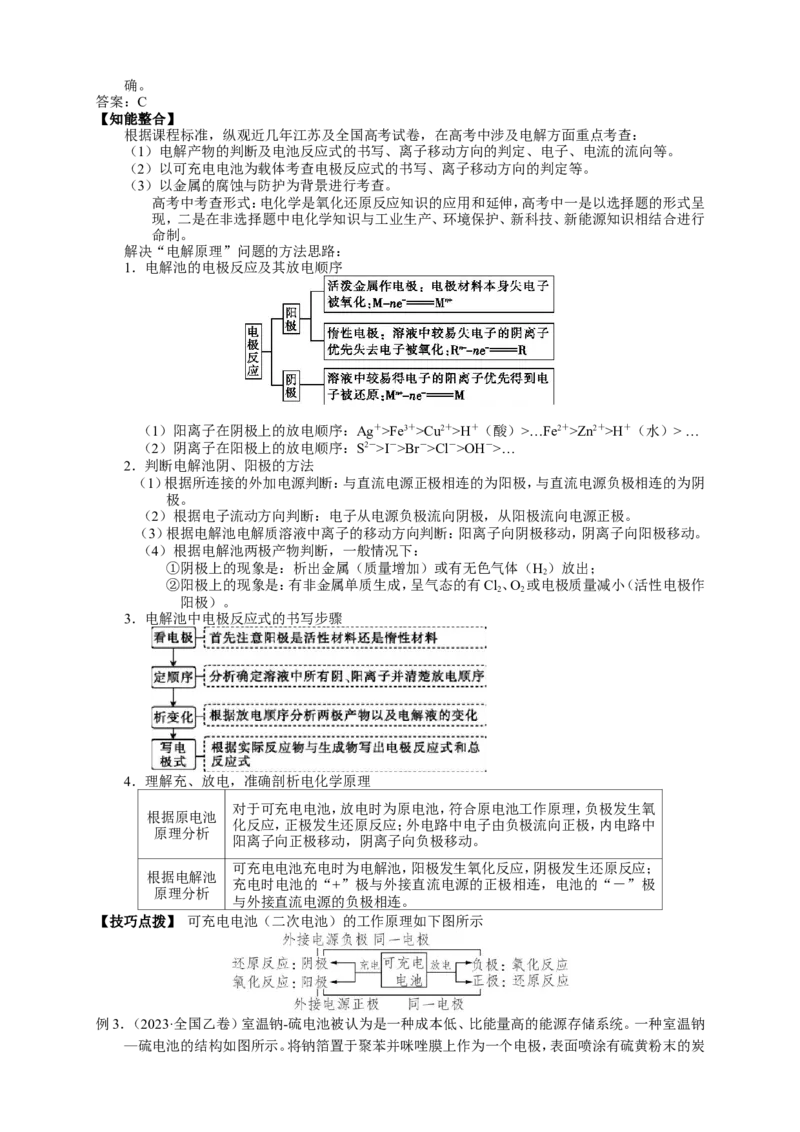
例3.(2023·全国乙卷)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠
—硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。 工作时,在硫电极发生反应:
S+e-→S,S+e-→S,2Na++S+2(1-)e-→NaS
8 2 x
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++S +2e-→NaS
8 2 x
D.炭化纤维素纸的作用是增强硫电极导电性能
解析:
充电时,阳离子Na+应向阴极钠电极迁移,A错误;放电时,Na失去的电子经外电路流向正极,即
电子流向是a→b,B正确;将题给硫电极发生的反应依次标号为①②③,由×①+×②+③ 可得正
极总反应,C正确;炭化纤维素纸具有良好的导电性,D正确。
答案:A
例4.(2022·浙江卷)通过电解废旧锂电池中的LiMn O 可获得难溶性的LiCO 和MnO ,电解示意图
2 4 2 3 2
如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不
计)。下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:2HO+Mn2+-2e-===MnO +4H+
2 2
C.电解一段时间后溶液中Mn2+浓度保持不变
D.电解结束,可通过调节pH除去Mn2+,再加入NaCO 溶液以获得LiCO
2 3 2 3
解析:A项,由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则电极B
2
为阳极,电极A为阴极,得电子,发生还原反应,正确;B项,由电解示意图可知,电极B上
Mn2+失电子转化为了MnO ,电极反应式为:2HO+Mn2+-2e-===MnO +4H+,正确;C项,电极A为
2 2 2
阴极, LiMn O 得电子,电极反应式为:2LiMn O+6e-+16H+===2Li++4Mn2++8H O,依据得失电子
2 4 2 4 2
守恒,电解池总反应为:2LiMn O+4H+===2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度
2 4 2 2
增大,错误;D项,电解池总反应为:2LiMn O+4H+===2Li++Mn2++3MnO+2H O,电解结束后,可
2 4 2 2
通过调节溶液pH将锰离子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,正确;
答案:C
小结:
【知能整合】1.根据介质判断析氢腐蚀和吸氧腐蚀:
正确判断“介质”溶液的酸碱性是分析析氢腐蚀和吸氧腐蚀的关键。潮湿的空气、酸性很弱或中
性溶液中发生吸氧腐蚀;NH Cl溶液、稀HSO 等酸性溶液中发生析氢腐蚀。
4 2 4
2.金属的防护
(1)电化学防护
①牺牲阳极的阴极保护法——原电池原理:正极为被保护的金属,负极为比被保护的金属活
泼的金属;
②外加电流的阴极保护法——电解原理:阴极为被保护的金属,阳极为惰性电极。
(2)改变金属的内部结构,如制成合金、不锈钢等。
(3)加防护层,如在金属表面喷油漆、涂油脂、电镀、喷镀或表面钝化等方法。
【体系再构】
【随堂反馈】
基础训练
1.将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情境中,下列有关说
法正确的是
A.阴极的电极反应式为Fe-2e-=Fe2+
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
2.我国科学家设计如图所示的电解池,实现了海水直接制备氢气技术的绿色化。
该装置工作时阳极无Cl 生成且KOH溶液的浓度不变,电解生成氢气的速率为x mol·h-1。下列
2
说法错误的是
A.b电极反应式为2HO+2e-==H ↑+2OH-
2 2
B.离子交换膜为阴离子交换膜
C.电解时海水中动能高的水分子可穿过PTFE膜
D.海水为电解池补水的速率为2x mol·h-1
3.电解法处理酸性含铬废水(主要含有Cr O)时,以铁板作阴、阳极,处理过程中存在反应Cr O+
2 2
6Fe2++14H+=2Cr3++6Fe3++7HO,最后Cr3+以Cr(OH) 形式除去,下列说法不正确的是
2 3
A.阳极反应为Fe-2e-===Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH) 沉淀生成
3
D.电路中每转移6mol电子,最多有1 mol Cr O被还原
2
4.一种锌钒超级电池的工作原理如图所示,电解质为(CHCOO) Zn溶液,电池总反应为Zn+
3 2
NaV (PO )===ZnNaV (PO )。下列说法正确的是
2 4 3 2 4 3
A.放电时,b电极为电池的负极
B.放电后,负极区c(Zn2+)增大
C.充电时,Zn2+向a电极移动
D.充电时,b电极的电极反应为:ZnNaV(PO )+2e-===Zn2++NaV (PO )
2 4 3 2 4 3
拓展训练
5.利用电解法将CO 转化为CH 的原理如图所示。下列说法正确的是
2 4
A.电解过程中化学能转化为电能
B.电极b上反应为CO + 8HCO −8e-== CH + 8CO+ 2HO
2 4 2
C.电解过程中, H+由a极区向b极区迁移D.电解时NaSO 溶液浓度保持不变
2 4
6.近年来电化学还原二氧化碳的课题吸引了大批研究者的关注,其中将双极膜应用于二氧化碳制备
甲醇过程中的电解原理如图所示。已知:双极膜由阳离子交换膜和阴离子交换膜构成,在直流电
场的作用下,双极膜间HO解离成H+和OH-,并向两极迁移。下列说法错误的是
2
A.a膜为阴离子交换膜
B.电解过程中KOH溶液的浓度逐渐降低
C.催化电极上的电极反应式为CO+6HCO+6e-===CH OH+6CO+HO
2 3 2
D.双极膜内每消耗18 g水,理论上石墨电极上产生11.2 L O(标准状况)
2
7.HPO 也可用电渗析法制备。“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子、
3 2
阴离子通过):
①写出阳极的电极反应式_________________________________________________。
②分析产品室可得到HPO 的原因___________________________________________。
3 2
③早期采用“三室电渗析法”制备HPO :将“四室电渗析法”中阳极室的稀硫酸用HPO 稀
3 2 3 2
溶液代替。并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室。其缺点是产品中
混有____杂质。该杂质产生的原因是_______________________________。
8.电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
(1)二氧化氯(ClO )为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
2
目前已开发出用电解法制取ClO 的新工艺如图所示。
2
①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO 。产生ClO 的电极应连接电
2 2
源的________(填“正极”或“负极”),对应的电极反应式为_____________________。
②a极区pH________(填“增大”“减小”或“不变”)。
③图中应使用________(填“阴”或“阳”)离子交换膜。
(2)电解KMnO 溶液制备KMnO 。工业上,通常以软锰矿(主要成分是MnO )与KOH的混合物
2 4 4 2
在铁坩埚(熔融池)中混合均匀,小火加热至熔融,即可得到绿色的KMnO ,化学方程式为
2 4
___________________________________________________________。
用镍片作阳极(镍不参与反应),铁板为阴极,电解KMnO 溶液可制备KMnO 。上述过程用
2 4 4
流程图表示如下:
则D的化学式为________;阳极的电极反应式为____________________________;阳离子
迁移方向是________________。
(3)电解硝酸工业的尾气NO可制备NH NO ,其工作原理如图所示:
4 3①阴极的电极反应式为__________________________________________________。
②将电解生成的HNO 全部转化为NH NO ,则通入的NH 与实际参加反应的NO的物质的
3 4 3 3
量之比至少为________________。
【随堂反馈】答案
1.C 2.D 3.D 4.C 5.C 6.D
7.①2HO-4e-===O ↑+4H+
2 2
②阳极室的H+穿过阳膜扩散至产品室,原料室的HPO穿过阴膜扩散至产品室,二者反应生成
2
HPO
3 2
③PO HPO或HPO 被氧化
2 3 2
8.(1)①正极 Cl--5e-+2HO===ClO ↑+4H+ ②增大 ③阳
2 2
(2)2MnO +4KOH+O===2KMnO +2HO KOH MnO-e-===MnO K+由阳离子交换膜左
2 2 2 4 2
侧向右侧迁移
(3)①NO+5e-+6H+===NH+HO ②1∶4
2
【课后作业】
1.中国科学院福建物质结构研究所谢奎课题组通过固体氧化物电解池, 实现了CH-CO 的电化学
4 2
重整制合成气,装置图如右。下列说法正确的是
A.a极为电源的负极
B.M极的电极反应式为CH-2e-+O2-===CO+2H
4 2
C.N极上发生氧化反应
D.电路中通过2 mol电子,阴、阳两极得到CO的质量共为28 g
2.一种利用双膜法电解回收CoCl 溶液中Co的装置如图所示,电解时
2
Co会析出在Co电极上。下列说法正确的是
A.a为电源的正极
B.电解后HSO 溶液的浓度减小
2 4
C.电解后盐酸溶液的浓度增大
D.常温时,Co电极的质量每增加5.9 g,Ti电极上会析出1.12 L气体(Co—59)
3.Li-CO 可充电电池在CO 固定及储能领域都存在着巨大的潜力,其结构如右图所示,主要由金属
2 2
锂负极、隔膜、含有醚或砜溶剂的非质子液态电解质和空气正极构成。电池的总反应为4Li +
3CO==2Li CO + C。下列有关说法正确的是
2 2 3
A.该电池也可用碳酸盐溶液作为电解质
B.氧化产物碳在正极上沉积,不利于电池放电
C.若有0.4mol电子转移,则在标况下消耗22.4L CO
2
D.充电时,阳极的电极反应为:2CO+ C-4e- ==3CO
2
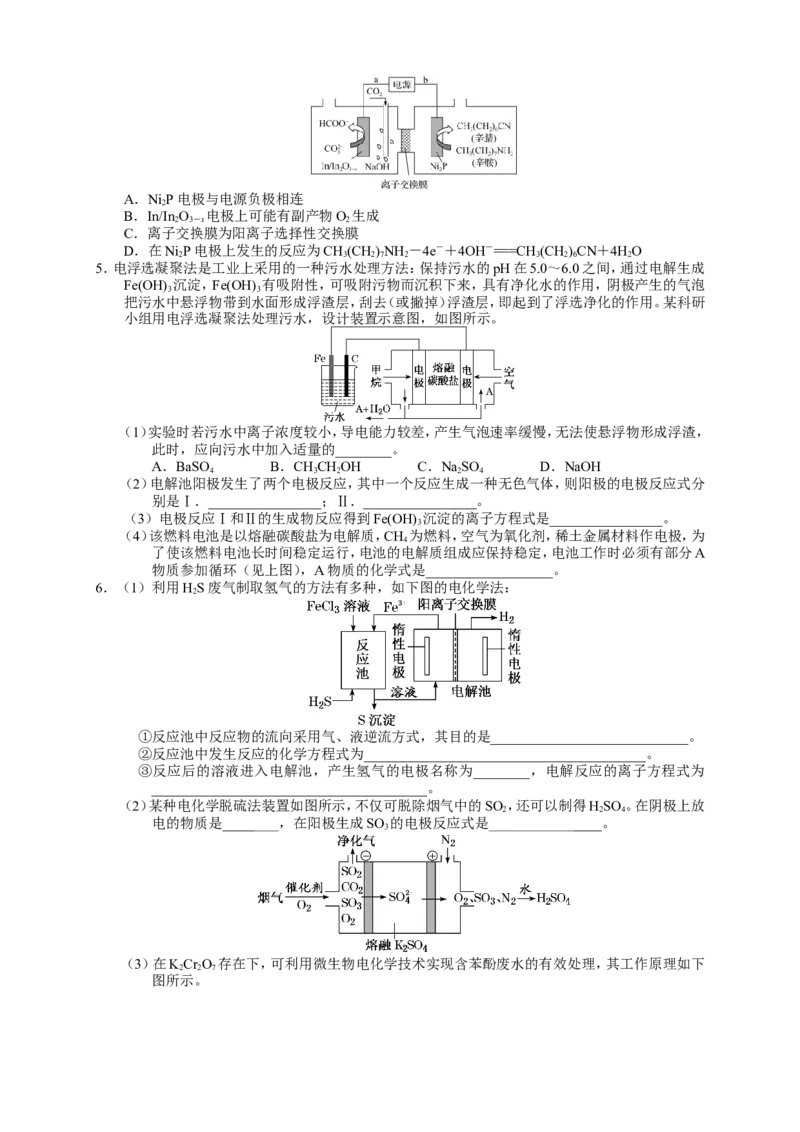
4.最近我国科学家以CO 与辛胺为原料实现了甲酸盐和辛腈的高
2
选择性合成,该合成的原理如图所示。下列说法正确的是A.Ni P电极与电源负极相连
2
B.In/In O 电极上可能有副产物O 生成
2 3-x 2
C.离子交换膜为阳离子选择性交换膜
D.在Ni P电极上发生的反应为CH(CH)NH -4e-+4OH-===CH (CH)CN+4HO
2 3 2 7 2 3 2 6 2
5.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成
Fe(OH) 沉淀,Fe(OH) 有吸附性,可吸附污物而沉积下来,具有净化水的作用,阴极产生的气泡
3 3
把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研
小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣,
此时,应向污水中加入适量的________。
A.BaSO B.CHCHOH C.NaSO D.NaOH
4 3 2 2 4
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分
别是Ⅰ.________________;Ⅱ.________________。
(3)电极反应Ⅰ和Ⅱ的生成物反应得到Fe(OH) 沉淀的离子方程式是________________。
3
(4)该燃料电池是以熔融碳酸盐为电解质,CH 为燃料,空气为氧化剂,稀土金属材料作电极,为
4
了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A
物质参加循环(见上图),A物质的化学式是__________________。
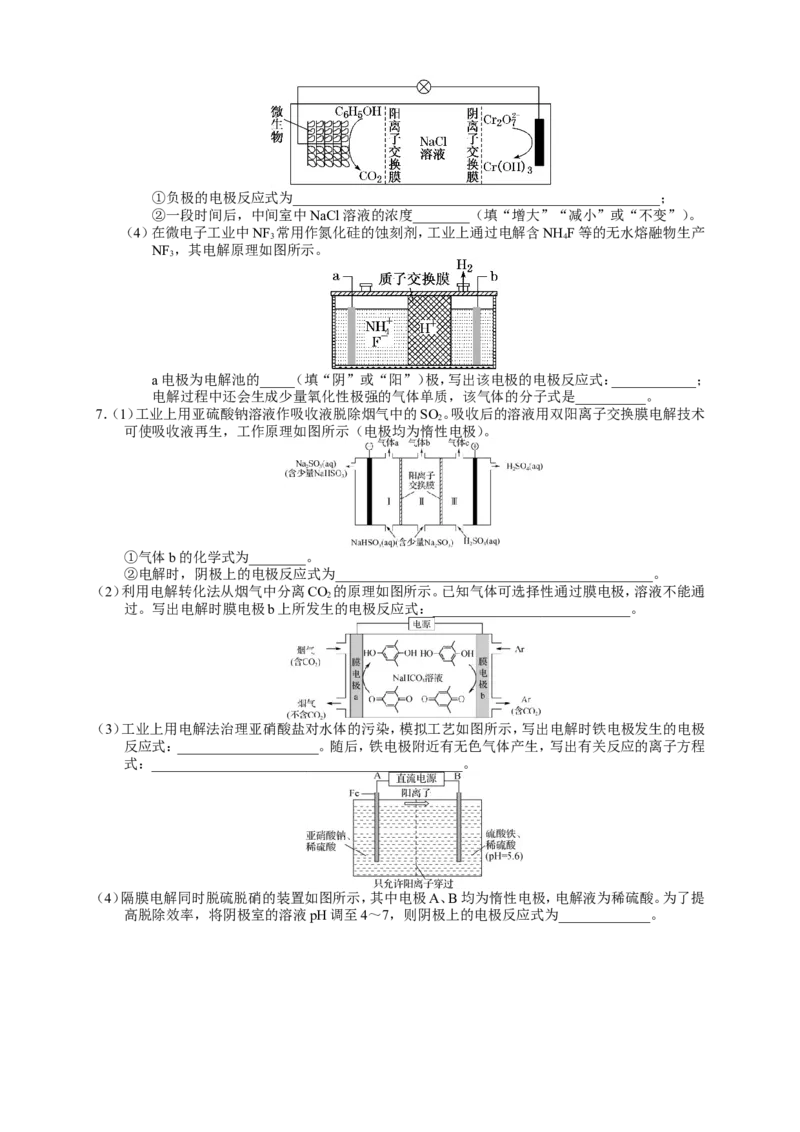
6.(1)利用HS废气制取氢气的方法有多种,如下图的电化学法:
2
①反应池中反应物的流向采用气、液逆流方式,其目的是____________________________。
②反应池中发生反应的化学方程式为________________________________________。
③反应后的溶液进入电解池,产生氢气的电极名称为________,电解反应的离子方程式为
_______________________________________。
(2)某种电化学脱硫法装置如图所示,不仅可脱除烟气中的SO ,还可以制得HSO 。在阴极上放
2 2 4
电的物质是________,在阳极生成SO 的电极反应式是________________。
3
(3)在KCr O 存在下,可利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如下
2 2 7
图所示。①负极的电极反应式为____________________________________________________;
②一段时间后,中间室中NaCl溶液的浓度________(填“增大”“减小”或“不变”)。
(4)在微电子工业中NF 常用作氮化硅的蚀刻剂,工业上通过电解含NH F等的无水熔融物生产
3 4
NF ,其电解原理如图所示。
3
a电极为电解池的_____(填“阴”或“阳”)极,写出该电极的电极反应式:____________;
电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是__________。
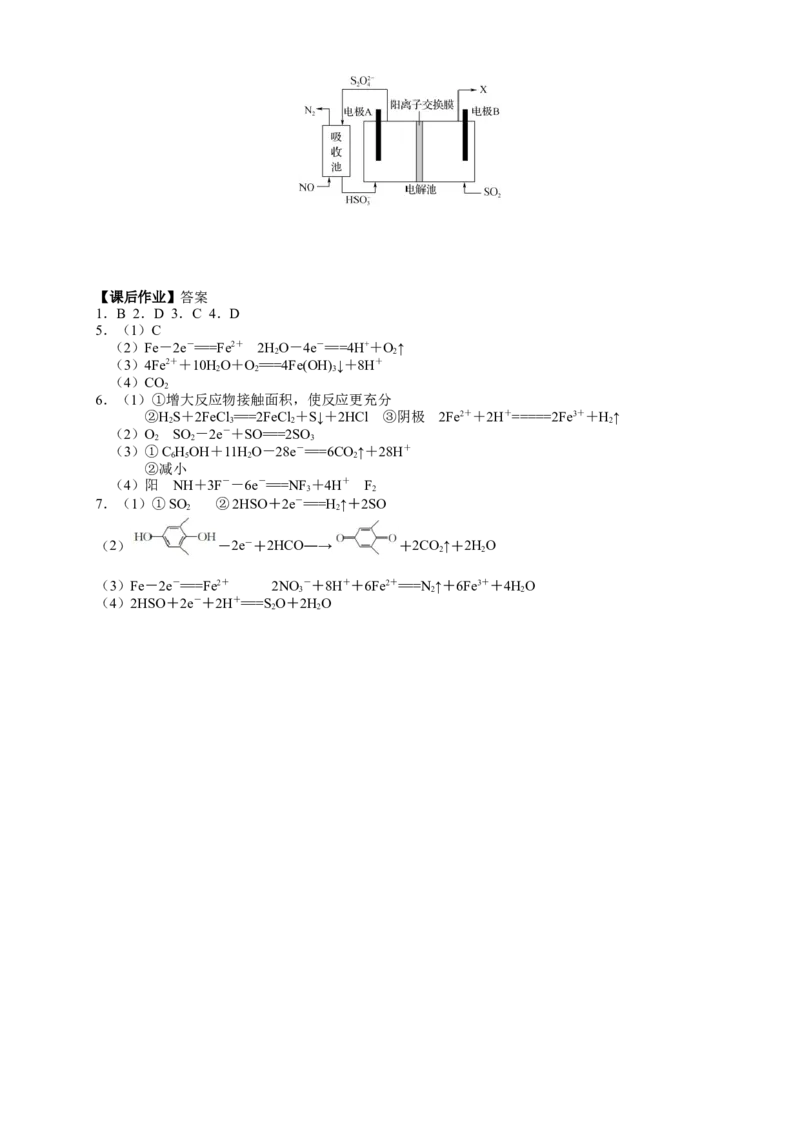
7.(1)工业上用亚硫酸钠溶液作吸收液脱除烟气中的SO 。吸收后的溶液用双阳离子交换膜电解技术
2
可使吸收液再生,工作原理如图所示(电极均为惰性电极)。
①气体b的化学式为________。
②电解时,阴极上的电极反应式为_____________________________________________。
(2)利用电解转化法从烟气中分离CO 的原理如图所示。已知气体可选择性通过膜电极,溶液不能通
2
过。写出电解时膜电极b上所发生的电极反应式:____________________________。
(3)工业上用电解法治理亚硝酸盐对水体的污染,模拟工艺如图所示,写出电解时铁电极发生的电极
反应式:____________________。随后,铁电极附近有无色气体产生,写出有关反应的离子方程
式:____________________________________________。
(4)隔膜电解同时脱硫脱硝的装置如图所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为了提
高脱除效率,将阴极室的溶液pH调至4~7,则阴极上的电极反应式为_____________。【课后作业】答案
1.B 2.D 3.C 4.D
5.(1)C
(2)Fe-2e-===Fe2+ 2HO-4e-===4H++O↑
2 2
(3)4Fe2++10HO+O===4Fe(OH) ↓+8H+
2 2 3
(4)CO
2
6.(1)①增大反应物接触面积,使反应更充分
②HS+2FeCl ===2FeCl +S↓+2HCl ③阴极 2Fe2++2H+=====2Fe3++H↑
2 3 2 2
(2)O SO -2e-+SO===2SO
2 2 3
(3)①C HOH+11HO-28e-===6CO ↑+28H+
6 5 2 2
②减小
(4)阳 NH+3F--6e-===NF+4H+ F
3 2
7.(1)①SO ②2HSO+2e-===H ↑+2SO
2 2
(2) -2e-+2HCO―→ +2CO↑+2HO
2 2
(3)Fe-2e-===Fe2+ 2NO -+8H++6Fe2+===N ↑+6Fe3++4HO
3 2 2
(4)2HSO+2e-+2H+===S O+2HO
2 2