文档内容
专练 15 金属及其化合物的制备流程
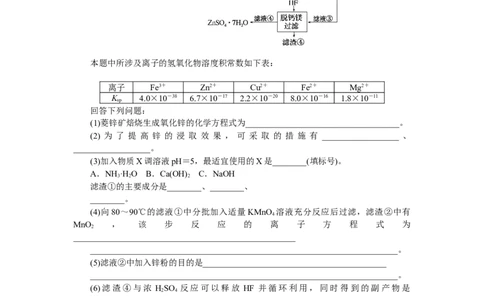
1.[2022·全国甲卷]硫酸锌(ZnSO)是制备各种含锌材料的原料,在防腐、电镀、医学
4
上有诸多应用。硫酸锌可由菱锌矿制备,菱锌矿的主要成分为 ZnCO ,杂质为SiO 以及
3 2
Ca、Mg、Fe、Cu等的化合物。其制备流程如下:
本题中所涉及离子的氢氧化物溶度积常数如下表:
离子 Fe3+ Zn2+ Cu2+ Fe2+ Mg2+
K 4.0×10-38 6.7×10-17 2.2×10-20 8.0×10-16 1.8×10-11
sp
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为____________________________________。
(2) 为 了 提 高 锌 的 浸 取 效 果 , 可 采 取 的 措 施 有 __________________ 、
__________________。
(3)加入物质X调溶液pH=5,最适宜使用的X是________(填标号)。
A.NH ·H O B.Ca(OH) C.NaOH
3 2 2
滤渣①的主要成分是________、________、
________。
(4)向80~90℃的滤液①中分批加入适量 KMnO 溶液充分反应后过滤,滤渣②中有
4
MnO , 该 步 反 应 的 离 子 方 程 式 为
2
____________________________________________________
________________________________________________________________________。
(5)滤液②中加入锌粉的目的是___________________________________________
________________________________________________________________________。
(6)滤渣④与浓 HSO 反应可以释放 HF 并循环利用,同时得到的副产物是
2 4
____________、______________。
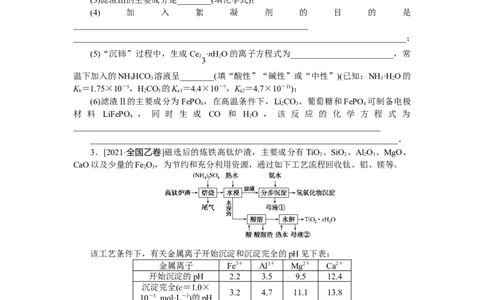
2.[2021·湖南卷]Ce (CO) 可用于催化剂载体及功能材料的制备。天然独居石中,铈
2 3 3
(Ce)主要以CePO 形式存在,还含有SiO、Al O、Fe O、CaF 等物质。以独居石为原料制
4 2 2 3 2 3 2
备Ce ·nHO的工艺流程如下:
2 2
3回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为________;
(2)为提高“水浸”效率,可采取的措施有________________________(至少写两条);
(3)滤渣Ⅲ的主要成分是________(填化学式);
(4) 加 入 絮 凝 剂 的 目 的 是
_______________________________________________________
______________________________________________________________________________;
(5)“沉铈”过程中,生成Ce ·nHO的离子方程式为________________________,常
2 2
3
温下加入的NH HCO 溶液呈________(填“酸性”“碱性”或“中性”)(已知:NH ·H O的
4 3 3 2
K =1.75×10-5,HCO 的K =4.4×10-7,K =4.7×10-11);
b 2 3 a1 a2
(6)滤渣Ⅱ的主要成分为FePO ,在高温条件下,LiCO 、葡萄糖和FePO 可制备电极
4 2 3 4
材 料 LiFePO , 同 时 生 成 CO 和 HO , 该 反 应 的 化 学 方 程 式 为
4 2
________________________________________________________________________
________________________________________________________________________。
3.[2021·全国乙卷]磁选后的炼铁高钛炉渣,主要成分有TiO 、SiO 、Al O 、MgO、
2 2 2 3
CaO以及少量的Fe O,为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
2 3
该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH见下表:
金属离子 Fe3+ Al3+ Mg2+ Ca2+
开始沉淀的pH 2.2 3.5 9.5 12.4
沉淀完全(c=1.0×
3.2 4.7 11.1 13.8
10-5 mol·L-1)的pH
回答下列问题:
(1)“焙烧”中,TiO 、SiO 几乎不发生反应,Al O 、MgO、CaO、Fe O 转化为相应
2 2 2 3 2 3
的 硫 酸 盐 。 写 出 Al O 转 化 为 NH Al(SO ) 的 化 学 方 程 式
2 3 4 4 2
________________________________________________________________________。
(2)“水浸”后“滤液”的pH约为 2.0,在“分步沉淀”时用氨水逐步调节 pH至
11.6 , 依 次 析 出 的 金 属 离 子 是
________________________________________________________________________。
(3)“母液①”中Mg2+浓度为________ mol·L-1。
(4)“水浸渣”在160 ℃“酸溶”,最适合的酸是________。“酸溶渣”的成分是
________、________。(5)“酸溶”后,将溶液适当稀释并加热,TiO2+水解析出TiO·xHO沉淀,该反应的离
2 2
子 方 程 式 是
________________________________________________________________________。
(6)将“母液①”和“母液②”混合,吸收尾气,经处理得________,循环利用。
4.[2021·福建卷]四钼酸铵是钼深加工的重要中间产品,具有广泛的用途。一种以钼精
矿(含MoS ,还有Cu、Fe的化合物及SiO 等)为原料制备四钼酸铵的工艺流程如下图所示。
2 2
回答下列问题:
(1)“焙烧”产生的气体用________吸收后可制取氮肥。
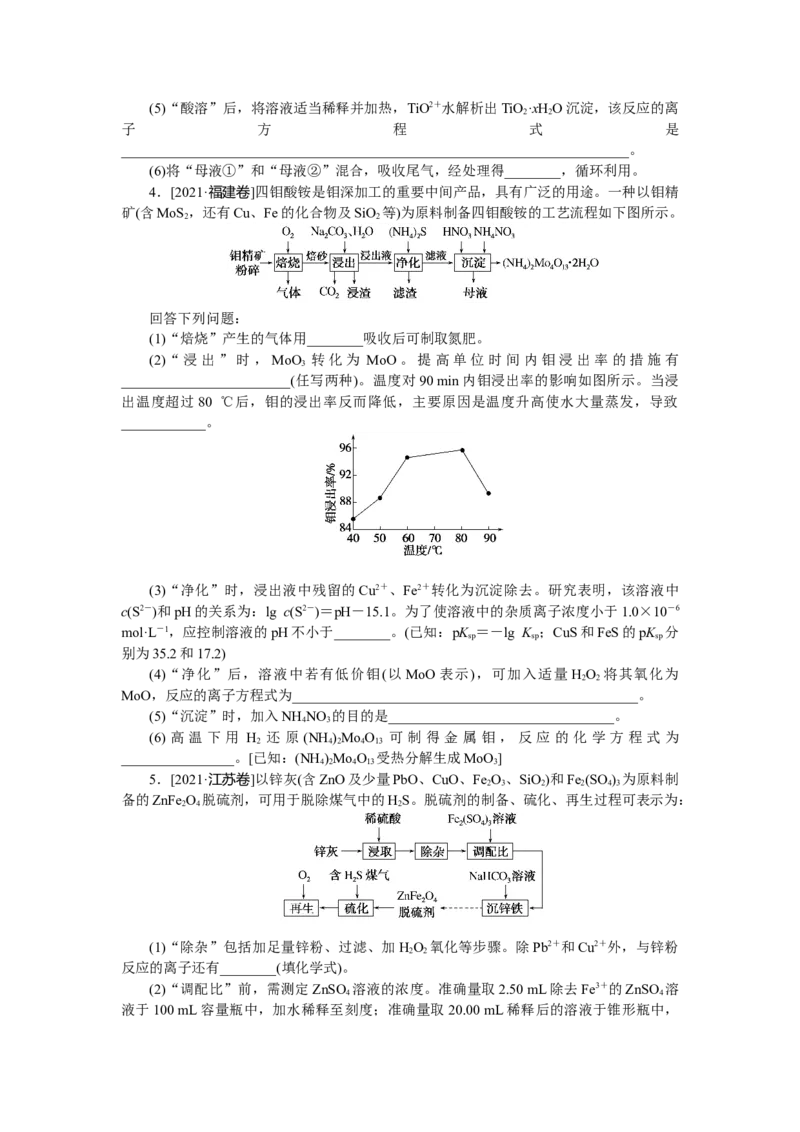
(2)“浸出”时,MoO 转化为 MoO。提高单位时间内钼浸出率的措施有
3
________________________(任写两种)。温度对90 min内钼浸出率的影响如图所示。当浸
出温度超过80 ℃后,钼的浸出率反而降低,主要原因是温度升高使水大量蒸发,导致
____________。
(3)“净化”时,浸出液中残留的Cu2+、Fe2+转化为沉淀除去。研究表明,该溶液中
c(S2-)和pH的关系为:lg c(S2-)=pH-15.1。为了使溶液中的杂质离子浓度小于1.0×10-6
mol·L-1,应控制溶液的pH不小于________。(已知:pK =-lg K ;CuS和FeS的pK 分
sp sp sp
别为35.2和17.2)
(4)“净化”后,溶液中若有低价钼(以 MoO 表示),可加入适量 HO 将其氧化为
2 2
MoO,反应的离子方程式为_________________________________________________。
(5)“沉淀”时,加入NH NO 的目的是________________________________。
4 3
(6) 高 温 下 用 H 还 原 (NH )MoO 可 制 得 金 属 钼 , 反 应 的 化 学 方 程 式 为
2 4 2 4 13
________________。[已知:(NH )MoO 受热分解生成MoO ]
4 2 4 13 3
5.[2021·江苏卷]以锌灰(含ZnO及少量PbO、CuO、Fe O、SiO)和Fe (SO ) 为原料制
2 3 2 2 4 3
备的ZnFe O 脱硫剂,可用于脱除煤气中的HS。脱硫剂的制备、硫化、再生过程可表示为:
2 4 2
(1)“除杂”包括加足量锌粉、过滤、加HO 氧化等步骤。除Pb2+和Cu2+外,与锌粉
2 2
反应的离子还有________(填化学式)。
(2)“调配比”前,需测定ZnSO 溶液的浓度。准确量取2.50 mL除去Fe3+的ZnSO 溶
4 4
液于100 mL容量瓶中,加水稀释至刻度;准确量取20.00 mL稀释后的溶液于锥形瓶中,滴加氨水调节溶液pH=10,用0.015 0 mol·L-1 EDTA(Na HY)溶液滴定至终点(滴定反应为
2 2
Zn2++Y4-===ZnY2-),平行滴定3次,平均消耗EDTA溶液25.00 mL。计算ZnSO 溶液的
4
物质的量浓度________(写出计算过程)。
(3)400 ℃时,将一定比例 H 、CO、CO 和 HS 的混合气体以一定流速通过装有
2 2 2
ZnFe O 脱硫剂的硫化反应器。
2 4
①硫化过程中,ZnFe O 与 H 、HS 反应生成 ZnS 和 FeS,其化学方程式为
2 4 2 2
________________________________。
②硫化一段时间后,出口处检测到COS。研究表明ZnS参与了HS与CO 生成COS的
2 2
反应,反应前后ZnS的质量不变,该反应过程可描述为________________。
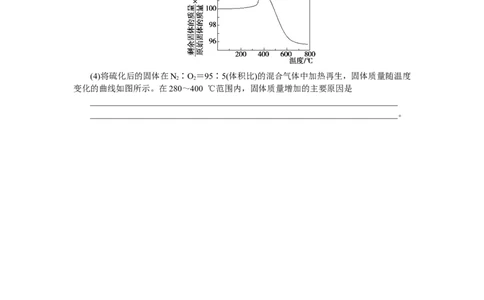
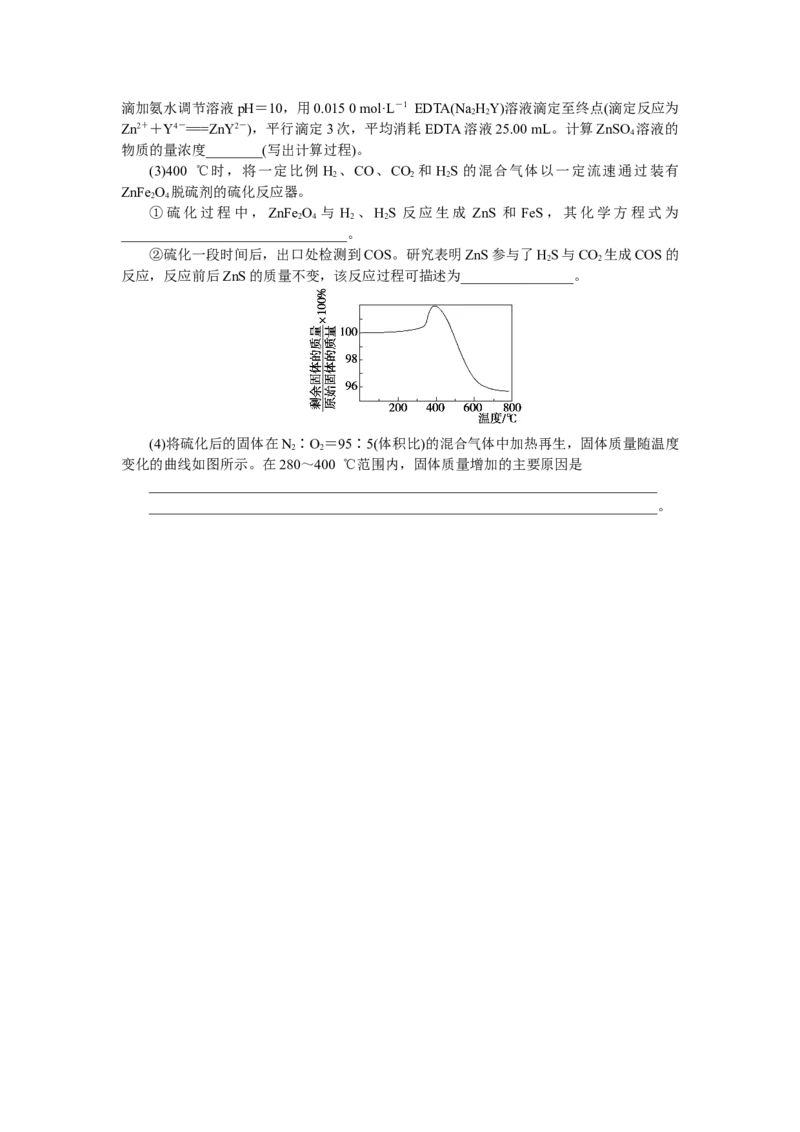
(4)将硫化后的固体在N∶O=95∶5(体积比)的混合气体中加热再生,固体质量随温度
2 2
变化的曲线如图所示。在280~400 ℃范围内,固体质量增加的主要原因是
________________________________________________________________________
________________________________________________________________________。