文档内容
专题 02 化学计量与化学计算
N
1.(2022·全国甲卷) A为阿伏加德罗常数的值,下列说法正确的是( )
25 ℃ 101 kPa 28L 2.5N
A. , 下, 氢气中质子的数目为 A
B.
2.0 L 1.0 molL1 AlCl 3溶液中,Al3
的数目为
2.0N
A
0.20mol CO 1.4N
C. 苯甲酸完全燃烧,生成 2的数目为 A
CuCl 6.4g 0.10N
D.电解熔融 2,阴极增重 ,外电路中通过电子的数目为 A
【答案】C
【解析】A.25℃、101kPa不是标准状况,不能用标况下的气体摩尔体积计算氢气的物质的量,故A错误;
B.Al3+在溶液中会发生水解生成Al(OH) ,因此2.0L 1.0 mol/L的AlCl 溶液中Al3+数目小于2.0N ,故B错
3 3 A
误;
C.苯甲酸燃烧的化学方程式为 ,1mol苯甲酸燃烧生成7molCO ,则
2
0.2mol苯甲酸完全燃烧生成1.4molCO,数目为1.4N ,故C正确;
2 A
D.电解熔融CuCl 时,阳极反应为 ,阴极反应为 ,阴极增加的重量为Cu的质
2
量,6.4gCu的物质的量为0.1mol,根据阴极反应可知,外电路中通过电子的物质的量为0.2mol,数目为
0.2N ,故D错误;
A
答案选C。
2.(2022·浙江卷) 为阿伏加德罗常数的值,下列说法正确的是
A. 中含有 个阳离子
B. 乙烷和丙烯的混合气体中所含碳氢键数为
C. 含有中子数为D. 和 于密闭容器中充分反应后, 分子总数为
【答案】C
【解析】A. 由钠离子和硫酸氢根离子构成,其中的阳离子只有钠离子, 的物质的量
为0.1mol,因此,其中只含有 个阳离子,A说法不正确;
B.没有指明气体的温度和压强,无法确定 乙烷和丙烯的混合气体的物质的量是多少,因此,无法确
定其中所含碳氢键的数目,B说法不正确;
C. 分子中有6个中子, 的物质的量为0.5mol,因此, 含有的中子数为 ,C说法正
确;
D. 和 发生反应生成 ,该反应是可逆反应,反应物不能完全转化为生成物,因此, 和
于密闭容器中充分反应后, 分子总数小于 ,D说法不正确。
综上所述,本题选C。
3.(2022·广东卷)我国科学家进行了如图所示的碳循环研究。下列说法正确的是
A.淀粉是多糖,在一定条件下能水解成葡萄糖
B.葡萄糖与果糖互为同分异构体,都属于烃类
C. 中含有 个电子
D. 被还原生成
【答案】A
【解析】A.淀粉是由葡萄糖分子聚合而成的多糖,在一定条件下水解可得到葡萄糖,故A正确;
B.葡萄糖与果糖的分子式均为C H O,结构不同,二者互为同分异构体,但含有O元素,不是烃类,属
6 12 6
于烃的衍生物,故B错误;C.一个CO分子含有14个电子,则1molCO中含有14×6.02×1023=8.428×1024个电子,故C错误;
D.未指明气体处于标况下,不能用标况下的气体摩尔体积计算其物质的量,故D错误;
答案选A。
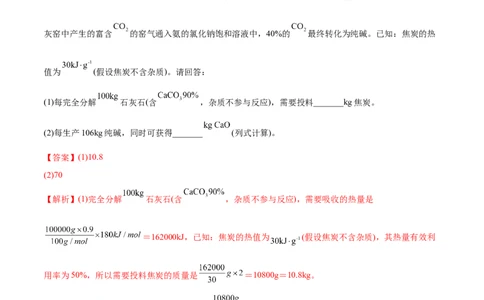
4.(2022·浙江卷)联合生产是化学综合利用资源的有效方法。煅烧石灰石反应:
,石灰石分解需要的能量由焦炭燃烧提供。将石灰石与焦
炭按一定比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成 ,其热量有效利用率为50%。石
灰窑中产生的富含 的窑气通入氨的氯化钠饱和溶液中,40%的 最终转化为纯碱。已知:焦炭的热
值为 (假设焦炭不含杂质)。请回答:
(1)每完全分解 石灰石(含 ,杂质不参与反应),需要投料_______kg焦炭。
(2)每生产106kg纯碱,同时可获得_______ (列式计算)。
【答案】(1)10.8
(2)70
【解析】(1)完全分解 石灰石(含 ,杂质不参与反应),需要吸收的热量是
=162000kJ,已知:焦炭的热值为 (假设焦炭不含杂质),其热量有效利
用率为50%,所以需要投料焦炭的质量是 =10800g=10.8kg。
(2)根据(1)中计算可知消耗焦炭的物质的量是 =900mol,参加反应的碳酸钙的物质的量是900mol,
这说明参加反应的碳酸钙和焦炭的物质的量之比为1:1,所以根据原子守恒可知生成氧化钙的质量是
=70kg。1.(2022·贵州遵义·二模)已知N 是阿伏加德罗常数的值,下列说法错误的是
A
A.1 mol C H 含有极性共价键的数目为12 N
5 12 A
B.标准状况下,4.48 L NO 中原子数为0.6 N
2 A
C.标准状况下,0.2 mol DO与HF的混合物中电子数有2 N
2 A
D.1 L 0.1 mol∙L−1的NaCO 溶液中Na+有0.2 N
2 3 A
【答案】B
【解析】A.C H 是烷烃,含有12个碳氢共价键,1 mol C H 含有极性共价键的数目为12 N ,故A正确;
5 12 5 12 A
B.标准状况下,NO 是非气态的物质,无法计算物质的量,故B错误;
2
C.DO、HF都有10个电子,标准状况下,0.2 mol DO与HF的混合物中电子数有2 N ,故C正确;
2 2 A
D.1 L 0.1 mol∙L−1的NaCO 溶液中NaCO 物质的量为0.1mol,含有Na+有0.2 N ,故D正确。
2 3 2 3 A
综上所述,答案为B。
2.(2022·贵州贵阳·一模)每年10月23日上午6:02到晚上6:02被誉为“摩尔日”。设N 为阿伏加德罗
A
常数的值,下列说法正确的是
A.1molO2-核外电子数为8N
A
B.常温时,22gTO中所含的中子数为12N
2 A
C.标准状况下,22.4LHF中含有HF分子数为N
A
D.1L0.1mol·L-1AlCl 溶液中含有A13+的数目为0.1N
3 A
【答案】B
【解析】A.O的质子数为8,O2-是O原子得到2个电子形成的,所以1个O2-的电子数为10,则1molO2-
核外电子数为10N ,故A错误;
A
B.22gTO的物质的量为1mol,1个TO中所含的中子数为12个,所以22gTO中所含的中子数为12N ,
2 2 2 A
故B正确;
C.标准状况下HF为液态,22.4LHF的物质的量不是1mol,所以22.4LHF中含有HF分子数不是N ,故C
A
错误;
D.Al3+在水溶液中会发生水解,所以1L0.1mol·L-1AlCl 溶液中含有A13+的数目小于0.1N ,故D错误;
3 A
故选B。
【点睛】TO中T为氚,1个T含有1个质子和2个中子,TO的相对分子质量为22。
2 2
3.(2022·四川自贡·三模)N 是阿伏加德罗常数的值。下列说法错误的是
A
A.18g重水(D O)中含有的质子数为9N
2 A
B.11.2L CH 和22.4L Cl (均为标准状况)在光照下充分反应后的分子数为1.5 N
4 2 AC.电解饱和食盐水时,若阴阳两极产生气体的总质量为73g,则转移电子数为N
A
NH+
D.1 L 0.1mol·L-1的NH C1溶液中通入适量氨气后呈中性,此时溶液中 4数目为0.1 N
4 A
【答案】C
m 18g
n(D O)= = =0.9mol
【解析】A.DO得到关系式为DO~(2+8)质子, 2 M (22+16)g/mol ,则n(质
2 2
子)=9mol,质子数为9N ,A项正确;
A
光照 光照
CH +Cl CH Cl+HCl CH Cl +Cl CH Cl +HCl
B.0.5molCH 与1molCl 反应为: 4 2 3 、 3 2 2 2 、
4 2
光照 光照
CH Cl +Cl CHCl +HCl CHCl +Cl CCl +HCl
2 2 2 3 和 3 2 4 ,以上几个反应为反应前后分子数不变的反应则
反应后为1.5mol,B项正确;
通电
(35.52+2)g 2mol
2NaCl+2H O 2NaOH+H +Cl =
C. 2 2 2 ,根据关系式为(Cl 2 +H 2 )~2e-得到 73g n(e-) ,则
n(e-)=2mol,所有电子转移数为2N ,C项错误;
A
c(NH+)+c(H+)=c(Cl-)+c(OH-)
D.NH Cl溶液中存在的电荷守恒式为 4 ,又溶液呈中性c(H+)=c(OH-)得
4
c(NH+)=c(Cl-)=0.1mol/L n(NH+)=0.1mol/L1L=0.1mol
4 ,则 4 数目为0.1N ,D项正确;
A
答案选C。
4.(2022·四川南充·三模)N 是阿伏加德罗常数的值,下列说法正确的是
A
A.22.4L (标准状况) HF中含有10N 个质子
A
B.2 mol SO 和1 molO 在一定条件下反应所得混合气体分子数为2N
2 2 A
C.将1 mol NH NO 溶于稀氨水中,若所得溶液呈中性,则溶液中NH4的数目为N
4 3 A
D.惰性电极电解CuSO 溶液,若电路中通过的电子数为N ,则阳极生成32 g铜
4 A
【答案】C
【解析】A.标准状况下,氟化氢为液态,无法计算22.4L氟化氢的物质的量和含有的质子数目,故A错
误;
B.二氧化硫和氧气的催化氧化反应为可逆反应,可逆反应不可能完全反应,所以2 mol SO 和1 molO 在
2 2一定条件下反应所得混合气体分子数大于2N ,故B错误;
A
C.由电荷守恒可知,将1 mol 硝酸铵溶于稀氨水中所得中性溶液中铵根离子浓度与硝酸根离子浓度相等,
则溶液中铵根离子的数目为1mol×N mol—1=N ,故C错误;
A A
D.惰性电极电解硫酸铜溶液,铜离子在阴极得到电子发生还原反应生成铜,故D错误;
故选C。
5.(2022·四川·遂宁中学三模)设N 为阿伏加德罗常数的值,下列说法不正确的是
A
A.100g质量分数为46%的乙醇水溶液中含有氧原子的数目为N
A
12gNaHSO MgSO
B. 4和 4的固体混合物中阳离子总数为0.1N
A
C.标准状况下,22.4 L CHCl中含有的共用电子对数目为4N
3 A
pH=7 NH+
D.常温下,1L0.1mol/L的氯化铵溶液中滴入氨水至 , 4数目为0.1N
A
【答案】A
【解析】A.乙醇溶液中除了乙醇外,水也含氧原子,100g46%的Z 醇溶液中,乙醇的质量为46g,物质
的量为1mol,故含1mol氧原子;水的质量为100g -46g=54g,物质的量为3mol,故含3mol氧原子,故此
溶液中含有的氧原子的物质的量共为4mol,个数为4N 个,选项A不正确;
A
B.NaHSO 固体是由钠离子和硫酸氢根离子组成,MgSO 固体是由镁离子和硫酸根离子组成,NaHSO 和
4 4 4
MgSO 的摩尔质量相同,均为120g/mol,12g固体混合物的物质的量为1 mol,则所含阳离子数为0.1N ,
4 A
选项B正确;
C.标准状况下,22.4 L CHCl为1mol,每个分子中含有4对共用电子对,故含有的共用电子对数目为
3
4N ,选项C正确;
A
pH=7 NH+ NH+
D.常温下,1L0.1mol/L的氯化铵溶液中滴入氨水至 ,c( 4)=c(Cl-), 4数目为0.1N ,选项D正
A
确;
答案选A。
6.(2022·四川德阳·二模)设N 为阿伏加德罗常数的值。下列有关叙述一定正确的是
A
A.4.6gC HO含C—H的数目为0.6N
2 6 A
B.1L0.1mol·L-1Fe (SO ) 溶液中含有的阳离子数目小于0.2N
2 4 3 A
C.在25℃、101kPa条件下,22.4LCO 中所含原子数目小于3N
2 A
D.500mL12mol·L-1浓盐酸与1.5molMnO 充分反应生成Cl 的分子数目为1.5N
2 2 A
【答案】C
【解析】A.4.6gC HO的物质的量为0.1mol,C HO为CHCHOH时C—H的数目为0.5N ,为CH-O-
2 6 2 6 3 2 A 3CH 时C—H的数目为0.6N ,故4.6gC HO含C—H的数目不一定为0.6N ,A错误;
3 A 2 6 A
B.1L0.1mol·L-1Fe (SO ) 溶液中Fe (SO ) 的物质的量为1L×0.1mol·L-1=0.1mol,铁离子发生水解反应Fe3+
2 4 3 2 4 3
+3H O Fe(OH) +3H+,显然水解导致阳离子数目增多,故1L0.1mol·L-1Fe (SO ) 溶液中含有的阳离子数目
2 3 2 4 3
大于0.2N ,B错误;
A
C.在25℃、101kPa条件下,气体摩尔体积V 大于22.4L/mol,22.4LCO 的物质的量小于1mol,所含原子
m 2
物质的量小于3mol,数目小于3N ,C正确;
A
Δ
D.MnO +4HCl(浓) MnCl +2H O+Cl ↑,500mL12mol·L-1浓盐酸中HCl的物质的量=6mol,随着反应的进
2 2 2 2
行浓盐酸变为稀盐酸,稀盐酸不发生上述反应,故生成Cl 的物质的量小于1.5mol,生成氯气分子数目小
2
于1.5N ,D错误;
A
答案选C。
7.(2022·四川南充·二模)N 是阿伏加德罗常数的值,下列说法正确的是
A
A.相同条件下,质量相等的CO和CO 它们所含的氧原子数目之比为11:7
2
B.1molLi N与过量水反应收集的气态氨分子数目为N
3 A
CO2-
C.NaCO 溶液中Na+和 3 个数比为2:1
2 3
D.标况下,1molN 和O 的混合气体总体积约为22.4L
2 2
【答案】D
【解析】A.设气体的质量为m,则质量相等的CO和CO 它们所含的氧原子物质的量之比为1
2
m
1
28 22 11
= =
m 28 14,所以氧原子数目之比为:11:14,故A错误;
2
44
Li N+3H O=3LiOH+NH
B.理论上,LiN与水反应 3 2 3 ,1molLi N与水反应收集的气态氨分子数目为N ,
3 3 A
NH+HO NHHO
但是水过量,氨气极易溶于水而且会发生 3 2 3 2 ,所以收集的气态氨分子数目小于N ,故B
A
错误;
CO2- CO2-
C.NaCO 中 3 是弱酸根离子在溶液中会水解,所以Na+和 3 个数比大于2:1,故C错误;
2 3
D.标况下,1mol任何气体的体积都约为22.4L,只要气体间不反应,不论是混合气体还是单一气体,故D正确;
故答案为:D。
N
8.(2022·河南新乡·三模)设 A为阿伏加德罗常数的值。下列说法正确的是
Al O 54gAl N
A.工业上电解 2 3制备 时,产生气体的分子数为3 A
220g PS N
B. 三硫化四磷( 4 3,如图所示)中含有的极性键的数目为6 A
N
C.标准状况下,22.4L氯气与足量烧碱溶液反应,转移的电子数为2 A
1molHOOCCH COOH N
D. 2 与足量乙醇在一定条件下反应,生成的酯基的数目为2 A
【答案】B
m 54g
n= = =2mol
【解析】A.电解 Al 2 O 3方程式为2 Al 2 O 3 通 == 电 4Al+3O 2 ↑,生成54gAl的物质的量为 M 27g/mol ,
N
则产生1.5mol O ,,产生气体的分子数为1.5 A,A错误;
2
m 220g
n= = =1mol
B.220g P
4
S
3
的物质的量为 M 220g/mol ,根据图可知含有的极性键P-S的数目为6 N A,B正确;
V 22.4L
n= = =1mol
C.标准状况下,22.4L氯气物质的量为 V 22.4L/mol ,氯气和NaOH反应生成NaClO和
m
N
NaCl,氯元素自身发生歧化反应,化合价从0价升到+1价,1mol氯气反应转移电子数为 A,C错误;
HOOCCH COOH N
D.酯化反应是可逆反应, 2 与乙醇反应不能完全转化,生成酯基的数目小于2 A,D错
误;
故选:B。9.(2022·河南新乡·二模)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.100g质量分数为46%的乙醇溶液中,含O—H键的数目为7N
A
B.0.1mol·L-1的CHCOONa溶液中,含CHCOO-的数目小于0.1N
3 3 A
C.含0.2molHSO 的浓硫酸与足量的镁反应,转移的电子数小于0.2N
2 4 A
D.常温下,1LpH=11的Ba(OH) 溶液中,含OH-的数目为0.002N
2 A
【答案】A
【解析】A.乙醇溶液溶质CHCHOH分子中有O—H键,每个乙醇分子中一个O—H键,溶剂HO分子
3 2 2
mC H OH 100g46%
中也有O—H键,每个水分子中两个O—H键;nC H OH= 2 5 = =1mol,O—H键数目
2 5 MC H OH 46g/mol
2 5
mH O 100g46g
1N ,nH O= 2 = =3mol,O—H键数目6N ,所以O—H键数目共7N ,描述正确,符合题
A 2 MH O 18g/mol A A
2
意;
B.溶液没有给出体积数据,无法计算微粒数目,描述错误,不符题意;
C.初始浓硫酸与镁发生反应,生成MgSO 、SO 和HO,随着硫酸浓度变稀,稀硫酸与镁反应生成
4 2 2
MgSO 和H;如果只发生第一个反应,每两个HSO 分子中有一个参与变价,转移电子2个(生成SO ),
4 2 2 4 2
但有第二个反应发生,每分子HSO 均参与变价,生成H,转移电子2个,故0.2mol H SO 中参与变价的
2 4 2 2 4
HSO 物质的量应大于0.1mol,转移电子总量应大于0.2N ,描述错误,不符题意;
2 4 A
D.pH=11的溶液中c(H+)=1×10-11mol/L,常温下Kw=1×10-14,故溶液中c(OH-)=1×10-3mol/L,1L溶液中
n(OH-)=1×10-3mol,描述错误,不符题意;
综上,本题选A。
10.(2022·河南信阳·二模)设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.常温常压下,1 mol Cl 溶于1.0 LHO中,溶液中Cl-、HClO、ClO-的个数之和为2N
2 2 A
B.46.0 gC HO完全燃烧,有5N 个C-H键断裂
2 6 A
C.56.0 gFe与1.0 mol Br 反应,转移电子数为2N
2 A
D.标准状况下,11.2 LNH 与11.2 L HF均含有5N 个质子
3 A
【答案】C
Cl-、HClO、ClO-
【解析】A.Cl 与HO的反应属于可逆反应,所得混合物中还含有Cl,溶液中 的个数之
2 2 2
和小于2N ,A错误;
A
C H O
B. 2 6 有乙醇和甲醚两种不同结构,若为纯净的乙醇,则含有C—H键的数目为5N ,正确,若为甲醚,
A
则含有C—H键的数目为6N ,B错误。
ABr
C.56.0 g Fe与1.0 mol 2反应时,铁过量,转移电子数取决于溴,则反应转移电子数为2N ,C正确;
A
D.标准状况下HF不是气体,故11.2 L HF不等于0.5 mol,无法计算所含质子数目,D错误;
故答案选C。
11.(2022·河南郑州·一模)N 代表阿佛加德罗常数的值。下列相关说法正确的是
A
A.100mL0.1mol·L-1FeCl 溶液中含有的Fe3+数目为0.01N
3 A
B.1L0.1mol·L-1NH HSO 溶液中阳离子的数目大于0.1N
4 4 A
C.标准状况下,11.2LH O 含有的非极性共价键数目为0.5N
2 2 A
D.常温下,将0.1molCl 溶于水中,充分反应后转移电子数目为0.1N
2 A
【答案】B
【解析】A.Fe3+易水解,100mL0.1mol·L-1FeCl 溶液中含有的Fe3+数目小于0.01N ,故A错误;
3 A
NH HSO =NH++H++SO2-
B.NH HSO 是强电解质,在水溶液电离方程式为 4 4 4 4 ,1L0.1mol·L-1NH HSO 溶液
4 4 4 4
中阳离子的数目大于0.1N ,故B正确;
A
C.标准状况下,HO 是液体,11.2LH O 的物质的量不是0.5mol,故C错误;
2 2 2 2
D.常温下,将0.1molCl 溶于水中,部分氯气和水反应生成盐酸和次氯酸,转移电子数目小于0.1N ,故
2 A
D错误;
选B。
12.(2022·河南新乡·一模)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.27g25Al中含有的中子数为12N
A
B.1molH O 在氧化还原反应中完全反应时转移的电子数一定为2N
2 2 A
C.标准状况下,11.2L由甲烷和乙烯组成的混合气体含极性键的数目为2N
A
D.1L0.5mol·L-1NaS溶液中含S2-和HS-的离子总数为0.5N
2 A
【答案】C
27g
1.08mol
【解析】A.27g25Al的物质的量n=25g/mol ,含有的中子数N=1.08mol(25-13) N
A
=12.96N 。故A错误;
A
催化剂
B.1molH O 在氧化还原反应中完全反应时转移的电子数不一定为2N ,如2HO 2HO + O 反
2 2 A 2 2 2 2 2
应中1molH O 转移1mol电子,故B错误;
2 2
C.甲烷和乙烯结构中,分别含有4条极性键,标准状况下,11.2L由甲烷和乙烯组成的混合气体为
0.5mol,含有极性键的数目N=0.5mol4 N =2N ,故C正确;
A AD.1L0.5mol·L-1NaS含有0.5molNa S,S2-能发生水解,生成HS-、HS,根据物料守恒,溶液中含S2-和
2 2 2
HS-、HS的粒子总数为0.5N ,故D错误;
2 A
故答案:C。
13.(2022·江西·二模)设N 为阿伏加德罗常数的值。下列有关叙述不正确的是
A
A.0.2 molC H 和C HO 的混合物完全燃烧,消耗O 分子数目为0.6N
2 4 3 4 2 2 A
B.含有FeI 的溶液中通入适量氯气,当有1 mol Fe2+被氧化时,反应中转移电子的数目至少为3 N
2 A
C.用电解粗铜的方法精炼铜,当电路中通过的电子数为0.5N 时,阳极应有16gCu转化为Cu2+
A
D.标准状况下,11.2LF 和C H 的混合物中含有电子的数目为9 N
2 2 6 A
【答案】C
【解析】A.C HO 可以改写为C H(CO),根据极限法结合烃完全燃烧耗氧公式可得0.2mol C H 或
3 4 2 2 4 2 2 4
0.2molC H(CO)完全燃烧消耗O 的物质的量均为0.2×(2+4/4)=0.6mol,A项正确;
2 4 2 2
B.因为还原性I->Fe2+,所以当1molFe2+被氧化时,根据FeI 的组成可知至少已有2molI-被氧化,转移电子的
2
物质的量至少为(1+1×2)=3mol,B项正确;
C.粗铜中还有活泼性比Cu强的Zn、Fe、Ni等杂质,在电解时优先于Cu失去电子成为阳离子,电路中通
过电子0.5N 包含这些杂质失去的电子,阳极粗铜中转化为Cu2+的Cu的质量小于16g,C项错误;
A
D.标准状况下11.2LF 含有电子0.5×9×2=9mol,11.2LC H 含有电子0.5×(6×2+6)=9mol,所以11.2L F 和
2 2 6 2
C H 的混合物中含有电子也为9mol,D项正确;
2 6
答案选C。
14.(2022·江西九江·二模)Cl O沸点3.8°C,熔点-116°C,是很好的氯化剂,利用HgO+2Cl =HgCl +ClO可
2 2 2 2
以制备高纯度的ClO。下列说法正确的是(N 为阿伏伽德罗常数)
2 A
A.标准状况下,2.24LCl O含有分子数为0.1N
2 A
B.0.2mol氯气与足量的HgO反应,转移电子数为0.2N
A
C.HgO与稀硝酸反应的离子方程式为O2-+2H+=H O
2
D.ClO与氢氧化钠溶液反应的离子方程式为ClO+2OH-=Cl-+ClO-+H O
2 2 2
【答案】B
【解析】A.标准状况下ClO为液体,无法计算2.24LCl O含有的分子数,A错误;
2 2
B.在反应HgO+2Cl =HgCl +ClO中,氯由0价变为HgCl 中-1价的氯和ClO中+1价氯,该反应转移2个
2 2 2 2 2
电子,故0.2mol氯气与足量的HgO反应,转移电子数为0.2N ,B正确;
A
C.HgO为金属氧化物,在写离子方程式的时候,正确的离子方程式为:HgO+2H+=H O+Hg2+,C错误;
2
D.在该反应中氧元素不守恒,D错误;
故选B。15.(2022·陕西西安·二模)N 是阿伏加德罗常数的值,下列说法正确的是
A
A.1mol重水比1mol水多2N 个中子
A
B.46g分子式为C HO的有机物,含极性键数目为7N
2 6 A
NH+
C.1L1mol/L溴化铵水溶液中 4与H+数目之和为N
A
D.常温下,1molCl 与足量水反应转移的电子数目为N
2 A
【答案】A
2H O 1H O
【解析】A.重水、水的化学式分别为1 2 、1 2 ,二者分子中的中子数相差2,则1mol重水比1mol水
多2N 个中子,A正确;
A
B.46g分子式为C HO的有机物,其物质的量为1mol,若其为CHOCH ,则含极性键数目为8N ,B不
2 6 3 3 A
正确;
NH+
C.1L1mol/L溴化铵水溶液中,根据电荷守恒:c( 4)+c(H+)=c(Br-)+c(OH-),由于c(Br-)=1mol/L,
NH+ NH+
c(OH-)>0,故c( 4)+c(H+)>1mol/L,所以 4与H+的数目之和大于N ,C不正确;
A
D.常温下,Cl 与水的反应为可逆反应,所以1molCl 与足量水反应转移的电子数目小于N ,D不正确;
2 2 A
故选A。
16.(2022·陕西汉中·二模)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,2.24L的氯仿中含有的氢原子数为0.1N
A
B.lmolSiO 晶体中所含Si-O键数目为2N
2 A
C.2.4g镁条在足量的N 和O 混合气体中完全燃烧转移电子总数为0.2N
2 2 A
D.0.1mol·L-1NaSO 溶液中,含硫元素的粒子数目之和为0.1N
2 3 A
【答案】C
【解析】A.标准状况下氯仿不是气态物质,不能根据体积计算其物质的量,故A错误;
B.lmolSiO 晶体中所含Si-O键数目为4N ,故B错误;
2 A
C.镁条在足量的N 和O 混合气体中完全燃烧镁失电子转变成镁离子,1molMg失2mol电子,则2.4g镁
2 2
为0.1mol,转移电子数为0.2N ,故C正确;
A
D.溶液体积未知不能确定溶质的物质的量,故D错误;
故选:C。
17.(2022·陕西宝鸡·三模)N 为阿伏加德罗常数的值,下列说法正确的是
A
A.常温下,pH=13的NaOH溶液中含有OH-的数目为0.1N
AB.在1L0.1mol·L-1CHCOONa溶液中,阴离子的总数等于0.1N
3 A
C.标准状况下,2.24LCH Cl 含有的C-Cl键数目为0.2N
2 2 A
D.20gDO中含有的质子中子和电子的数目均为10N
2 A
【答案】D
【解析】A.缺溶液的体积,无法计算pH=13的氢氧化钠溶液中含有氢氧根离子的数目,故A错误;
B.根据电荷守恒,在醋酸钠溶液中有:c(CHCOO-)+c(OH-)=c(H+)+c(Na+),由c(Na+)=1mol/L可知c(H+)
3
+c(Na+)>1mol/L,所以1L0.1mol·L-1醋酸钠溶液中N(H+)+N(Na+)大于0.1mol·L-1×1L×N mol—1=0.1N ,阴离子
A A
的总数N(CH COO-)+N(OH-)>0.1N ,故B错误;
3 A
C.标准状况下,二氯甲烷为液态,则无法计算2.24L二氯甲烷的物质的量和含有的碳氯键的数目,故C
错误;
20g
D.重水的质子数和中子数都为10,所以20g重水中含有的质子中子和电子的数目均为20g/mol ×10×N mol
A
—1=10N ,故D正确;
A
故选D。
18.(2022·陕西榆林·三模)设N 为阿伏加德罗常数的值。下列说法正确的是
A
A.1mol葡萄糖中含有的羟基的数目为6N
A
B.25℃、101kPa下,22.4L稀有气体混合物中含有的原子总数为N
A
CH H O(g)
C. 4和 2 在高温下制备1mol蓝氢(H )时,转移的电子数为2N
2 A
0.1molL-1NH H PO H PO HPO2 PO3
D.1L 4 2 4溶液中含有的 2 4、 4 、 4 总数为0.1N
A
【答案】C
【解析】A.葡萄糖分子为五羟基醛,则1mol葡萄糖中含有的羟基的数目为1mol×5×N mol—1=5N ,故A
A A
错误;
B.25℃、101kPa下,气体摩尔体积大于22.4L/mol,22.4L稀有气体混合物中含有的原子总数小于
22.4L
×1×N mol—1=N ,故B错误;
22.4L/mol A A
C.由化合价变化可知,甲烷和水蒸气在高温下反应生成1mol氢气时反应转移2mol电子,则转移的电子
数为1mol×2×N mol—1=2N ,故C正确;
A A
D.由物料守恒可知,1L0.1mol/L磷酸二氢铵中磷酸、磷酸二氢根、磷酸氢根、磷酸根的总数为0.1mol/L
×1L×N mol—1=0.1N ,故D错误;
A A故选C。
19.(2022·吉林长春·三模)设N 为阿伏加德罗常数的值,下列有关叙述正确的是
A
A.室温下pH =12的NaCO 溶液中,由水电离出的OH-数目为0.01N
2 3 A
B.1.0 L1.0 mol/L的NaAlO 溶液中含氧原子数为2N
2 A
C.0.2 mol SO 与0.2 mol O 在一定条件下充分反应生成SO 分子数为0.2N
2 2 3 A
D.3.9gNa O 固体中含有阴阳离子的总数目为0.15N
2 2 A
【答案】D
【解析】A.室温下pH =12的NaCO 溶液中,由于题干未告知溶液的体积,则无法计算由水电离出的OH-
2 3
数目,A错误;
B.由于溶剂水中也含有O原子,则无法计算1.0 L1.0 mol/L的NaAlO 溶液中含氧原子数,B错误;
2
催化 剂
C.由于2SO 2 +O 2 Δ 2SO 3 是一个可逆反应,则0.2 mol SO 2 与0.2 mol O 2 在一定条件下充分反应生成
SO 分子数小于0.2N ,C错误;
3 A
3.9g
×3×N mol-1
D.已知NaO 是由Na+和 O2- 组成的,则3.9gNa O 固体中含有阴阳离子的总数目为78g•mol-1 A
2 2 2 2 2
=0.15N ,D正确;
A
故答案为:D。
20.(2022·吉林白山·一模)用N 表示阿伏加德罗常数的值。溴蒸气与氨气相遇产生“白烟",化学方程式为
A
8NH +3Br =N +6NHBr。下列说法正确的是
3 2 2 4
A.生成14gN 时,反应中还原剂的分子数目为4N
2 A
B.标准状况下,11.2LBr 参与反应时转移的电子数为N
2 A
C.0.5mol·L-1的NH Br溶液中含有Br-的数目为0.5N
4 A
D.当生成29.4gNHBr时,消耗NH 分子的数目为0.4N
4 3 A
【答案】D
【解析】A.14gN 即0.5molN,生成0.5molN 时,根据N元素守恒,被氧化的氨气的物质的量是1mol,
2 2 2
反应中还原剂的分子数目为N ,故A错误;
A
B.标准状况下,Br 是液体,11.2LBr 的物质的量不是0.5mol,故B错误;
2 2
C.没有明确溶液体积,不能计算0.5mol·L-1的NH Br溶液中含有Br-的数目,故C错误;
4
29.4g
=0.3mol
D.29.4gNHBr的物质的量是98g/mol ,当生成0.3molNH Br时,消耗NH 分子的数目为0.4N ,
4 4 3 A
故D正确;选D。
21.(2022·山西太原·一模)设N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.5.6g Fe与足量的S反应转移的电子数为0.3N
A
B.标准状况下,1.12L苯含有C-H键的数目为0.3N
A
2
C.1L 0.1mol·L-1 KCr O 酸性溶液(pH=4)中,Cr O7 的数目为0.1N
2 2 7 2 A
D.11.2L CH 和22.4L Cl (均为标准状况)在光照条件下充分反应后,分子总数为1.5N
4 2 A
【答案】D
【解析】A.5.6g Fe的物质的量为0.1mol,S的氧化性较弱,产物为FeS,所以转移的电子为0.2N ,A错
A
误;
B.标况下苯不是气体,不能用V =22.4L/mol计算其物质的量,B错误;
m
2 2
C.经计算,溶液中KCr O 的物质的量为0.1mol,但溶液中存在反应Cr O7 +H O 2CrO4 +2H+,所以
2 2 7 2 2
2
Cr O7 的数目小于0.1N ,C错误;
2 A
D.标准状况下,11.2L CH 的物质的量为0.5mol,22.4L Cl 为1mol,CH 与Cl 在光照条件下发生取代反
4 2 4 2
应时,反应前后分子数目不变,所以充分反应后,分子总数为1.5N ,D正确;
A
综上所述,答案为D。
22.(2022·山西吕梁·一模)设N 为阿伏加德罗常数的值,下列叙述正确的是
A
A.常温下,5.4 g铝片投入足量的浓硫酸中,铝失去的电子数为0.3N
A
B.12 g NaHSO 晶体中阴离子所带电荷数为0.2N
4 A
C.0.1 mol FeI 与0.1 mol Cl 反应时转移电子的数日为0.3N
2 2 A
D.常温常压下,2.8 g CO和C H 的混合气体中含有的分子数目为0.1N
2 4 A
【答案】D
【解析】A.常温下,铝片遇浓硫酸会发生钝化而不能进一步发生反应,因此不能计算微粒数目,A错误;
HSO
B.12 g NaHSO 的物质的量是0.1 mol,由于在晶体中含有阳离子是Na+,阴离子是 4,所以0.1 mol阴
4
离子所带电荷数为 0.1N ,B错误;
A
C.由于还原性:I->Fe2+,所以0.1 mol FeI 与 0.1 mol Cl 反应时,生成FeCl 、I,反应过程中转移电子
2 2 2 2
的数目为0.2N ,C错误;
A
2.8g
n= =0.1mol
D.CO和C H 相对分子质量都是28,故2.8 g混合物中含有分子的物质的量为
28g×mol-1
,故
2 4混合气体中含有的分子个数约为0.1N ,D正确;
A
故合理选项是D。
23.(2022·甘肃兰州·一模)已知N 为阿伏加德罗常数的值,下列说法正确的是
A
A.18gH18O中所含中子数为10N
2 A
B.25°C时,1LpH=2的HC O 溶液中含H+的数目为0.02N
2 2 4 A
C.标准状况下,5.6LCO 与足量NaO 反应转移的电子数为0.5N
2 2 2 A
D.8.4g丙烯和环丙烷的混合物中含有共用电子对的数目为1.8N
A
【答案】D
18g
10N 9N
【解析】A.H18O含有10个中子,18gH18O中所含中子数为20g/mol A A ,故A错误;
2 2
B.25°C时,1LpH=2的HC O 溶液中含H+的数目为1L×0.01mol/L×N =0.01N ,故B错误;
2 2 4 A A
2CO 2Na O 2Na CO O
C.标准状况下,5.6LCO 的物质的量为0.25mol,与足量NaO 发生反应 2 2 2 2 3 2 ,
2 2 2
过氧化钠中氧元素化合价由-1降低为-2、由-1升高为0,转移的电子数为0.25N ,故C错误;
A
D.丙烯和环丙烷分子中都含有9个共用电子对,丙烯和环丙烷的摩尔质量都是42g/mol,8.4g丙烯和环丙
8.4g
9N 1.8N
烷的混合物中含有共用电子对的数目为42g/mol A A ,故D正确;
选D。
24.(2022·浙江台州·二模)已知某加碘盐(含 的食盐)中含碘量为 。现有1000kg该
加碘盐,计算:
(1)该加碘食盐中至少含碘_______mol
(2)若用 与 反应制 ,标准状况至少需要消耗 _______L(写出计算过程)。
【答案】(1)0.2
(2)用 与 反应制 反应为: ,根据 可知,则需
要消耗标准状况下 的物质的量为0.2mol×3=0.6mol,体积为: 。
【解析】(1)已知某加碘盐(含 的食盐)中含碘量为 ;则1000kg加碘食盐中至少含碘25.4g,I的物质的量为 ;
(2)用 与 反应制 反应为: ,根据 可知,则需
要消耗标准状况下 的物质的量为0.2mol×3=0.6mol,体积为: 。
25.(2022·浙江绍兴·二模)把密度为1.6g/ cm3的液态SCl 10mL溶于石油醚(一种溶剂), 得到100mL溶液,
2 2
把它慢慢加入50 mL3.2mol/L的SO 水溶液中,振荡使之充分反应,当加入的SCl 溶液为67.5mL时,恰
2 2 2
好反应完全。生成物用含0.32mol KOH的KOH溶液中和后,恰好完全转化为KCl和一种二元含氧酸的钾
盐晶体。请计算
(1)参与反应的n(S Cl): n(SO )=1:_______
2 2 2
(2)确定二元含氧酸的化学式_______。
【答案】(1)2
(2)H SO
2 4 6
【解析】(1) , ,则参与反应的
n(S Cl):n(SO )=1:2,故答案为:2;
2 2 2
(2)根据题意,反应过程中Cl、H、O元素的化合价不变,所以该反应为归中反应,设反应后硫元素化合价
为x,依据得失电子守恒有:2(x-1)=2(4-x),解得x= ,由此推断二元含氧酸的化学式为HSO,故答案
2 4 6
为:HSO。
2 4 6