文档内容
专题05 化学能与电能的转化
(本卷共19小题,满分100分,考试用时75分钟)
可能用到的相对原子质量:H 1 Li 7 B 11 C 12 N 14 O 16 Na 23 Mg 24 Al 27 S 32 Cl 35.5
第I卷 (选择题共50分)
一、选择题:本题共10个小题,每小题3分,共30分,在每小题给出的四个选项中,只有一项是符
合题目要求的。
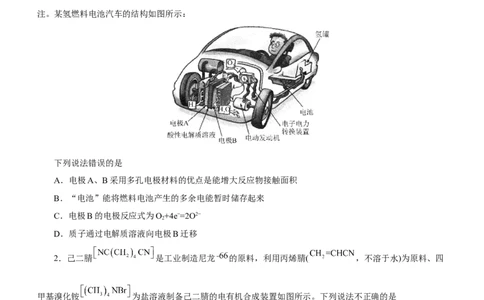
1.氢燃料电池汽车由于具备五大优势:零排放、零污染、无噪音、补充燃料快、续航能力强,而备受关
注。某氢燃料电池汽车的结构如图所示:
下列说法错误的是
A.电极A、B采用多孔电极材料的优点是能增大反应物接触面积
B.“电池”能将燃料电池产生的多余电能暂时储存起来
C.电极B的电极反应式为O+4e−=2O2−
2
D.质子通过电解质溶液向电极B迁移
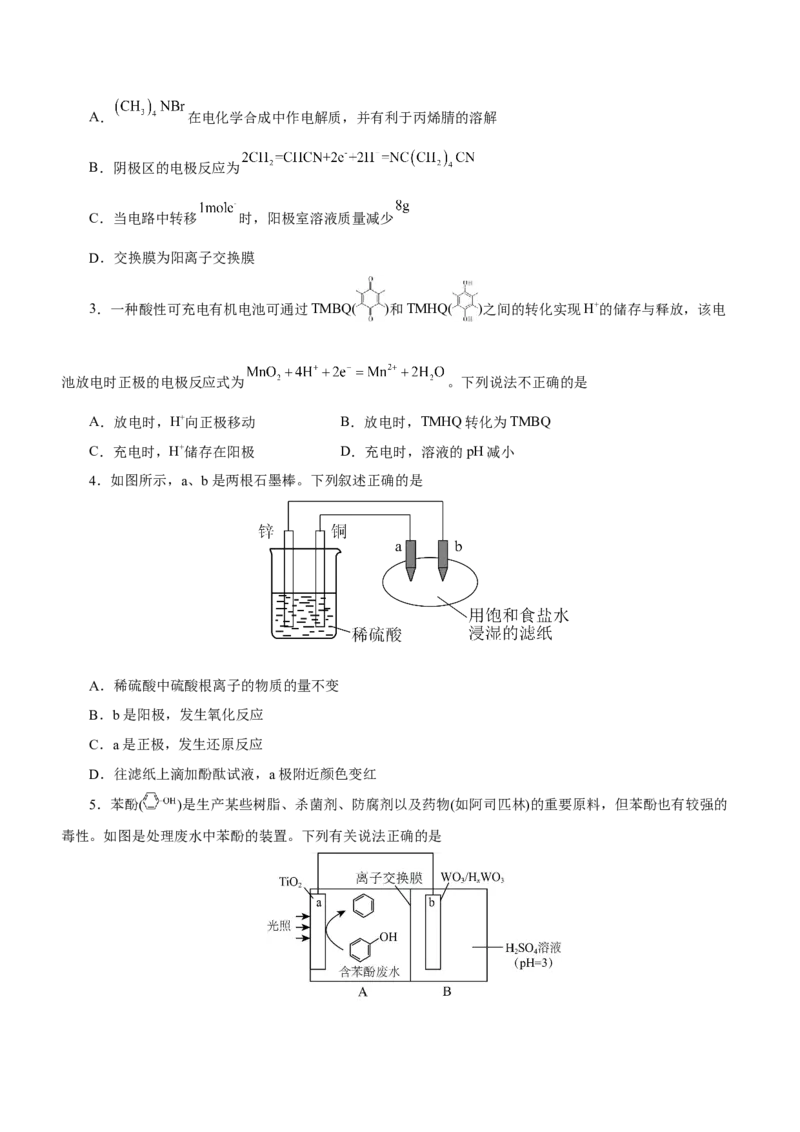
2.己二腈 是工业制造尼龙 的原料,利用丙烯腈( ,不溶于水)为原料、四
甲基溴化铵 为盐溶液制备己二腈的电有机合成装置如图所示。下列说法不正确的是A. 在电化学合成中作电解质,并有利于丙烯腈的溶解
B.阴极区的电极反应为
C.当电路中转移 时,阳极室溶液质量减少
D.交换膜为阳离子交换膜
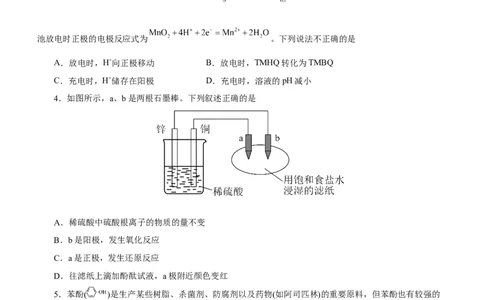
3.一种酸性可充电有机电池可通过TMBQ( )和TMHQ( )之间的转化实现H+的储存与释放,该电
池放电时正极的电极反应式为 。下列说法不正确的是
A.放电时,H+向正极移动 B.放电时,TMHQ转化为TMBQ
C.充电时,H+储存在阳极 D.充电时,溶液的pH减小
4.如图所示,a、b是两根石墨棒。下列叙述正确的是
A.稀硫酸中硫酸根离子的物质的量不变
B.b是阳极,发生氧化反应
C.a是正极,发生还原反应
D.往滤纸上滴加酚酞试液,a极附近颜色变红
5.苯酚( )是生产某些树脂、杀菌剂、防腐剂以及药物(如阿司匹林)的重要原料,但苯酚也有较强的
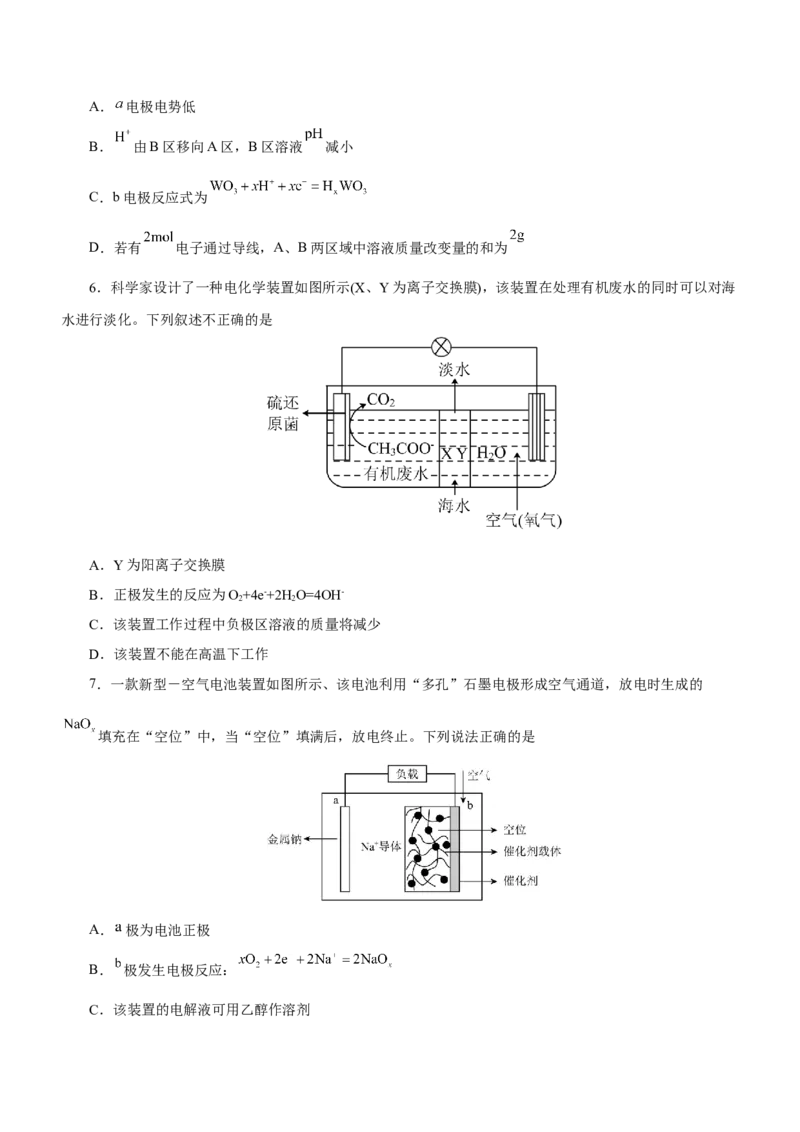
毒性。如图是处理废水中苯酚的装置。下列有关说法正确的是A. 电极电势低
B. 由B区移向A区,B区溶液 减小
C.b电极反应式为
D.若有 电子通过导线,A、B两区域中溶液质量改变量的和为
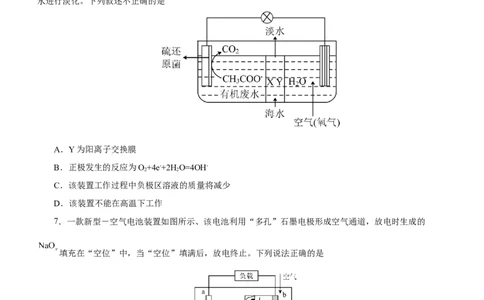
6.科学家设计了一种电化学装置如图所示(X、Y为离子交换膜),该装置在处理有机废水的同时可以对海
水进行淡化。下列叙述不正确的是
A.Y为阳离子交换膜
B.正极发生的反应为O+4e-+2H O=4OH-
2 2
C.该装置工作过程中负极区溶液的质量将减少
D.该装置不能在高温下工作
7.一款新型-空气电池装置如图所示、该电池利用“多孔”石墨电极形成空气通道,放电时生成的
填充在“空位”中,当“空位”填满后,放电终止。下列说法正确的是
A. 极为电池正极
B. 极发生电极反应:
C.该装置的电解液可用乙醇作溶剂D.理论上 极每减重 ,则 极消耗 (标准状况下)
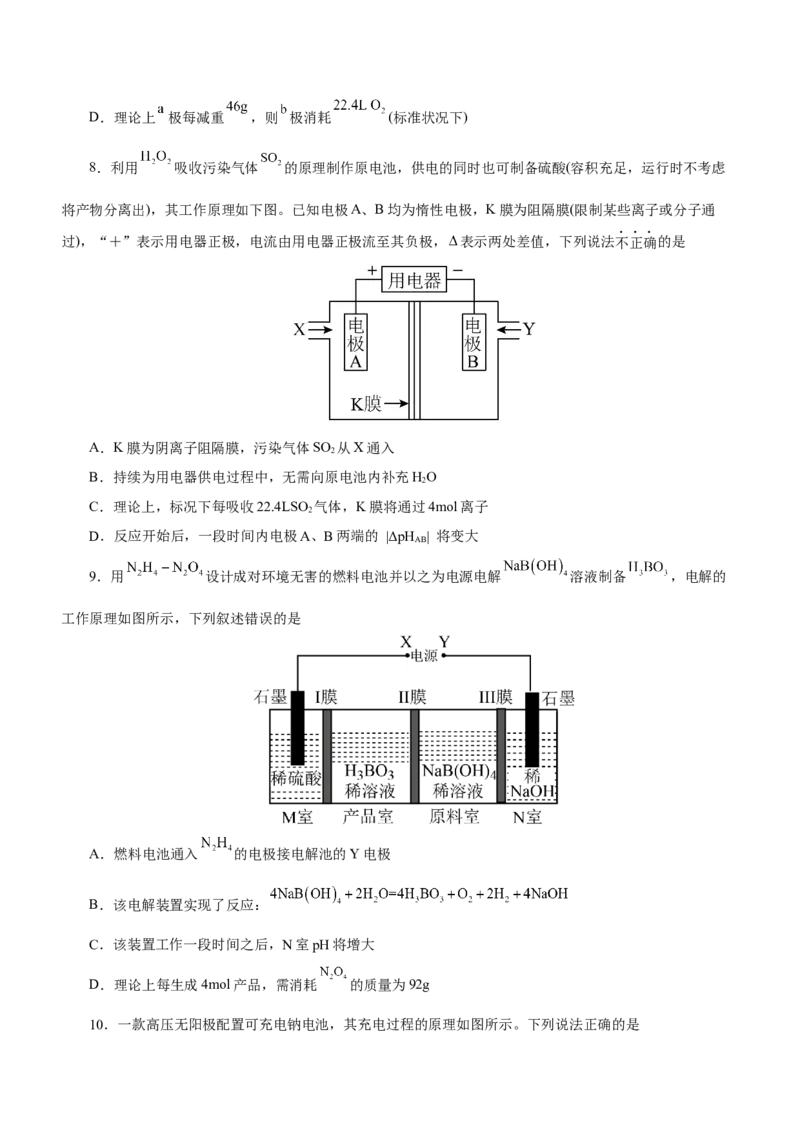
8.利用 吸收污染气体 的原理制作原电池,供电的同时也可制备硫酸(容积充足,运行时不考虑
将产物分离出),其工作原理如下图。已知电极A、B均为惰性电极,K膜为阻隔膜(限制某些离子或分子通
过),“+”表示用电器正极,电流由用电器正极流至其负极, 表示两处差值,下列说法不正确的是
A.K膜为阴离子阻隔膜,污染气体SO 从X通入
2
B.持续为用电器供电过程中,无需向原电池内补充HO
2
C.理论上,标况下每吸收22.4LSO 气体,K膜将通过4mol离子
2
D.反应开始后,一段时间内电极A、B两端的 |ΔpH | 将变大
AB
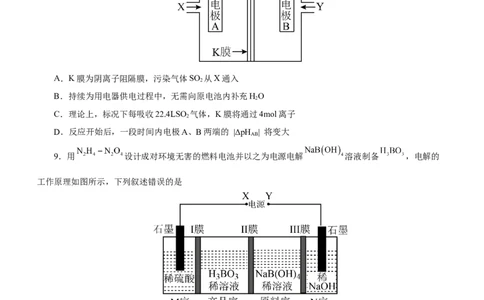
9.用 设计成对环境无害的燃料电池并以之为电源电解 溶液制备 ,电解的
工作原理如图所示,下列叙述错误的是
A.燃料电池通入 的电极接电解池的Y电极
B.该电解装置实现了反应:
C.该装置工作一段时间之后,N室pH将增大
D.理论上每生成4mol产品,需消耗 的质量为92g
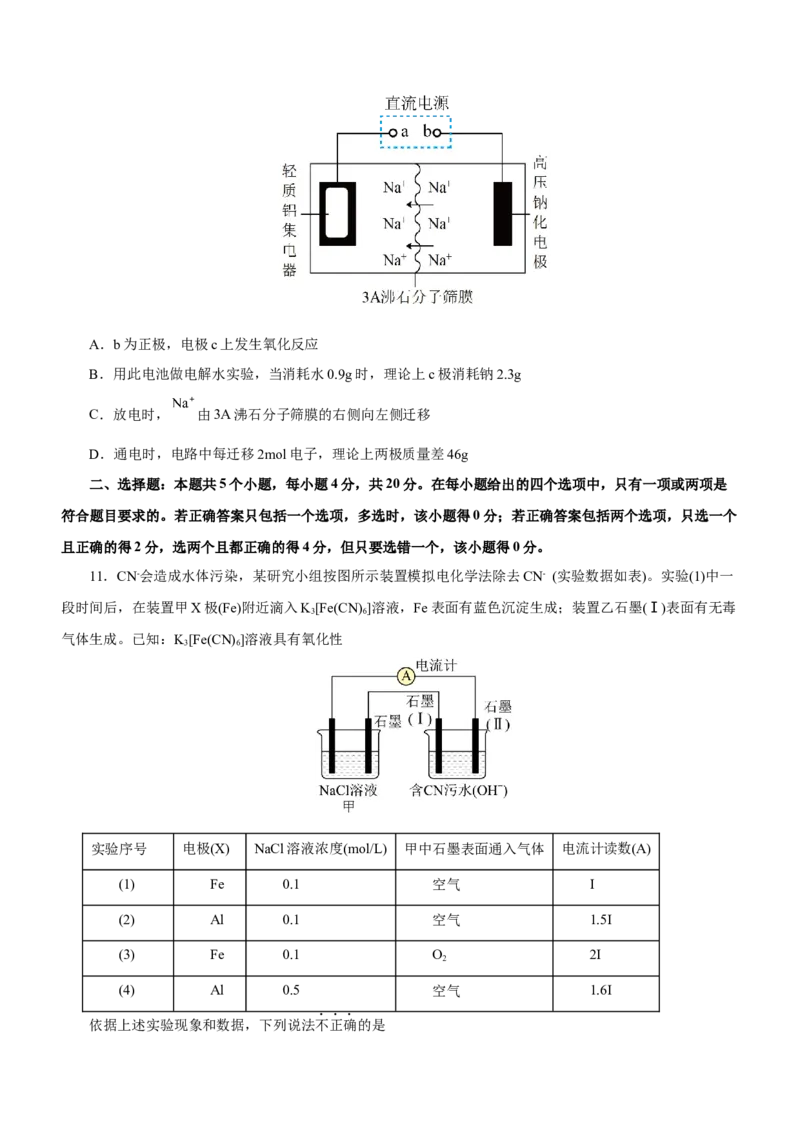
10.一款高压无阳极配置可充电钠电池,其充电过程的原理如图所示。下列说法正确的是A.b为正极,电极c上发生氧化反应
B.用此电池做电解水实验,当消耗水0.9g时,理论上c极消耗钠2.3g
C.放电时, 由3A沸石分子筛膜的右侧向左侧迁移
D.通电时,电路中每迁移2mol电子,理论上两极质量差46g
二、选择题:本题共5个小题,每小题4分,共20分。在每小题给出的四个选项中,只有一项或两项是
符合题目要求的。若正确答案只包括一个选项,多选时,该小题得0分;若正确答案包括两个选项,只选一个
且正确的得2分,选两个且都正确的得4分,但只要选错一个,该小题得0分。
11.CN-会造成水体污染,某研究小组按图所示装置模拟电化学法除去CN- (实验数据如表)。实验(1)中一
段时间后,在装置甲X极(Fe)附近滴入K[Fe(CN) ]溶液,Fe表面有蓝色沉淀生成;装置乙石墨(Ⅰ)表面有无毒
3 6
气体生成。已知:K[Fe(CN) ]溶液具有氧化性
3 6
实验序号 电极(X) NaCl溶液浓度(mol/L) 甲中石墨表面通入气体 电流计读数(A)
(1) Fe 0.1 空气 I
(2) Al 0.1 空气 1.5I
(3) Fe 0.1 O 2I
2
(4) Al 0.5 空气 1.6I
依据上述实验现象和数据,下列说法不正确的是A.仅依据实验(1)装置甲中的现象,不能确定X极(Fe)为负极
B.若实验(1)中X极换成Zn,则电流计读数的范围为1.5I~2I
C.石墨(Ⅰ)的电极反应式:2CN-+12OH--10e-=2CO +N ↑+6H O
2 2
D.相同条件下,X电极活性、O 浓度、电解质溶液浓度均会影响CN-处理效果
2
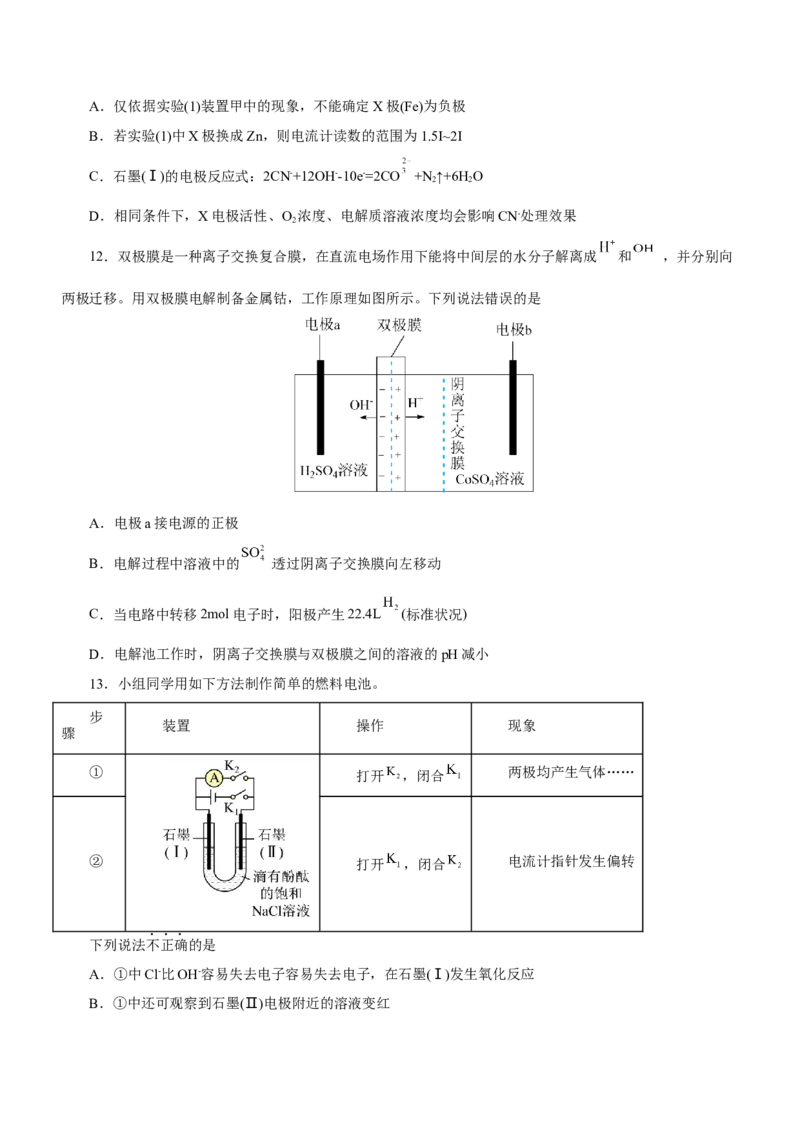
12.双极膜是一种离子交换复合膜,在直流电场作用下能将中间层的水分子解离成 和 ,并分别向
两极迁移。用双极膜电解制备金属钴,工作原理如图所示。下列说法错误的是
A.电极a接电源的正极
B.电解过程中溶液中的 透过阴离子交换膜向左移动
C.当电路中转移2mol电子时,阳极产生22.4L (标准状况)
D.电解池工作时,阴离子交换膜与双极膜之间的溶液的pH减小
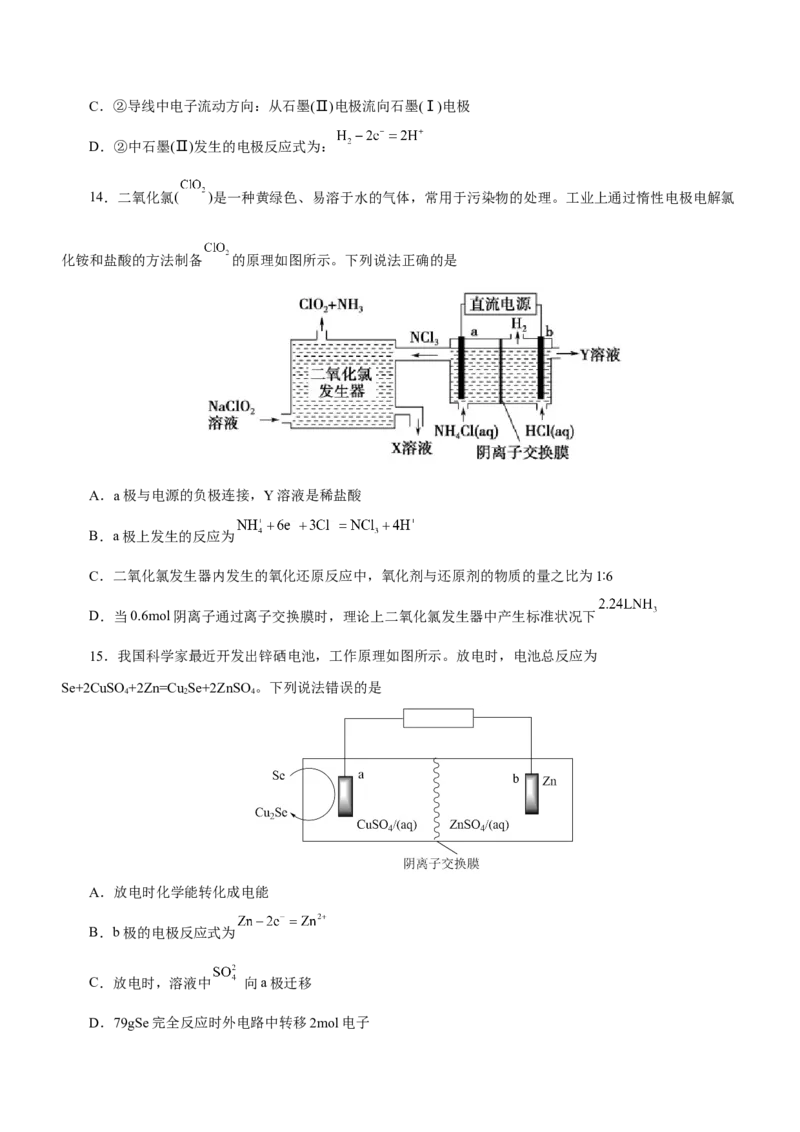
13.小组同学用如下方法制作简单的燃料电池。
步
装置 操作 现象
骤
① 打开 ,闭合 两极均产生气体……
② 打开 ,闭合 电流计指针发生偏转
下列说法不正确的是
A.①中Cl-比OH-容易失去电子容易失去电子,在石墨(Ⅰ)发生氧化反应
B.①中还可观察到石墨(Ⅱ)电极附近的溶液变红C.②导线中电子流动方向:从石墨(Ⅱ)电极流向石墨(Ⅰ)电极
D.②中石墨(Ⅱ)发生的电极反应式为:
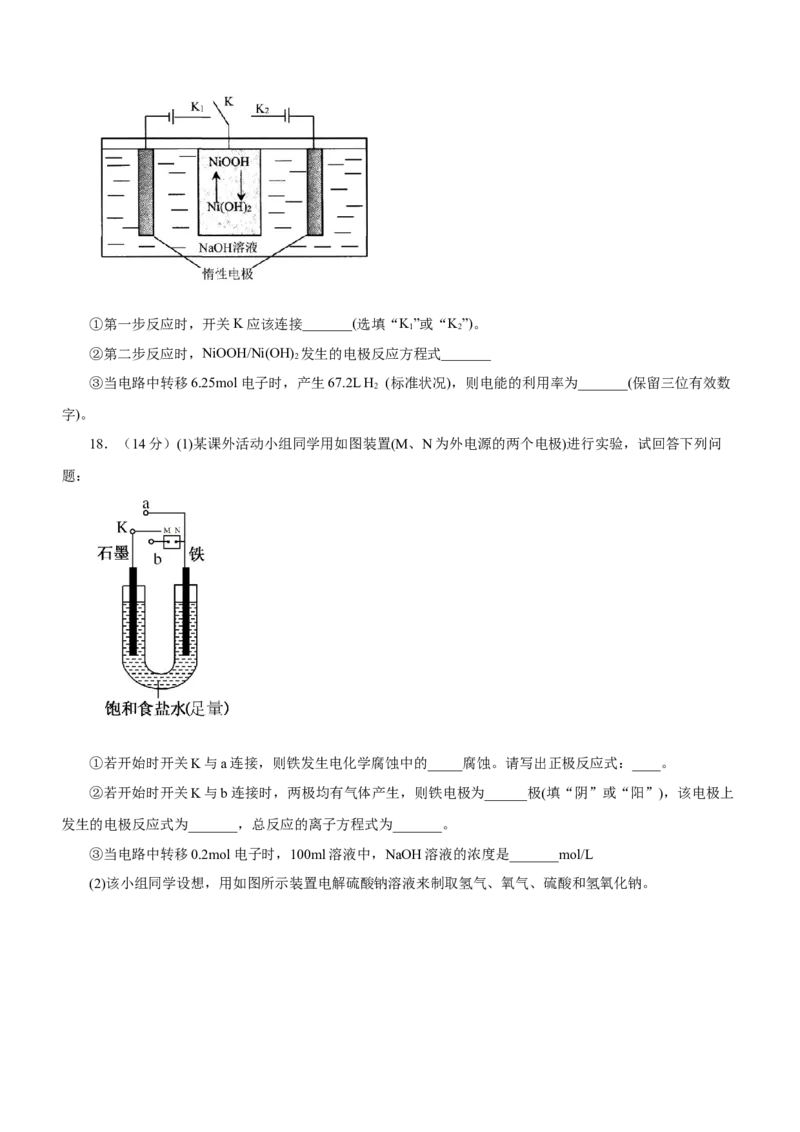
14.二氧化氯( )是一种黄绿色、易溶于水的气体,常用于污染物的处理。工业上通过惰性电极电解氯
化铵和盐酸的方法制备 的原理如图所示。下列说法正确的是
A.a极与电源的负极连接,Y溶液是稀盐酸
B.a极上发生的反应为
C.二氧化氯发生器内发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为1∶6
D.当0.6mol阴离子通过离子交换膜时,理论上二氧化氯发生器中产生标准状况下
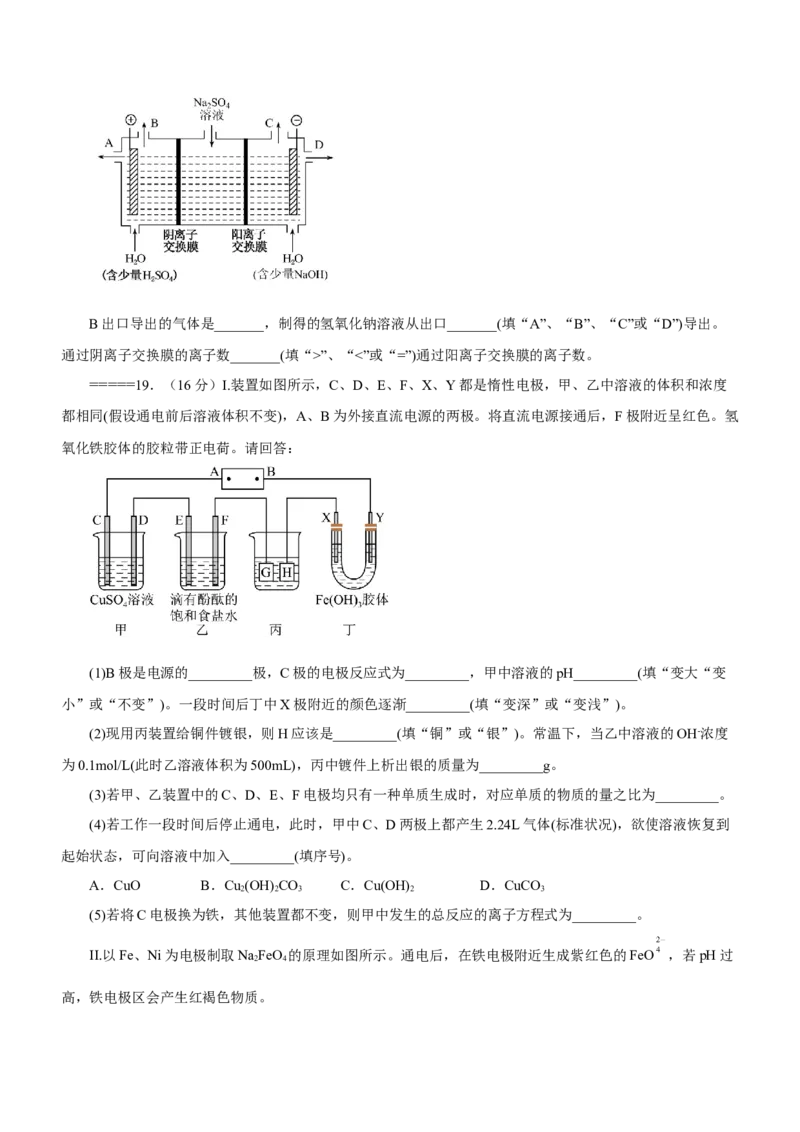
15.我国科学家最近开发出锌硒电池,工作原理如图所示。放电时,电池总反应为
Se+2CuSO+2Zn=Cu Se+2ZnSO 。下列说法错误的是
4 2 4
A.放电时化学能转化成电能
B.b极的电极反应式为
C.放电时,溶液中 向a极迁移
D.79gSe完全反应时外电路中转移2mol电子第II卷 (非选择题共50分)
三、非选择题:本题共4个小题,共50分。
16.(10分)某实验小组同学利用下图装置对电化学原理进行了一系列探究活动。回答下列问题:
(1)甲池为___________(填“原电池”或“电解池”)装置。
(2)甲池反应前,两电极质量相等,一段时间后,若Ag极的质量增加21.6 g,则两电极质量相差
___________g。
(3)实验过程中,甲池左侧烧杯中 的浓度___________(填“变大”“变小”或“不变”)。
(4)若乙池中的某盐溶液是足量CuSO 溶液,则乙池中左侧Pt电极的电极反应式为___________,工作一段
4
时间后,若要使乙池溶液恢复至原来浓度,可向溶液中加入___________(填化学式)。
17.(10分) 正戊烷异构化为异戊烷是油品升级的一项重要技术.正戊烷和异戊烷的部分性质如表:
名称 结构简式 熔点/℃ 沸点/℃ 燃烧热/
正戊烷 CHCHCHCHCH -130 36 3506.1
3 2 2 2 3
异戊烷 (CH)CHCH CH -159.4 27.8 3504.1
3 2 2 3
回答下列问题:
(1)稳定性:正戊烷_______异戊烷(填“>”或“=”或“<”)。
(2)25℃,101kPa时,正戊烷异构化成异戊烷的热化学反应方程式为______________________。
(3)在正戊烷中混入一定比例的H 有利于异构化反应的进行,一种“分步法电解制氢气”的装置如图.该方
2
法制氢气分两步,第一步在惰性电极产生H,NiOOH/Ni(OH) 电极发生氧化反应;第二步在另一个惰性电极
2 2
产生O。
2①第一步反应时,开关K应该连接_______(选填“K”或“K”)。
1 2
②第二步反应时,NiOOH/Ni(OH) 发生的电极反应方程式_______
2
③当电路中转移6.25mol电子时,产生67.2L H (标准状况),则电能的利用率为_______(保留三位有效数
2
字)。
18.(14分)(1)某课外活动小组同学用如图装置(M、N为外电源的两个电极)进行实验,试回答下列问
题:
①若开始时开关K与a连接,则铁发生电化学腐蚀中的_____腐蚀。请写出正极反应式:____。
②若开始时开关K与b连接时,两极均有气体产生,则铁电极为______极(填“阴”或“阳”),该电极上
发生的电极反应式为_______,总反应的离子方程式为_______。
③当电路中转移0.2mol电子时,100ml溶液中,NaOH溶液的浓度是_______mol/L
(2)该小组同学设想,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠。B出口导出的气体是_______,制得的氢氧化钠溶液从出口_______(填“A”、“B”、“C”或“D”)导出。
通过阴离子交换膜的离子数_______(填“>”、“<”或“=”)通过阳离子交换膜的离子数。
=====19.(16分)I.装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度
都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。氢
氧化铁胶体的胶粒带正电荷。请回答:
(1)B极是电源的_________极,C极的电极反应式为_________,甲中溶液的pH_________(填“变大“变
小”或“不变”)。一段时间后丁中X极附近的颜色逐渐_________(填“变深”或“变浅”)。
(2)现用丙装置给铜件镀银,则H应该是_________(填“铜”或“银”)。常温下,当乙中溶液的OH-浓度
为0.1mol/L(此时乙溶液体积为500mL),丙中镀件上析出银的质量为_________g。
(3)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为_________。
(4)若工作一段时间后停止通电,此时,甲中C、D两极上都产生2.24L气体(标准状况),欲使溶液恢复到
起始状态,可向溶液中加入_________(填序号)。
A.CuO B.Cu (OH) CO C.Cu(OH) D.CuCO
2 2 3 2 3
(5)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为_________。
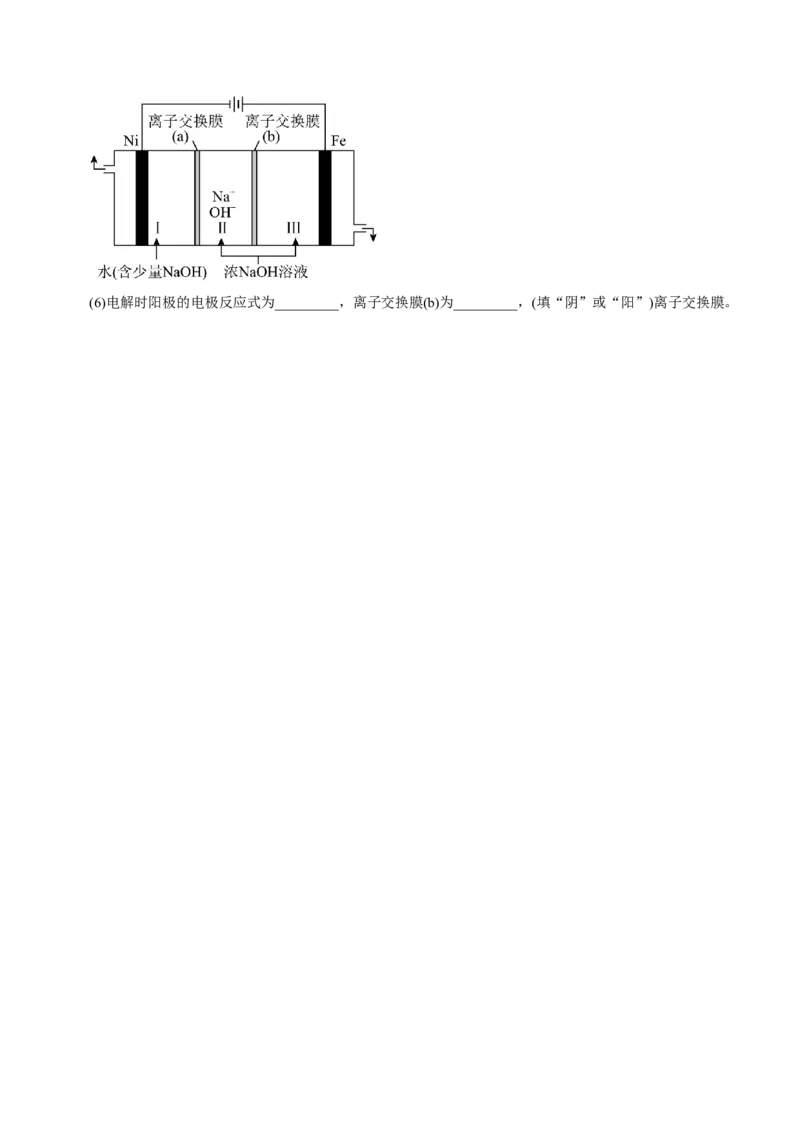
II.以Fe、Ni为电极制取NaFeO 的原理如图所示。通电后,在铁电极附近生成紫红色的FeO ,若pH过
2 4
高,铁电极区会产生红褐色物质。(6)电解时阳极的电极反应式为_________,离子交换膜(b)为_________,(填“阴”或“阳”)离子交换膜。