文档内容
专题 07 水溶液中的离子平衡
1.(2022·辽宁大连市高三模拟)下列实验中,现象及结论都正确,且二者之间有因果关系的是
选项 实验操作 现象 结论
A 向FeI 溶液中通入少量Cl 溶液变黄 则Cl 的氧化性强于Fe3+
2 2 2
FeCl 溶液和KSCN溶液混合反应后,再加 增大反应物浓度,平衡正向
3
B 溶液红色加深
入少量KCl溶液 移动
铜粉溶解,溶液变
C 将铜粉加入到1.0mol·L−1Fe (SO ) 溶液中 金属铁比铜活泼
2 4 3
蓝
溶液均变红,
常温下的水解平衡常数:
常温下,向等体积、等浓度的NaHCO 和
3
D NaHCO 溶液红色
3
CHCOONa溶液中分别滴加2滴酚酞 K (CHCOO−)<K (HCO )
3 h 3 h
更深
【答案】D
【解析】A.向FeI 溶液中通入少量Cl,Cl 与I-发生氧化还原反应生成I,溶液呈黄色,Fe2+未发生反应,
2 2 2 2
因此无法比较Cl 与Fe3+的氧化性强弱,故A错误;B.K+、Cl-对Fe3++3SCN- Fe(SCN) 平衡无影
2 3
响,故B错误;C.2Fe3++Cu=Cu2++2Fe2+只能说明还原性:Cu>Fe2+,不能据此判断Fe与Cu的活泼
性,故C错误;D.颜色深的溶液碱性越强,OH-浓度越大,说明等浓度的HCO 水解程度大于
CHCOO−,因此常温下的水解平衡常数:K (CHCOO−)<K (HCO ),故D正确;综上所述,答案为D。
3 h 3 h
2.(2022·河北张家口高三模拟)下列有关电解质溶液的说法正确的是( )
A.常温下 均为4的 和 溶液中水电离出的 之比为
B.等浓度的 和 溶液均加水稀释10倍, 溶液的 变化较大
C. 溶液的 小于7,溶液中粒子浓度大小顺序为:
D. 的 溶液与 的 溶液任意比例混合:
【答案】C
【解析】A.常温下 为4的 溶液中水电离的 等于溶液中的 ,mol/L, 为4的 溶液中水电离出的 等于溶液中的氢
离子总浓度=10-4mol/L,两溶液中水电离的 之比 ,故A错误;等浓度的 和
溶液均加水稀释10倍,因醋酸是弱酸能继续电离出氢离子,因此 溶液的 变化较小,故B
错误; 溶液的 小于7,说明 的电离程度大于其水解程度,则电离产生
的 大于水解产生的 ,离子浓度的大小: ,故C正
确; 溶液与 溶液混合时:由电荷守恒可知: ,
两者任意比例混合时 不一定等于 ,因此等式
不一定成立,故D错误;故选C。
3.(2022·山东青岛高三模拟)三甲胺 [N(CH )]是一种一元有机弱碱,可简写为MOH。常温下,向20mL
3 3
0.5mol/L MOH溶液中逐滴加入浓度为0.25mol/L的HCl溶液,溶液中lg 、pOH[pOH=-lgc(OH-)]、
中和率( )的变化如图所示。下列说法正确的是( )
A.三甲胺[N(CH )]的电离常数为10-4.8
3 3
B.a点时,c(MOH)+c(M+)=2c(Cl-)
C.b点时,c(M+)>c(Cl-)>c(MOH)>c(OH-)>c(H+)
D.溶液中水的电离程度:c点<d点
【答案】C
【解析】据图可知当lg =0时,pOH=4.2,即c(MOH)=c(M+)时c(OH-)=10-4.2mol/L,三甲胺的电离
常数K= =10-4.2,故A错误;a点中和率小于50%,即加入的2n(HCl)<n(MOH),根据物料
守恒可知c(MOH)+c(M+)>2c(Cl-),故B错误;b点中和率为50%,溶液中的溶质为等物质的量的MOH和MCl,据图可知此时pOH小于7,溶液显碱性,说明M+的水解程度小于MOH的电离程度,则溶液c(M+)
>c(Cl-)> c(MOH)> c(OH-)>c(H+),故C正确;c点中和率为100%溶液中溶质为MCl,d点溶液中溶质
为MCl和HCl,HCl的电离抑制水的电离,MCl的水解促进水的电离,所以c点水的电离程度更大,故D
错误;综上所述答案为C。
4.(2022·广东深圳高三模拟)常温下,向浓度均为 、体积为 的两种一元酸 、
的溶液中,分别加入 固体(忽略溶液体积的变化), 随加入 的物质的量的变化
如图所示。下列叙述正确的是( )
A. 为弱酸, 为强酸
B.a点溶液中由水电离出的 与由水电离出的 的乘积为
C.b点时 与 恰好完全反应
D.c点溶液中:
【答案】D
【解析】0.1 mol∙L−1 , =12,说明c(H+)=0.1mol∙L−1,则HA为强酸,0.1 mol∙L−1 ,
=8,说明c(H+)= 1.0×10−3mol∙L−1,则 为弱酸,故A错误;根据A选项分析a点溶液中c(H
+)=0.1mol∙L−1, ,由水电离出的 与由水电离出的
的乘积为 ,故B错误;b点 =0,说明c(H+)= 1.0×10−7mol∙L−1,溶液
呈中性,由于 是弱酸,因此混合溶液应该是NaB和HB的混合溶液,HB与 没有完全反应,故
C错误;c点为100mL 0.1 mol∙L−1 加入NaOH物质的量为5.0×10−3mol,反应后溶质为NaB和HB且浓
度相等, =6,说明c(H+)= 1.0×10−4mol∙L−1,即HB电离程度大于B-水解程度,则溶液中:
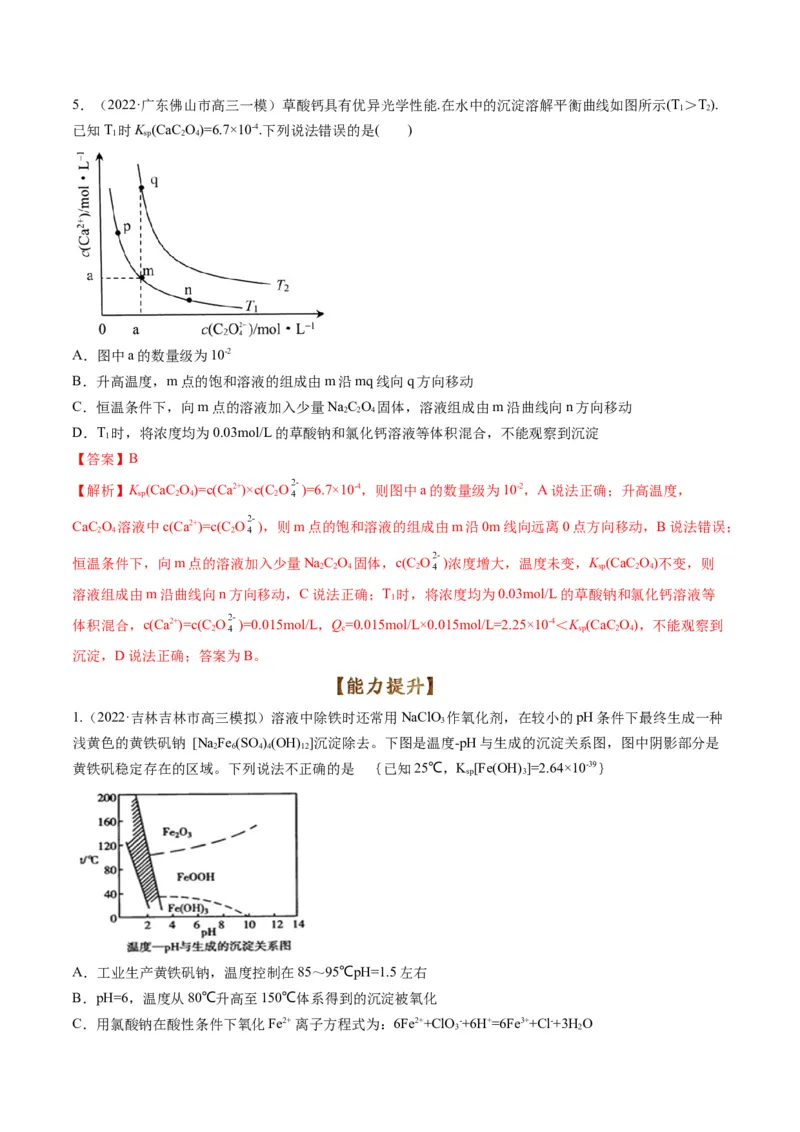
,故D正确;综上所述,答案为D。5.(2022·广东佛山市高三一模)草酸钙具有优异光学性能.在水中的沉淀溶解平衡曲线如图所示(T >T).
1 2
已知T 时K (CaC O)=6.7×10-4.下列说法错误的是( )
1 sp 2 4
A.图中a的数量级为10-2
B.升高温度,m点的饱和溶液的组成由m沿mq线向q方向移动
C.恒温条件下,向m点的溶液加入少量NaC O 固体,溶液组成由m沿曲线向n方向移动
2 2 4
D.T 时,将浓度均为0.03mol/L的草酸钠和氯化钙溶液等体积混合,不能观察到沉淀
1
【答案】B
【解析】K (CaC O)=c(Ca2+)×c(C O )=6.7×10-4,则图中a的数量级为10-2,A说法正确;升高温度,
sp 2 4 2
CaC O 溶液中c(Ca2+)=c(C O ),则m点的饱和溶液的组成由m沿0m线向远离0点方向移动,B说法错误;
2 4 2
恒温条件下,向m点的溶液加入少量NaC O 固体,c(C O )浓度增大,温度未变,K (CaC O)不变,则
2 2 4 2 sp 2 4
溶液组成由m沿曲线向n方向移动,C说法正确;T 时,将浓度均为0.03mol/L的草酸钠和氯化钙溶液等
1
体积混合,c(Ca2+)=c(C O )=0.015mol/L,Q=0.015mol/L×0.015mol/L=2.25×10-4<K (CaC O),不能观察到
2 c sp 2 4
沉淀,D说法正确;答案为B。
1.(2022·吉林吉林市高三模拟)溶液中除铁时还常用NaClO 作氧化剂,在较小的pH条件下最终生成一种
3
浅黄色的黄铁矾钠 [Na Fe (SO )(OH) ]沉淀除去。下图是温度-pH与生成的沉淀关系图,图中阴影部分是
2 6 4 4 12
黄铁矾稳定存在的区域。下列说法不正确的是 {已知25℃,K [Fe(OH) ]=2.64×10-39}
sp 3
A.工业生产黄铁矾钠,温度控制在85~95℃pH=1.5左右
B.pH=6,温度从80℃升高至150℃体系得到的沉淀被氧化
C.用氯酸钠在酸性条件下氧化Fe2+ 离子方程式为:6Fe2++ClO -+6H+=6Fe3++Cl-+3H O
3 2D.在25℃时溶液经氧化,调节溶液pH=4 ,此时溶液中c(Fe3+)=2.64×10-9 mol·L-1
【答案】B
【解析】由图像可知,生成黄铁矾钠所需要的合适温度为85℃~95℃,pH=1.5左右,故A正确;根据图
像,pH=6温度从80℃升高至150℃,FeOOH分解成Fe O,沉淀没有被氧化,故B错误;ClO -在酸性条
2 3 3
件下具有强氧化性,与Fe2+发生氧化还原反应,反应的离子方程式为6Fe2++ClO -+6H+=6Fe3++Cl-+3H O,故
3 2
C正确;25℃ pH=4时,c(OH-)=1×10-10mol/L,Fe(OH) 的K =2.64×10-39,则c(Fe3+)=2.64×10-39÷(1×10-10)
3 sp
3=2.64×10-9(mol/L),故D正确;答案为B。
2.(2022·陕西汉中市高三一模)常温下,用0.1 mol·L-1 NaOH溶液滴定10 mL 0.1 mol·L-1 HA溶液的滴定
曲线如图所示,下列说法不正确的是( )
A.a≈3,说明HA属于弱酸
B.水的电离程度:d点>e点
C.c点溶液中:c(Na+)=c(A-)+c(HA)
D.b点溶液中粒子浓度大小: c(A-)>c(Na+)>c(H+)>c(OH-)
【答案】C
【解析】 c(HA)=0.1mol/L,若为强酸,氢离子浓度应为c(H+)=0.1mol/L,溶液的pH=3,
c(H+)=0.001mol/L,说明HA电离程度较小,HA属于弱酸,故A不选;酸或碱抑制水电离,弱离子促进水
电离,d点溶质为NaA,促进水电离,e点溶质为NaA和NaOH,NaOH抑制水电离,所以水电离程度:d
点>e点,故B不选;c点溶液显中性,由电荷守恒 得:c(Na+)=c(A-) ,故
C选;b点溶液中溶质为等物质的量浓度的HA和NaA,溶液pH<7,溶液呈酸性,说明HA电离程度大于
A−水解程度,所以c(A−)>c(HA),钠离子不水解,且HA电离程度和A−水解程度都较小,所以c(A-)>c(Na
+)>c(H+)>c(OH-),故D不选;故选C。
3.(2022·福建宁德市高三一模)氯气常用于饮用水消毒,已知25℃时,氯水中Cl、ClO-两种微粒所占含
2
氯微粒的分数与pH的关系如下图。下列说法错误的是( )
A.用氯气处理饮用水时,溶液的pH在x~y之间,杀菌效果最佳
B.b点氯水中c(Cl-):c(ClO-)<1:1
C.a点有关粒子浓度大小关系是c(H+)>c(Cl-)>c(HClO)>c(OH-)D.氯气处理饮用水时,在冬季的效果比夏季好
【答案】B
【解析】根据图像可知,溶液的pH在x~y之间,HClO的浓度最大,HClO具有强氧化性,则用氯气处理
饮用水时,溶液的pH在x~y之间,杀菌效果最佳,A说法正确;b点时,根据物料守恒,c(Cl-)=c(HClO)
+c(ClO-),则氯水中c(Cl-):c(ClO-)>1:1,B说法错误;a点时,Cl
2
+H
2
O⇌H++Cl-+HClO,HClO⇌H+
+ClO-,c(H+)>c(Cl-)>c(HClO),溶液显酸性,c(HClO)>c(OH-),则有关粒子浓度大小关系是c(H+)>c(Cl-)
>c(HClO)>c(OH-),C说法正确;氯气处理饮用水时,冬季温度低,次氯酸的电离程度减小,且温度低,
不易分解,导致次氯酸的浓度增大,则在冬季的效果比夏季好,D说法正确;答案为B。
4.(2022·湖南株洲市高三一模)室温下,向 0.01 mol/L 的醋酸溶液中滴入 pH=7 的醋酸铵稀溶液,溶液
pH 随滴入醋酸铵溶液体积变化的曲线示意图如图所示,下列分析不正确的是( )
A.a 点溶液的 pH>2
B.a~c中的任意点,溶液中存在 c(CHCOO-)>c(NH )
3
C.a~c 中水的电离程度逐渐增大
D.a~c 中 pH 变化的原因主要是 CH
3
COOH⇌CH
3
COO-+H+逆向移动
【答案】D
【解析】a点为醋酸溶液,醋酸为弱电解质,不能完全电离,则溶液中c(H+)<0.01mol/L,溶液的pH>2,
A分析正确;a~c中的任意点,溶液显酸性,即c(H+)>c(OH-),根据溶液呈电中性,c(NH )+ c(H+)=
c(OH-)+c(CH COO-),溶液中存在 c(CHCOO-)>c(NH ),B分析正确;a~c 中溶液的酸性逐渐减弱,则酸
3 3
对水的电离抑制程度逐渐减小,故水的电离程度逐渐增大,C分析正确;a~b中,向醋酸中加入醋酸铵,
导致溶液中c(CHCOO-)增大,醋酸的电离平衡逆向移动,pH增大,随加入醋酸铵溶液的增多,在b ~c中,
3
溶液体积增大,醋酸根离子及氢离子浓度都减小,则 pH增大,溶液中pH变化的原因主要不都是
CH
3
COOH⇌CH
3
COO-+H+逆向移动导致,D分析错误;答案为D。
5.(2022·广东高三零模)综合利用炼锌矿渣(主要含铁酸镓Ga(Fe O)、铁酸锌ZnFe O)获得3种金属盐,
2 2 4 3 2 4
并进一步利用镓盐制备具有优异光电性能的氮化镓(GaN),部分工艺流程如下:
已知:①常温下,浸出液中各离子的浓度及其开始形成氢氧化物沉淀的pH见表1。②金属离子在工艺条件下的萃取率(进入有机层中金属离子的百分数)见表2。
表1金属离子浓度及开始沉淀的pH
金属离子 浓度(mol·L-1) 开始沉淀pH
Fe2+ 1.0×10-3 8.0
Fe3+ 4.0×10-2 1.7
Zn2+ 1.5 5.5
Ga3+ 3.0×10-3 3.0
表2金属离子的萃取率
金属离子 萃取率(%)
Fe2+ 0
Fe3+ 99
Zn2+ 0
Ga3+ 97-98.5
(1)Ga (Fe O) 中Ga的化合价为______,“浸出”时其发生反应的离子方程式为______。
2 2 4 3
(2)滤液1中可回收利用的物质是______,滤饼的主要成分是______;萃取前加入的固体X为______。
(3)Ga与Al同主族,化学性质相似。反萃取后,镓的存在形式为______ (填化学式)。
(4)电解过程包括电解反萃取液制粗镓和粗镓精炼两个步骤。精炼时,以粗镓为阳极,以NaOH溶液为电解
液,阴极的电极反应为______。
(5)GaN可采用MOCVD (金属有机物化学气相淀积)技术制得:以合成的三甲基镓为原料,使其与NH 发生
3
系列反应得到GaN和另一种产物,该过程的化学方程式为______。
(6)滤液1中残余的Ga3+的浓度为______ mol·L-1 (写出计算过程)。
【答案】(1)+3价 Fe O +8H+=2Fe3++4H O (2)硫酸锌 Fe(OH) 、Ga(OH) Fe (3)
2 2 3 3
NaGaO (4)GaO +3e-+2H O=Ga+4OH- (5) Ga(CH )+NH=3CH+GaN (6)3.0×10-10.2
2 2 3 3 3 4
【解析】炼锌矿渣用稀硫酸酸浸后所得滤液中含有亚铁离子、铁离子、锌离子、Ga3+,加入双氧水氧化亚
铁离子,调节pH=5.4,沉淀铁离子和Ga3+,滤液1中含有锌离子。得到的滤饼加入盐酸酸化得到氯化铁
和氯化镓,加入固体铁把铁离子转化为亚铁离子,然后利用萃取剂萃取Ga3+,加入氢氧化钠溶液使Ga3+转
化为NaGaO ,电解NaGaO 溶液生成单质Ga,据此解答。
2 2
(1)Ga (Fe O) 中Fe是+3价,O是-2价,根据化合价代数和为0可知Ga的化合价为+3价,“浸出”时其
2 2 4 3
发生反应的离子方程式为Fe O +8H+=2Fe3++4H O。
2 2
(2)根据以上分析可知滤液1中为硫酸锌,则可回收利用的物质是硫酸锌,调节pH=5.4,沉淀铁离子和
Ga3+,滤饼的主要成分是Fe(OH) 、Ga(OH) ;萃取前加入的固体X的目的是还原铁离子,则X为Fe。
3 3(3)Ga与Al同主族,化学性质相似;反萃取后加入氢氧化钠溶液使Ga3+转化为NaGaO ,即镓的存在形式为
2
NaGaO 。
2
(4)精炼时,以粗镓为阳极,以NaOH溶液为电解液,阴极是得到电子转化为Ga,电极反应为GaO +3e-
+2H O=Ga+4OH-。
2
(5)以合成的三甲基镓为原料,使其与NH 发生系列反应得到GaN和另一种产物,根据原子守恒可知还有
3
甲烷生成,该过程的化学方程式为Ga(CH )+NH=3CH+GaN。
3 3 3 4
(6)根据表中数据可知Ga(OH) 的溶度积常数为3.0×10-3×(10-11)3=3.0×10-36,溶液的pH=5.4,即氢氧根
3
离子浓度是10-8.6mol/L,所以滤液1中残余的Ga3+的浓度为 =3.0×10-10.2mol·L-1。
6.(2022·湖南高三零模)以镁铝复合氧化物( )为载体的负载型镍铜双金属催化剂(
)是一种新型高效加氢或脱氢催化剂,其制备流程如下:
已知:常温下, , 。回答下列问题:
(1)在加热条件下,尿素 在水中发生水解反应,放出______和______两种气体(写化学式)。
(2)“晶化”过程中,需保持恒温60℃,可采用的加热方式为______。
(3)“洗涤”过程中,检验滤饼是否洗净的方法是______。
(4)常温下,若“悬浊液”中 ,则溶液的 ______。
(5)“还原”过程中所发生反应的化学方程式为______。
(6) 在强碱溶液中被 氧化可得 ,该物质能用作碱性镍镉电池的正极材料。其电池反
应式:
①放电一段时间后,溶液的pH将______(填“增大”“减小”或“不变”)。
②充电时,阳极发生的电极反应式为______。
【答案】(1)NH CO (2)水浴加热 (3)取最后一次洗涤液少量于试管,向试管中加入稀盐酸,再加
3 2
入氯化钡,若有白色沉淀则未洗净,若无沉淀则已洗净 (4)10 (5)NiO+H Ni+HO,CuO+H
2 2 2
Cu+HO (6)增大 Ni(OH) +OH--e-=NiOOH+HO
2 2 2【解析】将MgSO 、Al (SO )、NiSO 、CuSO 混合溶液在90℃下加入尿素发生反应生成悬浊液
4 2 4 3 4 4
Mg(OH) 、Al(OH) 、Cu(OH) 、Ni(OH) ,在60℃净化过滤,得到滤饼,洗涤、干燥,焙烧得到MgO、
2 3 2 2
CuO、NiO、Al O,在550℃温度下用氢气还原。
2 3
(1)根据题意,尿素[CO(NH)]在加热条件下与水发生水解反应即CO(NH)+HO CO↑+2NH ↑,因此
2 2 2 2 2 2 3
放出NH 和CO 两种气体;
3 2
(2)“晶化”过程中,需保持恒温60℃,温度在100℃以下,因此采用的加热方式为水浴加热;
(3)“洗涤”过程中,检验滤饼是否洗净,主要检验洗涤液中是否还含有硫酸根,因此常用的方法是取最后
一次洗涤液少量于试管,向试管中加入稀盐酸,再加入氯化钡,若有白色沉淀则未洗净,若无沉淀则已洗
净;
(4)常温下,若“悬浊液”中 ,
,则
, ,则溶液的
10;(5)“还原”过程最终得到 ,说明是NiO、CuO与氢气发生还原反应,因此所发
生反应的化学方程式为NiO+H Ni+HO,CuO+H Cu+HO;
2 2 2 2
(6)①放电一段时间后,负极反应式为Cd-2e-+2OH-=Cd(OH) ,正极是2NiOOH+2e-+2HO =2Ni(OH)
2 2 2
+2OH-,正极生成的OH-物质的量与负极消耗的OH-物质的量相等,但是消耗了电解质中的水,使碱性
增强,因此溶液的pH将增大。
②根据放电时正极电极反应式NiOOH+e-+HO =Ni(OH) +OH-,则充电时,阳极发生的电极反应式为
2 2
Ni(OH) +OH--e-=NiOOH+HO。
2 2
7.(2022·山西太原·一模)已知HA为一元弱酸,K 为HA的电离常数,25℃时,某混合溶液中c(HA)
a
+c(A-)=0.1 mol·L-1, lgc(HA)、lgc(A-)、lgc(H+)和lgc(OH-)随pH变化的关系如图所示。下列说法错误的是
A.O点时,pH = 7
B.K(HA)的数量级为10-5
aC.M点时,存在c(H+)=c(OH-)+ (A-)
C
D.该体系中,c(HA)= mol·L-1
【答案】C
【解析】pH=-lgc(H+),所以随pH升高直线减小的是lgc(H+),则直线升高的是lgc(OH-),而pH升高时,
HA会与氢氧根发生反应HA+OH-=H O+A-,所以开始几乎不变,后续随pH增大而减少的是lgc(HA),随
2
pH增大而增加,后续几乎不变的是lgc(A-)。
A.据图可知O点处lgc(H+)=lgc(OH-),即c(H+)=c(OH-),溶液呈中性,温度为25℃,所以pH=7,A正确;
B.K(HA)= ,据图可知N点处c(A-)=c(HA),pH=4.74,即c(H+)=10-4.74mol/L,所以K(HA)=10-
a a
4.74,数量级为10-5,B正确;
C.据图可知M点处c(A-)=c(H+),C错误;
D.该体系中c(HA)+c(A-)=0.1 mol·L-1,即c(A-)=0.1mol/L-c(HA),c(HA)= = ,
解得c(HA)= mol/L,D正确;
综上所述答案为C。
8.(2022·吉林长春·二模)25 °C时,用0.1 mol·L-1 NaOH溶液滴定同浓度的HA溶液,HA被滴定分数
2 2
、pH及微粒分布分数 ,X表示HA、HA-或A2-]的关系如图所示:
2
下列说法正确的是
A.25 °C时,HA第一步电离平衡常数K ≈10-7
2 a1
B.c点溶液中: c(Na+)=2c(HA- )+ c(A2-)
C.b点溶液中: c(Na+ )>c(HA- )> c(A2- )>c(H+ )> c(HA)>c(OH- )
2
D.a、b、c、d四点溶液中水的电离程度: c>d>b>a
【答案】B【解析】由图可知,a、b、c、d所在实线为0.1 mol•L-1NaOH溶液滴定二元弱酸HA的滴定曲线,当
2
<1时,HA部分反应,溶液中溶质为NaHA和HA;当 =1时,反应生成NaHA,
2 2
NaHA溶液显酸性;当2> >1时,溶液中溶质为NaHA和NaA;当 =2时,反应生成
2
NaA,NaA溶液显碱性。
2 2
A. 25 °C时,pH=7时,c点c(HA- )= c(A2-),HA第二步电离平衡常数K = ≈10-
2 a2
7,HA第一步电离平衡常数K >10-7,故A错误;
2 a1
B.c点溶液中,溶液中溶质为NaHA和NaA,且c(HA-)=c(A2- ),由电荷守恒可知c(Na+)+c(H+)═c(HA-)
2
+c(OH-)+2c(A2- ),pH=7,c(H+)═c(OH-),故c(Na+)═c(HA-)+2c(A2- )═3c(HA-)==3c(A2- )= 2c(HA- )+ c(A2-),故
B正确;
C.b点溶液中,由图象可知c(Na+)>c(HA-)>c(A2- )>c(HA),b点pH<7,c(H+ )>c(OH- ),HA被滴定分
2 2
数 >1,c(OH- )> c(HA),故C错误;
2
D.未加氢氧化钠溶液时,HA电离出氢离子,抑制水的电离,加入氢氧化钠溶液,酸逐渐被中和为盐,
2
对水的抑制程度减弱,生成的NaHA、NaA能水解,促进水的电离,当酸碱恰好中和为NaA,即d点附
2 2
近(pH突变),对水的电离促进程度最大,故a、b、c、d四点溶液中水的电离程度:d>c>b>a,故D错误;
故选B。
9.(2022·陕西汉中·二模)常温下,用0.1mol·L-1的NaOH溶液滴定20mL0.1mol·L-1的HPO 溶液,滴定过
3 2
程中混合溶液的pH随加入的NaOH溶液体积变化关系如图所示,下列说法不正确的是
A.常温下,K (H PO )的数量级为10—5
a 3 2
B.B点对应的溶液中:2[c(H+)—c(OH—)]=c(H PO )—c(H PO )
2 3 2
C.HPO 为一元弱酸
3 2
D.滴定至V=20mL的过程中,溶液中由水电离出的c( H+)·(OH—)不变
【答案】D
【解析】由图可知,未加入氢氧化钠溶液时,0.1mol·L-1的HPO 溶液pH为3说明HPO 为弱酸,加入
3 2 3 2
20mL0.1mol·L-1氢氧化钠溶液时,20mL0.1mol·L-1的HPO 溶液恰好完全反应说明HPO 为一元弱酸,所得
3 2 3 2NaH PO 溶液呈碱性。
2 2
A.由分析可知,0.1mol·L-1的HPO 溶液pH为3,则K (H PO )= =1.0×10—5,数量级
3 2 a 3 2
为10—5,故A正确;
B.由图可知,B点时氢氧化钠溶液与HPO 溶液反应得到等浓度的HPO 和NaH PO 混合溶液,溶液中存
3 2 3 2 2 2
在电荷守恒关系c(Na+)+ c(H+)= c(OH—)+c(H PO )和物料守恒关系2 c(Na+)= c(H PO )+c(H PO ),整合可
2 2 3 2
得2[c(H+)—c(OH—)]=c(H PO )—c(H PO ),故B正确;
2 3 2
C.由分析可知,HPO 为一元弱酸,故C正确;
3 2
D.由分析可知,HPO 为一元弱酸,加入20mL0.1mol·L-1氢氧化钠溶液时,20mL0.1mol·L-1的HPO 溶液
3 2 3 2
恰好完全反应说明HPO 为一元弱酸,所得NaH PO 溶液呈碱性,则HPO 离子在溶液中水解促进水的电
3 2 2 2 2
离,溶液中由水电离出的c( H+)·(OH—)增大,故D错误;
故选C。
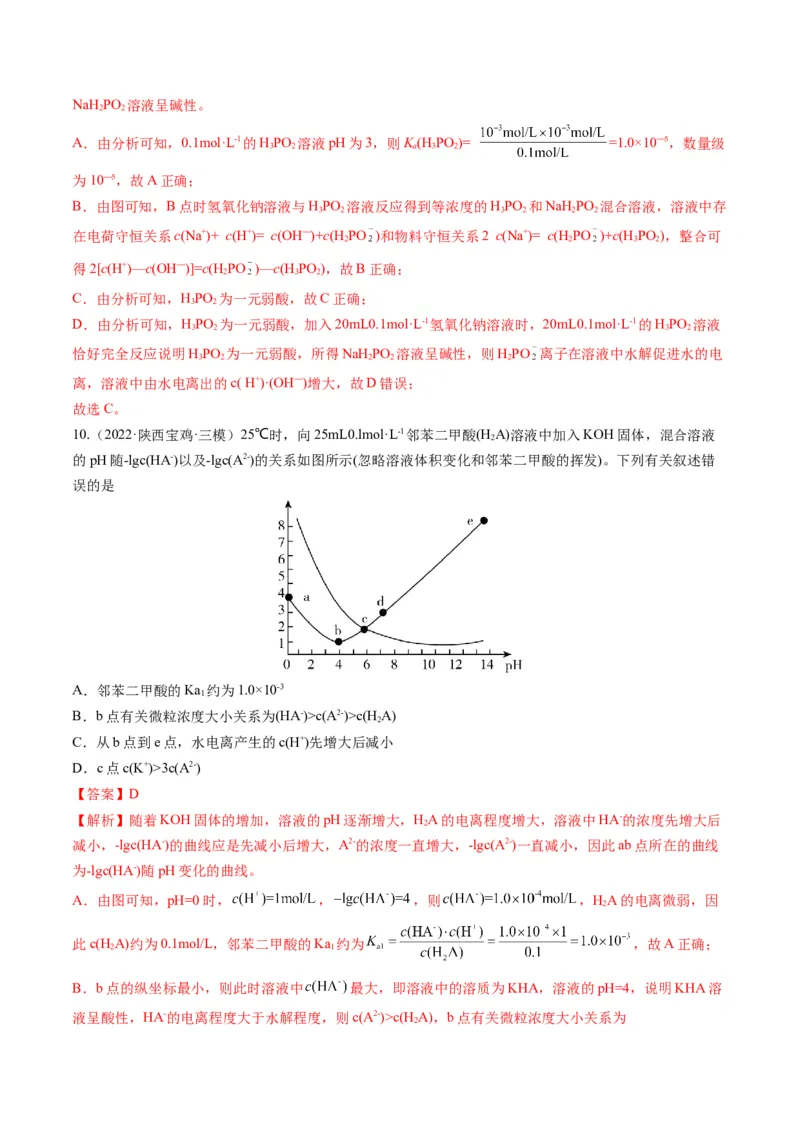
10.(2022·陕西宝鸡·三模)25℃时,向25mL0.lmol·L-1邻苯二甲酸(H A)溶液中加入KOH固体,混合溶液
2
的pH随-lgc(HA-)以及-lgc(A2-)的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发)。下列有关叙述错
误的是
A.邻苯二甲酸的Ka 约为1.0×10-3
1
B.b点有关微粒浓度大小关系为(HA-)>c(A2-)>c(H A)
2
C.从b点到e点,水电离产生的c(H+)先增大后减小
D.c点c(K+)>3c(A2-)
【答案】D
【解析】随着KOH固体的增加,溶液的pH逐渐增大,HA的电离程度增大,溶液中HA-的浓度先增大后
2
减小,-lgc(HA-)的曲线应是先减小后增大,A2-的浓度一直增大,-lgc(A2-)一直减小,因此ab点所在的曲线
为-lgc(HA-)随pH变化的曲线。
A.由图可知,pH=0时, , ,则 ,HA的电离微弱,因
2
此c(HA)约为0.1mol/L,邻苯二甲酸的Ka 约为 ,故A正确;
2 1
B.b点的纵坐标最小,则此时溶液中 最大,即溶液中的溶质为KHA,溶液的pH=4,说明KHA溶
液呈酸性,HA-的电离程度大于水解程度,则c(A2-)>c(H A),b点有关微粒浓度大小关系为
2(HA-)>c(A2-)>c(H A),故B正确;
2
C.b点溶质为KHA,溶液呈酸性,说明HA-电离程度大于水解程度,抑制水电离,从b到e点,继续加入
KOH固体生成KA,A2-水解而促进水电离,继续加入KOH,KOH抑制水电离,则水电离产生的c (H+)先
2
增大后减小,故C正确;
D.c点溶液中 ,溶液中由电荷守恒有 ,c点溶液呈酸
性, ,则 ,故D错误;
答案选D。