文档内容
有机化学实验
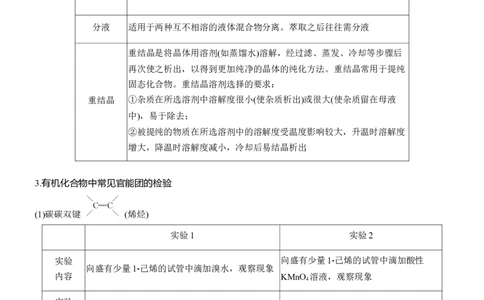
1.常见的三个物质制备实验比较
制取
仪器 除杂及收集 注意事项
物质
①催化剂为FeBr ;
3
含有溴、FeBr 等,用 ②长导管的作用:冷凝回流、导气;
3
溴苯 NaOH 溶液处理后分 ③右侧导管不能(填“能”或“不能”)伸入溶
液,然后蒸馏 液中;
④右侧锥形瓶中有白雾
可能含有未反应完的
①导管1的作用:冷凝回流;
硝 苯、硝酸、硫酸,用
②仪器2为温度计;
基 NaOH 溶液中和酸,分
③用水浴控制温度为50~60 ℃;
苯 液,然后用蒸馏的方法
④浓硫酸的作用:催化剂和吸水剂
除去苯
①浓硫酸的作用:催化剂和吸水剂;
含有乙酸、乙醇,先用 ②饱和Na CO 溶液的作用:溶解乙醇、中和乙
2 3
乙酸
饱和Na CO 溶液处理 酸、降低乙酸乙酯的溶解度;
2 3
乙酯
后,再分液 ③右边导管不能(填“能”或“不能”)接触试
管中的液面
回答下列问题:
(1)在溴苯的制备实验中,若向锥形瓶中滴加稀硝酸酸化的AgNO 溶液,有浅黄色沉淀生成,能不能证
3
明该反应中一定有HBr生成?为什么?
(2)在硝基苯的制备实验中,水浴加热有什么优点?
(3)在乙醇和乙酸的酯化反应中,写出加入试剂和碎瓷片的顺序。
(4)在乙醇和乙酸的酯化反应中,若乙酸中的氧为18O,在什么物质中含有18O?
答案 (1)不能,因为挥发出的Br 也能和AgNO 溶液反应生成AgBr。
2 3
(2)加热均匀,便于控制温度。
(3)在试管中先加入乙醇,然后边振荡试管边慢慢加入浓H SO 和乙酸,再加入几片碎瓷片。
2 4(4)乙酸、水、乙酸乙酯。
2.常见有机物的分离与提纯
分离、提
适用范围
纯方法
蒸馏 适用于沸点不同的互溶液体混合物分离
萃取包括液 液萃取和固 液萃取。液 液萃取是利用待分离组分在两种不
⁃ ⁃ ⁃
萃取 互溶的溶剂中的溶解度不同,将其从一种溶剂转移到另一种溶剂的过
程;固 液萃取是用溶剂从固体物质中溶解出待分离组分的过程
⁃
分液 适用于两种互不相溶的液体混合物分离。萃取之后往往需分液
重结晶是将晶体用溶剂(如蒸馏水)溶解,经过滤、蒸发、冷却等步骤后
再次使之析出,以得到更加纯净的晶体的纯化方法。重结晶常用于提纯
固态化合物。重结晶溶剂选择的要求:
重结晶 ①杂质在所选溶剂中溶解度很小(使杂质析出)或很大(使杂质留在母液
中),易于除去;
②被提纯的物质在所选溶剂中的溶解度受温度影响较大,升温时溶解度
增大,降温时溶解度减小,冷却后易结晶析出
3.有机化合物中常见官能团的检验
(1)碳碳双键 (烯烃)
实验1 实验2
实验 向盛有少量1⁃ 己烯的试管中滴加酸性
向盛有少量1⁃ 己烯的试管中滴加溴水,观察现象
内容 KMnO 溶液,观察现象
4
实验
溴水褪色,液体分层,下层为无色油状液体 KMnO 溶液褪色,有无色气泡冒出
4
现象
化学或
CH ==CH(CH ) CH +2MnO- +6H+―→
2 2 3 3 4
离子方 CH ==CH(CH ) CH +Br ―→CH BrCHBr(CH ) CH
2 2 3 3 2 2 2 3 3
CH (CH ) COOH+CO ↑+4H O+2Mn2+
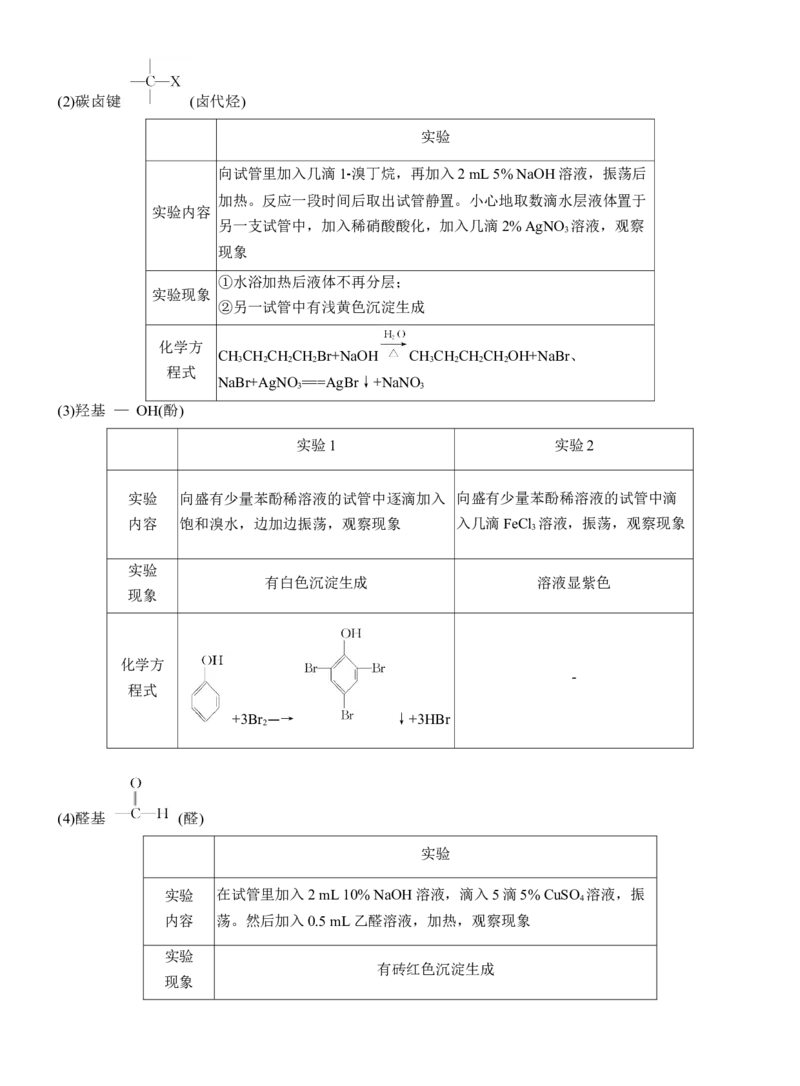
程式 3 2 3 2 2(2)碳卤键 (卤代烃)
实验
向试管里加入几滴1⁃ 溴丁烷,再加入2 mL 5% NaOH溶液,振荡后
加热。反应一段时间后取出试管静置。小心地取数滴水层液体置于
实验内容
另一支试管中,加入稀硝酸酸化,加入几滴2% AgNO 溶液,观察
3
现象
①水浴加热后液体不再分层;
实验现象
②另一试管中有浅黄色沉淀生成
化学方
CH CH CH CH Br+NaOH CH CH CH CH OH+NaBr、
3 2 2 2 3 2 2 2
程式
NaBr+AgNO ===AgBr↓+NaNO
3 3
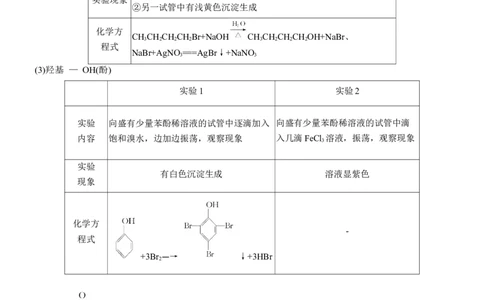
(3)羟基 — OH(酚)
实验1 实验2
实验 向盛有少量苯酚稀溶液的试管中逐滴加入 向盛有少量苯酚稀溶液的试管中滴
内容 饱和溴水,边加边振荡,观察现象 入几滴FeCl 溶液,振荡,观察现象
3
实验
有白色沉淀生成 溶液显紫色
现象
化学方
-
程式
+3Br ―→ ↓+3HBr
2
(4)醛基 (醛)
实验
实验 在试管里加入2 mL 10% NaOH溶液,滴入5滴5% CuSO 溶液,振
4
内容 荡。然后加入0.5 mL乙醛溶液,加热,观察现象
实验
有砖红色沉淀生成
现象化学方
CH CHO+2Cu(OH) +NaOH CH COONa+Cu O↓+3H O
程式 3 2 3 2 2
应用示例
填表:
(1)常见有机物的除杂
除杂试剂 分离方法
乙醇(水) 新制 CaO 蒸馏
乙醇(乙酸) 新制 CaO 蒸馏
乙酸乙酯(乙醇) 饱和 N a CO 溶液 分液
2 3
CH (C H ) 溴水 洗气
4 2 4
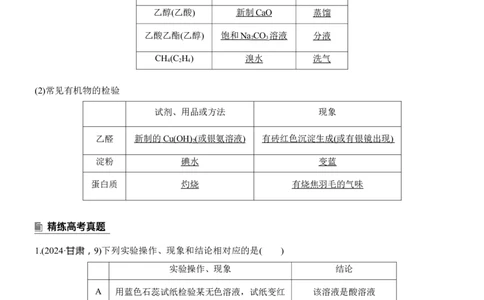
(2)常见有机物的检验
试剂、用品或方法 现象
乙醛 新制的 Cu(OH ) ( 或银氨溶液 ) 有砖红色沉淀生成 ( 或有银镜出现 )
2
淀粉 碘水 变蓝
蛋白质 灼烧 有烧焦羽毛的气味
1.(2024·甘肃,9)下列实验操作、现象和结论相对应的是( )
实验操作、现象 结论
A 用蓝色石蕊试纸检验某无色溶液,试纸变红 该溶液是酸溶液
B 用酒精灯灼烧织物产生类似烧焦羽毛的气味 该织物含蛋白质
C 乙醇和浓硫酸加热,产生的气体使溴水褪色 该气体是乙烯
氢氧化钠的碱性比氢氧化
D 氯化镁溶液中滴入氢氧化钠溶液,生成沉淀
镁强
答案 B解析 用蓝色石蕊试纸检验某无色溶液,试纸变红,该溶液显酸性,但不一定是酸溶液,A不符合题意;
乙醇和浓硫酸加热,主要产物为乙烯,还可能含有二氧化碳、二氧化硫等,二氧化硫也能使溴水褪色,不
能说明产生的气体是乙烯,C不符合题意;氯化镁溶液中滴入NaOH溶液生成Mg(OH) 沉淀,与NaOH和
2
Mg(OH) 的碱性强弱无关,D不符合题意。
2
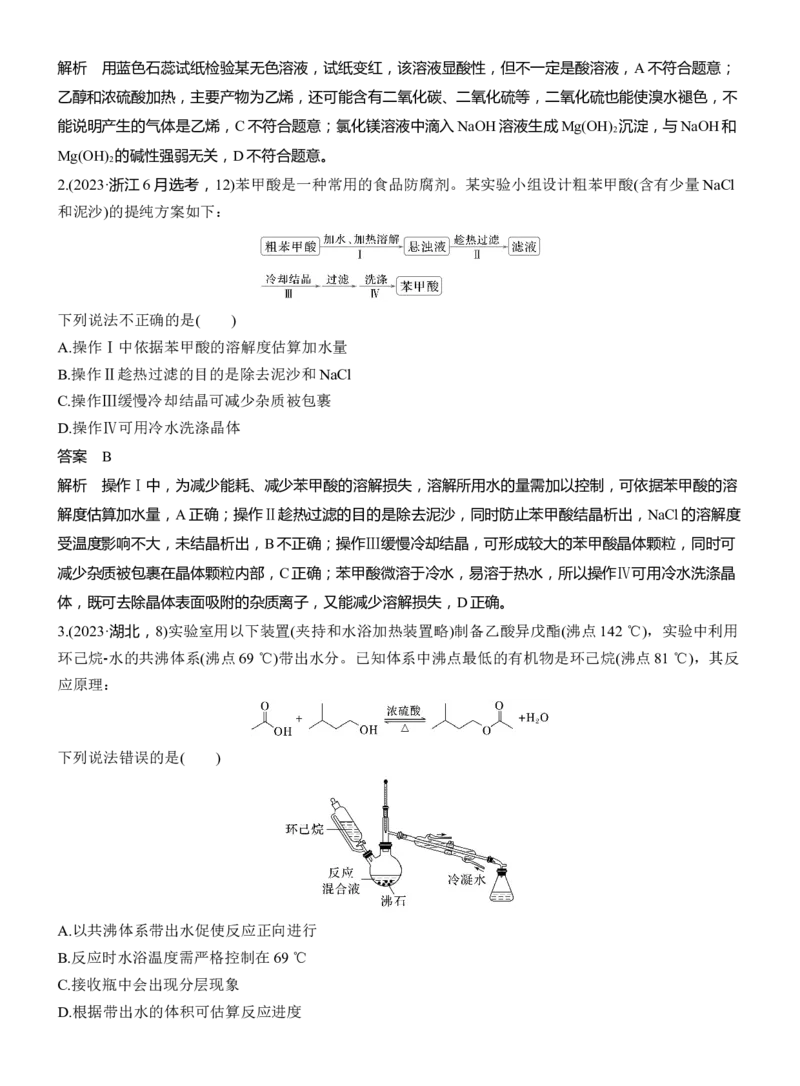
2.(2023·浙江6月选考,12)苯甲酸是一种常用的食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl
和泥沙)的提纯方案如下:
下列说法不正确的是( )
A.操作Ⅰ中依据苯甲酸的溶解度估算加水量
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaCl
C.操作Ⅲ缓慢冷却结晶可减少杂质被包裹
D.操作Ⅳ可用冷水洗涤晶体
答案 B
解析 操作Ⅰ中,为减少能耗、减少苯甲酸的溶解损失,溶解所用水的量需加以控制,可依据苯甲酸的溶
解度估算加水量,A正确;操作Ⅱ趁热过滤的目的是除去泥沙,同时防止苯甲酸结晶析出,NaCl的溶解度
受温度影响不大,未结晶析出,B不正确;操作Ⅲ缓慢冷却结晶,可形成较大的苯甲酸晶体颗粒,同时可
减少杂质被包裹在晶体颗粒内部,C正确;苯甲酸微溶于冷水,易溶于热水,所以操作Ⅳ可用冷水洗涤晶
体,既可去除晶体表面吸附的杂质离子,又能减少溶解损失,D正确。
3.(2023·湖北,8)实验室用以下装置(夹持和水浴加热装置略)制备乙酸异戊酯(沸点142 ℃),实验中利用
环己烷
⁃
水的共沸体系(沸点69 ℃)带出水分。已知体系中沸点最低的有机物是环己烷(沸点81 ℃),其反
应原理:
下列说法错误的是( )
A.以共沸体系带出水促使反应正向进行
B.反应时水浴温度需严格控制在69 ℃
C.接收瓶中会出现分层现象
D.根据带出水的体积可估算反应进度答案 B
解析 由反应方程式可知,生成物中含有水,若将水分离出去,可促进反应正向进行,该反应选择以共沸
体系带出水可以促使反应正向进行,A正确;产品的沸点为142 ℃,环己烷的沸点是81 ℃,环己烷⁃水的
共沸体系的沸点为69 ℃,温度可以控制在69~81 ℃之间,B错误;接收瓶中接收的是环己烷⁃水的共沸体
系,环己烷不溶于水,会出现分层现象,C正确;根据投料量,可估计生成水的体积,所以可根据带出水
的体积估算反应进度,D正确。
题型突破练 [分值:100 分]
(选择题1~5题,每小题2分,6~13题,每小题5分,共50分)
1.(2024·黑龙江齐齐哈尔三模)下列实验方法不能达到相应实验目的的是( )
选项 实验目的 实验方法
比较Na CO 和NaHCO 分别加热Na CO 和NaHCO 固体,将产生的
2 3 3 2 3 3
A
的热稳定性 气体通入澄清石灰水中,观察实验现象
向C H X中加入过量的NaOH溶液,加热一
2 5
验证C H X(X代表Cl、
2 5
B 段时间后静置,取少量上层清液于试管中,
Br、I)中卤素原子的种类
加入AgNO 溶液,观察实验现象
3
比较水分子中的氢原子和
相同条件下,用金属钠分别与水和乙醇反
C 乙醇羟基中的氢原子的活
应,观察实验现象
泼性
在试管中加入2 mL 10% NaOH溶液,滴入5
D 验证葡萄糖中含有醛基 滴5% CuSO 溶液,振荡后加入2 mL 10%葡
4
萄糖溶液,加热,观察实验现象
答案 B
解析 Na CO 受热不分解,澄清石灰水不会变浑浊,NaHCO 受热分解,产生的CO 能使澄清石灰水变浑
2 3 3 2
浊,说明热稳定性Na CO 强于NaHCO ,A正确;向C H X中加入过量的NaOH溶液,加热一段时间后静
2 3 3 2 5
置,取少量上层清液于试管中,直接加入AgNO 溶液,OH-会干扰X-的检验,无法确定卤代烃中卤素原子
3
的种类,B错误;钠与水反应非常剧烈,钠与乙醇反应较缓和,说明乙醇羟基中的氢原子不如水分子中的
氢原子活泼,C正确;在试管中加入2 mL 10% NaOH溶液,滴入5滴5% CuSO 溶液,振荡后加入2 mL
4
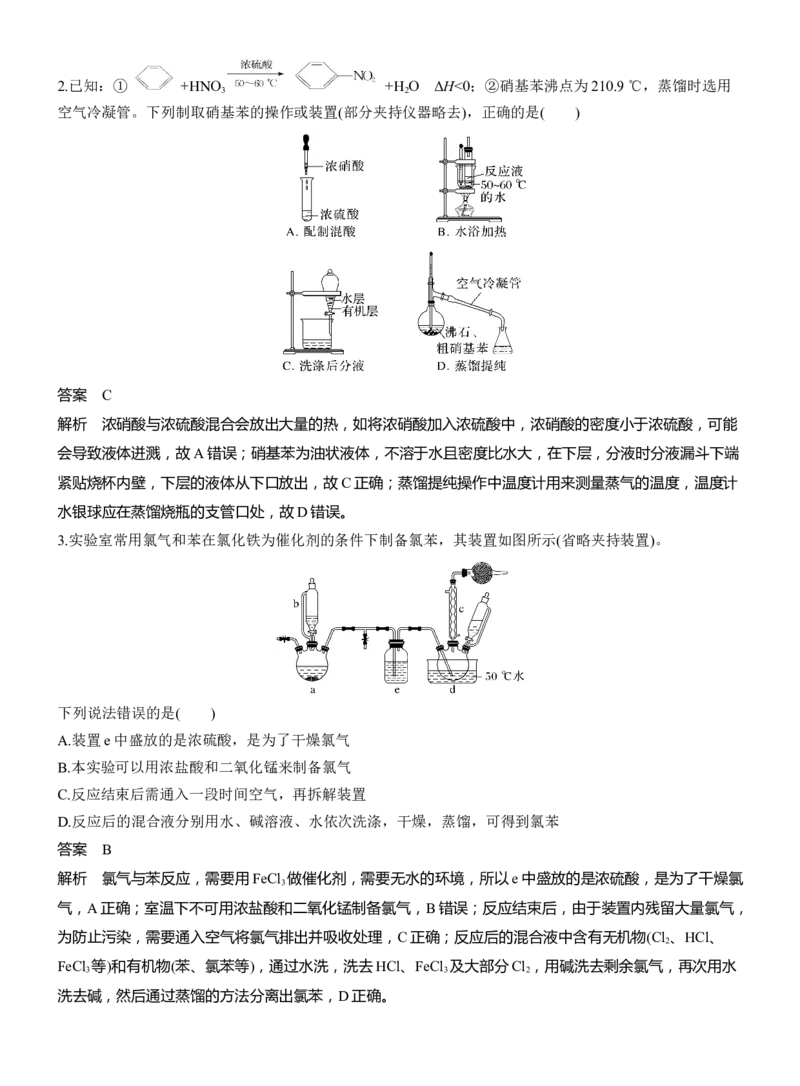
10%葡萄糖溶液,加热,有砖红色沉淀产生,说明葡萄糖中含有醛基,D正确。2.已知:① +HNO +H O ΔH<0;②硝基苯沸点为210.9 ℃,蒸馏时选用
3 2
空气冷凝管。下列制取硝基苯的操作或装置(部分夹持仪器略去),正确的是( )
答案 C
解析 浓硝酸与浓硫酸混合会放出大量的热,如将浓硝酸加入浓硫酸中,浓硝酸的密度小于浓硫酸,可能
会导致液体迸溅,故A错误;硝基苯为油状液体,不溶于水且密度比水大,在下层,分液时分液漏斗下端
紧贴烧杯内壁,下层的液体从下口放出,故C正确;蒸馏提纯操作中温度计用来测量蒸气的温度,温度计
水银球应在蒸馏烧瓶的支管口处,故D错误。
3.实验室常用氯气和苯在氯化铁为催化剂的条件下制备氯苯,其装置如图所示(省略夹持装置)。
下列说法错误的是( )
A.装置e中盛放的是浓硫酸,是为了干燥氯气
B.本实验可以用浓盐酸和二氧化锰来制备氯气
C.反应结束后需通入一段时间空气,再拆解装置
D.反应后的混合液分别用水、碱溶液、水依次洗涤,干燥,蒸馏,可得到氯苯
答案 B
解析 氯气与苯反应,需要用FeCl 做催化剂,需要无水的环境,所以e中盛放的是浓硫酸,是为了干燥氯
3
气,A正确;室温下不可用浓盐酸和二氧化锰制备氯气,B错误;反应结束后,由于装置内残留大量氯气,
为防止污染,需要通入空气将氯气排出并吸收处理,C正确;反应后的混合液中含有无机物(Cl 、HCl、
2
FeCl 等)和有机物(苯、氯苯等),通过水洗,洗去HCl、FeCl 及大部分Cl ,用碱洗去剩余氯气,再次用水
3 3 2
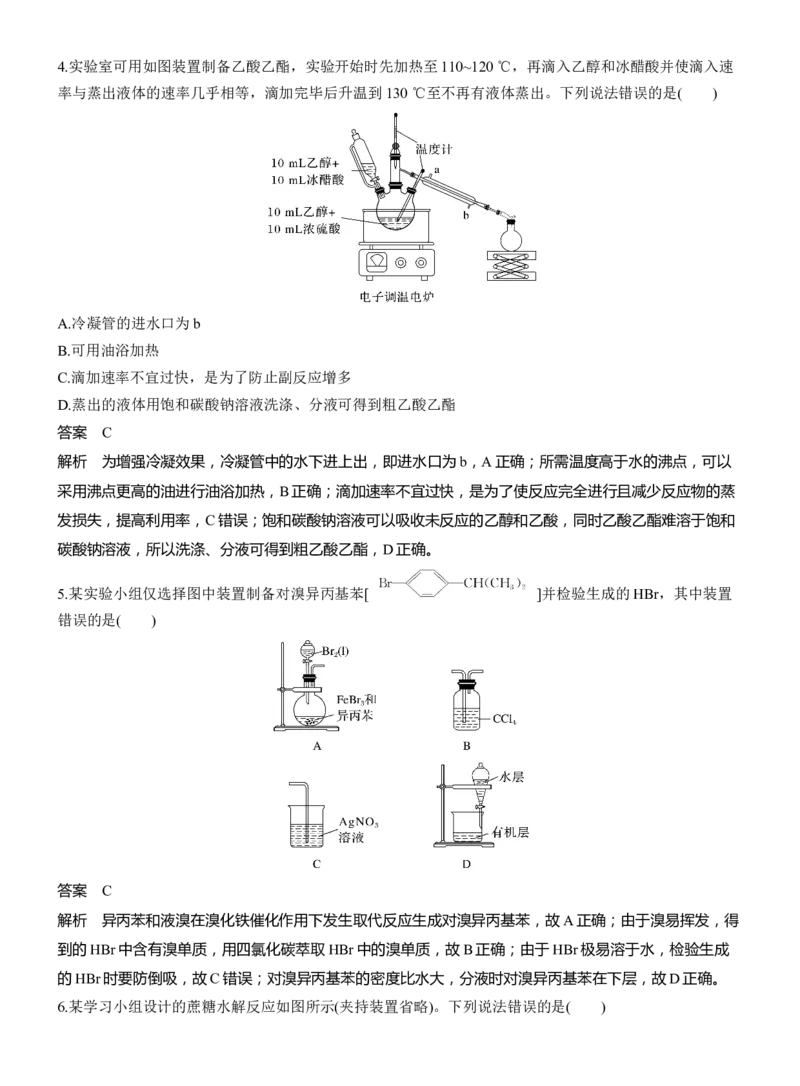
洗去碱,然后通过蒸馏的方法分离出氯苯,D正确。4.实验室可用如图装置制备乙酸乙酯,实验开始时先加热至110~120 ℃,再滴入乙醇和冰醋酸并使滴入速
率与蒸出液体的速率几乎相等,滴加完毕后升温到130 ℃至不再有液体蒸出。下列说法错误的是( )
A.冷凝管的进水口为b
B.可用油浴加热
C.滴加速率不宜过快,是为了防止副反应增多
D.蒸出的液体用饱和碳酸钠溶液洗涤、分液可得到粗乙酸乙酯
答案 C
解析 为增强冷凝效果,冷凝管中的水下进上出,即进水口为b,A正确;所需温度高于水的沸点,可以
采用沸点更高的油进行油浴加热,B正确;滴加速率不宜过快,是为了使反应完全进行且减少反应物的蒸
发损失,提高利用率,C错误;饱和碳酸钠溶液可以吸收未反应的乙醇和乙酸,同时乙酸乙酯难溶于饱和
碳酸钠溶液,所以洗涤、分液可得到粗乙酸乙酯,D正确。
5.某实验小组仅选择图中装置制备对溴异丙基苯[ ]并检验生成的HBr,其中装置
错误的是( )
答案 C
解析 异丙苯和液溴在溴化铁催化作用下发生取代反应生成对溴异丙基苯,故A正确;由于溴易挥发,得
到的HBr中含有溴单质,用四氯化碳萃取HBr中的溴单质,故B正确;由于HBr极易溶于水,检验生成
的HBr时要防倒吸,故C错误;对溴异丙基苯的密度比水大,分液时对溴异丙基苯在下层,故D正确。
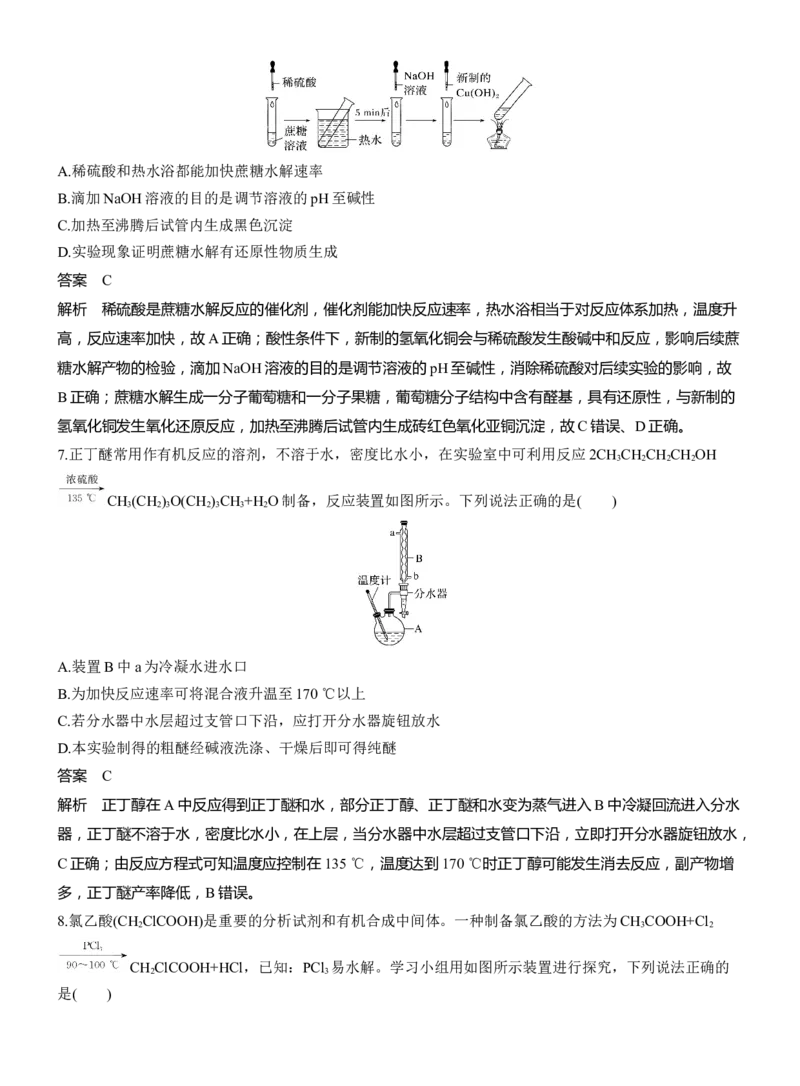
6.某学习小组设计的蔗糖水解反应如图所示(夹持装置省略)。下列说法错误的是( )A.稀硫酸和热水浴都能加快蔗糖水解速率
B.滴加NaOH溶液的目的是调节溶液的pH至碱性
C.加热至沸腾后试管内生成黑色沉淀
D.实验现象证明蔗糖水解有还原性物质生成
答案 C
解析 稀硫酸是蔗糖水解反应的催化剂,催化剂能加快反应速率,热水浴相当于对反应体系加热,温度升
高,反应速率加快,故A正确;酸性条件下,新制的氢氧化铜会与稀硫酸发生酸碱中和反应,影响后续蔗
糖水解产物的检验,滴加NaOH溶液的目的是调节溶液的pH至碱性,消除稀硫酸对后续实验的影响,故
B正确;蔗糖水解生成一分子葡萄糖和一分子果糖,葡萄糖分子结构中含有醛基,具有还原性,与新制的
氢氧化铜发生氧化还原反应,加热至沸腾后试管内生成砖红色氧化亚铜沉淀,故C错误、D正确。
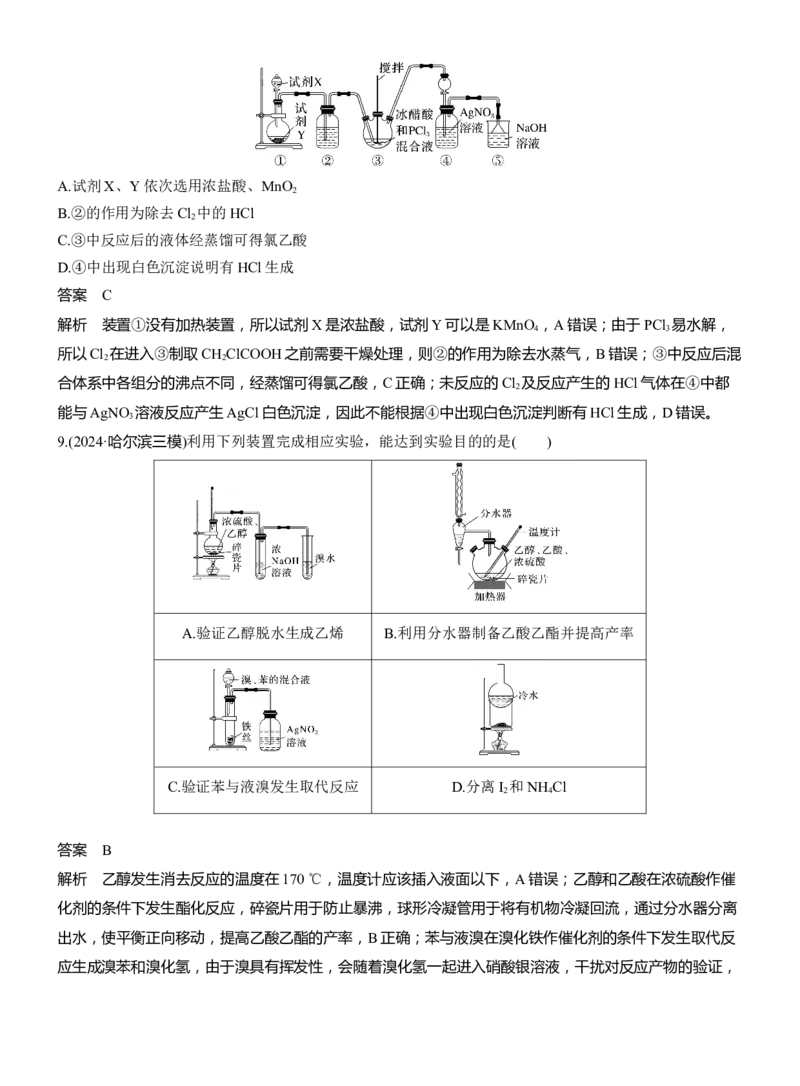
7.正丁醚常用作有机反应的溶剂,不溶于水,密度比水小,在实验室中可利用反应2CH CH CH CH OH
3 2 2 2
CH (CH ) O(CH ) CH +H O制备,反应装置如图所示。下列说法正确的是( )
3 2 3 2 3 3 2
A.装置B中a为冷凝水进水口
B.为加快反应速率可将混合液升温至170 ℃以上
C.若分水器中水层超过支管口下沿,应打开分水器旋钮放水
D.本实验制得的粗醚经碱液洗涤、干燥后即可得纯醚
答案 C
解析 正丁醇在A中反应得到正丁醚和水,部分正丁醇、正丁醚和水变为蒸气进入B中冷凝回流进入分水
器,正丁醚不溶于水,密度比水小,在上层,当分水器中水层超过支管口下沿,立即打开分水器旋钮放水,
C正确;由反应方程式可知温度应控制在135 ℃,温度达到170 ℃时正丁醇可能发生消去反应,副产物增
多,正丁醚产率降低,B错误。
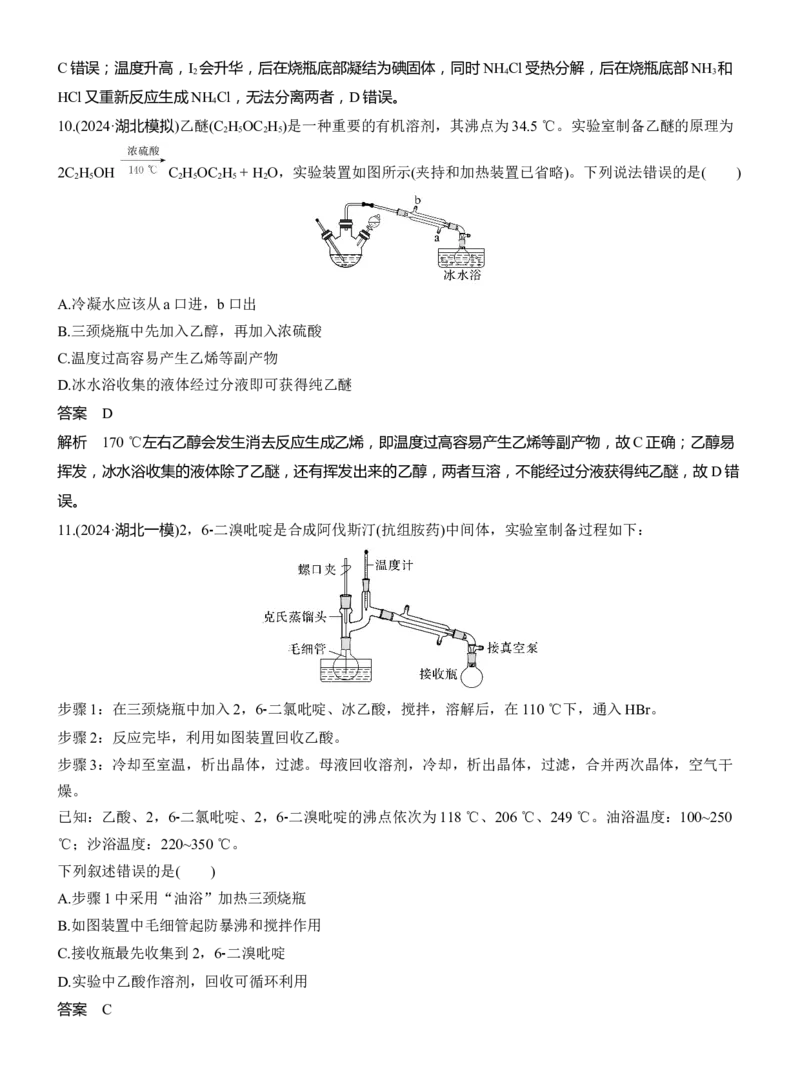
8.氯乙酸(CH ClCOOH)是重要的分析试剂和有机合成中间体。一种制备氯乙酸的方法为CH COOH+Cl
2 3 2
CH ClCOOH+HCl,已知:PCl 易水解。学习小组用如图所示装置进行探究,下列说法正确的
2 3
是( )A.试剂X、Y依次选用浓盐酸、MnO
2
B.②的作用为除去Cl 中的HCl
2
C.③中反应后的液体经蒸馏可得氯乙酸
D.④中出现白色沉淀说明有HCl生成
答案 C
解析 装置①没有加热装置,所以试剂X是浓盐酸,试剂Y可以是KMnO ,A错误;由于PCl 易水解,
4 3
所以Cl 在进入③制取CH ClCOOH之前需要干燥处理,则②的作用为除去水蒸气,B错误;③中反应后混
2 2
合体系中各组分的沸点不同,经蒸馏可得氯乙酸,C正确;未反应的Cl 及反应产生的HCl气体在④中都
2
能与AgNO 溶液反应产生AgCl白色沉淀,因此不能根据④中出现白色沉淀判断有HCl生成,D错误。
3
9.(2024·哈尔滨三模)利用下列装置完成相应实验,能达到实验目的的是( )
A.验证乙醇脱水生成乙烯 B.利用分水器制备乙酸乙酯并提高产率
C.验证苯与液溴发生取代反应 D.分离I 和NH Cl
2 4
答案 B
解析 乙醇发生消去反应的温度在170 ℃,温度计应该插入液面以下,A错误;乙醇和乙酸在浓硫酸作催
化剂的条件下发生酯化反应,碎瓷片用于防止暴沸,球形冷凝管用于将有机物冷凝回流,通过分水器分离
出水,使平衡正向移动,提高乙酸乙酯的产率,B正确;苯与液溴在溴化铁作催化剂的条件下发生取代反
应生成溴苯和溴化氢,由于溴具有挥发性,会随着溴化氢一起进入硝酸银溶液,干扰对反应产物的验证,C错误;温度升高,I 会升华,后在烧瓶底部凝结为碘固体,同时NH Cl受热分解,后在烧瓶底部NH 和
2 4 3
HCl又重新反应生成NH Cl,无法分离两者,D错误。
4
10.(2024·湖北模拟)乙醚(C H OC H )是一种重要的有机溶剂,其沸点为34.5 ℃。实验室制备乙醚的原理为
2 5 2 5
2C H OH C H OC H + H O,实验装置如图所示(夹持和加热装置已省略)。下列说法错误的是( )
2 5 2 5 2 5 2
A.冷凝水应该从a口进,b口出
B.三颈烧瓶中先加入乙醇,再加入浓硫酸
C.温度过高容易产生乙烯等副产物
D.冰水浴收集的液体经过分液即可获得纯乙醚
答案 D
解析 170 ℃左右乙醇会发生消去反应生成乙烯,即温度过高容易产生乙烯等副产物,故C正确;乙醇易
挥发,冰水浴收集的液体除了乙醚,还有挥发出来的乙醇,两者互溶,不能经过分液获得纯乙醚,故D错
误。
11.(2024·湖北一模)2,6⁃ 二溴吡啶是合成阿伐斯汀(抗组胺药)中间体,实验室制备过程如下:
步骤1:在三颈烧瓶中加入2,6⁃ 二氯吡啶、冰乙酸,搅拌,溶解后,在110 ℃下,通入HBr。
步骤2:反应完毕,利用如图装置回收乙酸。
步骤3:冷却至室温,析出晶体,过滤。母液回收溶剂,冷却,析出晶体,过滤,合并两次晶体,空气干
燥。
已知:乙酸、2,6⁃ 二氯吡啶、2,6⁃ 二溴吡啶的沸点依次为118 ℃、206 ℃、249 ℃。油浴温度:100~250
℃;沙浴温度:220~350 ℃。
下列叙述错误的是( )
A.步骤1中采用“油浴”加热三颈烧瓶
B.如图装置中毛细管起防暴沸和搅拌作用
C.接收瓶最先收集到2,6⁃ 二溴吡啶
D.实验中乙酸作溶剂,回收可循环利用
答案 C解析 步骤1反应温度为110 ℃,在油浴温度范围内,A项正确;通过调节螺口夹,微量空气进入烧瓶,
产生的小气泡可起到防暴沸、搅拌等作用,B项正确;蒸馏时沸点最低的物质最先汽化,接收瓶最先收集
到乙酸,C项错误;步骤1中2,6⁃二氯吡啶溶于乙酸,乙酸作溶剂,回收乙酸可循环利用,D项正确。
12.(2024·黑龙江三模)实验室初步分离苯甲酸乙酯、苯甲酸和环己烷的流程如下:
已知:苯甲酸乙酯的沸点为212.6 ℃,“乙醚
⁃
环己烷
⁃
水共沸物”的沸点为62.1 ℃。
下列说法错误的是( )
A.操作a为分液
B.操作b中需用到直形冷凝管
C.无水MgSO 的作用是干燥有机相2
4
D.“洗涤”苯甲酸,用乙醇的效果比用蒸馏水好
答案 D
解析 向苯甲酸乙酯、苯甲酸和环己烷的混合物中加入碳酸钠溶液,苯甲酸与碳酸钠反应生成苯甲酸钠、
水和二氧化碳,分液后得到有机相1和水相1;苯甲酸乙酯的沸点为212.6 ℃,“乙醚⁃环己烷⁃水共沸物”
的沸点为62.1 ℃,蒸馏(操作b)后得到有机相2和共沸物,向有机相2中加入无水硫酸镁,用于除去有机相
中的少量水;向水相1中加入乙醚萃取少量的有机物进入有机相,分液后得到水相2,水相2中的主要成
分为苯甲酸钠,加入硫酸可反应生成苯甲酸,经过滤后得到苯甲酸粗品,再经重结晶得到纯净的苯甲酸。
苯甲酸在乙醇中的溶解度大于其在水中的溶解度,“洗涤”苯甲酸,用蒸馏水的效果比用乙醇好,D错误。
13.(2024·黑龙江大庆模拟)实验室中初步分离环己醇、苯酚、苯甲酸混合液的流程如图。下列说法错误的是
( )
A.环己醇、苯酚、苯甲酸粗产品依次由①、②、③获得
B.若试剂a为碳酸钠,可以通过观察气泡现象控制试剂用量
C.“操作X”为蒸馏,“试剂b”可选用盐酸或CO
2
D.试剂c可以选用盐酸或硫酸答案 B
解析 实验室中初步分离环己醇、苯酚、苯甲酸混合液,先向混合液中加入碳酸氢钠溶液,苯甲酸与碳酸
氢钠反应生成苯甲酸钠进入水相Ⅰ,苯甲酸钠用稀盐酸或硫酸调节pH酸化可以得到苯甲酸,进一步处理
得产品③为苯甲酸,有机相Ⅰ中有环己醇和苯酚,可以加入氢氧化钠或碳酸钠将苯酚转化为苯酚钠使其进
入水相Ⅱ,调节pH进一步处理后得产品②为苯酚,则有机相Ⅱ为环己醇,通过洗涤、干燥等进一步处理
可分离出产品①环己醇。由分析知,有机相Ⅰ中有环己醇和苯酚,苯酚和碳酸钠反应得碳酸氢钠,没有气
泡产生,B错误;操作X是分离出环己醇,可以用蒸馏的方法,试剂b将苯酚钠转化为苯酚,可以用盐酸
或CO ,C正确;试剂c是将苯甲酸钠转化为苯甲酸,故试剂c可以选用盐酸或硫酸,D正确。
2