文档内容
专题十五 盐类的水解 基础过关检测
考试时间:70分钟 卷面分值:100分
学校:___________姓名:___________班级:___________考号:___________
注意事项:
1.答题前,务必将自己的姓名、考号填写在答题卡规定的位置上。
2.答选择题时,必须使用2B铅笔将答题卡上对应题目的答案标号涂黑。如需改动,用
橡皮擦擦干净后,再选涂其它答案标号。
3.答非选择题时,必须将答案书写在专设答题页规定的位置上。
4.所有题目必须在答题卡上作答。在试题卷上答题无效。
5.考试结束后,只交试卷答题页。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
选择题(本题含20小题,每题5分,共100分。每题只有一个选项符合题意)
1.(2023秋·上海普陀·高三校考期末)室温下,通过下列实验探究NaHCO 溶液的性
3
质。
实验1 用pH试纸测得0.1 NaHCO 溶液的pH约为8;
3
实验2 向0.1 NaHCO 溶液滴入等浓度Ba(OH) 溶液至恰好完全反应;
3 2
实验3 向0.1 NaHCO 溶液中加入等体积0.1 NaOH溶液;
3
实验4 向浓NaHCO 溶液中加入浓Al (SO ) 溶液,有气体和沉淀生成;
3 2 4 3
下列说法错误的是
A.实验1的溶液中存在c(HCO)>c(CO )
2 3
B.实验2过程中,水的电离程度先逐渐增大,然后逐渐减小
C.实验3反应后的溶液中存在c(OH-)=c(H+)+c(HCO )+c(H CO)
2 3
D.实验4所生成的气体一定是CO
2
【答案】C
【详解】A.0.1 NaHCO 溶液中pH约为8,则说明碳酸氢根离子水解大于电离,
3
水解反应为: ,电离反应为: ,所以
c(HCO)>c(CO ),A正确;
2 3B.向0.1 NaHCO 溶液滴入等浓度Ba(OH) 溶液至恰好完全反应,则发生离子
3 2
反应为: ,滴入过程中先变成碳酸根离子,水解程度
先增大,随意碳酸根离子与钡离子结合后氢氧根离子过量,所以随后水的电离程度会
逐渐减小,B正确;
C.向0.1 NaHCO 溶液中加入等体积0.1 NaOH溶液,会生成碳酸钠溶
3
液,溶液中存在质子守恒,即c(OH-)=c(H+)+c(HCO )+2c(H CO),C错误;
2 3
D.向浓NaHCO 溶液中加入浓Al (SO ) 溶液,溶质会发生双水解,生成氢氧化铝和
3 2 4 3
二氧化碳,D正确;
故选C。
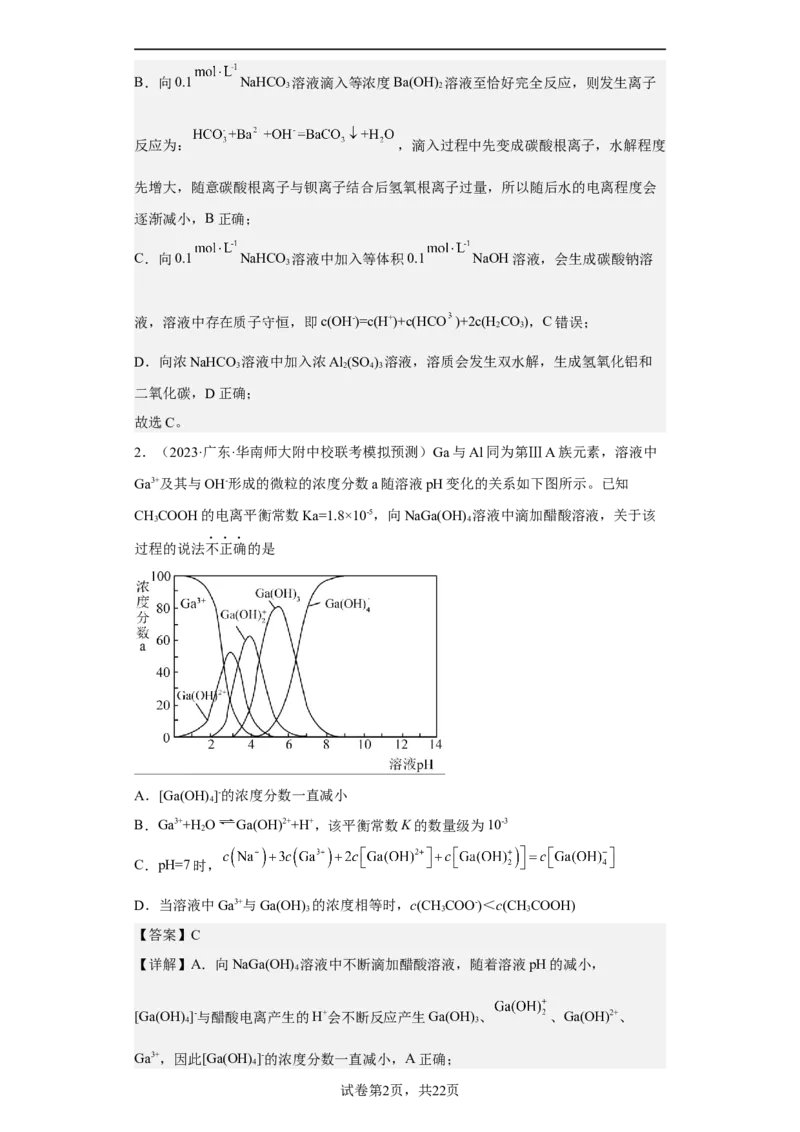
2.(2023·广东·华南师大附中校联考模拟预测)Ga与Al同为第ⅢA族元素,溶液中
Ga3+及其与OH-形成的微粒的浓度分数a随溶液pH变化的关系如下图所示。已知
CHCOOH的电离平衡常数Ka=1.8×10-5,向NaGa(OH) 溶液中滴加醋酸溶液,关于该
3 4
过程的说法不正确的是
A.[Ga(OH)]-的浓度分数一直减小
4
B.Ga3++H O Ga(OH)2++H+,该平衡常数K的数量级为10-3
2
C.pH=7时,
D.当溶液中Ga3+与Ga(OH) 的浓度相等时,c(CHCOO-)<c(CHCOOH)
3 3 3
【答案】C
【详解】A.向NaGa(OH) 溶液中不断滴加醋酸溶液,随着溶液pH的减小,
4
[Ga(OH)]-与醋酸电离产生的H+会不断反应产生Ga(OH) 、 、Ga(OH)2+、
4 3
Ga3+,因此[Ga(OH)]-的浓度分数一直减小,A正确;
4
试卷第2页,共22页B.反应Ga3++H O Ga(OH)2++H+的平衡常数K= ,由图可知,在
2
溶液pH=2.5左右时c[Ga(OH)2+]=c(Ga3+),此时K=c(H+)=10-2.5,所以平衡常数K的数量
级为10-3,B正确;
C.在室温下,pH=7时的溶液显中性,c(H+)=c(OH-),根据溶液中存在电荷守恒可得关
系式: +c(CHCOO-),故
3
,C错误;
D.由图可知:当溶液中Ga3+与Ga(OH) 的浓度相等时,溶液pH=3.5,溶液显酸性,
3
说明CHCOOH的电离作用大于CHCOO-的水解作用,故微粒浓度关系为:
3 3
c(CHCOO-)<c(CHCOOH),D正确;
3 3
故合理选项是C。
3.(2022秋·黑龙江牡丹江·高三牡丹江一中校考期末)下面的问题中,与盐类水解有
关的是
①为保存 溶液,要在溶液中加入少量盐酸
②实验室盛放 溶液的试剂瓶应用橡胶塞
③在 或 溶液中加入镁条会产生气泡
④配制 溶液时加入铁粉
⑤向 溶液中加入CuO调节pH,可除去溶液中混有的
A.只有①②⑤ B.只有①②③ C.只有①②③⑤ D.只有①②④⑤
【答案】C
【详解】①亚铁离子水解显酸性,加入盐酸抑制亚铁离子的水解,与盐类水解有关,
故①正确;
②碳酸根离子水解使溶液显碱性,和玻璃中的二氧化硅反应,生成的硅酸钠是矿物胶,
粘结瓶口和瓶塞,故应用橡胶塞,与盐类水解有关,故②正确;
③铵根离子、铝离子水解显酸性,和镁反应生成氢气,与盐类水解有关,故③正确;
④Fe2+易被空气中的氧气氧化物Fe3+,而Fe具有还原性,能把Fe3+还有成Fe2+,因此可
以防止FeSO 被氧化而变质,与盐类水解无关,故④错误;
4⑤向CuCl 溶液中加入CuO,调节pH,促进Fe3+的水解生成氢氧化铁,可除去溶液中
2
混有的Fe3+,与盐类水解有关,故⑤正确;
综上,正确的有①②③⑤;
答案选C。
4.(2023·广东·华南师大附中校联考模拟预测)肼( )又称联氨,为二元弱碱,与
硫酸反应可生成 、 。下列说法正确的是
A.室温下0.01mol/L 水溶液
B.稀释0.01mol/L 水溶液, 升高
C. 的水溶液中存在:
D.水溶液中 的电离方程式为
【答案】D
【详解】A.肼( )为二元弱碱,故室温下0.01mol/L 水溶液中氢氧根浓度小
于0.02mol/L, ,A错误;
B.稀释0.01mol/L 水溶液,虽促进了肼的电离,但溶液被稀释,氢氧根浓度减小,
故 降低,B错误;
C. 的水溶液中存在质子守恒,即 ,C错误;
D. 属于盐且是强电解质,所以水溶液中的电离方程式为
,D正确;
故选D。
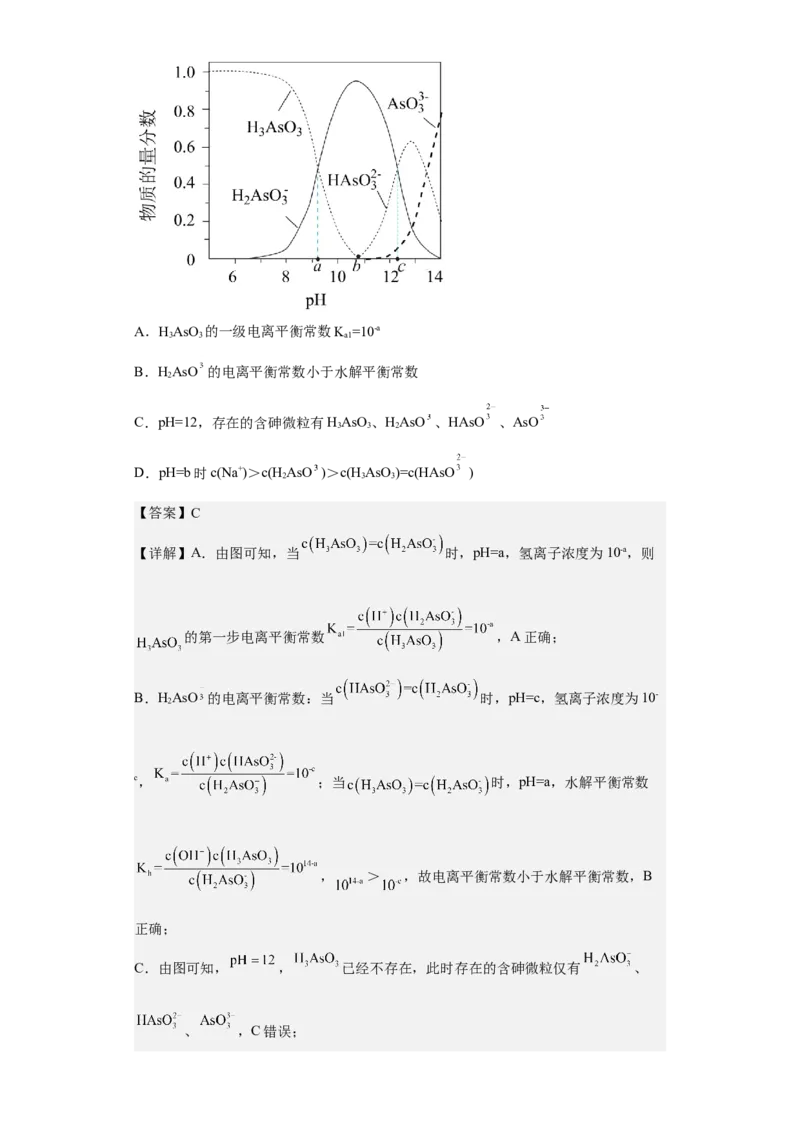
5.(2023秋·河北邢台·高三邢台市第二中学校考期末)三元弱酸亚砷酸(H AsO )在溶
3 3
液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示。向
1mol•L-1HAsO 溶液中滴加NaOH溶液,关于该过程的说法错误的是
3 3
试卷第4页,共22页A.HAsO 的一级电离平衡常数K =10-a
3 3 a1
B.HAsO 的电离平衡常数小于水解平衡常数
2
C.pH=12,存在的含砷微粒有HAsO 、HAsO 、HAsO 、AsO
3 3 2
D.pH=b时c(Na+)>c(HAsO )>c(HAsO )=c(HAsO )
2 3 3
【答案】C
【详解】A.由图可知,当 时,pH=a,氢离子浓度为10-a,则
的第一步电离平衡常数 ,A正确;
B.HAsO 的电离平衡常数:当 时,pH=c,氢离子浓度为10-
2
c, ;当 时,pH=a,水解平衡常数
, > ,故电离平衡常数小于水解平衡常数,B
正确;
C.由图可知, , 已经不存在,此时存在的含砷微粒仅有 、
、 ,C错误;D.由图可知, 时 浓度最大且 ,则此时溶质主
要为 ,故有 ,D正确;
故选B。
6.(2023秋·江苏南通·高三统考期末)铜、银位于周期表中第ⅠB族。铜、硫酸铜、
硝酸银、银氨溶液是实验室常用的含铜或银的化学试剂。从废定影液[主要含有 、
、 、 等微粒]中回收Ag和 的主要步骤:向该废定影液中加入
氢氧化钠调节pH在7.5~8.5之间,然后再加入稍过量 溶液沉银,过滤、洗涤及干
燥,灼烧 制Ag;滤液中通入 氧化 ,用苯萃取分液。下列有关从废定影液
中回收Ag和 的说法正确的是
A.过滤时,为加快滤液流下,可以用玻璃棒搅拌漏斗中的液体
B.配制 溶液时,向其中加入少量NaOH溶液, 的值增大
C.灼烧 生成 和 ,该反应每生成 转移3mol电子
D.分液时,先放出水层,再从分液漏斗下口放出含有苯和溴的有机层
【答案】C
【详解】A.过滤时,不能用玻璃棒搅拌漏斗中的液体,防止滤纸破损,A错误;
B.配制 溶液时,向其中加入少量NaOH溶液,可抑制硫离子水解,但氢氧根浓
度增大的更多, 的值减小,B错误;
C.灼烧 生成 和 ,S元素化合价从-2价升高到+4价,失去6个电子,所
以该反应每生成 ,同时有0.5mol硫元素被氧化,转移3mol电子,C正确;
D.分液时,先放出水层,再从分液漏斗上口倒出含有苯和溴的有机层,D错误;
试卷第6页,共22页答案选C。
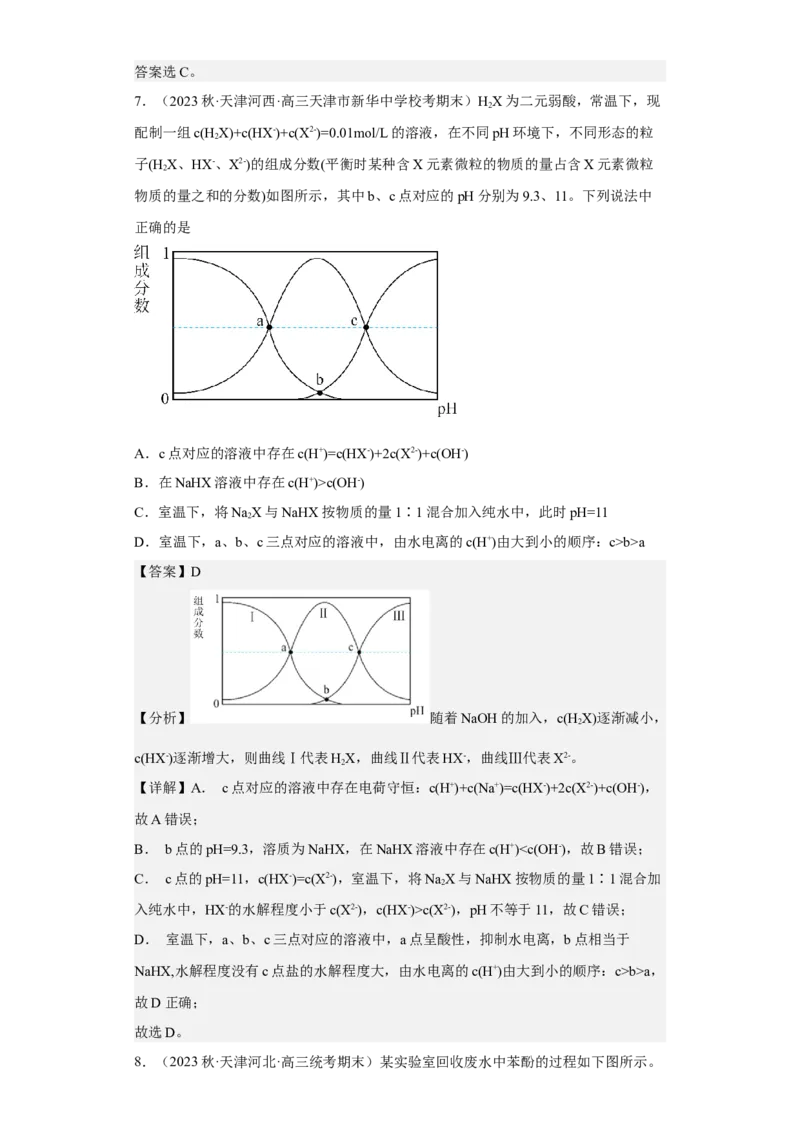
7.(2023秋·天津河西·高三天津市新华中学校考期末)HX为二元弱酸,常温下,现
2
配制一组c(HX)+c(HX-)+c(X2-)=0.01mol/L的溶液,在不同pH环境下,不同形态的粒
2
子(H X、HX-、X2-)的组成分数(平衡时某种含X元素微粒的物质的量占含X元素微粒
2
物质的量之和的分数)如图所示,其中b、c点对应的pH分别为9.3、11。下列说法中
正确的是
A.c点对应的溶液中存在c(H+)=c(HX-)+2c(X2-)+c(OH-)
B.在NaHX溶液中存在c(H+)>c(OH-)
C.室温下,将NaX与NaHX按物质的量1∶1混合加入纯水中,此时pH=11
2
D.室温下,a、b、c三点对应的溶液中,由水电离的c(H+)由大到小的顺序:c>b>a
【答案】D
【分析】 随着NaOH的加入,c(HX)逐渐减小,
2
c(HX-)逐渐增大,则曲线Ⅰ代表HX,曲线Ⅱ代表HX-,曲线Ⅲ代表X2-。
2
【详解】A. c点对应的溶液中存在电荷守恒:c(H+)+c(Na+)=c(HX-)+2c(X2-)+c(OH-),
故A错误;
B. b点的pH=9.3,溶质为NaHX,在NaHX溶液中存在c(H+)c(X2-),pH不等于11,故C错误;
D. 室温下,a、b、c三点对应的溶液中,a点呈酸性,抑制水电离,b点相当于
NaHX,水解程度没有c点盐的水解程度大,由水电离的c(H+)由大到小的顺序:c>b>a,
故D正确;
故选D。
8.(2023秋·天津河北·高三统考期末)某实验室回收废水中苯酚的过程如下图所示。已知:苯酚的电离常数 , 的电离常数 ,
。
下列有关说法正确的是
A. 溶液中存在:
B.若反应1后溶液中存在 ,此时溶液中
C.反应2通入少量 时,离子方程式为
D.反应2中通入 至溶液 时,此时溶液中存在
【答案】D
【分析】苯酚与苯互溶得到有机层和水层,操作1为分液,反应1中苯酚与碳酸钠溶
液反应生成苯酚钠,操作2为分液,得到水层含苯酚钠,反应2中苯酚钠溶液与二氧
化碳反应生成苯酚,操作3为分液,分离出苯酚;
【详解】A. 溶液中存在质子守恒:
,A错误;
B.反应1中苯酚与碳酸钠溶液反应生成C HONa,存在物料守恒
6 5
,则c(Na CO):c(C HOH)=1:1,碳酸根离子存在
2 3 6 5
水解平衡,第一步水解常数为 ,苯酚的电离常数
试卷第8页,共22页,说明碳酸钠的水解程度大于苯酚的电离程度,则生成碳酸氢根离子浓
度大于苯酚根离子,此时溶液中 ,B错误;
C.根据弱酸的电离平衡常数越大其酸性越强,已知苯酚和碳酸的电离常数可知酸性:
> > ,反应2通入少量 时生成苯酚和碳酸氢钠,离子方程式为
,C错误;
D.苯酚的电离常数 ,当 时,
c(H+)=1.0×10-10mol/L,此时pH=10,D正确;
故选:D。
9.(2023秋·山东菏泽·高三校考期末)常温下,弱酸 与弱碱 分别用强碱或
强酸调节 时,HA、 、MOH和 的分布分数 与溶液 的关系如图所示。
已知:以 分子为例,存在 。下列说法正确的是
A. 付电离常数
B.等物质的量浓度的 与 溶液中:
C.等物质的量㳖度的 和 的混合溶液中
D. 的 与 的混合溶液及 的 与 的混合溶液中,后者
大于前者【答案】C
【分析】M+、MOH分布分数相同时,c(M+)=c(MOH),MOH的电离常数K (MOH)=
b
=10-4.75;HA分布分数相同时,pH=4.75,
c(A-)=c(HA),HA电离平衡常数K (HA)= ×c(H+)=c(H+)=10-4.75mol/L,A-的水解
a
平衡常数K = mol/L=10-9.25mol·L-1。
h
【详解】A. M+、MOH分布分数相同时,c(M+)=c(MOH),MOH的电离常数
K (MOH)= =10-4.75,故A错误;
b
B. 等物质的量浓度的 与 溶液中存在电荷守恒
物料守恒 ,消去得
,故B错误;
C. 是强酸弱碱盐,水解后呈碱性,等物质的量㳖度的 和 的混合溶液中
,故C正确;
D. 温度不变电离平衡常数不变,pH=8的溶液中c(H+)一定,K (HA)= ×c(H+)
a
中 一定,所以两种混合溶液中δ(HA)相同,故D错误;
故选C。
10.(2022秋·北京·高三统考期末)食醋中含有醋酸等有机酸及少量氨基酸。食醋的
酸度是指每 食醋中含酸(均折合成醋酸计)的质量。国家标准规定酿造食醋酸度
试卷第10页,共22页不得低于 。可用滴定法测定食醋的酸度。某小组同学量取 自制食
醋样品稀释至 (溶液几乎无色),每次量取 于锥形瓶中,加入
中性甲醛溶液(掩蔽氨基的碱性),以酚酞为指示剂,用 标准溶液
滴定,滴定管读数记录如下表。
溶液的体积 第一次 第二次 第三次
滴定前 溶液的体积读数 0.00 1.00 2.00
滴定后 溶液的体积读数 9.90 11.00 12.10
下列说法不正确的是A.醋酸易溶于水与“醋酸分子和水分子之间能形成氢键”有关
B.锥形瓶中溶液由无色变为粉红色,且半分钟内不褪色时停止滴定
C.该自制食醋样品的酸度不符合国家标准
D.若不加甲醛溶液,测定结果会偏低
【答案】C
【详解】A.醋酸分子与水分子间可以形成氢键,所以醋酸易溶于水,A正确;
B.达到滴定终点时,锥形瓶中溶液由无色变为粉红色,且半分钟内不褪色,B正确;
C.三次平均消耗的NaOH体积为
mL=10.00mL,根据CHCOOH+NaOH=CH COONa+H O, 自制食醋中醋酸的
3 3 2
物质的量为 ,酸度为 =6g/
100mL> ,符合国家标准,C错误;
D.若不加甲醛溶液,由于氨基的碱性,导致所需的NaOH偏少,测定结果会偏低,D
正确;
故选C。
11.(2022秋·河南驻马店·高三统考期末)常温下,下列有关电解质溶液的叙述正确
的是
A.向0.1mol·L-1的HF溶液中演加NaOH溶液至中性:c(Na+)=c(F-)=c(H+)=c(OH-)
B.0.1mol·L-1的HC O 溶液中:c(HC O )>c(H C O)>c(C O )
2 2 4 2 2 2 4 2
C.0.1mol·L-1的NaHS溶液中:c(HS-)+c(S2-)=0.1mol·L-1D.0.1mol·L-1的NH HPO 溶液中:c(H+)+c(H PO )>c(NH·H O)+c(HPO )+c(PO )
4 2 4 3 4 3 2
【答案】D
【详解】A.向0.1mol·L-1的HF溶液中演加NaOH溶液至中性,所得为NaF、HF的混
合溶液,溶质主要为NaF、含少量HF,按电荷守恒可知:c(Na+)=c(F-)>
c(H+)=c(OH-),A错误;
B.HC O 难电离,一级电离为主,则0.1mol·L-1的HC O 溶液中:c(HC O)>
2 2 4 2 2 4 2 2 4
c(HC O )>c(C O ),B错误;
2 2
C.NaHS溶液中HS-既电离又水解 ,按物料守恒可知,0.1mol·L-1的NaHS溶液中:
c(HS)+c(HS-)+c(S2-)=0.1mol·L-1,C错误;
2
D.0.1mol·L-1的NH HPO 溶液中,电荷守恒:
4 2 4
,物料守恒:
,二式合并可得:
c(H+)+c(H PO )= c(OH-)+c(NH·H O)+c(HPO )+2c(PO ),则c(H+)+c(H PO )>
3 4 3 2 3 4
c(NH ·H O)+c(HPO )+c(PO ),D正确;
3 2
答案选D。
12.(2022秋·山东济宁·高三统考期末) 溶液中存在以下两个平衡
(25℃)
(25℃)
25℃时, 溶液中
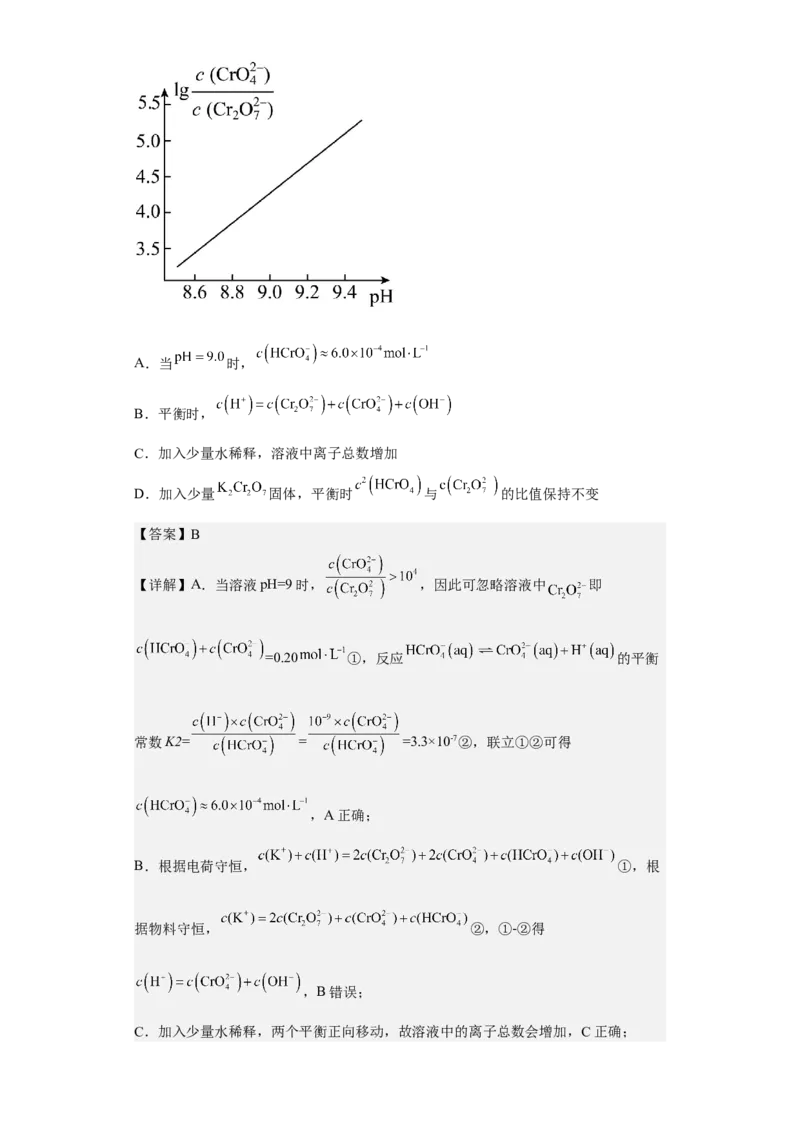
随pH的变化关系如图,下列选项错误的是
试卷第12页,共22页A.当 时,
B.平衡时,
C.加入少量水稀释,溶液中离子总数增加
D.加入少量 固体,平衡时 与 的比值保持不变
【答案】B
【详解】A.当溶液pH=9时, ,因此可忽略溶液中 即
=0.20 ①,反应 的平衡
常数K2= = =3.3×10-7②,联立①②可得
,A正确;
B.根据电荷守恒, ①,根
据物料守恒, ②,①-②得
,B错误;
C.加入少量水稀释,两个平衡正向移动,故溶液中的离子总数会增加,C正确;D.平衡时 =K ,溶液中的反应的平衡常数只与温度有关,与浓度无关,故
1
比值应不变,D正确;
故选B。
13.(2022秋·江苏扬州·高三统考期末)常温下,用如图1所示装置,分别向
25mL0.3mol•L-1NaCO 溶液和25mL0.3mol•L-1NaHCO 溶液中逐滴滴加0.3mol•L-1的稀
2 3 3
盐酸,用压强传感器测得压强随盐酸体积的变化曲线如图2所示。下列说法正确的是
A.X曲线为NaCO 溶液的滴定曲线
2 3
B.b点的溶液中:2c(Na+)=3c(CO )+3c(HCO )+3c(H CO)
2 3
C.用pH试纸测得c点的pH约为8,可知:K (H CO)<
a2 2 3
D.a、d两点水的电离程度:a7
A.实验1得到的溶液中:
B.实验2混合后的溶液中存在:
C.实验3所得溶液中:
D.实验4反应过程中水的电离程度逐渐减小
【答案】A
【详解】A.向10mL1.0mol/LNaOH溶液通入 首先发生反应生成亚硫酸钠,为强
碱弱酸盐,溶液显碱性;继续通入二氧化硫反应生成亚硫酸氢钠,其水解常数为
试卷第16页,共22页,其电离大于水解,溶液显酸性;反
应后得到的溶液pH=7,则溶液中溶质以亚硫酸钠为主,故: ,A
正确;
B.实验2混合后的溶液中根据物料守恒可知:
,B错误;
C.实验3所得溶液中根据电荷守恒可知,
,C错误;
D.酸和碱均会已知水的电离,实验4反应过程中亚硫酸氢钠和氢氧化钠恰好反应生成
硫酸钠时,水的电离程度最大;氢氧化钠过量后又会已知水的电离,故水的电离程度
先增大后减小,D错误;
故选A。
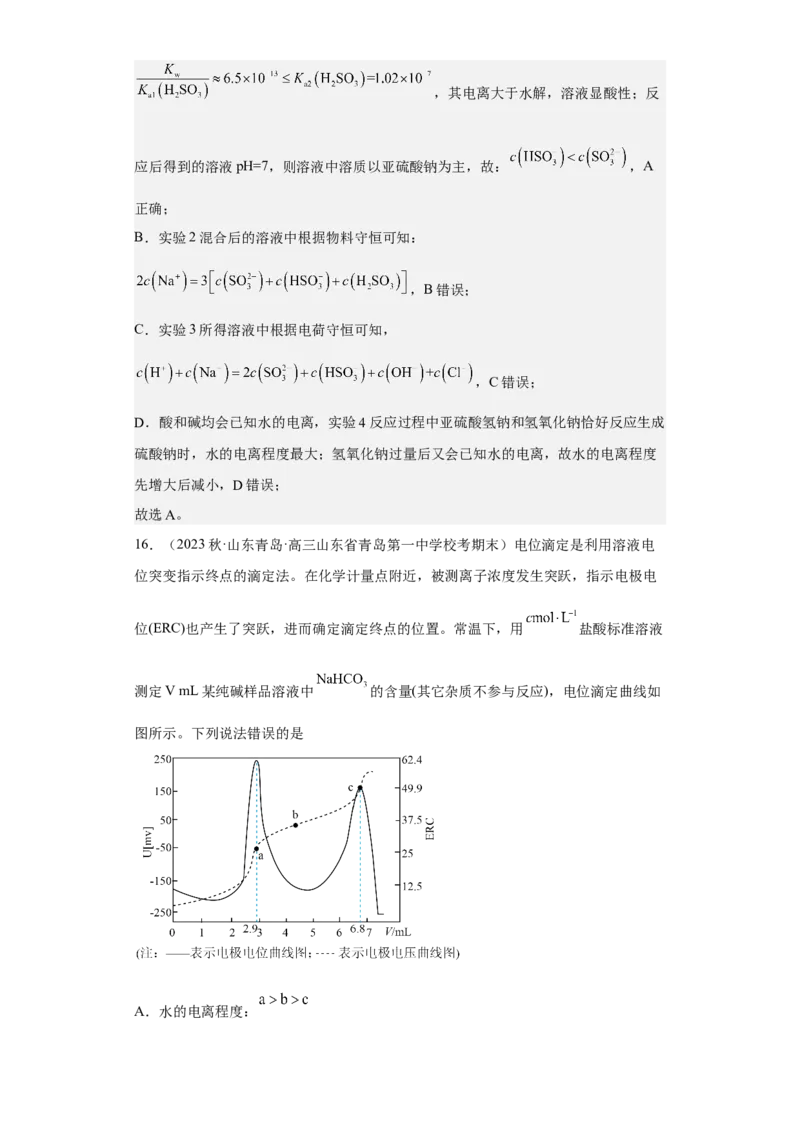
16.(2023秋·山东青岛·高三山东省青岛第一中学校考期末)电位滴定是利用溶液电
位突变指示终点的滴定法。在化学计量点附近,被测离子浓度发生突跃,指示电极电
位(ERC)也产生了突跃,进而确定滴定终点的位置。常温下,用 盐酸标准溶液
测定V mL某纯碱样品溶液中 的含量(其它杂质不参与反应),电位滴定曲线如
图所示。下列说法错误的是
A.水的电离程度:B.a点溶液中存在关系:
C.V mL该纯碱样品溶液中含有 的质量为0.084c g
D.c点指示的是第二滴定终点,b到c过程中存在
【答案】D
【分析】由图可知a点为第一个计量点,反应为: ,c点为第二个计
量点,反应为: ,
【详解】A.水解促进水的电离,由以上分析得a点时,溶液中存在能水解的 ,
随着加入盐酸的量的增加, 逐渐减少,生成CO,所以水的电离程度逐渐减弱,
2
c点时, 完全转化为CO 和水,水的电离程度不被促进,则水的电离程度
2
,故A正确;
B.a点为第一个计量点,反应为: ,a点的溶质为NaCl、
NaHCO ,溶液中存在物料守恒: ,故B
3
正确;
C.滴定的两个计量点的反应中,若没有 杂质,两个计量点消耗的盐酸应相等,
根据两个计量点的反应,可以推得,第二个计量点的反应中的 包括反应生成
的和杂质,所以杂质 的量可以根据多消耗的盐酸计算:(6.8-2.9)mL×10-3×c
mol/L×84g/mol=0.084c g,故C正确;
D.在整个滴定过程中,参加反应的离子是 ,溶液中的Na+不参加反
应,守恒不变,c点位第二个滴定终点,消耗盐酸最多的点,所以在c点之前盐酸不足,
则 ,故D错误;
试卷第18页,共22页故答案选D。
17.(2023秋·河南商丘·高三商丘市回民中学校考期末)已知常温下浓度为
的几种溶液的 如下表。下列有关说法正确的是
溶
质
7.5 11.6 9.7 8.3
A.相同温度相同浓度下,酸性由强到弱的顺序为
B. 的水解平衡常数为
C.将 通入 溶液至溶液呈中性,则溶液中:
D.等物质的量浓度的 和 混合溶液中粒子浓度大小关系为
【答案】A
【详解】A.相同温度下,相同浓度的强碱弱酸盐碱性越强说明弱酸根离子水解程度
越大,对应的酸酸性越弱,由表中的数据可得酸性由强到弱的顺序为
,故A正确;
B.常温下0.1mol/L的NaF溶液 =7.5,则 ,溶液中存在水解平
衡 ,则F-的水解平衡常数为
,故B错误;
C.将 通入 溶液,溶液中存在电荷守恒:,溶液呈中性 ,所以
,故C错误;
D. HF的电离平衡常数
,而水解平衡常
数 ,所以等物质的量浓度的 和 混合溶液中F-的水解程度小于HF
的电离程度,则溶液中粒子浓度大小关系为 ,故D
错误;
故答案为:A。
18.(2023秋·湖南长沙·高三统考期末)25℃时,往 溶液中滴
入 溶液,体系中 、 、 溶液的体积与溶液pH
的关系如图所示。下列说法正确的是
A.曲线②表示 与溶液pH的关系
B.a点对应的溶液中:
C.b点对应的溶液中:
D.25℃时,HA的电离平衡常数的数量级为
试卷第20页,共22页【答案】C
【详解】A.往 溶液中滴入 溶液,发生反应:
,体系中 随溶液 的增大而增大, 随溶
液 的增大而减小,故曲线①表示 与溶液 的关系,A错误;
B. 点对应的溶液中存在 和 两种溶质,且二者的物质的量之比为 ,该溶
液中的电荷守恒式为 ,物料守恒式为
,联立电荷守恒式及物料守恒式可得:
,B错误;
C.b点对应的溶液 即 ,结合电荷守恒式可得溶液中:
,故 ,C正确;
D.曲线①、曲线②的交点处有 ,即 , 的电离
平衡常数 ,其数量级为 ,D错误;
答案选C。
19.(2022秋·黑龙江牡丹江·高三牡丹江一中校考期末)已知 为二元弱酸,常
温下将0.1 mol·L 的NaOH溶液滴入20 mL 0.1 mol·L 的 溶液中,溶液中
(或 )的分布系数 、NaOH溶液体积V与pH的关系如图所示[已知
]。下列叙述错误的是A.曲线b表示的是 的分布系数变化曲线
B.n点对应的溶液中,
C. 的水解平衡常数的数量级为
D.在n、p、q三点中,水的电离程度最大的是q点
【答案】C
【分析】0.1 mol·L 的NaOH溶液滴入20 mL 0.1 mol·L 的 溶液中,由反应
的方程式: ,可知,随着氢氧化钠的加入,
增大, 减小,故a曲线代表 ,b曲线代表 ,其余曲线为
滴定曲线,据此分析。
【详解】A.由上述分析可知,a曲线代表 ,b曲线代表 ,A正确;
B.在n点溶液中,溶质为浓度相等的 和 ,则电荷守恒:
;
物料守恒: ;
两式相减,消去钠离子,得 ,溶
液显酸性,氢离子浓度大于氢氧根浓度,故 ,B正
确;
C.根据m点, 与 的分布系数相等,即 = ,pH=4.2,可
试卷第22页,共22页知: ,故 ,
数量级为 ,C错误;
D.由滴定过程可知:n点加10mlNaOH,溶质为 和 ,且二者的浓度
相等;p点pH=7,溶为 和 (少量);q点加入20mlNaOH,溶质为
, 越多水解程度越大,水的电离程度越大,故水离程度最大是q点 ,
D正确;
故本题选C。
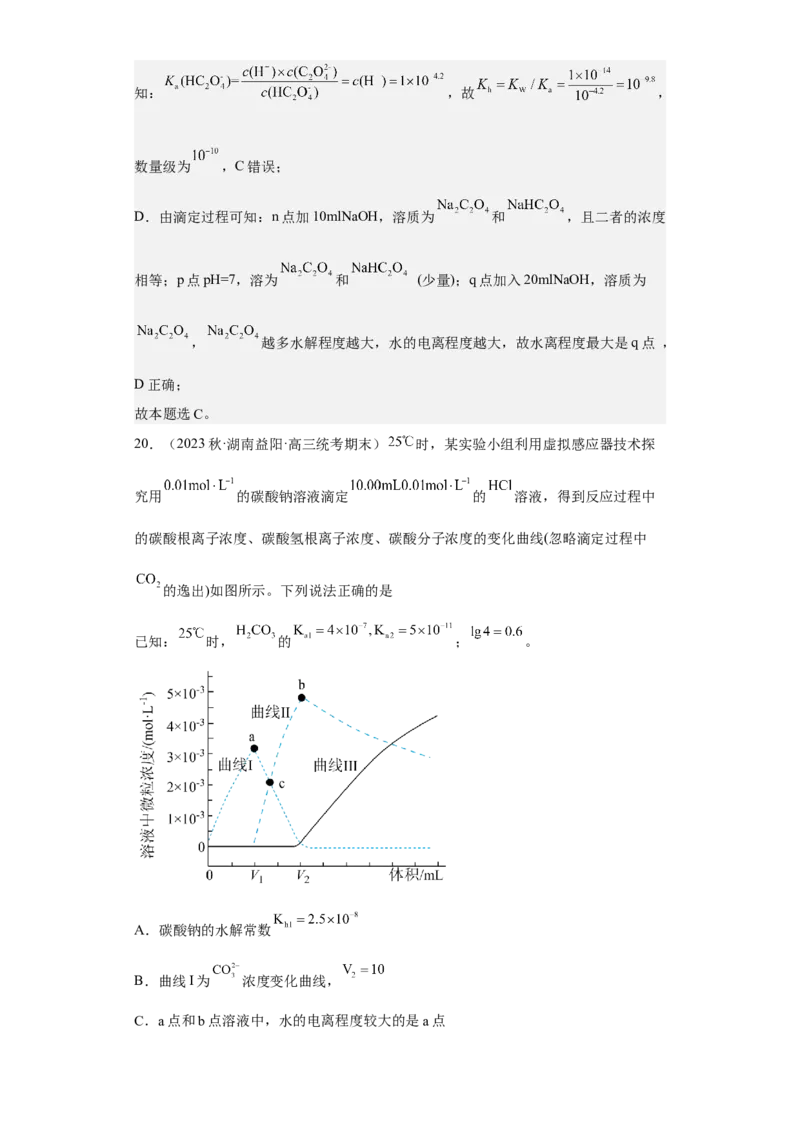
20.(2023秋·湖南益阳·高三统考期末) 时,某实验小组利用虚拟感应器技术探
究用 的碳酸钠溶液滴定 的 溶液,得到反应过程中
的碳酸根离子浓度、碳酸氢根离子浓度、碳酸分子浓度的变化曲线(忽略滴定过程中
的逸出)如图所示。下列说法正确的是
已知: 时, 的 ; 。
A.碳酸钠的水解常数
B.曲线I为 浓度变化曲线,
C.a点和b点溶液中,水的电离程度较大的是a点D.c点溶液
【答案】D
【分析】向 的盐酸溶液中滴加 的碳酸钠溶液,溶液中
依次发生反应: 、 ,故
溶液中 先增大后减小,当盐酸完全反应后,滴加碳酸钠溶液过程中,
逐渐增大,当 反应完全后, 溶液过量, 逐渐增大,
因此曲线Ⅰ为 浓度变化曲线,曲线Ⅱ为 浓度变化曲线,曲线Ⅲ为 浓
度变化曲线,据此分析解答。
【详解】A. 时,碳酸钠的
,A错误;
B.根据分析, 的总反应为 ,根据化学方程式可
知, ,解得 ,B错误;
C.酸会抑制水的电离,能水解的盐会促进水的电离,a点的溶质为 ,b
点的溶质为 ,因此b点溶液中水的电离程度较大,C错误;
D.c点溶液中 ,溶液中 ,溶液
,D正确;
故选D。
二、多选题(共0分)
试卷第24页,共22页21.(2023秋·山东烟台·高三统考期末)室温下,向一定浓度的 溶液中滴加盐
酸,溶液中lg 、lg 、lg 随溶液酸度 的
变化如图所示。下列说法错误的是
A. 的
B.室温下, 溶液显碱性
C. 时, c(Cl-)+c(OH-)+5c(PO )+c(H PO )> c(Na+)+c(H+)
2
D.随着 的增大, 不断增大
【答案】CD
【分析】室温下,向一定浓度的 溶液中滴加盐酸,随着氢离子浓度变大,磷酸
根离子依次反应转变为 、 、 ,则曲线ⅠⅡⅢ分别为 、lg
、lg ;当 时,AG=-0.4,则 ,则
的 ;同理, 、 ;
【详解】A.由分析可知, 的 ,A正确;
B. 的水解常数为 ,则水解大于电离,溶液显碱性,B正确;C.由电荷守恒可知,c(Na+)+c(H+)= c(OH-)+c(Cl-)+ c(HPO )+2c(HPO )+3c(PO ),由
2
图可知 时,c(HPO )>c(PO ),则c(Na+)+c(H+)> c(Cl-)+c(OH-)+5c(PO )
+c(H PO ),C错误;
2
D. ,故随着 的增大,
不变,D错误;
故选CD。
试卷第26页,共22页