文档内容
绝密 ★ 启用前
2021 年普通高等学校招生全国统一考试
班级
姓名
化 学
准考证号
A.图1装置:检验有丙烯生成
注意事项:
考场号
此卷只 B.图2装置:除去二氧化碳中的少量氯化氢气体
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答题前,考生务必将自己
装订座不位密号封
的姓名、考生号填写在答题卡上。 C.图3装置:验证乙炔的还原性
2.回答第Ⅰ卷时,选出每小题的答案后,用铅笔把答题卡上对应题目的答案标号涂黑,
D.图4装置:验证浓硫酸具有强氧化性
如需改动,用橡皮擦干净后,再选涂其他答案标号。写在试卷上无效。
3.回答第Ⅱ卷时,将答案填写在答题卡上,写在试卷上无效。 3.设N
A
为阿伏加德罗常数的值,下列有关叙述正确的是
4.考试结束,将本试卷和答题卡一并交回。
A.标准状况下,11.2L环戊烯中含有双键的数目为0.5N
A
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 P 31 S 32 Cl 35.5
B.用惰性电极电解1L 0.2mol·L−1 AgNO 溶液,当两极产生气体的物质的量相等时,阴极得到
3
的气体体积为2.24L
一、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项是符
C.常温下,2L pH=1的HCl溶液中,H+数目为0.2N
A
合题目要求的。
D.1mol Na与足量O 反应,生成NaO和NaO 的混合物,钠失去电子数为2N
2 2 2 2 A
1.下列对有关文献的理解错误的是
4.不能正确表示下列反应的离子方程式是
A.《天工开物》记载:“每炉甘石(碳酸锌)十斤,装载入一泥罐内,....然后逐层用碳饼垫
A.在氯化亚铁溶液中通入氧气:4Fe2++O +4H+=4Fe3++2H O
盛,发火煅烧,.....,冷定毁罐取出,即倭铅”。“泥封”的主要目的是防止得到的锌被氧化 2 2
B.用石墨作阴极、铁作阳极电解饱和食盐水:2Cl−+2H O=====2OH−+Cl↑+H ↑
B.《物理小识》记载“青矾(绿矾)厂气熏人,衣服当之易烂,栽木不没,“气”凝即得“矾 2 2 2
油”。青矾厂气是SO 和SO
2 3
C.向稀硝酸中加入少量FeS:
C.《开宝本草》中记载了中药材铁华粉的制作方法:“取钢煅作时如笏或团,平面磨错令光净,
D.NaAlO 溶液中通入过量CO:AlO+CO+2H O=Al(OH) ↓+HCO
以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣。”中药材铁华粉是醋酸亚铁 2 2 2 2 3
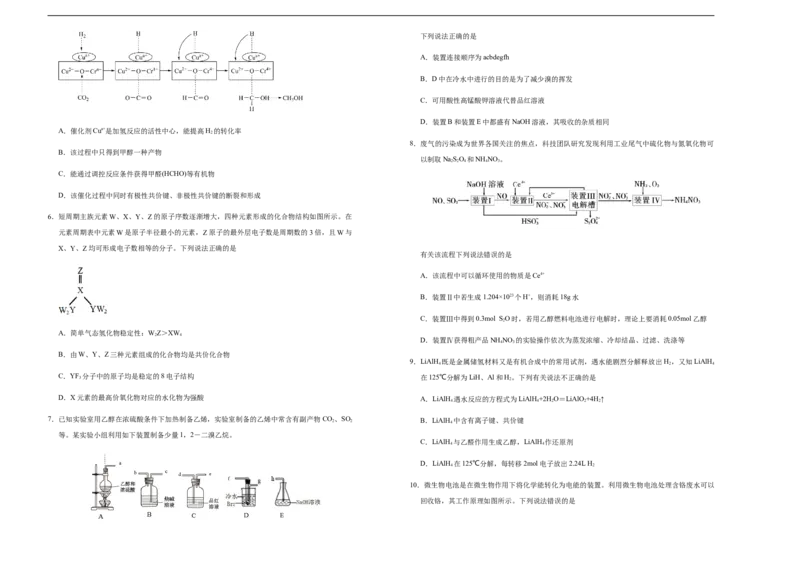
5.某科研小组采用铜基催化剂(Cua+,其中a=0或者1),CO 多步加氢合成甲醇,其合成反应历
D.《淮南子·万比术》所载“曾青得铁则化铜”是火法炼铜的先驱 2
程如下。下列说法中正确的是
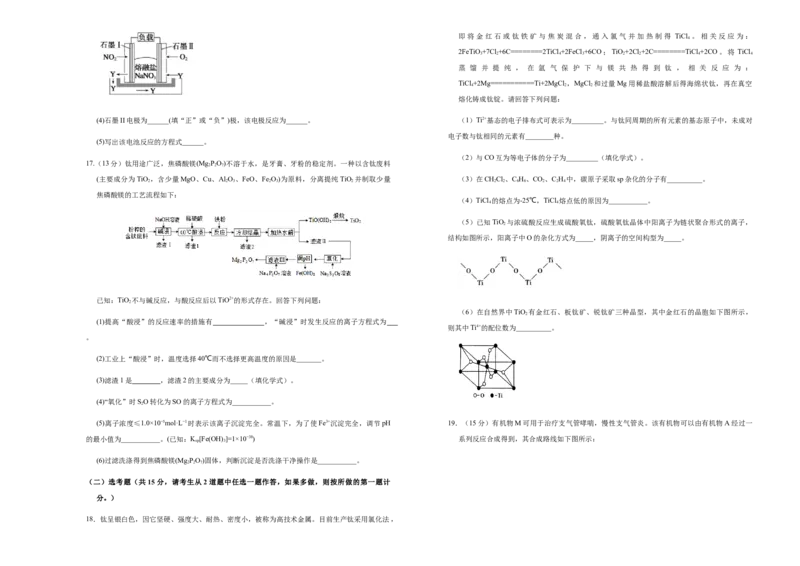
2.室温时用下列实验装置进行相应实验,能达到目的的是下列说法正确的是
A.装置连接顺序为acbdegfh
B.D中在冷水中进行的目的是为了减少溴的挥发
C.可用酸性高锰酸钾溶液代替品红溶液
D.装置B和装置E中都盛有NaOH溶液,其吸收的杂质相同
A.催化剂Cua+是加氢反应的活性中心,能提高H 的转化率
2
8.废气的污染成为世界各国关注的焦点,科技团队研究发现利用工业尾气中硫化物与氮氧化物可
B.该过程中只得到甲醇一种产物
以制取NaSO 和NH NO 。
2 2 4 4 3
C.能通过调控反应条件获得甲醛(HCHO)等有机物
D.该催化过程中同时有极性共价键、非极性共价键的断裂和形成
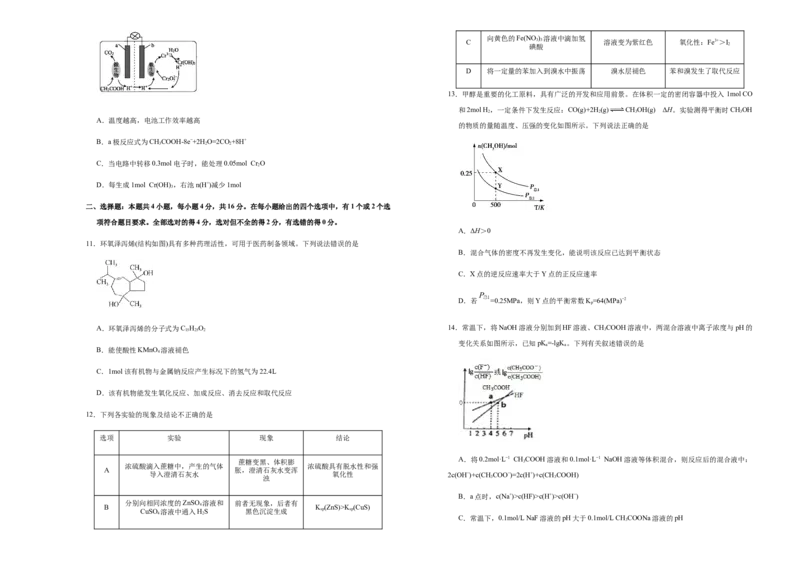
6.短周期主族元素W、X、Y、Z的原子序数逐渐增大,四种元素形成的化合物结构如图所示。在
元素周期表中元素W是原子半径最小的元素,Z原子的最外层电子数是周期数的3倍,且W与
X、Y、Z均可形成电子数相等的分子。下列说法正确的是
有关该流程下列说法错误的是
A.该流程中可以循环使用的物质是Ce4+
B.装置Ⅱ中若生成1.204×1023个H+,则消耗18g水
C.装置Ⅲ中得到0.3mol SO时,若用乙醇燃料电池进行电解时,理论上要消耗0.05mol乙醇
2
A.简单气态氢化物稳定性:WZ>XW
2 4
D.装置Ⅳ获得粗产品NH NO 的实验操作依次为蒸发浓缩、冷却结晶、过滤、洗涤等
4 3
B.由W、Y、Z三种元素组成的化合物均是共价化合物
9.LiAlH 既是金属储氢材料又是有机合成中的常用试剂,遇水能剧烈分解释放出H ,又知LiAlH
4 2 4
C.YF 3 分子中的原子均是稳定的8电子结构 在125℃分解为LiH、Al和H 2 。下列有关说法不正确的是
D.X元素的最高价氧化物对应的水化物为强酸 A.LiAlH 遇水反应的方程式为LiAlH +2H O=LiAlO +4H ↑
4 4 2 2 2
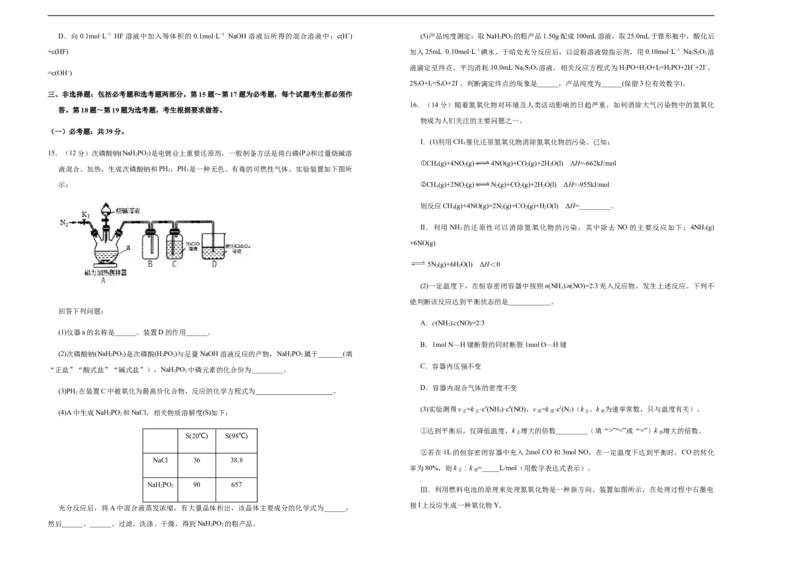
7.已知实验室用乙醇在浓硫酸条件下加热制备乙烯,实验室制备的乙烯中常含有副产物CO 2 、SO 2 B.LiAlH 4 中含有离子键、共价键
等。某实验小组利用如下装置制备少量1,2-二溴乙烷。
C.LiAlH 与乙醛作用生成乙醇,LiAlH 作还原剂
4 4
D.LiAlH 在125℃分解,每转移2mol电子放出2.24L H
4 2
10.微生物电池是在微生物作用下将化学能转化为电能的装置。利用微生物电池处理含铬废水可以
回收铬,其工作原理如图所示。下列说法错误的是向黄色的Fe(NO ) 溶液中滴加氢
C 3 3 溶液变为紫红色 氧化性:Fe3+>I
碘酸 2
D 将一定量的苯加入到溴水中振荡 溴水层褪色 苯和溴发生了取代反应
13.甲醇是重要的化工原料,具有广泛的开发和应用前景。在体积一定的密闭容器中投入 1mol CO
和2mol H,一定条件下发生反应:CO(g)+2H(g) CHOH(g) ΔH。实验测得平衡时CHOH
2 2 3 3
A.温度越高,电池工作效率越高
的物质的量随温度、压强的变化如图所示。下列说法正确的是
B.a极反应式为CHCOOH-8e−+2H O=2CO+8H+
3 2 2
C.当电路中转移0.3mol电子时,能处理0.05mol Cr O
2
D.每生成1mol Cr(OH) ,右池n(H+)减少1mol
3
二、选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,有1个或2个选
项符合题目要求。全部选对的得4分,选对但不全的得2分,有选错的得0分。
A.ΔH>0
11.环氧泽泻烯(结构如图)具有多种药理活性,可用于医药制备领域。下列说法错误的是
B.混合气体的密度不再发生变化,能说明该反应已达到平衡状态
C.X点的逆反应速率大于Y点的正反应速率
D.若 =0.25MPa,则Y点的平衡常数K=64(MPa)−2
p
A.环氧泽泻烯的分子式为C H O 14.常温下,将NaOH溶液分别加到HF溶液、CHCOOH溶液中,两混合溶液中离子浓度与pH的
15 25 2 3
变化关系如图所示,已知pK=-lgK。下列有关叙述错误的是
a a
B.能使酸性KMnO 溶液褪色
4
C.1mol该有机物与金属钠反应产生标况下的氢气为22.4L
D.该有机物能发生氧化反应、加成反应、消去反应和取代反应
12.下列各实验的现象及结论不正确的是
选项 实验 现象 结论
A.将0.2mol·L−1 CHCOOH溶液和0.1mol·L−1 NaOH溶液等体积混合,则反应后的混合液中:
蔗糖变黑、体积膨 3
浓硫酸滴入蔗糖中,产生的气体 浓硫酸具有脱水性和强
A 胀,澄清石灰水变浑
导入澄清石灰水 氧化性 2c(OH−)+c(CH COO−)=2c(H+)+c(CH COOH)
浊 3 3
B.a点时,c(Na+)>c(HF)>c(H+)>c(OH−)
分别向相同浓度的ZnSO 溶液和 前者无现象,后者有
B 4 K (ZnS)>K (CuS)
CuSO 溶液中通入HS 黑色沉淀生成 sp sp
4 2
C.常温下,0.1mol/L NaF溶液的pH大于0.1mol/L CH COONa溶液的pH
3D.向0.1mol·L−1 HF溶液中加入等体积的0.1mol·L−1 NaOH溶液后所得的混合溶液中:c(H+) (5)产品纯度测定:取NaH PO 的粗产品1.50g配成100mL溶液,取25.0mL于锥形瓶中,酸化后
2 2
+c(HF) 加入25mL 0.10mol·L−1碘水,于暗处充分反应后,以淀粉溶液做指示剂,用0.10mol·L−1 Na SO 溶
2 2 3
液滴定至终点,平均消耗10.0mL Na SO 溶液,相关反应方程式为HPO+H O+I =H PO+2H++2I−,
2 2 3 2 2 2 2
=c(OH−)
2SO+I =S O+2I−。判断滴定终点的现象是______,产品纯度为______(保留3位有效数字)。
2 2 4
三、非选择题:包括必考题和选考题两部分。第15题~第17题为必考题,每个试题考生都必须作
16.(14分)随着氮氧化物对环境及人类活动影响的日趋严重,如何消除大气污染物中的氮氧化
答。第18题~第19题为选考题,考生根据要求做答。
物成为人们关注的主要问题之一。
(一)必考题:共39分。
I.(1)利用CH 催化还原氮氧化物消除氮氧化物的污染。已知:
4
15.(12分)次磷酸钠(NaH PO )是电镀业上重要还原剂,一般制备方法是将白磷(P )和过量烧碱溶
2 2 4
①CH(g)+4NO (g) 4NO(g)+CO (g)+2HO(l) ΔH=-662kJ/mol
4 2 2 2
液混合、加热,生成次磷酸钠和PH ,PH 是一种无色、有毒的可燃性气体。实验装置如下图所
3 3
示: ②CH (g)+2NO (g) N(g)+CO (g)+2HO(l) ΔH=-955kJ/mol
4 2 2 2 2
则反应CH(g)+4NO(g)=2N (g)+CO (g)+HO(l) ΔH=_________。
4 2 2 2
II.利用NH 的还原性可以消除氮氧化物的污染,其中除去 NO的主要反应如下:4NH (g)
3 3
+6NO(g)
5N(g)+6HO(l) ΔH<0
2 2
(2)一定温度下,在恒容密闭容器中按照n(NH )∶n(NO)=2∶3充入反应物,发生上述反应。下列不
3
能判断该反应达到平衡状态的是____________。
回答下列问题:
A.c(NH )∶c(NO)=2∶3
3
(1)仪器a的名称是______。装置D的作用______。
B.1mol N—H键断裂的同时断裂1mol O—H键
(2)次磷酸钠(NaH PO )是次磷酸(H PO )与足量NaOH溶液反应的产物,NaH PO 属于_______(填
2 2 3 2 2 2
C.容器内压强不变
“正盐”“酸式盐”“碱式盐”),NaH PO 中磷元素的化合价为_________。
2 2
D.容器内混合气体的密度不变
(3)PH 在装置C中被氧化为最高价化合物,反应的化学方程式为 。
3
(3)实验测得v =k ·c4(NH )·c6(NO),v =k ·c5(N )(k 、k 为速率常数,只与温度有关)。
(4)A中生成NaH PO 和NaCl,相关物质溶解度(S)如下: 正 正 3 逆 逆 2 正 逆
2 2
①达到平衡后,仅降低温度,k 增大的倍数_________(填“>”“<”或“=”)k 增大的倍数。
正 逆
S(20℃) S(98℃)
②若在1L的恒容密闭容器中充入2mol CO和3mol NO,在一定温度下达到平衡时,CO的转化
NaCl 36 38.8
率为80%,则k ︰k =_____L/mol(用数字表达式表示)。
正 逆
NaH PO 90 657
2 2 Ⅲ.利用燃料电池的原理来处理氮氧化物是一种新方向。装置如图所示,在处理过程中石墨电
极I上反应生成一种氧化物Y。
充分反应后,将A中混合液蒸发浓缩,有大量晶体析出,该晶体主要成分的化学式为______,
然后______、______、过滤、洗涤、干燥,得到NaH PO 的粗产品。
2 2即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得 TiCl 。相关反应为:
4
2FeTiO +7Cl+6C========2TiCl +2FeCl +6CO;TiO +2Cl+2C========TiCl +2CO。将 TiCl
3 2 4 3 2 2 4 4
蒸 馏 并 提 纯 , 在 氩 气 保 护 下 与 镁 共 热 得 到 钛 , 相 关 反 应 为 :
TiCl +2Mg===========Ti+2MgCl ,MgCl 和过量Mg用稀盐酸溶解后得海绵状钛,再在真空
4 2 2
熔化铸成钛锭。请回答下列问题:
(4)石墨II电极为______(填“正”或“负”)极,该电极反应为______。 (1)Ti2+基态的电子排布式可表示为_________。与钛同周期的所有元素的基态原子中,未成对
电子数与钛相同的元素有________种。
(5)写出该电池反应的方程式______。
(2)与CO互为等电子体的分子为_________(填化学式)。
17.(13分)钛用途广泛,焦磷酸镁(Mg PO)不溶于水,是牙膏、牙粉的稳定剂。一种以含钛废料
2 2 7
(主要成分为TiO ,含少量MgO、Cu、Al O 、FeO、Fe O)为原料,分离提纯TiO 并制取少量 (3)在CHCl、C H、CO、C H 中,碳原子采取sp杂化的分子有__________。
2 2 3 2 3 2 2 2 6 6 2 2 4
焦磷酸镁的工艺流程如下:
(4)TiCl 的熔点为-25℃,TiCl 熔点低的原因为___________。
4 4
(5)已知TiO 与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,
2
结构如图所示,阳离子中O的杂化方式为_____,阴离子的空间构型为_____。
已知:TiO 不与碱反应,与酸反应后以TiO2+的形式存在。回答下列问题:
2
(6)在自然界中TiO 有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如下图所示,
2
(1)提高“酸浸”的反应速率的措施有 ,“碱浸”时发生反应的离子方程式为
则其中Ti4+的配位数为__________。
。
(2)工业上“酸浸”时,温度选择40℃而不选择更高温度的原因是_______。
(3)滤渣1是 ,滤渣2的主要成分为_____(填化学式)。
(4)“氧化”时SO转化为SO的离子方程式为___________。
2
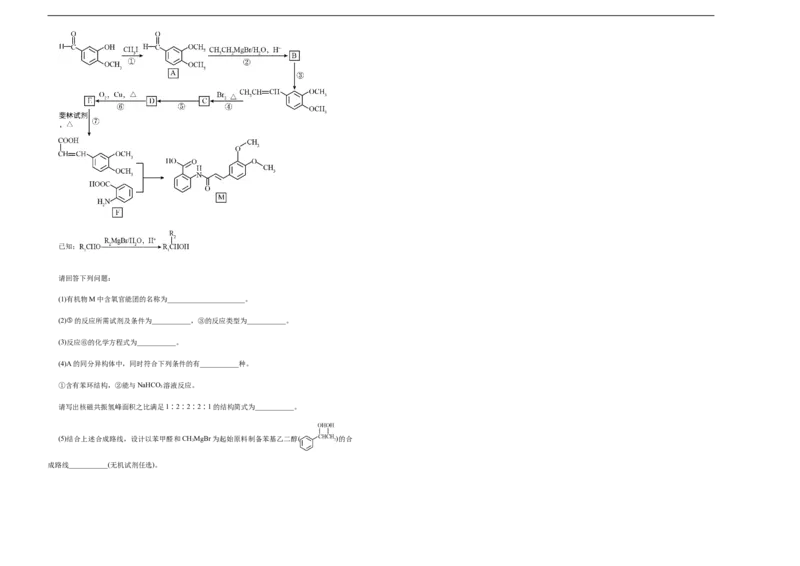
(5)离子浓度≤1.0×10−5mol·L−1时表示该离子沉淀完全。常温下,为了使Fe3+沉淀完全,调节pH 19.(15分)有机物M可用于治疗支气管哮喘,慢性支气管炎。该有机物可以由有机物A经过一
的最小值为___________。(已知:K [Fe(OH) ]=1×10−38) 系列反应合成得到,其合成路线如下图所示:
sp 3
(6)过滤洗涤得到焦磷酸镁(Mg PO)固体,判断沉淀是否洗涤干净操作是___________。
2 2 7
(二)选考题(共 15分,请考生从2道题中任选一题作答,如果多做,则按所做的第一题计
分。)
18.钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属。目前生产钛采用氯化法,已知;
请回答下列问题:
(1)有机物M中含氧官能团的名称为______________________。
(2)⑤的反应所需试剂及条件为___________,③的反应类型为___________。
(3)反应⑥的化学方程式为___________。
(4)A的同分异构体中,同时符合下列条件的有___________种。
①含有苯环结构,②能与NaHCO 溶液反应。
3
请写出核磁共振氢峰面积之比满足1∶2∶2∶2∶1的结构简式为___________。
(5)结合上述合成路线,设计以苯甲醛和CHMgBr为起始原料制备苯基乙二醇( )的合
3
成路线___________(无机试剂任选)。