文档内容
微专题 34 非金属及其化合物制备流程与实验探究(Si、N、P、
As)
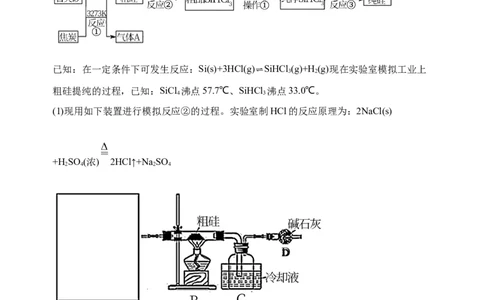
1.晶体硅是信息科学和能源科学中的一种重要材料,以下是工业上制取纯硅的方法。
已知:在一定条件下可发生反应:Si(s)+3HCl(g)⇌SiHCl
3
(g)+H
2
(g)现在实验室模拟工业上
粗硅提纯的过程,已知:SiCl 沸点57.7℃、SiHCl 沸点33.0℃。
4 3
(1)现用如下装置进行模拟反应②的过程。实验室制HCl的反应原理为:2NaCl(s)
+H SO (浓) 2HCl↑+Na SO
2 4 2 4
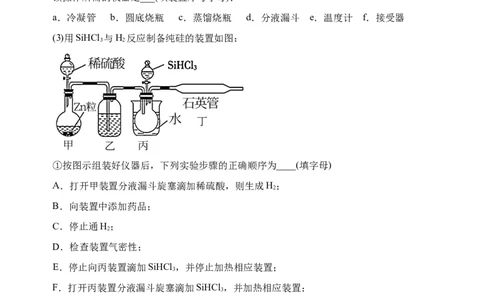
A中是HCl的发生装置,你认为应选择下图哪套装置___(填装置的字母);(2)已知液态粗品SiHCl 中含有杂质SiCl ,则流程中操作①为___(填操作名称),下列不是
3 4
该操作所需的仪器是___(填装置序号字母);
a.冷凝管 b.圆底烧瓶 c.蒸馏烧瓶 d.分液漏斗 e.温度计 f.接受器
(3)用SiHCl 与H 反应制备纯硅的装置如图:
3 2
①按图示组装好仪器后,下列实验步骤的正确顺序为____(填字母)
A.打开甲装置分液漏斗旋塞滴加稀硫酸,则生成H;
2
B.向装置中添加药品;
C.停止通H;
2
D.检查装置气密性;
E.停止向丙装置滴加SiHCl ,并停止加热相应装置;
3
F.打开丙装置分液漏斗旋塞滴加SiHCl ,并加热相应装置;
3
步骤c中需要加热的装置为___(填装置序号“甲”、“乙”、“丙”、“丁”)
②该套装置的设计缺陷是___。
【答案】(1)d (2) 分馏 bd (3) DBAFEC 丙和丁 装置中无尾气处理装置
【分析】
工业上制取纯硅的方法,是将焦炭和石英砂在高温下反应生成粗硅和一氧化碳,再发生
反应Si(s)+3HCl(g)⇌SiHCl
3
(g)+H
2
(g),液态粗品SiHCl
3
中含有杂质SiCl
4
等,根据物质的沸点相差不大,可选择分馏的方法进行除杂,根据分馏操作的装置可选择仪器,最后用
SiHCl 与H 反应制备纯硅;根据题中制HCl的实验原理2NaCl(s)+HSO (浓)
3 2 2 4
2HCl↑+Na SO ,为固体和液体加热,据此选择装置,反应中有剩余的氯化氢气体未反应,
2 4
要吸收,同时SiHCl 易水解,要防止空气中的水分进入装置,所以使用碱石灰;用
3
SiHCl 与H 反应制备纯硅,组装好仪器后,要先进行气密性检验,再在装置中通氢气,
3 2
排尽空气后再进行SiHCl 与H 的反应,实验结束时还要继续通氢气,直到装置冷却,防
3 2
止空气中的成分对反应干扰,根据装置可知,丙处是水浴,丁处进行SiHCl 与H 的反应,
3 2
都要进行加热,实验尾气中有氯化氢等气体不能直接排到空气中,据此分析。
【解析】
(1)根据题中制HCl的实验原理2NaCl(s)+HSO (浓) 2HCl↑+Na SO ,为固体和液体加热,
2 4 2 4
所以选择d装置;
(2)液态粗品SiHCi中含有杂质SiCls,根据这些物质的沸点不同,可选择分馏的方法进行
除杂,所以流程中操作①为分馏,根据分馏操作的装置可知,分馏需要使用冷凝管进行
冷凝蒸气,在蒸馏烧瓶中进行加热,用温度计测量蒸汽的温度,用接受器接收冷凝后的
蒸汽,圆底烧瓶和分液漏斗不是分馏操作所需的仪器;
(3)③用SiHCl 与H 反应制备纯硅,组装好仪器后,要先进行气密性检验,再在装置中通
3 2
氢气,排尽空气后再进行SiHCl 与H 的反应,实验结束时还要继续通氢气,直到装置冷
3 2
却,防止空气中的成分对反应干扰,所以实验步骤的顺序为DBAFEC,根据装置可知,
丙处是水浴,丁处进行SiHCl与H 的反应,都要进行加热,所以步骤F中需要加热的装
2
置为丙、丁;
②实验尾气中有氯化氢等气体不能直接排到空气中,而根据装置可知,装置中无尾气处
理装置。
2.氨基甲酸铵(H NCOONH )是一种重要的化工原料,可用作化学肥料、灭火剂、洗涤剂
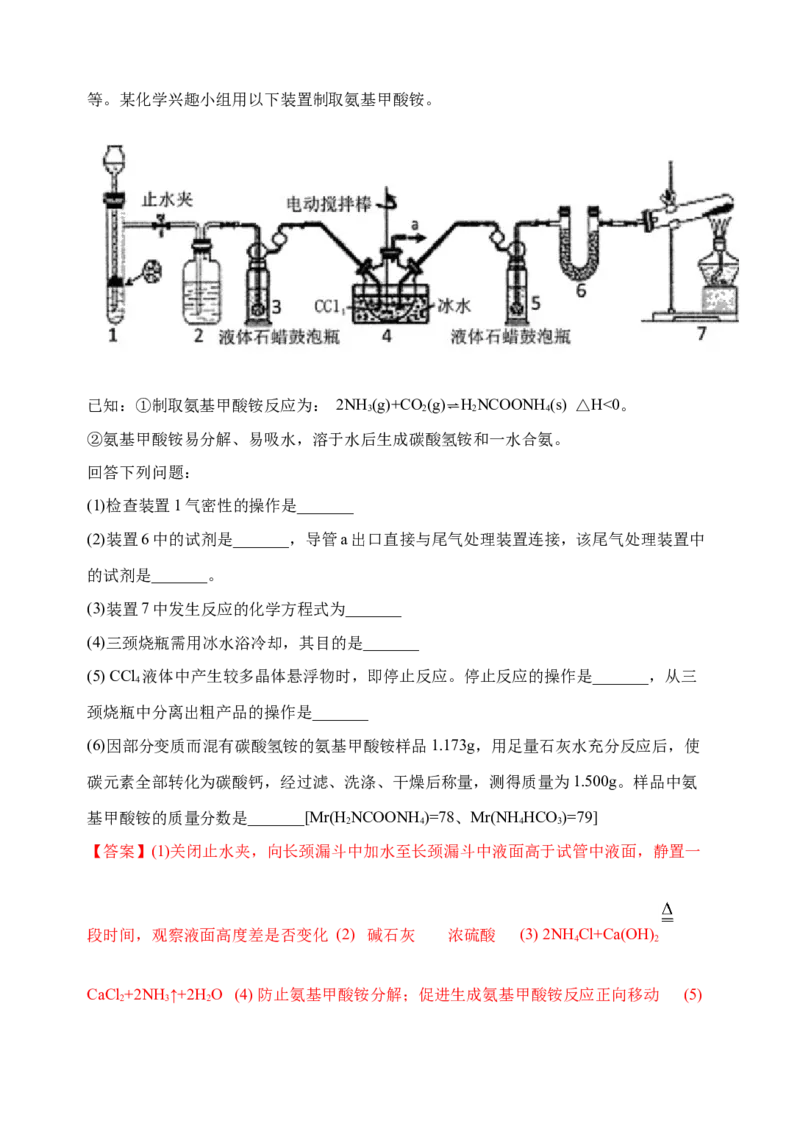
2 4等。某化学兴趣小组用以下装置制取氨基甲酸铵。
已知:①制取氨基甲酸铵反应为: 2NH
3
(g)+CO
2
(g)⇌H
2
NCOONH
4
(s) △H<0。
②氨基甲酸铵易分解、易吸水,溶于水后生成碳酸氢铵和一水合氨。
回答下列问题:
(1)检查装置1气密性的操作是_______
(2)装置6中的试剂是_______,导管a出口直接与尾气处理装置连接,该尾气处理装置中
的试剂是_______。
(3)装置7中发生反应的化学方程式为_______
(4)三颈烧瓶需用冰水浴冷却,其目的是_______
(5) CCl 液体中产生较多晶体悬浮物时,即停止反应。停止反应的操作是_______,从三
4
颈烧瓶中分离出粗产品的操作是_______
(6)因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173g,用足量石灰水充分反应后,使
碳元素全部转化为碳酸钙,经过滤、洗涤、干燥后称量,测得质量为1.500g。样品中氨
基甲酸铵的质量分数是_______[Mr(H NCOONH )=78、Mr(NHHCO )=79]
2 4 4 3
【答案】(1)关闭止水夹,向长颈漏斗中加水至长颈漏斗中液面高于试管中液面,静置一
段时间,观察液面高度差是否变化 (2) 碱石灰 浓硫酸 (3) 2NHCl+Ca(OH)
4 2
CaCl +2NH↑+2H O (4) 防止氨基甲酸铵分解;促进生成氨基甲酸铵反应正向移动 (5)
2 3 2关闭止水夹,熄灭酒精灯 过滤 (6) 79.80%
【分析】
根据题中已知原理,制取氨基甲酸铵,需要二氧化碳和氨气,又由于氨基甲酸铵易分解、
易吸水,所以二氧化碳和氨气必须干燥,且在冰水低温环境中反应,根据实验室制取二
氧化碳和制氨气的原理,1中为碳酸钙和盐酸混合制二氧化碳的反应,经过2中浓硫酸干
燥二氧化碳,7中为固体加热制氨气的反应(比如氯化铵和氢氧化钙混合加热),6中碱石
灰干燥氨气,干燥的氨气和二氧化碳分别通过5,3的液体石蜡鼓泡瓶,通过气泡硫酸控制
反应物的用量,在4中三颈烧瓶中发生反应制取氨基甲酸铵,尾气为氨气和二氧化碳,其
中氨气有毒,在a处接酸液进行吸收处理,又由于氨基甲酸铵易吸水,要用浓硫酸进行尾
气处理。
【解析】
(1)装置1为带分液漏斗的试管,故检查装置气密性的操作为:关闭止水夹,向长颈漏斗
中加水至长颈漏斗中液面高于试管中液面,静置一段时间,观察液面高度差是否变化
(2)据分析,装置6为氨气的干燥装置,氨气为碱性气体,故6中试剂为:碱石灰;该反
应尾气为氨气和二氧化碳,其中氨气有毒,需要尾气处理,故a处应接的尾气处理装置中
应装有酸液,又由于产物氨基甲酸铵易吸水,故需要用浓硫酸,不能用稀硫酸,故答:
浓硫酸;
(3)装置7为实验室固体加热制氨气的反应,用氯化铵和熟石灰混合加热制氨气,反应的
化学方程式为:2NH Cl+Ca(OH) CaCl +2NH↑+2H O;
4 2 2 3 2
(4)已知2NH
3
(g)+CO
2
(g)⇌H
2
NCOONH
4
(s) △H<0,反应放热,降低温度可以使平衡正向
移动,提高产率,同时,产物氨基甲酸铵易分解,低温下可以防止其分解,故答:防止
氨基甲酸铵分解;促进生成氨基甲酸铵反应正向移动;
(5)停止反应需要停止反应物CO 和氨气的生成,故要停止反应需要关闭1处的止水夹,
2
和熄灭7处的酒精灯;得到产物在CCl 中是悬浮晶体,固液分离需要过滤操作;
4
(6)设碳酸氢铵为xmol,氨基甲酸铵为ymol,由样品总质量可得:79g/mol xmol+78g/molymol=1.173g,又因为n(C)=n(CaCO )= =0.015mol,由碳原子守恒可得:
3
xmol+ymol=0.015mol,解x=0.003,y=0.012,则m(HNCOONH )=0.012mol 78g/
2 4
mol=0.936g,则氨基甲酸铵的质量分数= 79.80%
3.三氯氧磷(POCl )是一种工业化工原料,可用于制取有机磷农药、长效磺胺药物等,还
3
可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O 和PCl 为原料可制
2 3
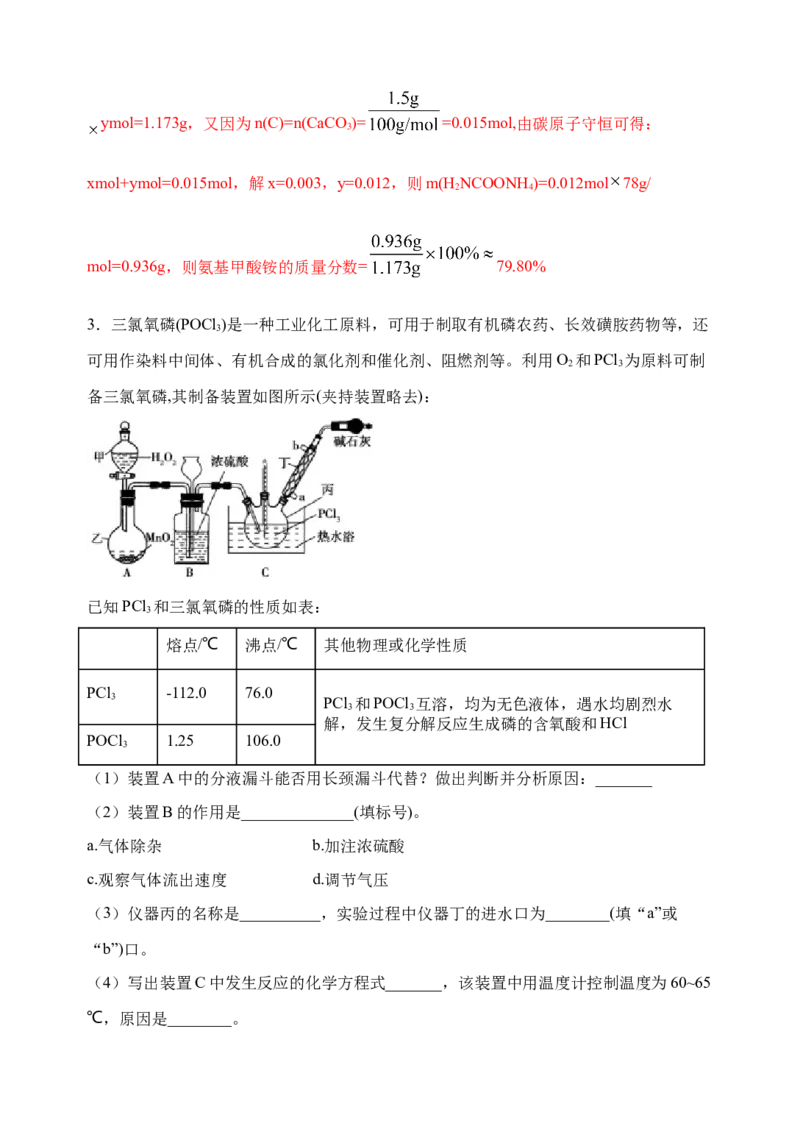
备三氯氧磷,其制备装置如图所示(夹持装置略去):
已知PCl 和三氯氧磷的性质如表:
3
熔点/℃ 沸点/℃ 其他物理或化学性质
PCl -112.0 76.0
3 PCl 和POCl 互溶,均为无色液体,遇水均剧烈水
3 3
解,发生复分解反应生成磷的含氧酸和HCl
POCl 1.25 106.0
3
(1)装置A中的分液漏斗能否用长颈漏斗代替?做出判断并分析原因:_______
(2)装置B的作用是______________(填标号)。
a.气体除杂 b.加注浓硫酸
c.观察气体流出速度 d.调节气压
(3)仪器丙的名称是__________,实验过程中仪器丁的进水口为________(填“a”或
“b”)口。
(4)写出装置C中发生反应的化学方程式_______,该装置中用温度计控制温度为60~65
℃,原因是________。(5)称取16.73 g POCl 样品,配制成100 mL溶液;取10.00 mL溶液于锥形瓶中,加入
3
3.2 mol·L-1的AgNO 溶液10.00 mL,并往锥形瓶中滴入5滴Fe (SO ) 溶液;用0.20
3 2 4 3
mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00 mL(已知:Ag++SCN-
=AgSCN↓)。则加入Fe (SO ) 溶液的作用是________,样品中POCl 的纯度为
2 4 3 3
_____________。
【答案】(1)否,长颈漏斗不能调节滴液速度 (2) acd (3) 三颈烧瓶 a
(4)2PCl +O =2POCl 温度过低反应速度过慢;温度过高,PCl 易挥发,利用率低
3 2 3 3
(5) 指示剂 91.8%
【分析】
A装置中用双氧水与二氧化锰反应制备氧气,通过加入双氧水的量,可以控制产生氧气
的速率,氧气中含有的水蒸气用浓硫酸除去,装置B中有长颈漏斗,可以平衡装置内外
的压强,起到安全瓶的作用,纯净的氧气与三氯化磷在装置C中反应生成POCl ,为了控
3
制反应速率,同时防止三氯化磷挥发,反应的温度控制在60~65℃,所以装置C中用水
浴加热,POCl 遇水剧烈水解为含氧酸和氯化氢,为防止空气中水蒸汽进入装置,同时吸
3
收尾气,所以在装置的最后连有碱石灰的干燥管,据此分析解答(1)~(4);
(5)测定POCl 产品含量,用POCl 与水反应生成氯化氢,然后用硝酸银标准溶液沉淀溶液
3 3
中的氯离子,KSCN溶液滴定过量的AgNO 溶液,根据KSCN的物质的量可计算出溶液
3
中剩余的AgNO,结合AgNO 的总物质的量得知与氯离子反应的硝酸银,进而计算出溶
3 3
液中氯离子的物质的量,根据元素守恒可计算出样品中POCl 的质量,进而确定POCl 的
3 3
质量分数。
【解析】
(1)装置A中的分液漏斗不能用长颈漏斗代替,因为长颈漏斗不能调节滴液速度,故答案
为否,长颈漏斗不能调节滴液速度;
(2)装置B中装有浓硫酸,可作干燥剂,另外气体通过液体时可观察到气泡出现,长颈漏
斗,可以平衡装置内外的压强,起到安全瓶的作用,则装置B的作用是观察O 的流速、
2
平衡气压、干燥氧气,故答案为acd;
(3)根据装置图,仪器丙为三颈烧瓶,为了提高冷却效果,应该从冷凝管的下口进水,即进水口为a,故答案为三颈烧瓶;a;
(4)氧气氧化PCl 生成POCl ,根据原子守恒,反应的化学方程式2PCl +O =2POCl ,根据
3 3 3 2 3
上面的分析可知,反应温度应控制在60~65℃,原因是温度过低,反应速率小,温度过
高,三氯化磷会挥发,利用率低,故答案为2PCl +O =2POCl ;温度过低,反应速率小,
3 2 3
温度过高,三氯化磷会挥发,利用率低;
(5)Fe3+的溶液中滴加KSCN溶液,溶液显红色,则用 KSCN溶液滴定过量的AgNO 溶
3
液时,可选择硫酸铁溶液为指示剂,达到终点时的现象是溶液会变红色;KSCN的物质的
量为0.20mol•L-1×0.010L=0.002mol,根据反应Ag++SCN-=AgSCN↓,可知溶液中剩余的银
离子的物质的量为0.002mol,POCl 与水反应生成氯化氢的物质的量为
3
3.2mol•L-1×0.01L-0.002mol=0.03mol,即16.73 g POCl 产品中POCl 的物质的量为
3 3
× =0.1mol,则所得产品中POCl 的纯度为
3
×100%=91.8%,故答案为指示剂;91.8%。
4.As O 为白色霜状粉末,俗称砒霜,为剧毒物质,对人的致死量为0.1g,法医学中可
2 3
采用马氏(Marsh)试砷法验证砒霜中毒。某实验室使用马氏试砷法检验某待测试样中As O
2 3
的含量,如图所示。马氏试砷法的原理是将Zn、盐酸和待测试样混合,若试样中含砒霜,
则可反应生成AsH ,将其导入硬质玻璃试管中,在250-300℃时AsH 分解,会在玻璃管
3 3
壁上生成黑色的“砷镜”。
已知:AsH 是一种有大蒜味的有毒气体,易自燃,As的熔点为817℃,在6149℃时升华。
3(1)仪器B的名称为____。
(2)AsH 的还原性极强,能与大多数无机氧化剂反应,例如与AgNO 溶液反应可生成
3 3
As O 和一种黑色沉淀,相关化学方程式为:__。
2 3
(3)若试样中含有砒霜,则仪器B中发生的用锌还原砒霜反应的离子方程式为___。
(4)打开仪器A的活塞前,应先打开K、K 通一段时间H,其目的是__,反应过程中还应
1 2 2
继续通入H,但流速不应过快,原因是___。
2
(5)仪器D的作用是收集储存尾气,C的作用是___。
(6)实验时应严格控制硬质玻璃管处加热温度,原因是___。
(7)若实验时试样质量为10.00g,当实验结束时,AsH 传感器未检测出AsH ,玻璃管中收
3 3
集到0.020mgAs,则试样(假设试样中的含砷化合物只有As O)中As O 的含量为___mg/
2 3 2 3
100g(结果取三位有效数字)。
【答案】(1)三颈圆底烧瓶(或三口烧瓶)
(2)2AsH+12AgNO +3H O=As O+12HNO +12Ag↓ (3) 6Zn+As O+12H+=6Zn2+
3 3 2 2 3 3 2 3
+2AsH ↑+3H O (4) 排净装置内的空气,防止AsH 发生自燃 将AsH 全部带入玻璃管
3 2 3 3
中反应,并防止流速过快导致AsH 没有完全分解(或损耗) (5) 接收D中储存尾气时排出
3
的水 (6) 防止As升华,不易形成砷镜 (7) 0.264
【解析】
(1)仪器B的名称为三颈圆底烧瓶(或三口烧瓶);
(2)AsH 的还原性极强,能与大多数无机氧化剂反应,例如与AgNO 溶液反应可生成
3 3
As O 和一种黑色沉淀,As的化合价升高,则Ag化合价降低,黑色沉淀为:Ag。相关化
2 3
学方程式为:2AsH +12AgNO +3H O=As O+12HNO +12Ag↓;
3 3 2 2 3 3
(3) 在酸性溶液中,锌还原砒霜,锌氧化为锌离子,As O 还原为AsH ,反应的离子方程
2 3 3
式为:6Zn+As O+12H+=6Zn2++2AsH ↑+3H O;
2 3 3 2
(4)打开仪器A的活塞前,应先打开K、K 通一段时间H,其目的是排净装置内的空气,
1 2 2
防止AsH 发生自燃。反应过程中还应继续通入H,但流速不应过快,原因是:将AsH
3 2 3
全部带入玻璃管中反应,并防止流速过快导致AsH 没有完全分解(或损耗);
3
(5)仪器D的作用是收集储存尾气,C的作用是接收D中储存尾气时排出的水;(6)实验时应严格控制硬质玻璃管处加热温度,原因是防止As升华,不易形成砷镜;
(7)实验所用试样为10.00g当实验结束时,AsH 传感器未检测出AsH ,说明AsH 全部在
3 3 3
玻璃管中受热分解为0.020mgAs,则试样中As O 的含量为
2 3
=0.264mg/100g。
5.氮化硅硬度大、熔点高、不溶于酸(氢氟酸除外),是一种重要的结构陶瓷材料。一种
用工业硅(含少量钾、钠、铁、铜的氧化物),已知硅的熔点是1420℃,高温下氧气及水蒸
气能明显腐蚀氮化硅。一种合成氮化硅的工艺流程如下:
注:原料中的N 是采用空气分离法制备。
2
(1)净化N 和H 时,铜屑的作用是_______;硅胶的作用是_______。
2 2
(2)氮化炉中发生反应:3SiO(s)+2N(g)=Si N(s),同时会剧烈放热,反应时要严格控制氮
2 2 3 4
气的流速以控制_______,原因是_______。
(3)X可能是_______(选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(4)如何说明氮化硅产品已用水洗干净?_______。
(5)用硅粉作硅源、叠氮化钠(NaN )作氮源,直接燃烧生成氮化硅(发生置换反应),该反应
3
的化学方程式为:_______。
【答案】(1)除去原料气中残存的氧气 除去生成的水蒸气 (2) 温度 防止局部过热,
导致硅熔化熔合成团,阻碍与N 的接触 (3) 硝酸 (4) 用pH试纸测得最后一次洗涤的
2
滤出液呈中性 (5) 9Si+4NaN 3Si N +4Na↑
3 3 4【分析】
将N 和H 分别分别经过无水氯化钙、铜屑、硅胶除去水和氧气;净化后的N 和H 在氮
2 2 2 2
化炉中与粉碎的硅在1200~1400℃反应生成氮化硅,制取的氮化硅中混有Cu,用硝酸酸
洗除去杂质铜,再用蒸馏水水洗、后处理得到纯净的氮化硅,据此分析解答。
【解析】
(1) 原料中的N 是采用空气分离法制备的其中混有少量氧气,Cu能与氧气反应,可以除
2
去原料气中的氧气;高温下,氢气能够与氧气反应生成水,硅胶具有吸水性,可除去生
成的水蒸气,故答案为:除去原料气中残存的氧气;除去生成的水蒸气;
(2)氮化炉中3SiO(s)+2N(g)=Si N(s),该反应为放热反应,硅的熔点是1420℃,反应过
2 2 3 4
快,温度过高,会导致硅熔化熔合成团,阻碍与N 的接触,故应严格控制温度,故答案
2
为:温度;防止局部过热,导致硅熔化熔合成团,阻碍与N 的接触;
2
(3)氮化硅能与HF酸反应,盐酸、稀硫酸均不与Cu反应,氮化硅中混有铜粉,为除去混
有的Cu,可选择硝酸,Cu与硝酸能够反应,而氮化硅与硝酸不反应,故答案为:硝酸;
(4)氮化硅不溶于水、不溶于酸(HF酸除外),若氮化硅产品用水洗干净,则洗涤后的滤出
液呈中性,故可以使用pH试纸测得最后一次洗涤的滤出液的酸碱性,故答案为:用pH
试纸测得最后一次洗涤的滤出液呈中性;
(5)硅粉作硅源、叠氮化钠(NaN )作氮源,直接燃烧发生置换反应生成氮化硅,同时生成
3
Na,反应的化学方程式为9Si+4NaN 3Si N+4Na,故答案为:9Si+4NaN
3 3 4 3
3Si N+4Na。
3 4
6.工业上利用氨氧化获得的高浓度NOx气体(含NO、NO )制备NaNO 、NaNO ,工艺流
2 2 3
程如下:已知:NaCO+NO+NO =2NaNO +
2 3 2 2 CO2
(1)中和液所含溶质除NaNO 及少量NaCO 外,还有__________(填化学式)。
2 2 3
(2)中和液进行蒸发Ⅰ操作时,应控制水的蒸发量,避免浓度过大,目的是_______。
蒸发Ⅰ产生的蒸气中含有少量的NaNO 等有毒物质,不能直接排放,将其冷凝后用于流
2
程中的_______(填操作名称)最合理。
(3)母液Ⅰ进行转化时加入稀HNO 的目的是_______。母液Ⅱ需回收利用,下列处理方
3
法合理的是________。
a.转入中和液 b.转入结晶Ⅰ操作
c.转入转化液 d.转入结晶Ⅱ操作
(4)若将NaNO 、NaNO 两种产品的物质的量之比设为2:1,则生产1.38吨NaNO 时,
2 3 2
NaCO 的理论用量为______吨(假定NaCO 恰好完全反应)。
2 3 2 3
【答案】(1)NaNO (2) 防止NaNO 的析出 溶碱 (3) 将NaNO 氧化为
3 2 2
NaNO c、d (4) 1.59
3
【解析】
(1)NO 与碱液反应可生成NaNO ;
2 3
(2)浓度过大时,NaNO 可能会析出;NaNO 有毒,不能直接排放,回收后可用于流程
2 2
中的溶碱;
(3)NaNO 在酸性条件下易被氧化,加入稀硝酸可提供酸性环境;母液Ⅱ的溶质主要是
2
NaNO ,所以回收利用时应转入转化液,或转入结晶Ⅱ操作,故c、d正确;
3
(4)1.38吨NaNO 的物质的量为:1.38×106÷69g/mol=2×104mol,则生成的NaNO 物质的
2 3
量为:1×104mol,故NaCO 的理论用量= ×(2×104+1×104)mol×106g/
2 3
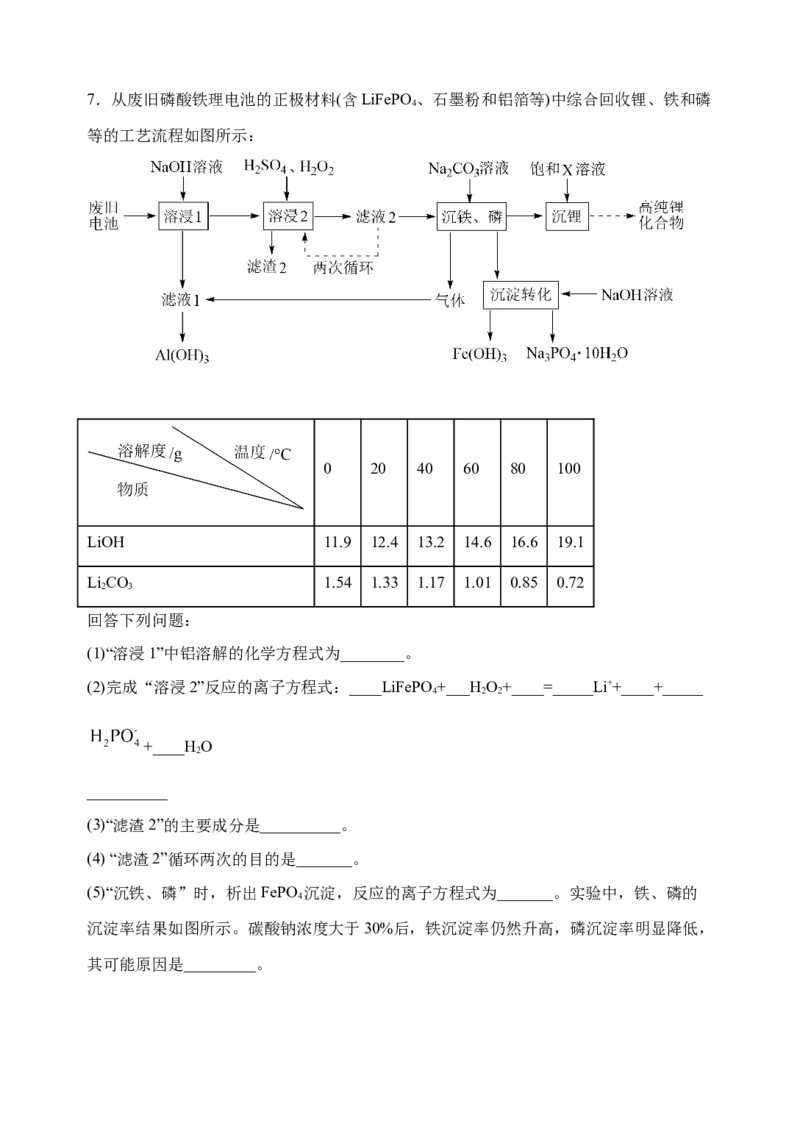
mol=1.59×106g=1.59吨。7.从废旧磷酸铁理电池的正极材料(含LiFePO 、石墨粉和铝箔等)中综合回收锂、铁和磷
4
等的工艺流程如图所示:
0 20 40 60 80 100
LiOH 11.9 12.4 13.2 14.6 16.6 19.1
LiCO 1.54 1.33 1.17 1.01 0.85 0.72
2 3
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为________。
(2)完成“溶浸2”反应的离子方程式:____LiFePO +___H O+____=_____Li++____+_____
4 2 2
+____H O
2
__________
(3)“滤渣2”的主要成分是__________。
(4) “滤渣2”循环两次的目的是_______。
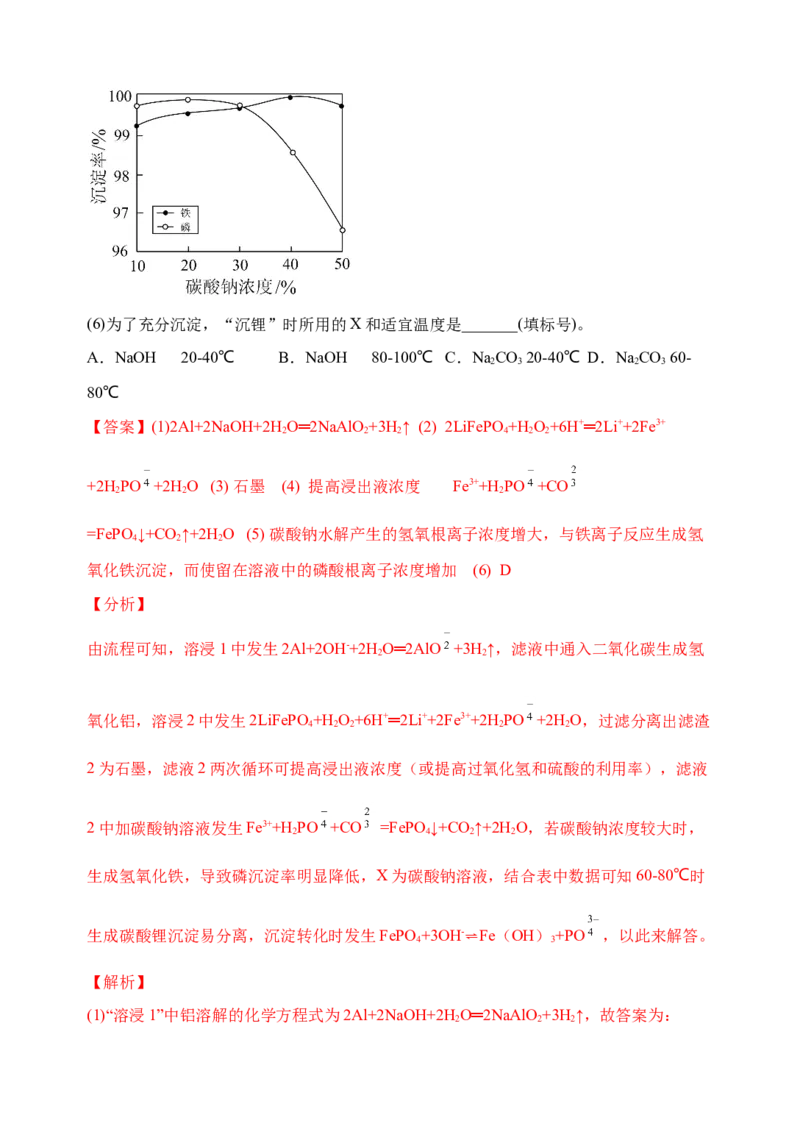
(5)“沉铁、磷”时,析出FePO 沉淀,反应的离子方程式为_______。实验中,铁、磷的
4
沉淀率结果如图所示。碳酸钠浓度大于30%后,铁沉淀率仍然升高,磷沉淀率明显降低,
其可能原因是_________。(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是_______(填标号)。
A.NaOH 20-40℃ B.NaOH 80-100℃ C.NaCO 20-40℃ D.NaCO 60-
2 3 2 3
80℃
【答案】(1)2Al+2NaOH+2H O═2NaAlO+3H ↑ (2) 2LiFePO +H O+6H+═2Li++2Fe3+
2 2 2 4 2 2
+2H PO +2H O (3) 石墨 (4) 提高浸出液浓度 Fe3++H PO +CO
2 2 2
=FePO↓+CO ↑+2H O (5) 碳酸钠水解产生的氢氧根离子浓度增大,与铁离子反应生成氢
4 2 2
氧化铁沉淀,而使留在溶液中的磷酸根离子浓度增加 (6) D
【分析】
由流程可知,溶浸1中发生2Al+2OH-+2H O═2AlO +3H ↑,滤液中通入二氧化碳生成氢
2 2
氧化铝,溶浸2中发生2LiFePO +H O+6H+═2Li++2Fe3++2H PO +2H O,过滤分离出滤渣
4 2 2 2 2
2为石墨,滤液2两次循环可提高浸出液浓度(或提高过氧化氢和硫酸的利用率),滤液
2中加碳酸钠溶液发生Fe3++H PO +CO =FePO↓+CO ↑+2H O,若碳酸钠浓度较大时,
2 4 2 2
生成氢氧化铁,导致磷沉淀率明显降低,X为碳酸钠溶液,结合表中数据可知60-80℃时
生成碳酸锂沉淀易分离,沉淀转化时发生FePO
4
+3OH- ⇌Fe(OH)
3
+PO ,以此来解答。
【解析】
(1)“溶浸1”中铝溶解的化学方程式为2Al+2NaOH+2H O═2NaAlO+3H ↑,故答案为:
2 2 22Al+2NaOH+2H O═2NaAlO+3H ↑;
2 2 2
(2)“溶浸2”过程中LiFePO 和HO 在酸性条件下发生氧化还原反应,离子方程式为
4 2 2
2LiFePO +H O+6H+═2Li++2Fe3++2H PO +2H O,故答案为:2LiFePO +H O+6H+═2Li+
4 2 2 2 2 4 2 2
+2Fe3++2H PO +2H O;
2 2
(3)“滤渣2”的主要成分是石墨,故答案为:石墨;
(4)“滤液2”循环两次的目的是提高浸出液浓度,故答案为:提高浸出液浓度;
(5)“沉铁、磷”时,析出FePO 沉淀,反应的离子方程式为Fe3++H PO +CO
4 2
=FePO↓+CO ↑+2H O,实验中,铁、磷的沉淀率 结果如图所示。碳酸钠浓度大于30%后,
4 2 2
铁沉淀率仍然升高,磷沉淀率明显降低,其可能原因是碳酸钠水解产生的氢氧根离子浓
度增大,与铁离子反应生成氢氧化铁沉淀,而使留在溶液中的磷酸根离子浓度增加,故
答案为:Fe3++H PO +CO =FePO↓+CO ↑+2H O;碳酸钠水解产生的氢氧根离子浓度增
2 4 2 2
大,与铁离子反应生成氢氧化铁沉淀,而使留在溶液中的磷酸根离子浓度增加;
(6)由表中数据可知,相同温度下碳酸锂的溶解度比LiOH小,且升高温度碳酸锂的溶解度
减小,为了充分沉淀,需要碳酸锂的溶解度小,温度控制在60−80℃,则“沉锂”时所用
的X和适宜温度是NaCO、60−80℃,故答案为:D。
2 3
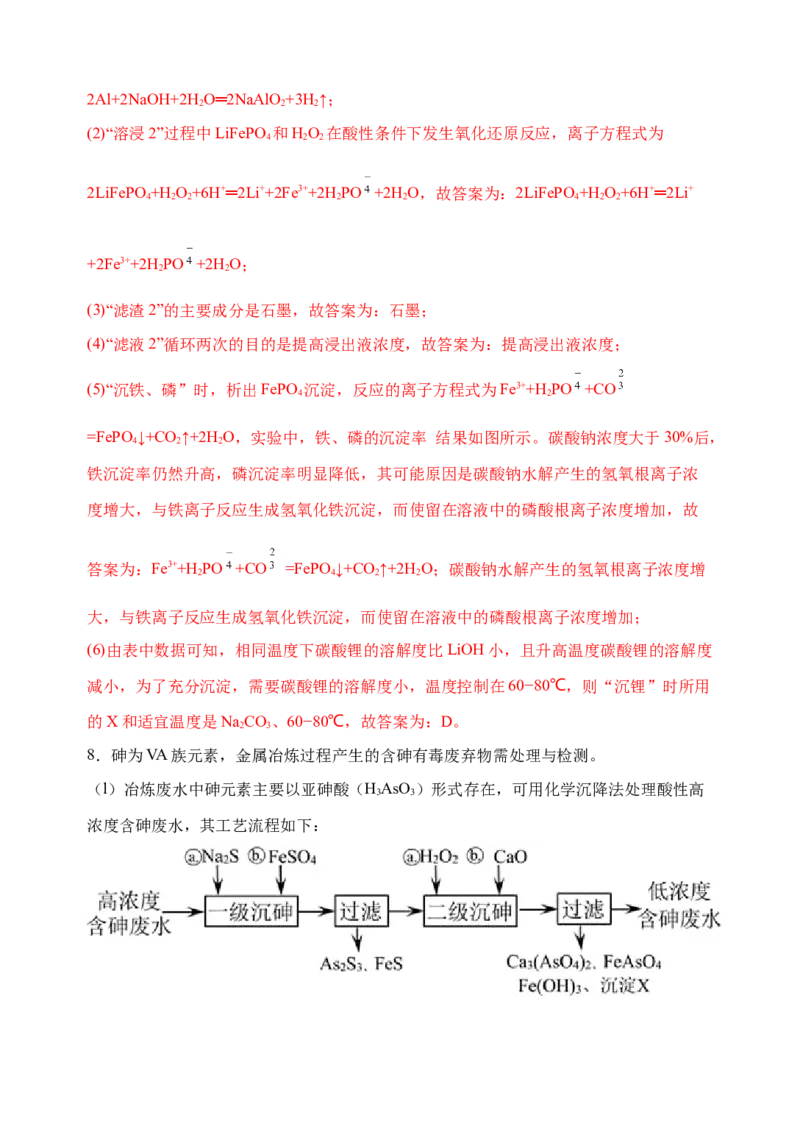
8.砷为VA族元素,金属冶炼过程产生的含砷有毒废弃物需处理与检测。
(l)冶炼废水中砷元素主要以亚砷酸(HAsO )形式存在,可用化学沉降法处理酸性高
3 3
浓度含砷废水,其工艺流程如下:已知:I .As S 与过量的S2一存在以下反应:As S(s)+3S2—(aq) 2AsS 3—(aq);
2 3 2 3 3
II.亚砷酸盐的溶解性大于相应砷酸盐。
①亚砷酸中砷元素的化合价为______;
②砷酸的第一步电离方程式为____________________________;
③“一级沉砷”中FeSO 的作用是________________;
4
④“二级沉砷”中HO 与含砷物质反应的化学方程式为_____________________;
2 2
⑤沉淀X为_________________(填化学式)。
(2)冶炼废渣中的砷元素主要以As O 的形式存在,可用古氏试砷法半定量检测(As的
2 3
最低检出限为3.0×10-6g)。
步骤1:取10 g废渣样品,粉碎后与锌粉混合,加入HSO 共热,生成HAs气体。
2 4 3
步骤2:将HAs气体通入AgNO 溶液中,生成银镜和As O。
3 3 2 3
步骤3:取1g废渣样品,重复上述实验,未见银镜生成。
①AsH 的电子式为______________;
3
②步骤2的离子方程式为_________________________;
③固体废弃物的排放标准中,砷元素不得高于4.0×10一5g·kg一1,请通过计算说明该排放的
废渣中砷元素的含量(填“符合”、“不符合”)排放标准,原因是
_____________________。
【答案】(l)+①3 ② HAsO H++H AsO — ③ 沉淀过量的S2—,使As S(s)+3S2—
3 4 2 4 2 3
(aq) 2AsS 3—(aq)平衡左移,提高沉砷效果 ④ HAsO +H O=H AsO +H O ⑤
3 3 3 2 2 3 4 2
CaSO (2)① ②12Ag++2H As+3H O==12Ag↓+AsO+12H+ ③ 不符合,
4 3 2 2 3
因为该废渣砷含量为(3.0×10-6g÷10g)×1000g/kg=3.0×10—4g/kg大于排入标准4.0×10一5g·kg
一1
【解析】试题分析:(1)①根据HAsO ,氧元素显-2价,H元素显+1价,化合价代数和为0,
3 3
As的价态为+3价;②砷酸为弱酸,要分步电离,第一步电离:HAsO H++H AsO
3 4 2 4
—;③根据流程图,以及信息I,得出一级沉砷中加入FeSO 的作用是:沉淀过量的S2—,
4
使As S(s)+3S2—(aq) 2AsS 3—(aq)平衡左移,提高沉砷效果;④根据流程图,HO 作氧
2 3 3 2 2
化剂,把+3价As氧化成+5价,化合价升高2价,HO 中O的化合价降低2价,最小
2 2
公倍数为2,因此化学反应方程式为:HAsO +H O=H AsO +H O;⑤一级沉砷中加入
3 3 2 2 3 4 2
FeSO ,硫酸钙微溶于水,因此沉淀X为CaSO;(2)①As和N同主族,因此AsH 的电子
4 4 3
式,与NH 电子式相似,因此AsH 的电子式为: ;②银镜为Ag,AgNO 作氧
3 3 3
化剂,化合价有+1价→0价,化合价降低1价,HAs作还原剂,化合价由-3价→+3
3
价,化合价升高6价,最小公倍数为6,离子反应方程式为:12Ag+
+2H As+3H O==12Ag↓+AsO+12H+;③千克溶液中含As的质量为3.0×10-6×1000/10g/
3 2 2 3
kg=3.0×10-4>4.0×10-5,因此不合格。