文档内容
微专题35 非金属及其化合物制备流程与实验探究
(S、Se、Te、Cl、Br、I)
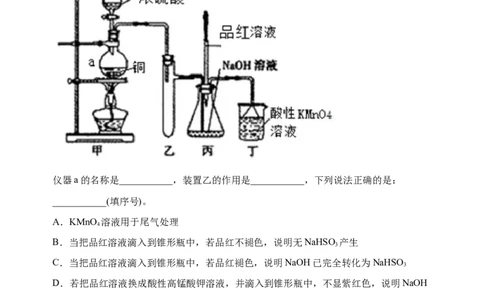
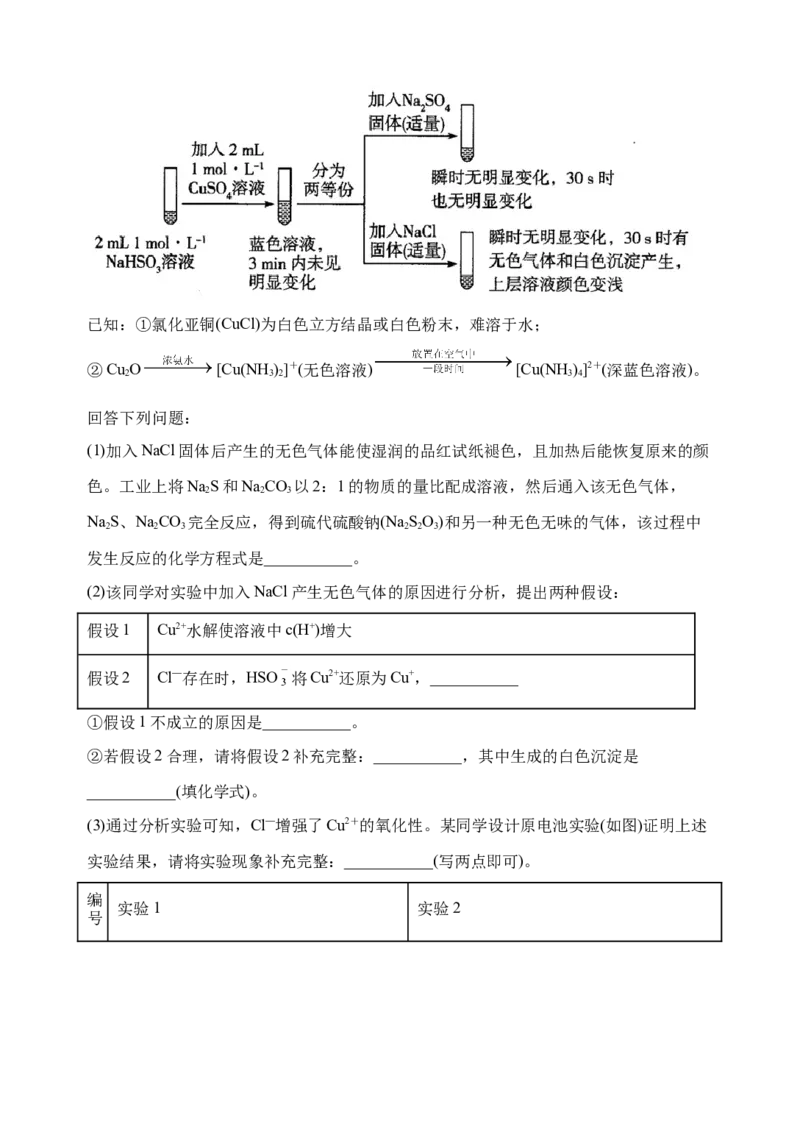
1.Ⅰ.实验室用浓硫酸与铜的反应制取少量NaHSO,实验装置如图所示:
3
仪器a的名称是___________,装置乙的作用是___________,下列说法正确的是:
___________(填序号)。
A.KMnO 溶液用于尾气处理
4
B.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO 产生
3
C.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO
3
D.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH
已完全转化为NaHSO
3
Ⅱ.某同学为探究NaHSO 溶液与Cu2+的反应,查阅资料设计如下实验:
3已知:①氯化亚铜(CuCl)为白色立方结晶或白色粉末,难溶于水;
②Cu O [Cu(NH )]+(无色溶液) [Cu(NH )]2+(深蓝色溶液)。
2 3 2 3 4
回答下列问题:
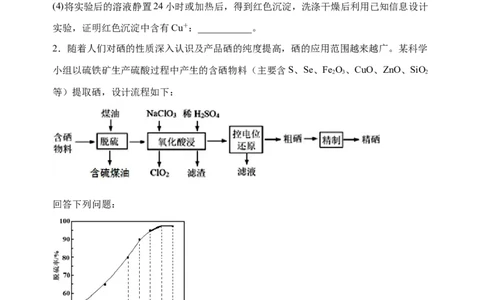
(1)加入NaCl固体后产生的无色气体能使湿润的品红试纸褪色,且加热后能恢复原来的颜
色。工业上将NaS和NaCO 以2:1的物质的量比配成溶液,然后通入该无色气体,
2 2 3
NaS、NaCO 完全反应,得到硫代硫酸钠(Na SO)和另一种无色无味的气体,该过程中
2 2 3 2 2 3
发生反应的化学方程式是___________。
(2)该同学对实验中加入NaCl产生无色气体的原因进行分析,提出两种假设:
假设1 Cu2+水解使溶液中c(H+)增大
假设2 Cl—存在时,HSO 将Cu2+还原为Cu+,___________
①假设1不成立的原因是___________。
②若假设2合理,请将假设2补充完整:___________,其中生成的白色沉淀是
___________(填化学式)。
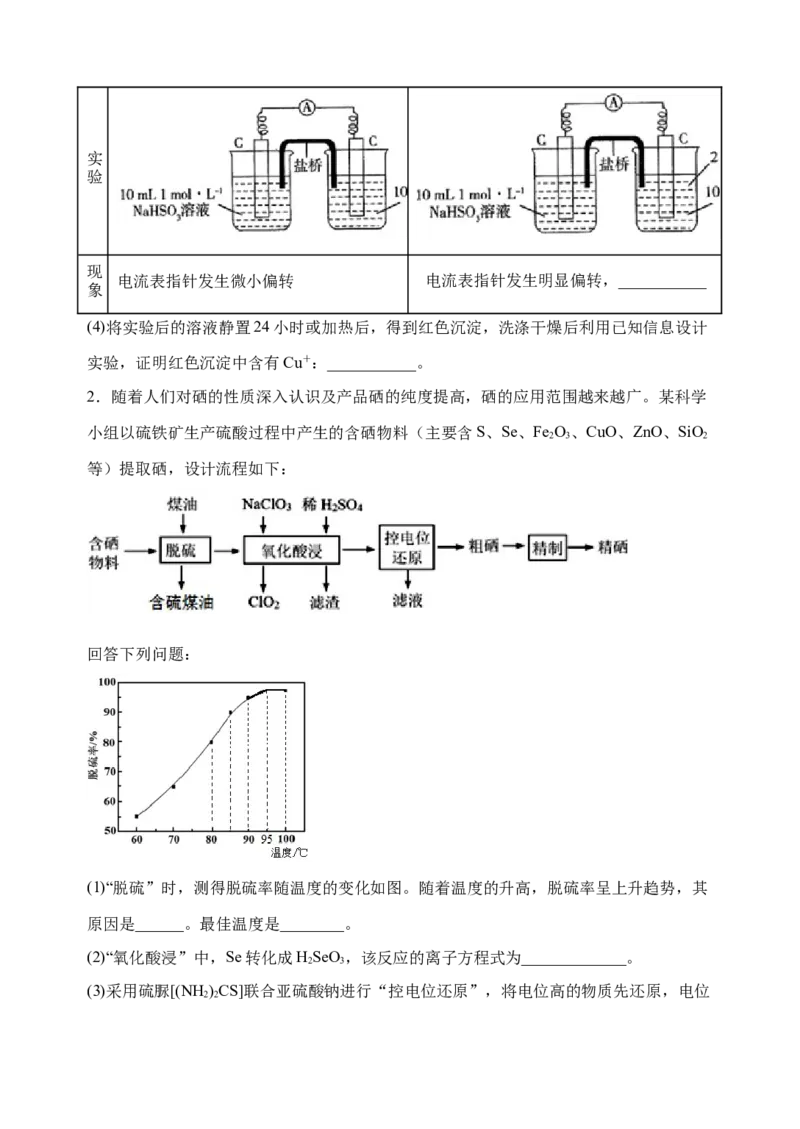
(3)通过分析实验可知,Cl—增强了Cu2+的氧化性。某同学设计原电池实验(如图)证明上述
实验结果,请将实验现象补充完整:___________(写两点即可)。
编
实验1 实验2
号实
验
现
电流表指针发生微小偏转 电流表指针发生明显偏转,___________
象
(4)将实验后的溶液静置24小时或加热后,得到红色沉淀,洗涤干燥后利用已知信息设计
实验,证明红色沉淀中含有Cu+:___________。
2.随着人们对硒的性质深入认识及产品硒的纯度提高,硒的应用范围越来越广。某科学
小组以硫铁矿生产硫酸过程中产生的含硒物料(主要含S、Se、Fe O、CuO、ZnO、SiO
2 3 2
等)提取硒,设计流程如下:
回答下列问题:
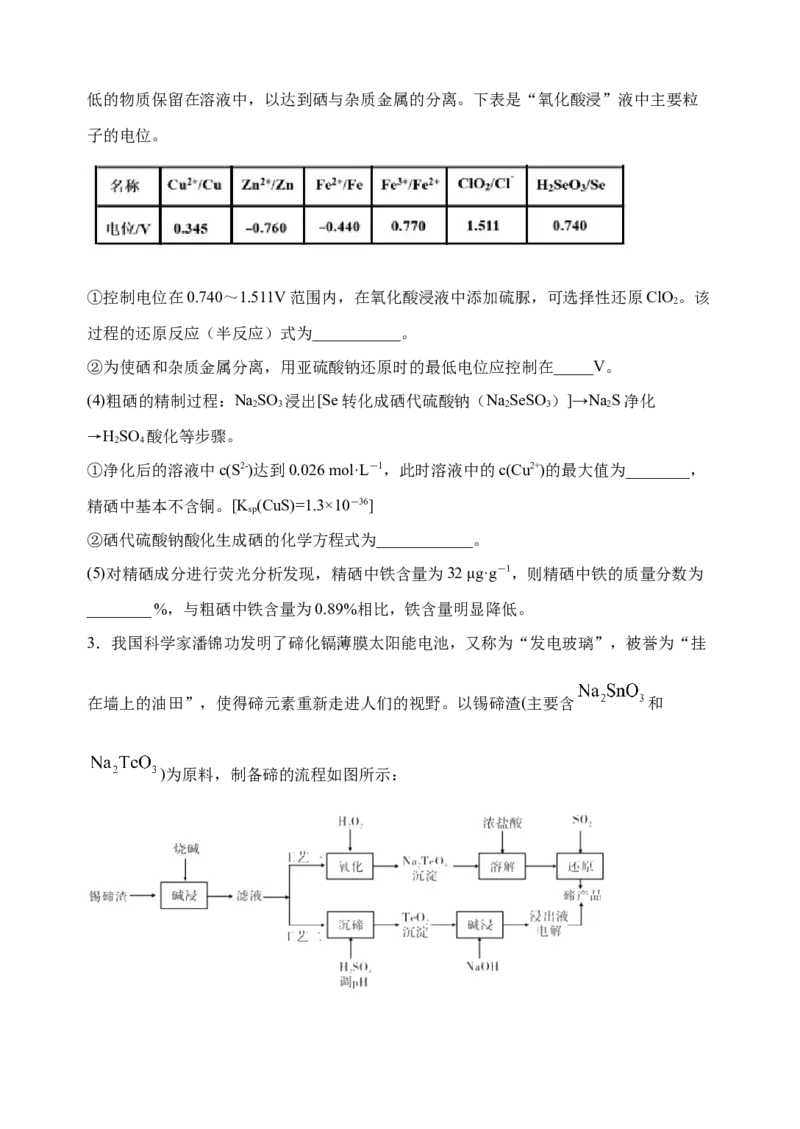
(1)“脱硫”时,测得脱硫率随温度的变化如图。随着温度的升高,脱硫率呈上升趋势,其
原因是______。最佳温度是________。
(2)“氧化酸浸”中,Se转化成HSeO,该反应的离子方程式为_____________。
2 3
(3)采用硫脲[(NH )CS]联合亚硫酸钠进行“控电位还原”,将电位高的物质先还原,电位
2 2低的物质保留在溶液中,以达到硒与杂质金属的分离。下表是“氧化酸浸”液中主要粒
子的电位。
①控制电位在0.740~1.511V范围内,在氧化酸浸液中添加硫脲,可选择性还原ClO 。该
2
过程的还原反应(半反应)式为___________。
②为使硒和杂质金属分离,用亚硫酸钠还原时的最低电位应控制在_____V。
(4)粗硒的精制过程:NaSO 浸出[Se转化成硒代硫酸钠(NaSeSO )]→Na S净化
2 3 2 3 2
→HSO 酸化等步骤。
2 4
①净化后的溶液中c(S2-)达到0.026 mol·L-1,此时溶液中的c(Cu2+)的最大值为________,
精硒中基本不含铜。[K (CuS)=1.3×10-36]
sp
②硒代硫酸钠酸化生成硒的化学方程式为____________。
(5)对精硒成分进行荧光分析发现,精硒中铁含量为32 μg·g-1,则精硒中铁的质量分数为
________ %,与粗硒中铁含量为0.89%相比,铁含量明显降低。
3.我国科学家潘锦功发明了碲化镉薄膜太阳能电池,又称为“发电玻璃”,被誉为“挂
在墙上的油田”,使得碲元素重新走进人们的视野。以锡碲渣(主要含 和
)为原料,制备碲的流程如图所示:已知:Ⅰ.锡酸钠( )和亚碲酸钠( )均易溶于碱;
Ⅱ. 微溶于水,易溶于较浓的强酸和强碱。
(1)在生产过程中,要将锡碲渣粉碎,其目的是___________。
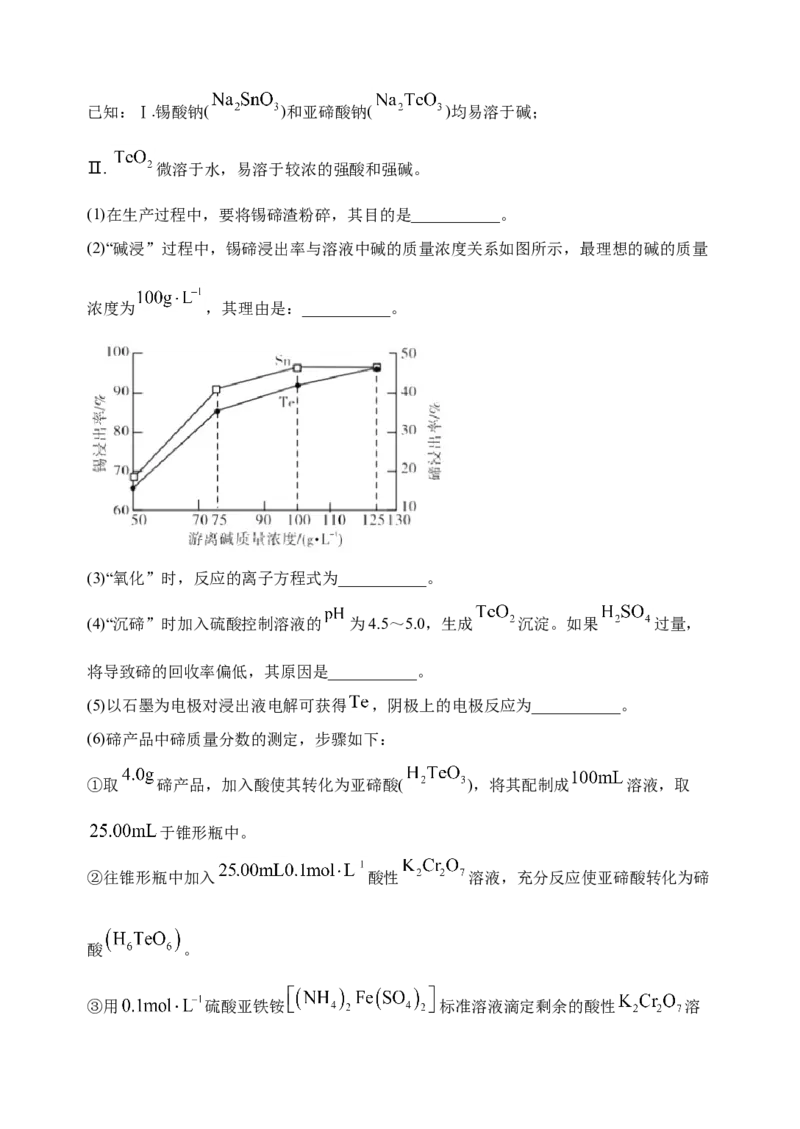
(2)“碱浸”过程中,锡碲浸出率与溶液中碱的质量浓度关系如图所示,最理想的碱的质量
浓度为 ,其理由是:___________。
(3)“氧化”时,反应的离子方程式为___________。
(4)“沉碲”时加入硫酸控制溶液的 为4.5~5.0,生成 沉淀。如果 过量,
将导致碲的回收率偏低,其原因是___________。
(5)以石墨为电极对浸出液电解可获得 ,阴极上的电极反应为___________。
(6)碲产品中碲质量分数的测定,步骤如下:
①取 碲产品,加入酸使其转化为亚碲酸( ),将其配制成 溶液,取
于锥形瓶中。
②往锥形瓶中加入 酸性 溶液,充分反应使亚碲酸转化为碲
酸 。
③用 硫酸亚铁铵 标准溶液滴定剩余的酸性 溶液,滴入几滴试亚铁灵指示剂至终点显红色,进行三次平行实验,平均消耗 硫
酸亚铁铵标准溶液。试计算该碲产品中碲的质量分数为___________。(保留小数点后面二
位数字)
4.亚硝酰氯(NOCl,熔点:-64.5℃,沸点:-5.5℃)为红褐色液体或黄色气体,具有刺鼻
恶臭味,遇水剧烈水解生成氮的两种氧化物与氯化氢,易溶于浓硫酸。常可用于合成清
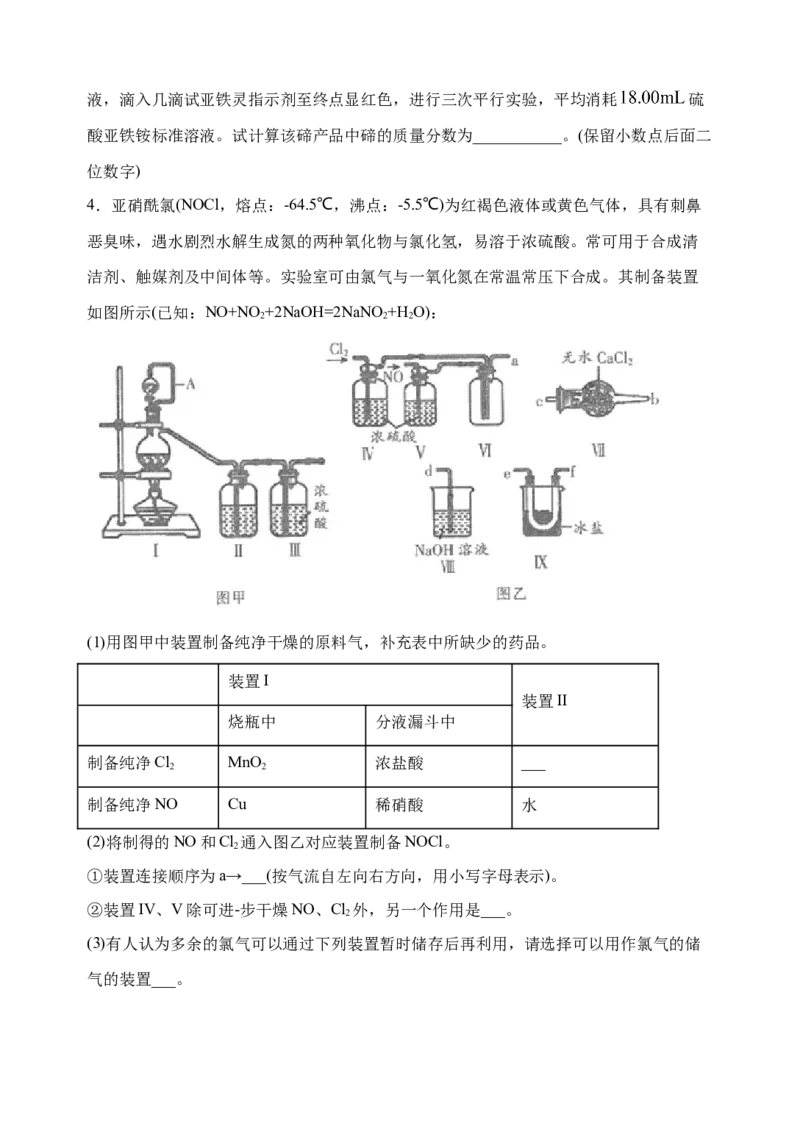
洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。其制备装置
如图所示(已知:NO+NO +2NaOH=2NaNO +H O):
2 2 2
(1)用图甲中装置制备纯净干燥的原料气,补充表中所缺少的药品。
装置I
装置II
烧瓶中 分液漏斗中
制备纯净Cl MnO 浓盐酸 ___
2 2
制备纯净NO Cu 稀硝酸 水
(2)将制得的NO和Cl 通入图乙对应装置制备NOCl。
2
①装置连接顺序为a→___(按气流自左向右方向,用小写字母表示)。
②装置IV、V除可进-步干燥NO、Cl 外,另一个作用是___。
2
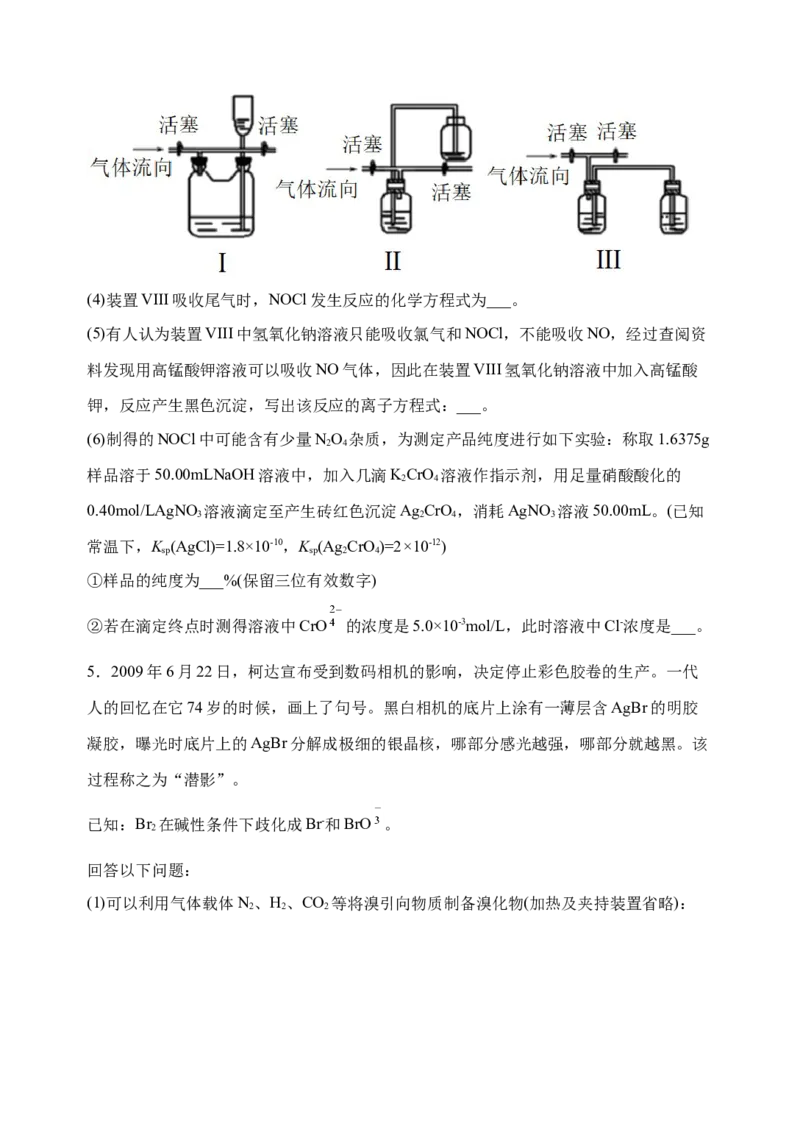
(3)有人认为多余的氯气可以通过下列装置暂时储存后再利用,请选择可以用作氯气的储
气的装置___。(4)装置VIII吸收尾气时,NOCl发生反应的化学方程式为___。
(5)有人认为装置VIII中氢氧化钠溶液只能吸收氯气和NOCl,不能吸收NO,经过查阅资
料发现用高锰酸钾溶液可以吸收NO气体,因此在装置VIII氢氧化钠溶液中加入高锰酸
钾,反应产生黑色沉淀,写出该反应的离子方程式:___。
(6)制得的NOCl中可能含有少量NO 杂质,为测定产品纯度进行如下实验:称取1.6375g
2 4
样品溶于50.00mLNaOH溶液中,加入几滴KCrO 溶液作指示剂,用足量硝酸酸化的
2 4
0.40mol/LAgNO 溶液滴定至产生砖红色沉淀Ag CrO,消耗AgNO 溶液50.00mL。(已知
3 2 4 3
常温下,K (AgCl)=1.8×10-10,K (Ag CrO)=2×10-12)
sp sp 2 4
①样品的纯度为___%(保留三位有效数字)
②若在滴定终点时测得溶液中CrO 的浓度是5.0×10-3mol/L,此时溶液中Cl-浓度是___。
5.2009年6月22日,柯达宣布受到数码相机的影响,决定停止彩色胶卷的生产。一代
人的回忆在它74岁的时候,画上了句号。黑白相机的底片上涂有一薄层含AgBr的明胶
凝胶,曝光时底片上的AgBr分解成极细的银晶核,哪部分感光越强,哪部分就越黑。该
过程称之为“潜影”。
已知:Br 在碱性条件下歧化成Br-和BrO 。
2
回答以下问题:
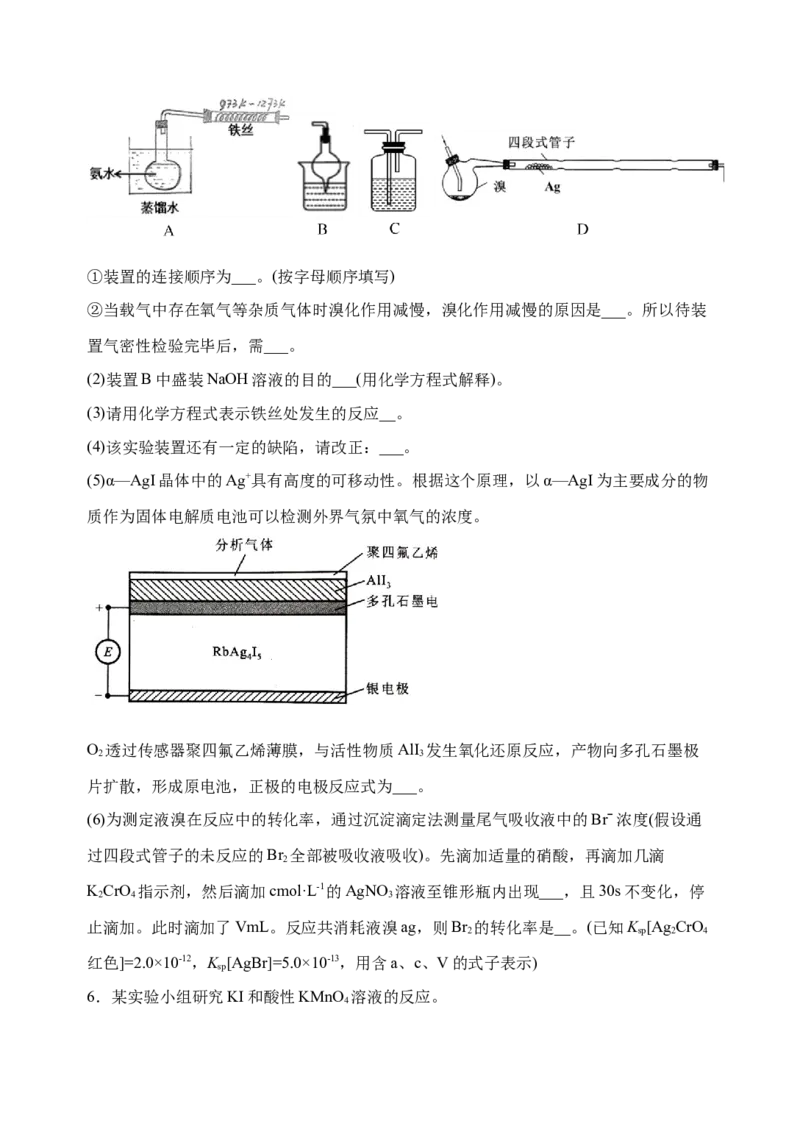
(1)可以利用气体载体N、H、CO 等将溴引向物质制备溴化物(加热及夹持装置省略):
2 2 2①装置的连接顺序为___。(按字母顺序填写)
②当载气中存在氧气等杂质气体时溴化作用减慢,溴化作用减慢的原因是___。所以待装
置气密性检验完毕后,需___。
(2)装置B中盛装NaOH溶液的目的___(用化学方程式解释)。
(3)请用化学方程式表示铁丝处发生的反应__。
(4)该实验装置还有一定的缺陷,请改正:___。
(5)α—AgI晶体中的Ag+具有高度的可移动性。根据这个原理,以α—AgI为主要成分的物
质作为固体电解质电池可以检测外界气氛中氧气的浓度。
O 透过传感器聚四氟乙烯薄膜,与活性物质AlI 发生氧化还原反应,产物向多孔石墨极
2 3
片扩散,形成原电池,正极的电极反应式为___。
(6)为测定液溴在反应中的转化率,通过沉淀滴定法测量尾气吸收液中的Brˉ浓度(假设通
过四段式管子的未反应的Br 全部被吸收液吸收)。先滴加适量的硝酸,再滴加几滴
2
KCrO 指示剂,然后滴加cmol·L-1的AgNO 溶液至锥形瓶内出现___,且30s不变化,停
2 4 3
止滴加。此时滴加了VmL。反应共消耗液溴ag,则Br 的转化率是__。(已知K [Ag CrO
2 sp 2 4
红色]=2.0×10-12,K [AgBr]=5.0×10-13,用含a、c、V的式子表示)
sp
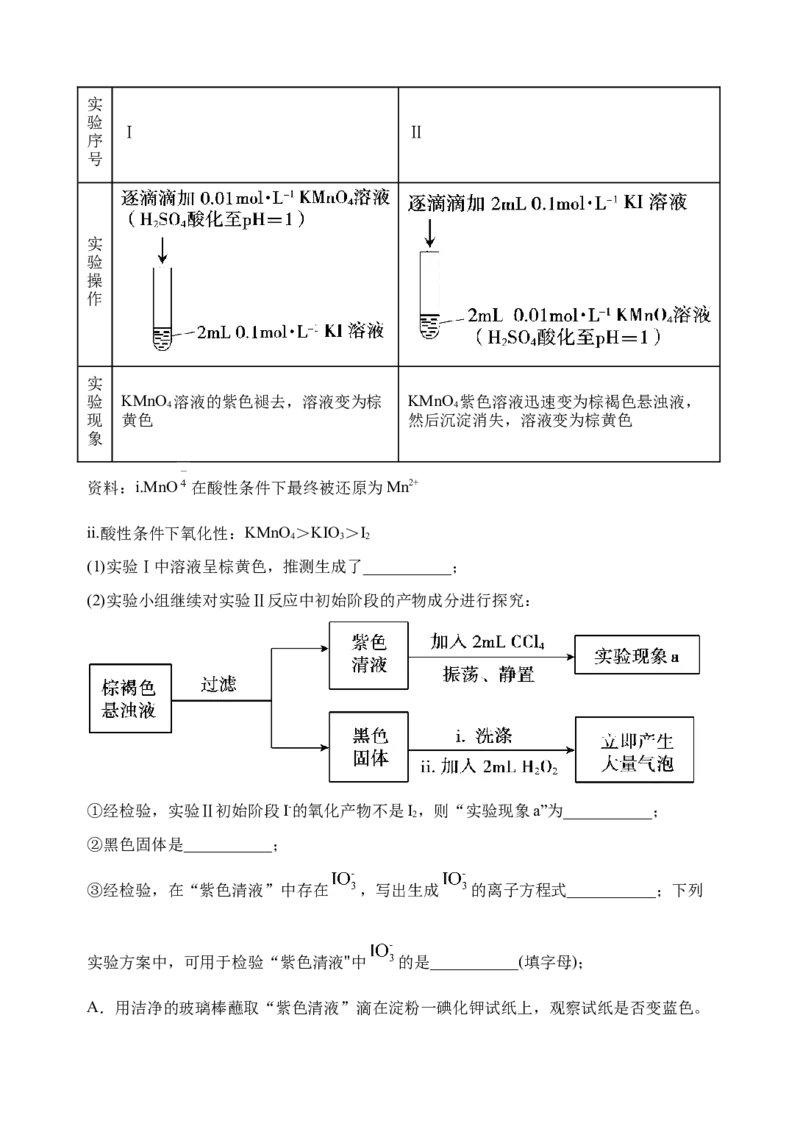
6.某实验小组研究KI和酸性KMnO 溶液的反应。
4实
验
Ⅰ Ⅱ
序
号
实
验
操
作
实
验 KMnO 溶液的紫色褪去,溶液变为棕 KMnO 紫色溶液迅速变为棕褐色悬浊液,
4 4
现 黄色 然后沉淀消失,溶液变为棕黄色
象
资料:i.MnO 在酸性条件下最终被还原为Mn2+
ii.酸性条件下氧化性:KMnO >KIO >I
4 3 2
(1)实验Ⅰ中溶液呈棕黄色,推测生成了___________;
(2)实验小组继续对实验Ⅱ反应中初始阶段的产物成分进行探究:
①经检验,实验Ⅱ初始阶段I-的氧化产物不是I,则“实验现象a”为___________;
2
②黑色固体是___________;
③经检验,在“紫色清液”中存在 ,写出生成 的离子方程式___________;下列
实验方案中,可用于检验“紫色清液"中 的是___________(填字母);
A.用洁净的玻璃棒蘸取“紫色清液”滴在淀粉一碘化钾试纸上,观察试纸是否变蓝色。B.取少量“紫色清液”于试管中,向其中加入几滴淀粉溶液,溶液不变蓝,再加入过量
NaHSO 溶液,观察溶液是否变蓝色。
3
C.取少量“紫色清液”于试管中,向其中加入稀硝酸酸化,再加入几滴硝酸银溶液,观
察是否生成黄色沉淀。
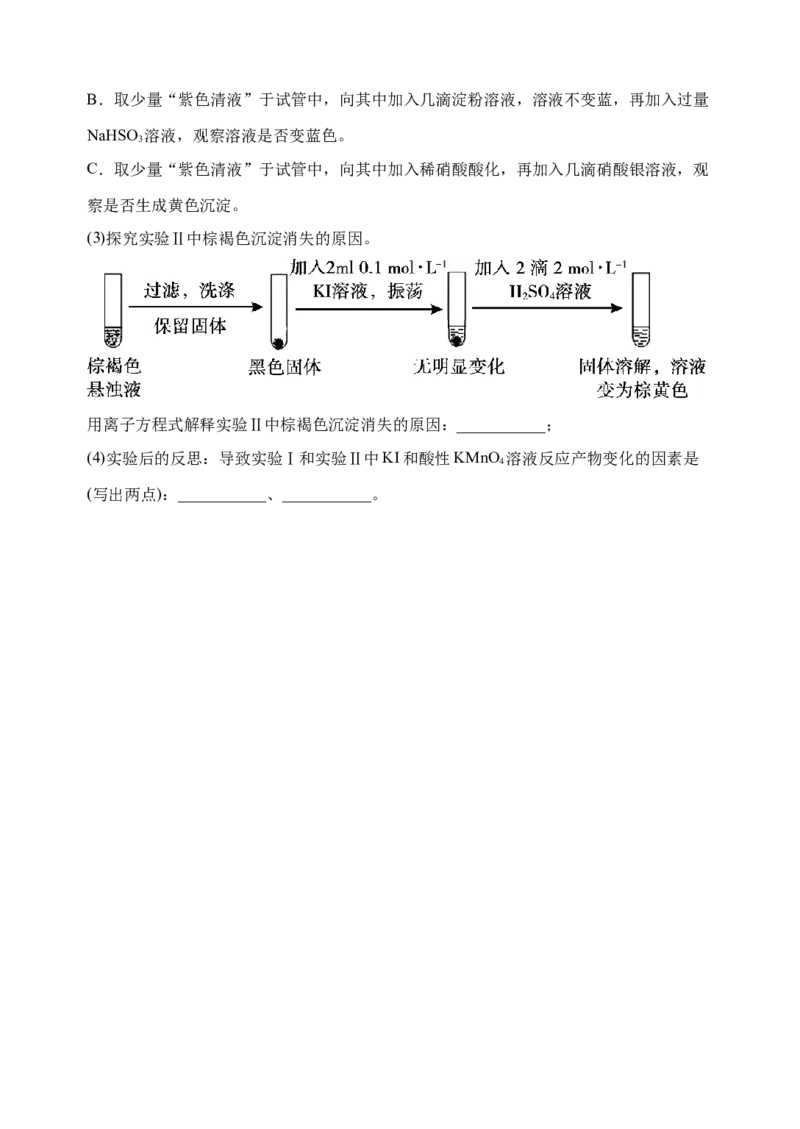
(3)探究实验Ⅱ中棕褐色沉淀消失的原因。
用离子方程式解释实验Ⅱ中棕褐色沉淀消失的原因:___________;
(4)实验后的反思:导致实验Ⅰ和实验Ⅱ中KI和酸性KMnO 溶液反应产物变化的因素是
4
(写出两点):___________、___________。