文档内容
押广东卷第 9-10 题
原电池、电解池的基本工作原理 价类二维图
核心考点 考情统计 考向预测 备考策略
原电池的基本 2023·广东卷,6 考查原电池的工作原理,主要 1.回归教材,掌握原电池的
工作原理 2021·广东卷,9 考查正负极的判断,体现基础 工作原理,形成解题模型。
性。 2.回归教材,将氯碱工业、
电解池的基本 考查电解池的工作原理,主要 电镀、电解精炼知识进行迁
2022·广东卷,10
工作原理 基于氯碱工业、电镀、电解精 移。
炼,体现应用性。 3. 归纳典型元素的价类二维
2023·广东卷,10 考查元素及其化合物的相互转 图,掌握元素及其化合物的相
价类二维图
2021·广东卷,10 化,体现基础性和综合性。 互转化和性质。
1.(2023广东卷,6)负载有 和 的活性炭,可选择性去除 实现废酸的纯化,其工作原理如图。
下列说法正确的是
A. 作原电池正极
B.电子由 经活性炭流向
C. 表面发生的电极反应:
D.每消耗标准状况下 的 ,最多去除
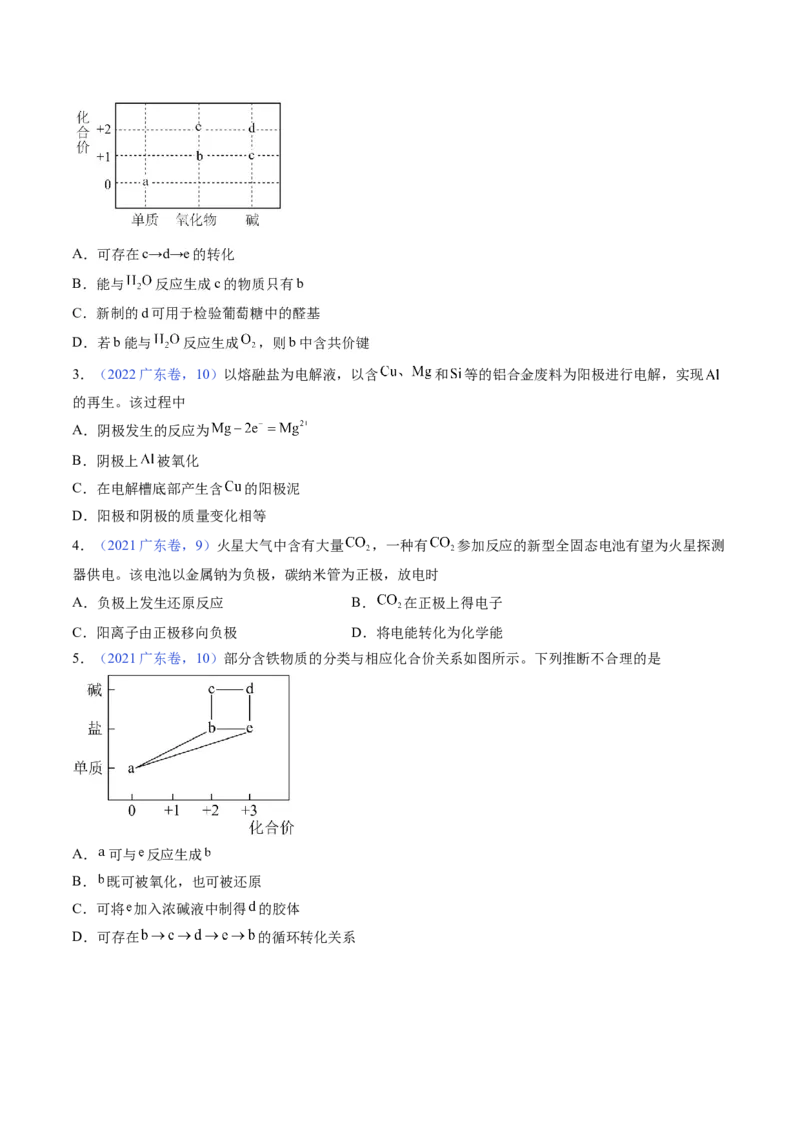
2.(2023广东卷,10)部分含 或含 物质的分类与相应化合价关系如图所示。下列推断不合理的是A.可存在c→d→e的转化
B.能与 反应生成c的物质只有b
C.新制的d可用于检验葡萄糖中的醛基
D.若b能与 反应生成 ,则b中含共价键
3.(2022广东卷,10)以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,实现
的再生。该过程中
A.阴极发生的反应为
B.阴极上 被氧化
C.在电解槽底部产生含 的阳极泥
D.阳极和阴极的质量变化相等
4.(2021广东卷,9)火星大气中含有大量 ,一种有 参加反应的新型全固态电池有望为火星探测
器供电。该电池以金属钠为负极,碳纳米管为正极,放电时
A.负极上发生还原反应 B. 在正极上得电子
C.阳离子由正极移向负极 D.将电能转化为化学能
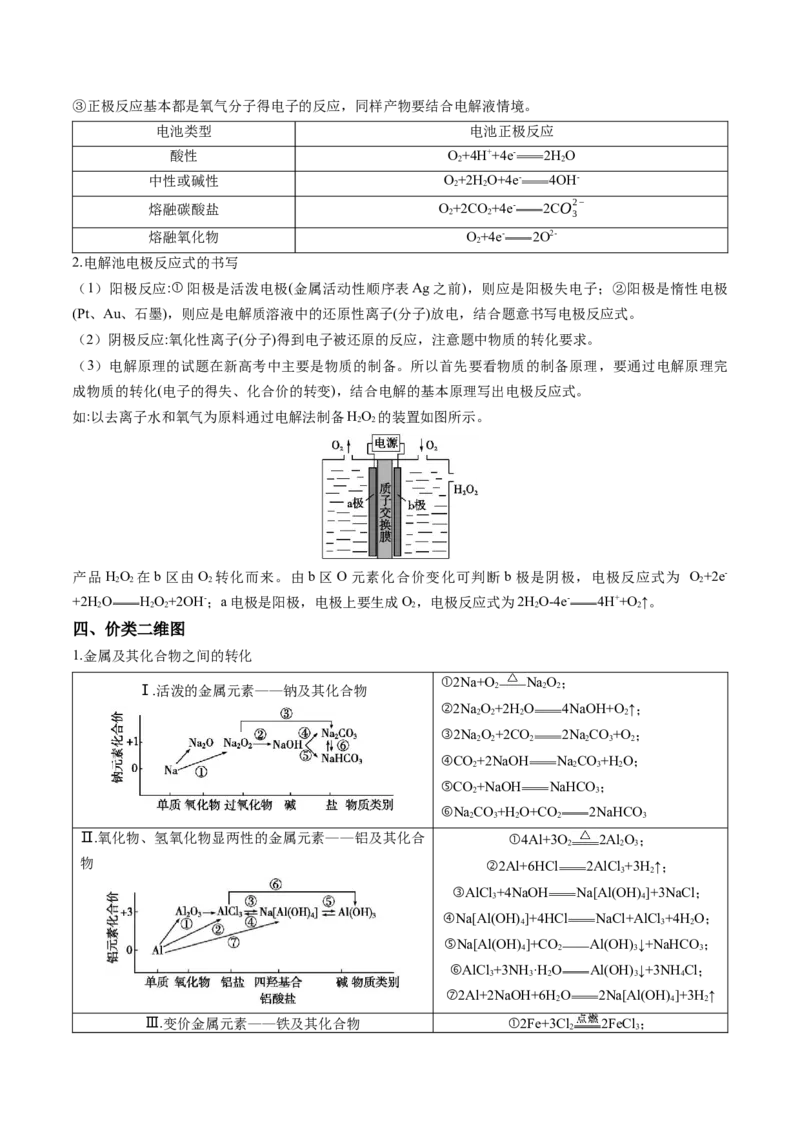
5.(2021广东卷,10)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是
A. 可与 反应生成
B. 既可被氧化,也可被还原
C.可将 加入浓碱液中制得 的胶体
D.可存在 的循环转化关系一、原电池的基本工作原理
1.原电池模型和原理
2.确定正、负极的依据
依据 正极 负极
反应类型 还原反应 氧化反应
电极变化 质量增加,逸出气体 溶解、质量变轻
电流方向 流出 流入
电子流向 流入 流出
离子移动方向 阳离子移动方向 阴离子移动方向
电极材料 较不活泼金属或导电非金属 较活泼金属
[注意] 根据电极材料确定正、负极通常情况适用,但根本依据为自发的氧化还原反应。如 Mg-Al、NaOH
溶液形成的原电池中,铝作负极,因为只有铝与NaOH溶液发生氧化还原反应。
二、电解池的基本工作原理
1.电解池模型和原理
(1)直流电源的正极(阳极)有强的氧化能力;直流电源的负极(阴极)有强的还原能力。
(2)电极上微粒的放电顺序。
①阴极:取决于微粒的氧化性强弱,氧化性强的先得到电子,与电极材料无关。
常见阳离子放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>Pb2+>Sn2+>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+。
②阳极:若是非惰性电极作阳极,则电极失电子;若是惰性电极(Pt、C)作阳极,还原性强的先失去电子。
常见阴离子放电顺序:S2->I->Br->Cl->OH->含氧酸根离子(NO- 、SO2− 、CO2− )>F-。
3 4 3
③电极上离子的放电顺序取决于其氧化性、还原性,可能会出现强氧化性阴离子在阴极放电;强还原性阳
离子在阳极放电。
2.惰性电极电解电解质溶液的四种类型
电解 常见电解 阳极 阴极 电解质类型 质实例 产物 产物 溶液变化
NaOH、
电解水 HSO 、 O H 浓度增大
2 4 2 2
NaSO
2 4
电解 HCl、 卤素 H、
2
浓度减小
电解质 CuCl 单质(Cl ) 金属(Cu)
2 2
放氢 卤素
NaCl H 生成强碱
2
生碱型 单质(Cl )
2
放氧 CuSO 、 金属 生成
4
O
2
生酸型 AgNO (Cu、Ag) 含氧酸
3
[注意] (1)电解后溶液pH的变化一方面要考虑酸碱的生成,还要考虑电解质溶液浓度变化导致水解程度
的变化。
(2)电解质溶液的复原问题要本着两电极析出什么(元素),就加入什么(恰当物质)的原则。
3.电解池阳极和阴极确定
(1)若装置中给出直流电源,则可直接确定电解装置的阳极、阴极。
(2)若装置中没有给出直流电源,则要根据电解过程的特征先确定电解装置的阳极、阴极。
依据 阴极 阳极
电流方向 流出 流入
电子流向 流入 流出
离子移
阳离子移动方向 阴离子移动方向
动方向
电极产物 金属(增重)、H 电极溶解、O、Cl 等非金属单质
2 2 2
pH变化 增大(碱性增强) 减小(酸性增强)
反应类型 还原反应 氧化反应
三、电极反应式的书写
1.原电池电极反应式的书写
(1)结合电池的电解液情境写出电极反应式。
①负极反应:还原剂失去电子的氧化反应(注意负极失电子产物与电解质溶液反应生成恰当生成物)。
②正极反应:氧化剂得到电子的还原反应(注意正极得电子产物与电解质溶液反应生成恰当生成物)。
当正极上的反应物是O 时,若电解质溶液为中性或碱性,则水必须写入正极反应式中,与O 反应生成
2 2
OH-,电极反应式为O+2H O+4e- 4OH-;若电解质溶液为酸性,则H+必须写入正极反应式中,O 得电
2 2 2
子与H+反应生成水,电极反应式为O+4H++4e- 2HO。
2 2
(2)燃料电池电极反应式的书写。
①燃料电池基本都是燃料(还原剂)与氧气(或氧化性气体)进行的氧化还原反应。
②负极反应都是燃料物质失电子的反应,一定要结合电解液情境确定产物:有机物燃料电池在酸性电解质溶
液或熔融固体电解质中生成CO;有机物燃料电池在碱性电解质溶液中生成CO2−
。
2 3③正极反应基本都是氧气分子得电子的反应,同样产物要结合电解液情境。
电池类型 电池正极反应
酸性 O+4H++4e- 2HO
2 2
中性或碱性 O+2H O+4e- 4OH-
2 2
熔融碳酸盐 O+2CO +4e- 2CO2−
2 2 3
熔融氧化物 O+4e- 2O2-
2
2.电解池电极反应式的书写
(1)阳极反应:①阳极是活泼电极(金属活动性顺序表Ag之前),则应是阳极失电子;②阳极是惰性电极
(Pt、Au、石墨),则应是电解质溶液中的还原性离子(分子)放电,结合题意书写电极反应式。
(2)阴极反应:氧化性离子(分子)得到电子被还原的反应,注意题中物质的转化要求。
(3)电解原理的试题在新高考中主要是物质的制备。所以首先要看物质的制备原理,要通过电解原理完
成物质的转化(电子的得失、化合价的转变),结合电解的基本原理写出电极反应式。
如:以去离子水和氧气为原料通过电解法制备HO 的装置如图所示。
2 2
产品HO 在b区由O 转化而来。由b区O元素化合价变化可判断 b极是阴极,电极反应式为 O+2e-
2 2 2 2
+2H O HO+2OH-;a电极是阳极,电极上要生成O,电极反应式为2HO-4e- 4H++O ↑。
2 2 2 2 2 2
四、价类二维图
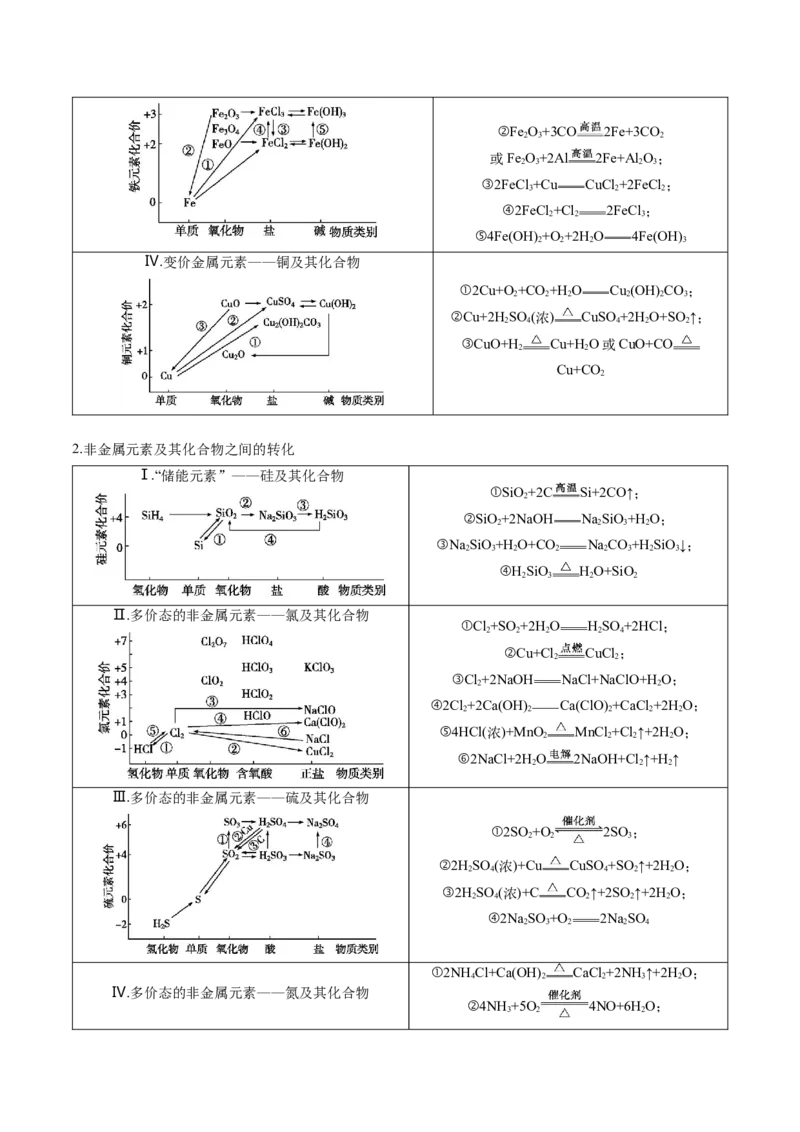
1.金属及其化合物之间的转化
①2Na+O NaO;
Ⅰ.活泼的金属元素——钠及其化合物 2 2 2
②2Na O+2H O 4NaOH+O ↑;
2 2 2 2
③2Na O+2CO 2NaCO+O ;
2 2 2 2 3 2
④CO +2NaOH NaCO+H O;
2 2 3 2
⑤CO+NaOH NaHCO ;
2 3
⑥Na CO+H O+CO 2NaHCO
2 3 2 2 3
Ⅱ.氧化物、氢氧化物显两性的金属元素——铝及其化合 ①4Al+3O 2Al O;
2 2 3
物
②2Al+6HCl 2AlCl +3H ↑;
3 2
③AlCl +4NaOH Na[Al(OH)]+3NaCl;
3 4
④Na[Al(OH) ]+4HCl NaCl+AlCl +4H O;
4 3 2
⑤Na[Al(OH) ]+CO Al(OH) ↓+NaHCO;
4 2 3 3
⑥AlCl +3NH·H O Al(OH) ↓+3NHCl;
3 3 2 3 4
⑦2Al+2NaOH+6H O 2Na[Al(OH)]+3H ↑
2 4 2
Ⅲ.变价金属元素——铁及其化合物 ①2Fe+3Cl 2FeCl ;
2 3②Fe O+3CO 2Fe+3CO
2 3 2
或Fe O+2Al 2Fe+Al O;
2 3 2 3
③2FeCl +Cu CuCl +2FeCl ;
3 2 2
④2FeCl +Cl 2FeCl ;
2 2 3
⑤4Fe(OH) +O +2H O 4Fe(OH)
2 2 2 3
Ⅳ.变价金属元素——铜及其化合物
①2Cu+O +CO +H O Cu (OH) CO;
2 2 2 2 2 3
②Cu+2HSO (浓) CuSO +2H O+SO ↑;
2 4 4 2 2
③CuO+H Cu+H O或CuO+CO
2 2
Cu+CO
2
2.非金属元素及其化合物之间的转化
Ⅰ.“储能元素”——硅及其化合物
①SiO+2C Si+2CO↑;
2
②SiO +2NaOH NaSiO+H O;
2 2 3 2
③Na SiO+H O+CO NaCO+H SiO↓;
2 3 2 2 2 3 2 3
④H SiO HO+SiO
2 3 2 2
Ⅱ.多价态的非金属元素——氯及其化合物
①Cl+SO+2H O HSO +2HCl;
2 2 2 2 4
②Cu+Cl CuCl ;
2 2
③Cl+2NaOH NaCl+NaClO+H O;
2 2
④2Cl +2Ca(OH) Ca(ClO) +CaCl +2H O;
2 2 2 2 2
⑤4HCl(浓)+MnO MnCl +Cl↑+2H O;
2 2 2 2
⑥2NaCl+2H O 2NaOH+Cl ↑+H ↑
2 2 2
Ⅲ.多价态的非金属元素——硫及其化合物
①2SO +O 2SO ;
2 2 3
②2H SO (浓)+Cu CuSO +SO↑+2H O;
2 4 4 2 2
③2HSO (浓)+C CO↑+2SO↑+2H O;
2 4 2 2 2
④2Na SO +O 2NaSO
2 3 2 2 4
①2NH Cl+Ca(OH) CaCl +2NH↑+2H O;
4 2 2 3 2
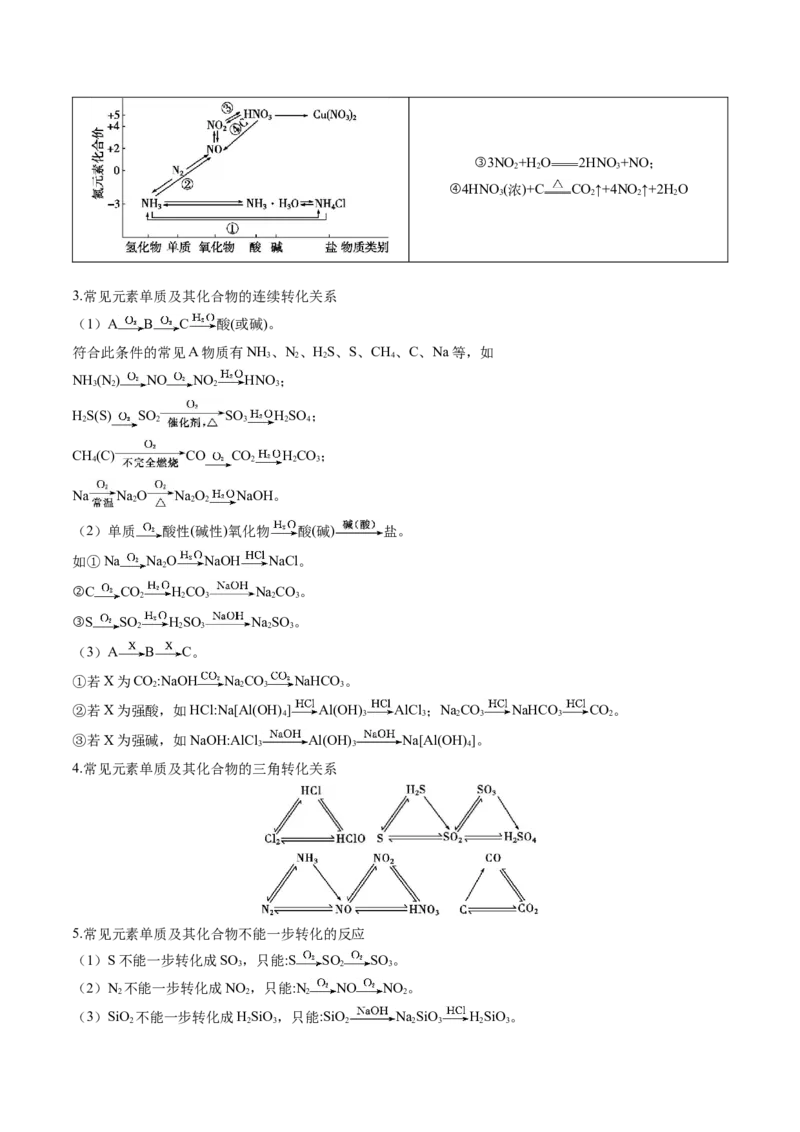
Ⅳ.多价态的非金属元素——氮及其化合物
②4NH +5O 4NO+6H O;
3 2 2③3NO +H O 2HNO+NO;
2 2 3
④4HNO (浓)+C CO↑+4NO↑+2H O
3 2 2 2
3.常见元素单质及其化合物的连续转化关系
(1)A B C 酸(或碱)。
符合此条件的常见A物质有NH 、N、HS、S、CH、C、Na等,如
3 2 2 4
NH (N ) NO NO HNO;
3 2 2 3
HS(S) SO SO HSO ;
2 2 3 2 4
CH(C) CO CO HCO;
4 2 2 3
Na NaO NaO NaOH。
2 2 2
(2)单质 酸性(碱性)氧化物 酸(碱) 盐。
如①Na NaO NaOH NaCl。
2
②C CO HCO NaCO。
2 2 3 2 3
③S SO HSO NaSO 。
2 2 3 2 3
(3)A B C。
①若X为CO:NaOH NaCO NaHCO 。
2 2 3 3
②若X为强酸,如HCl:Na[Al(OH) ] Al(OH) AlCl ;NaCO NaHCO CO。
4 3 3 2 3 3 2
③若X为强碱,如NaOH:AlCl Al(OH) Na[Al(OH)]。
3 3 4
4.常见元素单质及其化合物的三角转化关系
5.常见元素单质及其化合物不能一步转化的反应
(1)S不能一步转化成SO ,只能:S SO SO 。
3 2 3
(2)N 不能一步转化成NO ,只能:N NO NO 。
2 2 2 2
(3)SiO 不能一步转化成HSiO,只能:SiO NaSiO HSiO。
2 2 3 2 2 3 2 3(4)Cl 不能一步转化成FeCl ,需多步转化。
2 2
(5)CuO(等金属氧化物)不能一步转化成Cu(OH) (等金属氢氧化物),需多步转化。
2
考点一 原电池的基本工作原理
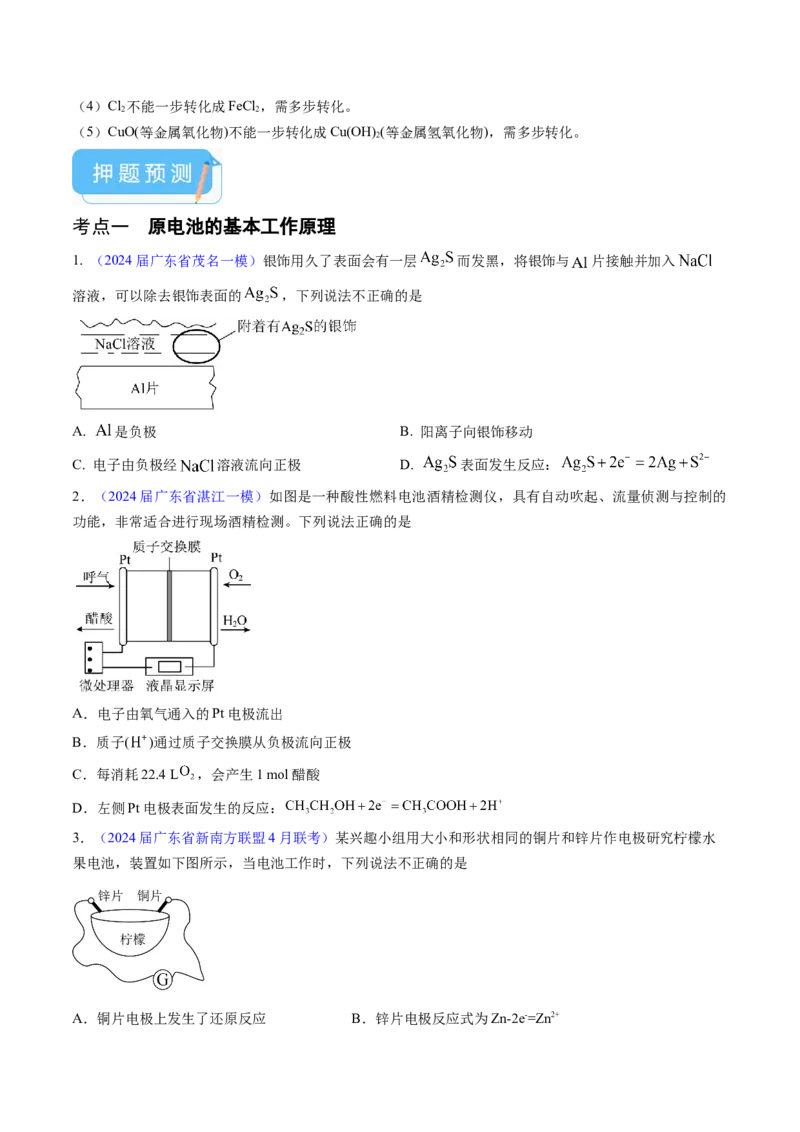
1. (2024届广东省茂名一模)银饰用久了表面会有一层 而发黑,将银饰与 片接触并加入
溶液,可以除去银饰表面的 ,下列说法不正确的是
A. 是负极 B. 阳离子向银饰移动
C. 电子由负极经 溶液流向正极 D. 表面发生反应:
2.(2024届广东省湛江一模)如图是一种酸性燃料电池酒精检测仪,具有自动吹起、流量侦测与控制的
功能,非常适合进行现场酒精检测。下列说法正确的是
A.电子由氧气通入的Pt电极流出
B.质子( )通过质子交换膜从负极流向正极
C.每消耗22.4 L ,会产生1 mol醋酸
D.左侧Pt电极表面发生的反应:
3.(2024届广东省新南方联盟4月联考)某兴趣小组用大小和形状相同的铜片和锌片作电极研究柠檬水
果电池,装置如下图所示,当电池工作时,下列说法不正确的是
A.铜片电极上发生了还原反应 B.锌片电极反应式为Zn-2e-=Zn2+C.该装置实现了从化学能向电能的转化 D.电流从锌片经导线流向铜片
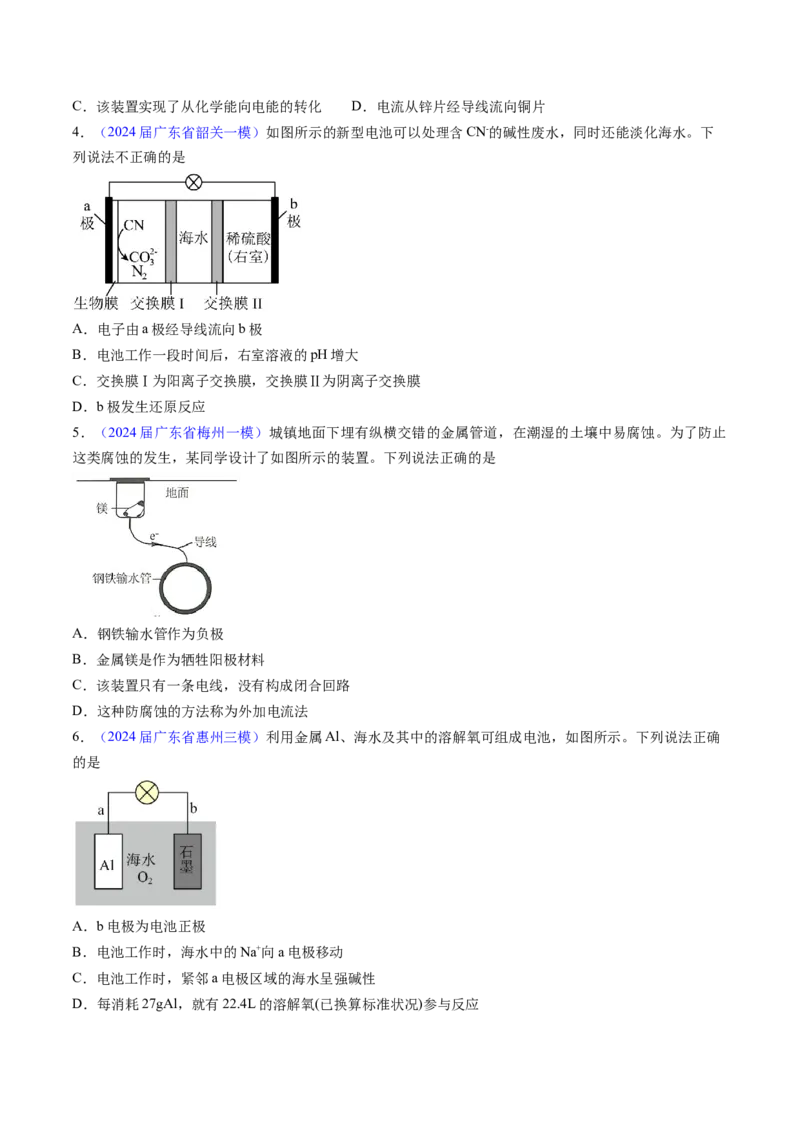
4.(2024届广东省韶关一模)如图所示的新型电池可以处理含CN-的碱性废水,同时还能淡化海水。下
列说法不正确的是
A.电子由a极经导线流向b极
B.电池工作一段时间后,右室溶液的pH增大
C.交换膜Ⅰ为阳离子交换膜,交换膜Ⅱ为阴离子交换膜
D.b极发生还原反应
5.(2024届广东省梅州一模)城镇地面下埋有纵横交错的金属管道,在潮湿的土壤中易腐蚀。为了防止
这类腐蚀的发生,某同学设计了如图所示的装置。下列说法正确的是
A.钢铁输水管作为负极
B.金属镁是作为牺牲阳极材料
C.该装置只有一条电线,没有构成闭合回路
D.这种防腐蚀的方法称为外加电流法
6.(2024届广东省惠州三模)利用金属Al、海水及其中的溶解氧可组成电池,如图所示。下列说法正确
的是
A.b电极为电池正极
B.电池工作时,海水中的Na+向a电极移动
C.电池工作时,紧邻a电极区域的海水呈强碱性
D.每消耗27gAl,就有22.4L的溶解氧(已换算标准状况)参与反应7.(2024届广东省广州一模)一种在室温下可循环充放电的新型纤维 电池有望应用于可穿戴设备
的储能,其工作原理为: ,放电时
A. 发生还原反应 B. 在正极失电子
C.阳离子由正极移向负极 D.每消耗 ,转移 电子
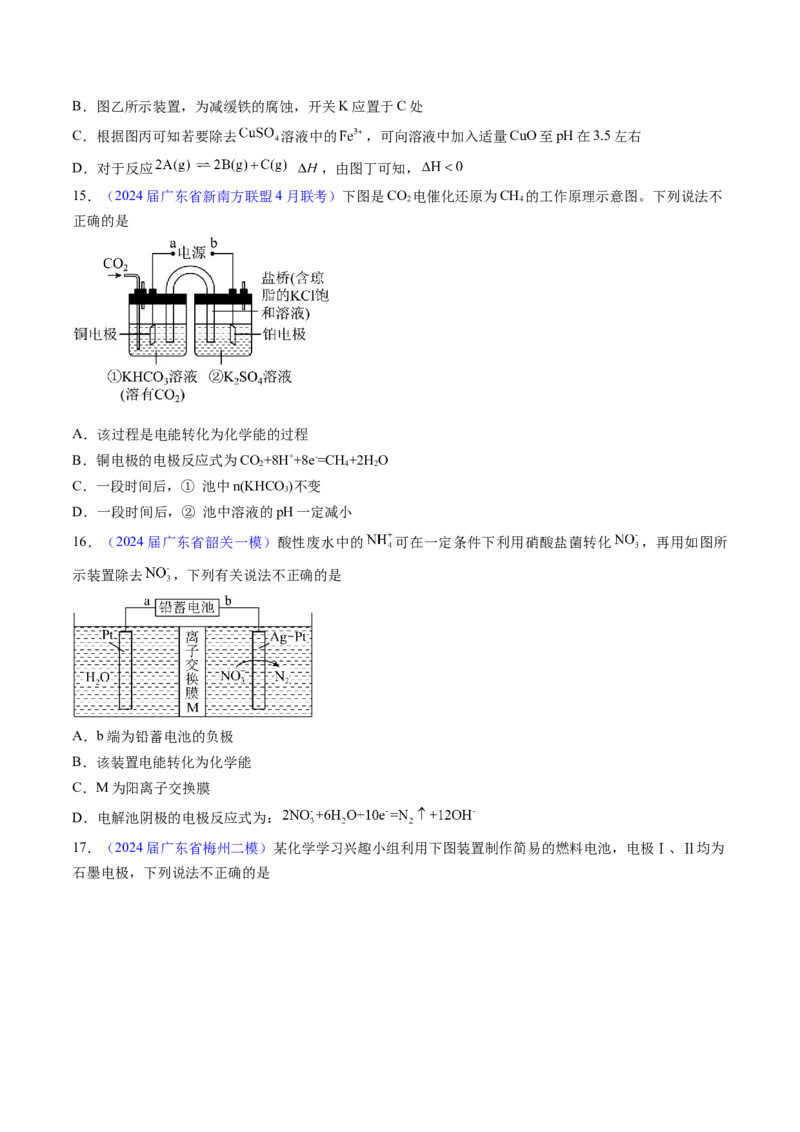
8.(2024届广东省省二模)一种基于原电池原理的氧气传感器可用于测定样气中氧气的含量,其装置如
图所示。下列说法正确的是
A.铅电极为正极
B.银电极上发生的反应为
C.电子由铅电极经过KOH溶液流向银电极
D.工作过程中,传感器的质量不变
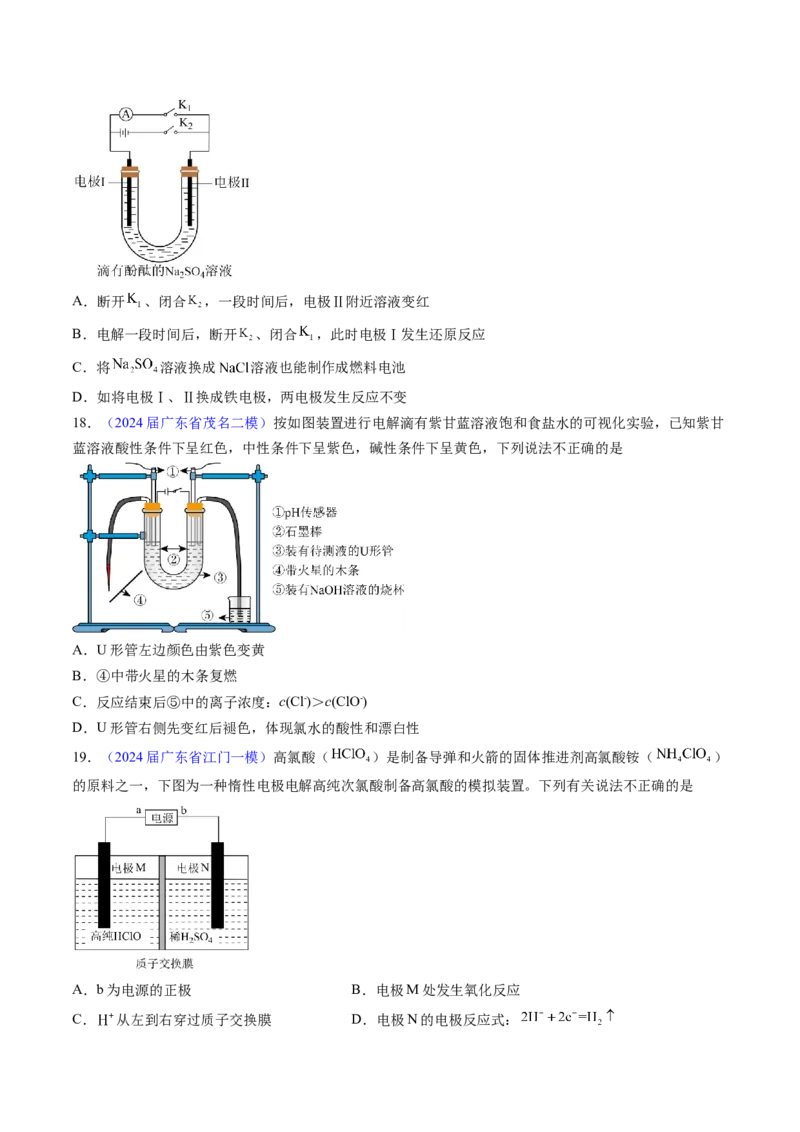
9.(2024届广东省省一模)微生物燃料电池能在较低的有机负荷下将化学能转化为电能,可用于有机污
染的生物修复,其反应原理如图所示。设 为阿伏加德罗常数的值,下列说法错误的是
A.a极是电池负极
B.电子从 极经电解质溶液流向 极
C. 向 极移动
D.若“有机物”是甲烷,则a极每产生 ,转移电子数为
10.(2024届广东省肇庆二模)SO -空气电池是一种新型环保电池,可在发电的同时制得硫酸,电池内部
2
以稀硫酸为电解液。电池工作时,下列说法正确的是
A.SO 发生还原反应
2
B.HSO 在电池的负极生成
2 4
C.电子从负极通过电解液移向正极D.通入空气发生的电极反应为O+4e-+2H O=4OH-
2 2
11.(2024届广东省深圳一模)我国科学家设计了水/有机混合高能锂硫电池,其工作原理如图所示。下列
说法正确的是
A.硫电极为负极
B. 通过阳离子交换膜向锂电极方向迁移
C.硫电极上发生的反应为
D.理论上,每消耗1mol ,同时消耗2 mol
12.(2024届广东省广州市白云区调研)微电解技术处理高盐、难降解、高色度废水的一种工艺,其原理
是在不通电的条件下,将酸性废水通过铁、碳构成的填料,利用电化学反应进行废水处理。下列叙述错误
的是
A.铁失电子产生的 可以还原废水中的
B.碳表面的废水 降低
C.若向装置内通入 ,则 在碳表面发生还原反应
D.溶液中产生的 ,能净化废水中悬浮的微小颗粒
13.(2024届广东省顺德一模)我国科学家发明一种新型电池,该电池以碳纳米管为正极、锌线为负极,
放电时消耗二氧化碳,同时生成天然气。下列说法正确的是
A.碳纳米管参与电极反应
B.负极发生还原反应
C.阳离子由正极移向负极
D.正极产物为
考点二 电解池的基本工作原理
14.(2024届广东省湛江二模)下列对关系图像或实验装置(如图)的分析错误的是
A.图甲表示等浓度的NaOH溶液滴定20mLHF溶液的滴定曲线,其中c点水的电离程度最大B.图乙所示装置,为减缓铁的腐蚀,开关K应置于C处
C.根据图丙可知若要除去 溶液中的 ,可向溶液中加入适量CuO至pH在3.5左右
D.对于反应 ,由图丁可知,
15.(2024届广东省新南方联盟4月联考)下图是CO 电催化还原为CH 的工作原理示意图。下列说法不
2 4
正确的是
A.该过程是电能转化为化学能的过程
B.铜电极的电极反应式为CO+8H++8e-=CH +2H O
2 4 2
C.一段时间后,① 池中n(KHCO)不变
3
D.一段时间后,② 池中溶液的pH一定减小
16.(2024届广东省韶关一模)酸性废水中的 可在一定条件下利用硝酸盐菌转化 ,再用如图所
示装置除去 ,下列有关说法不正确的是
A.b端为铅蓄电池的负极
B.该装置电能转化为化学能
C.M为阳离子交换膜
D.电解池阴极的电极反应式为:
17.(2024届广东省梅州二模)某化学学习兴趣小组利用下图装置制作简易的燃料电池,电极Ⅰ、Ⅱ均为
石墨电极,下列说法不正确的是A.断开 、闭合 ,一段时间后,电极Ⅱ附近溶液变红
B.电解一段时间后,断开 、闭合 ,此时电极Ⅰ发生还原反应
C.将 溶液换成 溶液也能制作成燃料电池
D.如将电极Ⅰ、Ⅱ换成铁电极,两电极发生反应不变
18.(2024届广东省茂名二模)按如图装置进行电解滴有紫甘蓝溶液饱和食盐水的可视化实验,已知紫甘
蓝溶液酸性条件下呈红色,中性条件下呈紫色,碱性条件下呈黄色,下列说法不正确的是
A.U形管左边颜色由紫色变黄
B.④中带火星的木条复燃
C.反应结束后⑤中的离子浓度:c(Cl-)>c(ClO-)
D.U形管右侧先变红后褪色,体现氯水的酸性和漂白性
19.(2024届广东省江门一模)高氯酸( )是制备导弹和火箭的固体推进剂高氯酸铵( )
的原料之一,下图为一种惰性电极电解高纯次氯酸制备高氯酸的模拟装置。下列有关说法不正确的是
A.b为电源的正极 B.电极M处发生氧化反应
C. 从左到右穿过质子交换膜 D.电极N的电极反应式:20.(2024届广东省省二调)一种用于析氯和还原硝酸盐的单原子钌电极工作原理如图所示。下列说法不
正确的是
A.该电池将电能转化为化学能 B.阴阳两极的产物不能大量共存
C.阳极电极反应式为 D.一段时间后,阴极区电解质溶液的 减小
考点三 价类二维图
21.(2024届广东省湛江一模)部分含Fe物质的分类与相应化合价的关系如图所示。下列推断不合理的
是
A.可存在a→e→b的转化 B.e溶液可与KSCN溶液反应生成红色沉淀
C.能用a制作的容器运输浓硫酸 D.a可与稀硝酸恰好反应,生成只含b的溶液
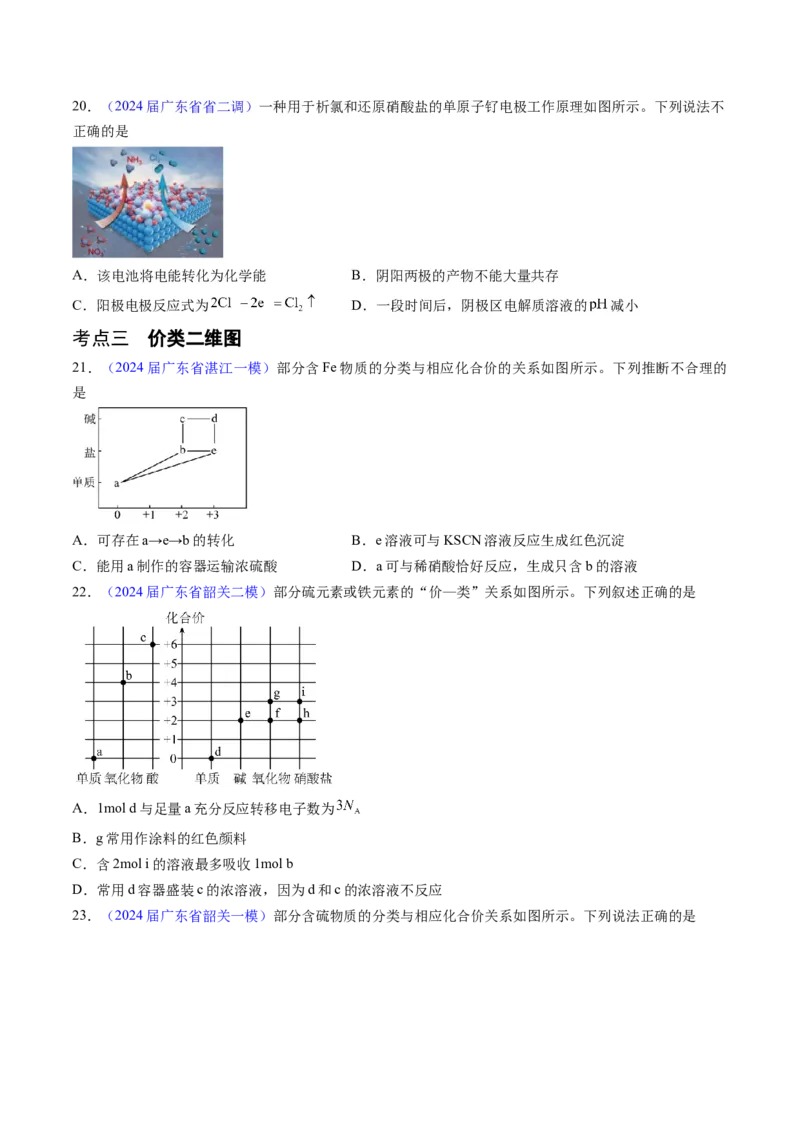
22.(2024届广东省韶关二模)部分硫元素或铁元素的“价—类”关系如图所示。下列叙述正确的是
A.1mol d与足量a充分反应转移电子数为
B.g常用作涂料的红色颜料
C.含2mol i的溶液最多吸收1mol b
D.常用d容器盛装c的浓溶液,因为d和c的浓溶液不反应
23.(2024届广东省韶关一模)部分含硫物质的分类与相应化合价关系如图所示。下列说法正确的是A.b与O 经过一步反应生成 d
2
B.f的浓溶液具有脱水性,可使胆矾晶体由蓝色变为白色
C.c通入a的水溶液中出现浑浊,体现了c的氧化性
D.c均能使品红溶液和酸性高锰酸钾溶液褪色,其褪色原理相同
24.(2024届广东省梅州二模)部分含C或含N物质的分类与相应化合价关系如下图所示。下列推断不合
理的是
A.存在a→b→c的转化 B.c一定是酸性氧化物
C.d、f中心原子均为sp2杂化 D.c、e可能有两种化学式
25.(2024届广东省梅州一模)下图为氯及其化合物的“价-类”二维图。下列说法不正确的是
A.a物质是由离子构成的
B. 、 的物质间转化均能一步反应实现
C.c可作为自来水消毒剂是因为其具有强氧化性
D.d分子中形成的共价键为 键和
26.(2024届广东省茂名二模)部分含钠或硫的“价类二维图”如下图所示。下列推断合理的是A.b、c均具有还原性 B.d、g、h中均存在共价键
C.a可与氧气一步生成d或e D.f一定可用做膨松剂
27.(2024届广东省江门一模)部分含Fe物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.可存在f→d→e的转化
B.高温下a与 反应制备c
C.KSCN溶液可用于鉴别f和g
D.a在g溶液中反应生成f
28.(2024届广东省广州一模)部分含氯物质的分类与相应化合价关系如图所示。下列推断不合理的是
A.a与强碱溶液反应可生成c和d B.电解c的水溶液可生成a
C.e在光照条件下可生成a D.可存在b→a→e→d的转化关系
29.(2024届广东省佛山一模)部分含Fe或含Cu物质的分类与相应化合价关系如下图所示,下列推断不
合理的是A.c为黑色固体 B.a与 反应只生成d
C.g与h均含有σ键 D.可存在a→c→d→h的转化
30.(2024届广东省佛山二模)部分含Mg或含Al物质的类别与化合价关系如图所示。下列推断不合理的
是
A.a不能与 反应生成d或g
B.b和e均可用于制造耐高温材料
C.可存在a→f→g→e→a的循环转化关系
D.直接加热蒸干c或f溶液无法得到无水氯化物