文档内容
易错类型 07 化工流程中的常考问题
【易错点01】不清楚常见的工艺操作方法措施(研磨、焙烧、水浸、酸(碱)浸等)
【易错点02】不清楚常见的工艺操作控制条件(调节溶液pH、控制温度等)
【易错点03】不掌握理解物质分离、提纯的方法及要点
【易错点04】不能正确书写流程中陌生的反应方程式
【易错点05】热重曲线的相关问题
【易错点06】工艺流程题中有关K 的计算类型
sp
【易错点07】工艺流程中有关物质的纯度、转化率、产品的产率的计算
易错点1 不清楚常见的工艺操作方法措施
【分析】
工艺操作(结果) 目的评价(或操作名称)
方 研磨(粉碎) 增大接触面积,加快反应(溶解)速率
法 煅烧(焙烧) 矿物分解、燃烧,转化为易溶于酸、碱的物质
措 水浸 利用水溶性把物质进行分离
施 酸浸(碱浸) 利用物质与酸(碱)反应除掉杂质或把目标物质转化为可溶性离子
易错点2 不清楚常见的工艺操作控制条件
【分析】
调节pH的原理及目的
控 调节溶液pH 某些金属离子的沉淀,控制物质的溶解
制 控制温度 加快反应速率,促进平衡移动;物质的溶解、析出、挥发等
条 增大某反应物用量 增大另一反应物的转化率
件 某种试剂的选择 是否带入杂质、是否影响产品的纯度
1.需要的物质:含主要阳离子(不引入新杂质即可)的难溶性氧化物或氢氧化物或碳酸盐,即能与H+反
应,使pH增大的物质如MgO、Mg(OH) 等类型的物质。
2
2.原理:加入的物质能与溶液中的H+反应,降低了H+的浓度
3.pH控制的范围:杂质离子完全沉淀时pH值-主要离子开始沉淀时pH,注意端值取等。
4.控制pH的目的:
(1)pH调小:抑制某离子水解;防止某离子沉淀
(2)pH调大:确保某离子完全沉淀;防止某物质溶解等。
(3)控制反应的发生,增强物质的氧化性或还原性,或改变水解程度。
【淘宝店铺:向阳百分百】5.控制某反应的pH值使某些金属离子以氢氧化物的形式沉淀的原理,例如:
(1)Fe3+溶液中存在水解平衡:Fe3++3H O Fe(OH) +3H+,加入CuO后,溶液中H+浓度降低,平衡正
2 3
向移动,Fe(OH) 越聚越多,最终形成沉淀。
3
(2)如若要除去Al3+、Mn2+溶液中含有的Fe2+,先用氧化剂把Fe2+氧化为Fe3+,再调溶液的pH。
调节pH所需的物质一般应满足两点:能与H+反应,使溶液pH增大;不引入新杂质。例如:若要除去Cu2
+溶液中混有的Fe3+,可加入CuO、Cu(OH) 、Cu (OH) CO 等物质来调节溶液的pH。
2 2 2 3
(3)PH控制的范围:大于除去离子的完全沉淀值,小于主要离子的开始沉淀的PH。
易错点3 不掌握理解物质分离、提纯的方法及要点
不相溶液体 分液
相溶性液体 蒸馏
分
难溶性固体 过滤
离
易溶性固体 蒸发浓缩、冷却结晶
提
趁热过滤 防止温度降低,某物质析出
纯
冰水洗涤 减少晶体的溶解损失
乙醇、有机溶剂洗涤 减少晶体的水溶性损失
易错点4 不能正确书写流程中陌生的反应方程式
【分析】
1.书写思路
首先根据题给材料中的信息写出部分反应物和生成物的化学式,再根据反应前后元素化合价有无变化判断
反应类型:
(1)元素化合价无变化则为非氧化还原反应,遵循质量守恒定律;
(2)元素化合价有变化则为氧化还原反应,既遵循质量守恒定律,又遵循得失电子守恒规律。
2.流程中陌生的氧化还原反应的书写流程
(1)首先根据题给材料中的信息确定氧化剂(或还原剂)与还原产物(或氧化产物),结合已学知识根据加入的
还原剂(或氧化剂)判断氧化产物(或还原产物)。
(2)根据得失电子守恒配平氧化还原反应。
(3)根据电荷守恒和反应物的酸碱性,在方程式左边或右边补充H+、OH-或HO等。
2
(4)根据质量守恒配平反应方程式。
易错点5 热重曲线的相关问题
【分析】
1.热重曲线模型
由热重分析记录的质量变化对温度的关系曲线称热重曲线,曲线的横轴为温度,纵轴为质量。如固体物质
A热分解反应:A(固体) B(固体)+C(气体)的典型热重曲线如图所示。图中T 为固体A开始分解的温度,
1
T 为质量变化达到最大值时的终止温度。若试样初始质量为 W ,失重后试样质量为W ,则失重百分数为
2 0 1
【淘宝店铺:向阳百分百】。
2.热重曲线的分析法的思考路径
坐标曲线体解题时可以拆分为识图、析图、用图三个步骤。其中识图是基础,析图是关键,用图是目的。
(1)识图
识图的关键是三看:一看轴即横、纵坐标所表示的化学含义(自变量 X轴和函数Y轴表示的意义),寻找
X、Y轴之间的关系,因为这是理解题意和进行正确思维的前提;二看点即曲线中的特殊点(顶点、始点、
终点、拐点、交叉点);三看线即曲线的走势(变化趋势是上升、下降、波动、正态、偏态等变化)。
(2)析图
分析图中为什么会出现这些特殊点,曲线为什么有这样的变化趋势和走向,分析曲线变化的因果关系;通
过联想,把课本内的有关化学概念、原理、规律等与图像曲线中的图形与相关点建立联系。
(3)用图
将相关的化学知识与图像曲线紧密结合,在头脑中构建新的曲线——知识体系,然后运用新的曲线——知
识体系揭示问题的实质,解决实际问题。
3.热重分析的一般方法和规律
(1)设晶体为1 mol。
(2)失重一般是先失水,再失非金属氧化物。
(3)计算每步的剩余固体质量,×100%=固体残留率。
(4)晶体中金属质量不减少,仍在m(剩余)中。
(5)失重最后一般为金属氧化物,由质量守恒得m(O),由n(金属)∶n(O)即可求出失重后物质的化学式。
【方法指导】
“两步法”突破热重分析及计算题
突破技法
第一步 阅读题给信息,找出物质之间发生的变化,一般结晶水合物先失结晶水,后发生分
读题,找变化 解,碳酸盐产生CO,硫酸盐产生SO 或SO ,氢氧化物产生HO
2 2 3 2
第二步
根据固体质量变化,列出定量关系式,求出未知数,确定剩余固体的化学式
列式,求未知
易错点6 工艺流程题中有关K 的计算的类型
sp
【分析】
类型一 已知溶度积求溶液中的某种离子的浓度
1:1型 x=√K
sp
√K
饱和溶液时的物质的量浓度与K sp 的关系 1:2型或2:1型 x= 3 sp
4
应用:比较溶解度的大小
√K
1:3型或3:1型 x= 4 sp
27
类型二 已知溶度积、溶液中某离子的浓度,求溶液中的另一种离子的浓度
【淘宝店铺:向阳百分百】类型三 根据溶度积规则判断沉淀是否生成
类型四 沉淀溶解平衡中的除杂和提纯
类型五 沉淀溶解平衡中沉淀转化的计算
类型六 Ksp与水解常数的关系
易错点7 工艺流程中有关物质的纯度、转化率、产品的产率的计算
【分析】
化工流程题中涉及的计算主要有:样品的质量分数或纯度的计算,物质的转化率或产率、物质的量浓度、
物质的质量的计算。
计算公式:
(1)n=,n=,n=cV(aq)
(2)=×100%
(3)产品产率=×100%
(4)物质的转化率=×100%
突破1 不清楚常见的工艺操作方法措施
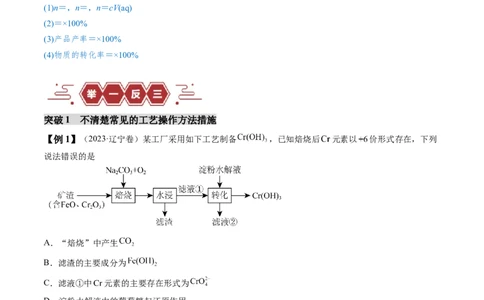
【例1】(2023·辽宁卷)某工厂采用如下工艺制备 ,已知焙烧后 元素以 价形式存在,下列
说法错误的是
A.“焙烧”中产生
B.滤渣的主要成分为
C.滤液①中 元素的主要存在形式为
D.淀粉水解液中的葡萄糖起还原作用
【答案】B
【分析】焙烧过程中铁、铬元素均被氧化,同时转化为对应钠盐,水浸时铁酸钠遇水水解生成氢氧化铁沉
淀,滤液中存在铬酸钠,与淀粉的水解产物葡萄糖发生氧化还原得到氢氧化铬沉淀。
【解析】A.铁、铬氧化物与碳酸钠和氧气反应时生成对应的钠盐和二氧化碳,A正确;
B.焙烧过程铁元素被氧化,滤渣的主要成分为氧化铁,B错误;
C.滤液①中 元素的化合价是+6价,铁酸钠遇水水解生成氢氧化铁沉淀溶液显碱性,所以Cr 元素主要
存在形式为 ,C正确;
【淘宝店铺:向阳百分百】D.由分析知淀粉水解液中的葡萄糖起还原作用,D正确;
故选B。
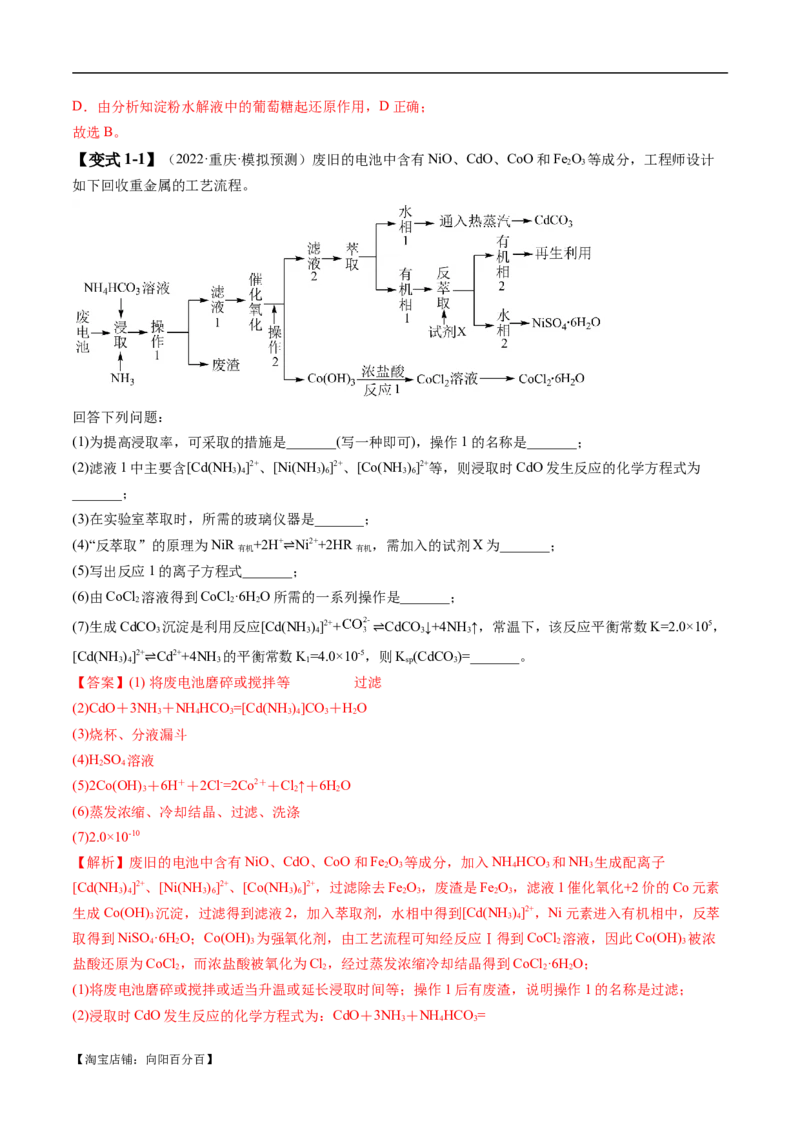
【变式1-1】(2022·重庆·模拟预测)废旧的电池中含有NiO、CdO、CoO和Fe O 等成分,工程师设计
2 3
如下回收重金属的工艺流程。
回答下列问题:
(1)为提高浸取率,可采取的措施是_______(写一种即可),操作1的名称是_______;
(2)滤液1中主要含[Cd(NH )]2+、[Ni(NH )]2+、[Co(NH )]2+等,则浸取时CdO发生反应的化学方程式为
3 4 3 6 3 6
_______;
(3)在实验室萃取时,所需的玻璃仪器是_______;
(4)“反萃取”的原理为NiR +2H+ Ni2++2HR ,需加入的试剂X为_______;
有机 有机
(5)写出反应1的离子方程式_______;
⇌
(6)由CoCl 溶液得到CoCl ·6H O所需的一系列操作是_______;
2 2 2
(7)生成CdCO 沉淀是利用反应[Cd(NH )]2++ CdCO↓+4NH↑,常温下,该反应平衡常数K=2.0×105,
3 3 4 3 3
[Cd(NH
3
)
4
]2+ Cd2++4NH
3
的平衡常数K
1
=4.0×10-5,⇌则K
sp
(CdCO
3
)=_______。
【答案】(1) 将废电池磨碎或搅拌等 过滤
⇌
(2)CdO+3NH +NH HCO =[Cd(NH)]CO+HO
3 4 3 3 4 3 2
(3)烧杯、分液漏斗
(4)H SO 溶液
2 4
(5)2Co(OH) +6H++2Cl-=2Co2++Cl↑+6HO
3 2 2
(6)蒸发浓缩、冷却结晶、过滤、洗涤
(7)2.0×10-10
【解析】废旧的电池中含有NiO、CdO、CoO和Fe O 等成分,加入NH HCO 和NH 生成配离子
2 3 4 3 3
[Cd(NH )]2+、[Ni(NH )]2+、[Co(NH )]2+,过滤除去Fe O,废渣是Fe O,滤液1催化氧化+2价的Co元素
3 4 3 6 3 6 2 3 2 3
生成Co(OH) 沉淀,过滤得到滤液2,加入萃取剂,水相中得到[Cd(NH )]2+,Ni元素进入有机相中,反萃
3 3 4
取得到NiSO ·6H O;Co(OH) 为强氧化剂,由工艺流程可知经反应Ⅰ得到CoCl 溶液,因此Co(OH) 被浓
4 2 3 2 3
盐酸还原为CoCl ,而浓盐酸被氧化为Cl,经过蒸发浓缩冷却结晶得到CoCl ·6H O;
2 2 2 2
(1)将废电池磨碎或搅拌或适当升温或延长浸取时间等;操作1后有废渣,说明操作1的名称是过滤;
(2)浸取时CdO发生反应的化学方程式为:CdO+3NH +NH HCO =
3 4 3
【淘宝店铺:向阳百分百】[Cd(NH )]CO+HO;
3 4 3 2
(3)在实验室萃取时,所需的玻璃仪器是烧杯、分液漏斗;
(4)“反萃取”的原理为NiR +2H+ Ni2++2HR ,反萃取后,生成NiSO ,所以试剂X是HSO 溶液;
有机 有机 4 2 4
(5)反应1把+3价Co变成了+2价Co,说明Co(OH) 与盐酸发生氧化还原反应,离子方程式为:2Co(OH)
⇌ 3 3
+6H++2Cl-=2Co2++Cl↑+6HO;
2 2
(6)由CoCl 溶液得到含有结晶水的化合物CoCl ·6H O所需的一系列操作是:蒸发浓缩、冷却结晶、过滤、
2 2 2
洗涤;
(7)[Cd(NH )]2++ CdCO↓+4NH↑的平衡常数为: ;
3 4 3 3
⇌
[Cd(NH )]2+ Cd2++4NH 的平衡常数 ;则K (CdCO)=
3 4 3 sp 3
⇌
突破2 不清楚常见的工艺操作控制条件
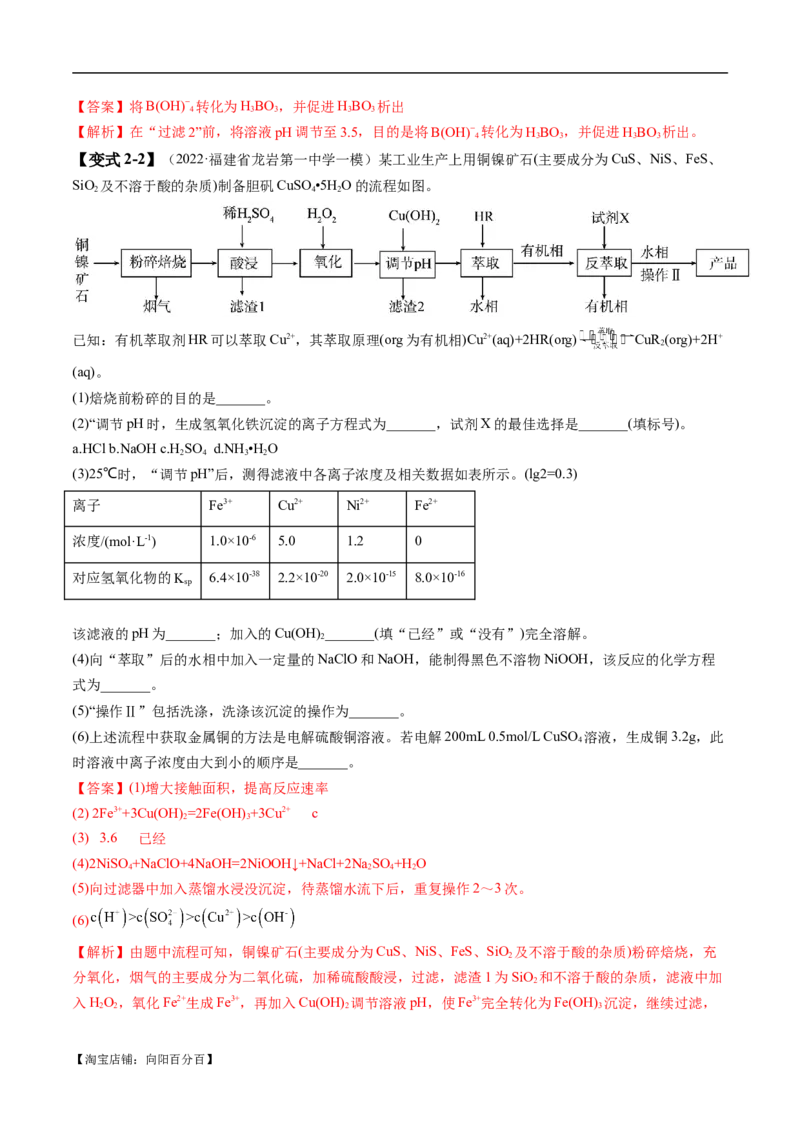
【例2】(2022·山东卷)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂
质)为主要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
Fe(OH) Cu(OH) Zn(OH)
3 2 2
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是
A.固体X主要成分是Fe(OH) 和S;金属M为Zn
3
B.浸取时,增大O 压强可促进金属离子浸出
2
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
【答案】D
【解析】CuS精矿(含有杂质Zn、Fe元素)在高压O 作用下,用硫酸溶液浸取,CuS反应产生为CuSO 、
2 4
S、HO,Fe2+被氧化为Fe3+,然后加入NH 调节溶液pH,使Fe3+形成Fe(OH) 沉淀,而Cu2+、Zn2+仍以离子
2 3 3
形式存在于溶液中,过滤得到的滤渣中含有S、Fe(OH) ;滤液中含有Cu2+、Zn2+;然后向滤液中通入高压
3
H,根据元素活动性:Zn>H>Cu,Cu2+被还原为Cu单质,通过过滤分离出来;而Zn2+仍然以离子形式存
2
【淘宝店铺:向阳百分百】在于溶液中,再经一系列处理可得到Zn单质。
A.经过上述分析可知固体X主要成分是S、Fe(OH) ,金属M为Zn,A正确;
3
B.CuS难溶于硫酸,在溶液中存在沉淀溶解平衡CuS(s) Cu2+(aq)+S2-(aq),增大O 的浓度,可以反应消
2
耗S2-,使之转化为S,从而使沉淀溶解平衡正向移动,从而可促进金属离子的浸取,B正确;
C.根据流程图可知:用NH 调节溶液pH时,要使Fe3+转化为沉淀,而Cu2+、Zn2+仍以离子形式存在于溶
3
液中,结合离子沉淀的pH范围,可知中和时应该调节溶液pH范围为3.2~4.2,C正确;
D.在用H 还原Cu2+变为Cu单质时,H 失去电子被氧化为H+,与溶液中OH-结合形成HO,若还原时增
2 2 2
大溶液的酸度,c(H+)增大,不利于H 失去电子还原Cu单质,因此不利于Cu的生成,D错误;
2
故合理选项是D。
【例3】我国是世界上最早制得和使用金属锌的国家。湿法炼锌产生的铜镉渣(主要含锌、铜、铁、镉
(Cd)、钴(Co)等单质)用于生产金属镉的工艺流程如下:
表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1 mol·L-1)
金属离子 Fe3+ Fe2+ Cd2+
开始沉淀的pH 1.5 6.3 7.4
沉淀完全的pH 2.8 8.3 9.4
①操作Ⅲ中先加入适量HO 的作用是 。
2 2
②再加入ZnO控制反应液的pH,合适的pH范围为______________________________。
2.答案 将Fe2+氧化为Fe3+ 2.8≤pH<7.4
解析 ①双氧水具有氧化性,能把亚铁离子氧化为铁离子,便于调节pH使Fe3+沉淀后经过滤除去;
②加入氧化锌调节pH使Fe3+沉淀后经过滤除去,由表格可知,合适的pH范围为:2.8≤pH<7.4。
【变式2-1】硼酸(HBO)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁
3 3
矿(含MgB O·H O、SiO 及少量Fe O、Al O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
2 2 5 2 2 2 3 2
回答下列问题:
在“过滤2”前,将溶液pH调节至3.5,目的是_____________________________________________。
【淘宝店铺:向阳百分百】【答案】将B(OH)− 转化为HBO,并促进HBO 析出
4 3 3 3 3
【解析】在“过滤2”前,将溶液pH调节至3.5,目的是将B(OH)− 转化为HBO,并促进HBO 析出。
4 3 3 3 3
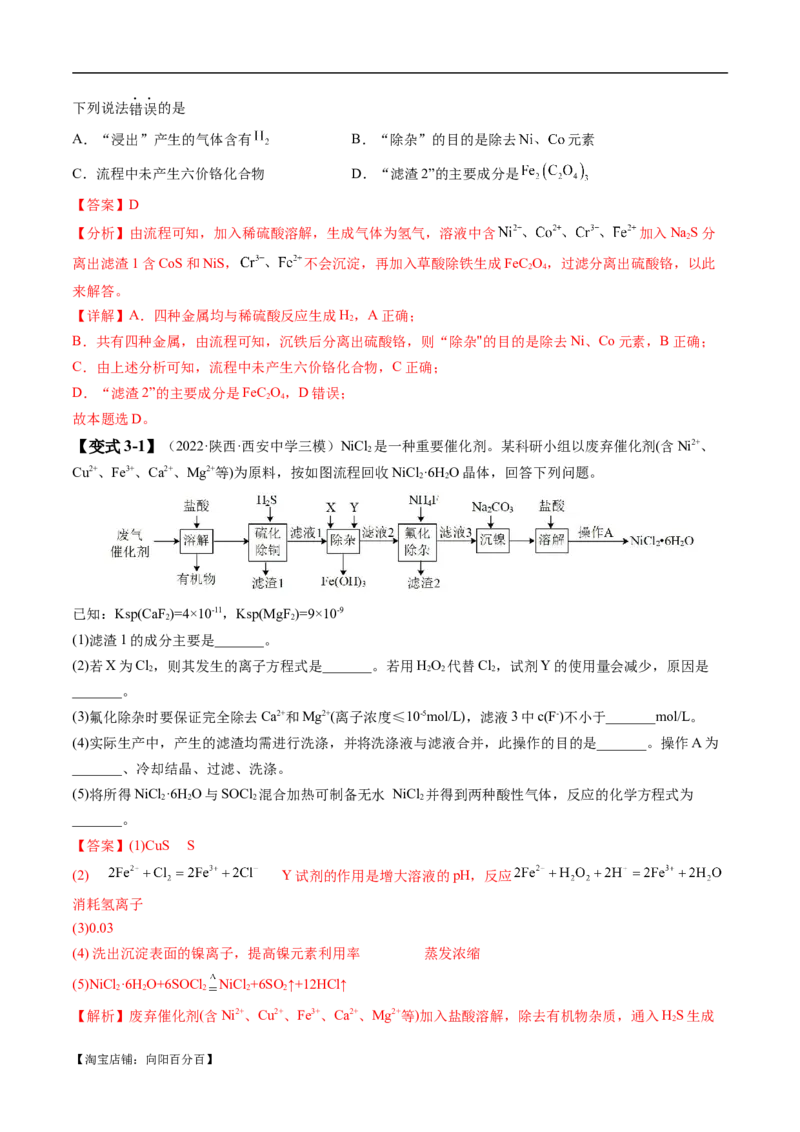
【变式2-2】(2022·福建省龙岩第一中学一模)某工业生产上用铜镍矿石(主要成分为CuS、NiS、FeS、
SiO 及不溶于酸的杂质)制备胆矾CuSO •5H O的流程如图。
2 4 2
已知:有机萃取剂HR可以萃取Cu2+,其萃取原理(org为有机相)Cu2+(aq)+2HR(org) CuR (org)+2H+
2
(aq)。
(1)焙烧前粉碎的目的是_______。
(2)“调节pH时,生成氢氧化铁沉淀的离子方程式为_______,试剂X的最佳选择是_______(填标号)。
a.HCl b.NaOH c.H SO d.NH•H O
2 4 3 2
(3)25℃时,“调节pH”后,测得滤液中各离子浓度及相关数据如表所示。(lg2=0.3)
离子 Fe3+ Cu2+ Ni2+ Fe2+
浓度/(mol·L-1) 1.0×10-6 5.0 1.2 0
对应氢氧化物的K 6.4×10-38 2.2×10-20 2.0×10-15 8.0×10-16
sp
该滤液的pH为_______;加入的Cu(OH) _______(填“已经”或“没有”)完全溶解。
2
(4)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,该反应的化学方程
式为_______。
(5)“操作Ⅱ”包括洗涤,洗涤该沉淀的操作为_______。
(6)上述流程中获取金属铜的方法是电解硫酸铜溶液。若电解200mL 0.5mol/L CuSO 溶液,生成铜3.2g,此
4
时溶液中离子浓度由大到小的顺序是_______。
【答案】(1)增大接触面积,提高反应速率
(2) 2Fe3++3Cu(OH) =2Fe(OH) +3Cu2+ c
2 3
(3) 3.6 已经
(4)2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O
4 2 4 2
(5)向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流下后,重复操作2~3次。
(6)
【解析】由题中流程可知,铜镍矿石(主要成分为CuS、NiS、FeS、SiO 及不溶于酸的杂质)粉碎焙烧,充
2
分氧化,烟气的主要成分为二氧化硫,加稀硫酸酸浸,过滤,滤渣1为SiO 和不溶于酸的杂质,滤液中加
2
入HO,氧化Fe2+生成Fe3+,再加入Cu(OH) 调节溶液pH,使Fe3+完全转化为Fe(OH) 沉淀,继续过滤,
2 2 2 3
【淘宝店铺:向阳百分百】滤渣2为Fe(OH) ,滤液中加入HR进行萃取,除去镍离子,有机相中加入硫酸进行反萃取,水相的主要成
3
分为硫酸铜溶液,加热蒸发,冷却结晶,过滤,洗涤,干燥即可获得产品。
(1)由上述分析可知,焙烧前粉碎的目的是增大接触面积,提高反应速率,使矿石充分氧化;答案为增大接
触面积,提高反应速率;
(2)由上述分析可知,加入Cu(OH) 调节溶液pH,使Fe3+完全转化为Fe(OH) 沉淀,生成氢氧化铁沉淀的离
2 3
子方程式为2Fe3++3Cu(OH) =2Fe(OH) ↓+3Cu2+;由题中信息Cu2+(aq)+2HR(org) CuR (org)+2H+(aq)
2 3 2
可知,要使平衡逆向移动,则增加H+浓度,即有机相中加入硫酸进行反萃取,可以分离铜离子,还不会产
生杂质,所以选项c正确;答案为2Fe3++3Cu(OH) =2Fe(OH) ↓+3Cu2+;c;
2 3
(3)由题中表格数据可知,25℃时,“调节pH”后,测得滤液中c(Fe3+)=1.0×10-6mol/L,c(Cu2+)=5.0mol/L,因
为K [Fe(OH) ]= 6.4×10-38,所以c(Fe3+)×c3(OH-)= K [Fe(OH) ],则c(OH-)= =
sp 3 sp 3
=4×10-11mol/L,c(H+)= = ×10-3mol/L,pH=3+lg4=3+2lg2=3.6;又
c(Cu2+)×c2(OH-)=5×(4×10-11)2=8×10-21<K [Cu(OH) ]=2.2×10-20,所以Cu(OH) 已经完全溶解;答案为3.6;已
sp 2 2
经;
(4)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,即NiSO 与NaClO
4
发生氧化还原反应,该反应的化学方程式为2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O;答案
4 2 4 2
为2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O;
4 2 4 2
(5)“操作Ⅱ”包括洗涤,洗涤该沉淀的操作为向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流下后,重复操
作2~3次;答案为向过滤器中加入蒸馏水浸没沉淀,待蒸馏水流下后,重复操作2~3次;
(6)电解CuSO 溶液,发生反应2CuSO +2H O 2Cu+2H SO +O ↑,200mL 0.5mol/L的CuSO 溶液中
4 4 2 2 4 2 4
n(CuSO )=0.2L×0.5mol/L=0.1mol,生成铜3.2g,物质的量为 =0.05mol,故生成HSO 0.05mol,溶
4 2 4
液中CuSO 为0.1mol-0.05mol=0.05mol,电解后的溶液为CuSO 、HSO 混合溶液,溶液呈酸性,溶液中铜
4 4 2 4
离子水解、水发生电离,故n(H+)>0.05mol×2=0.1mol,n( )=0.1mol,n(Cu2+)<0.05mol,溶液中氢氧根
浓度很小,故 ,故答案为:. 。
突破3 不掌握理解物质分离、提纯的方法及要点
【例4】(2022·福建卷)用铬铁合金(含少量 单质)生产硫酸铬的工艺流程如下:
【淘宝店铺:向阳百分百】下列说法错误的是
A.“浸出”产生的气体含有 B.“除杂”的目的是除去 元素
C.流程中未产生六价铬化合物 D.“滤渣2”的主要成分是
【答案】D
【分析】由流程可知,加入稀硫酸溶解,生成气体为氢气,溶液中含 加入NaS分
2
离出滤渣1含CoS和NiS, 不会沉淀,再加入草酸除铁生成FeC O,过滤分离出硫酸铬,以此
2 4
来解答。
【详解】A.四种金属均与稀硫酸反应生成H,A正确;
2
B.共有四种金属,由流程可知,沉铁后分离出硫酸铬,则“除杂"的目的是除去Ni、Co元素,B正确;
C.由上述分析可知,流程中未产生六价铬化合物,C正确;
D.“滤渣2”的主要成分是FeC O,D错误;
2 4
故本题选D。
【变式3-1】(2022·陕西·西安中学三模)NiCl 是一种重要催化剂。某科研小组以废弃催化剂(含Ni2+、
2
Cu2+、Fe3+、Ca2+、Mg2+等)为原料,按如图流程回收NiCl ·6H O晶体,回答下列问题。
2 2
已知:Ksp(CaF )=4×10-11,Ksp(MgF)=9×10-9
2 2
(1)滤渣1的成分主要是_______。
(2)若X为Cl,则其发生的离子方程式是_______。若用HO 代替Cl,试剂Y的使用量会减少,原因是
2 2 2 2
_______。
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于_______mol/L。
(4)实际生产中,产生的滤渣均需进行洗涤,并将洗涤液与滤液合并,此操作的目的是_______。操作A为
_______、冷却结晶、过滤、洗涤。
(5)将所得NiCl ·6H O与SOCl 混合加热可制备无水 NiCl 并得到两种酸性气体,反应的化学方程式为
2 2 2 2
_______。
【答案】(1)CuS S
(2) Y试剂的作用是增大溶液的pH,反应
消耗氢离子
(3)0.03
(4) 洗出沉淀表面的镍离子,提高镍元素利用率 蒸发浓缩
(5)NiCl ·6H O+6SOCl NiCl +6SO↑+12HCl↑
2 2 2 2 2
【解析】废弃催化剂(含Ni2+、Cu2+、Fe3+、Ca2+、Mg2+等)加入盐酸溶解,除去有机物杂质,通入HS生成
2
【淘宝店铺:向阳百分百】CuS沉淀除去Cu2+,同时Fe3+被还原为Fe2+;滤液1中加入氧化剂把Fe2+氧化为Fe3+,调节pH生成Fe(OH)
3
沉淀除去Fe3+;向滤液2中加入NH F生成CaF 沉淀、MgF 沉淀除去Ca2+和Mg2+;向滤液3中加入NaCO
4 2 2 2 3
溶液生成NiCO 沉淀,NiCO 沉淀中加盐酸溶解,蒸发浓缩、冷却结晶、过滤、洗涤得NiCl •6H O晶体;
3 3 2 2
据此解答。
(1)向含Ni2+、Cu2+、Fe3+、Ca2+、Mg2+离子的溶液中通入HS,Fe3+被还原为Fe2+,HS被氧化为S单质,即
2 2
2Fe3++H S=2Fe2++S↓+2H+,Cu2+和HS反应生成CuS沉淀,即Cu2++H S=CuS↓+2H+,所以滤渣1的成分主要
2 2 2
是CuS、S;答案为CuS、S。
(2)若X为Cl,Cl 把Fe2+氧化为Fe3+,其离子方程式为2Fe2++Cl=2Fe3++2Cl-;加入试剂Y的目的是调节pH
2 2 2
生成Fe(OH) 沉淀,若用HO 代替Cl,发生反应2Fe2++H O+2H+=2Fe3++2H O,反应消耗H+,所以试剂Y
3 2 2 2 2 2 2
的使用量会减少;答案为2Fe2++Cl=2Fe3++2Cl-;Y试剂的作用是增大溶液的pH,反应
2
消耗氢离子。
(3)由题中信息可知,K (CaF )=4×10-11,K (MgF )=9×10-9,CaF 比MgF 更难溶,氟化除杂时要保证完全除
sp 2 sp 2 2 2
去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于 mol/L=3×10-2mol/L=0.03mol/L;答案
为0.03。
(4)实际生产中,产生的滤渣均需进行洗涤,并将洗涤液与滤液合并,此操作的目的是减少镍离子损失,提
高镍元素利用率;NiCO 沉淀中加盐酸溶解得NiCl 溶液,蒸发浓缩、冷却结晶、过滤、洗涤得NiCl •6H O
3 2 2 2
晶体;答案为洗出沉淀表面的镍离子,提高镍元素利用率;蒸发浓缩。
(5)将所得NiCl ·6H O与SOCl 混合加热可制备无水 NiCl 并得到两种酸性气体,反应的化学方程式为
2 2 2 2
NiCl ·6H O+6SOCl NiCl +6SO↑+12HCl↑;答案为NiCl ·6H O+6SOCl NiCl +6SO↑+12HCl↑。
2 2 2 2 2 2 2 2 2 2
突破4 不能正确书写流程中陌生的反应方程式
【例5】(2021·全国甲卷)碘(紫黑色固体,微溶于水)及其化合物广泛用于医药、染料等方面。回答下列
问题:
(1) 的一种制备方法如下图所示:
①加入 粉进行转化反应的离子方程式为___________________________________,生成的沉淀与硝酸反
应,生成_________________后可循环使用。
②通入 的过程中,若氧化产物只有一种,反应的化学方程式为____________________________;若反
应物用量比 时,氧化产物为____________;当 ,单质碘的收
率会降低,原因是________________________________________________________。
(2)以 为原料制备 的方法是:先向 溶液中加入计量的 ,生成碘化物;再向混合溶
【淘宝店铺:向阳百分百】液中加入 溶液,反应得到 ,上述制备 的总反应的离子方程式为__________________________。
【答案】2AgI+Fe=2Ag+ Fe2++2I- AgNO FeI +Cl= I+FeCl I、FeCl I 被过量的 进一步
3 2 2 2 2 2 3 2
氧化 (2)
【解析】(1) ①由流程图可知悬浊液中含AgI ,AgI可与Fe反应生成FeI 和Ag,FeI 易溶于水,在离子方
2 2
程式中能拆,故加入 粉进行转化反应的离子方程式为2AgI+Fe=2Ag+ Fe2++2I-,生成的银能与硝酸反应
生成硝酸银参与循环中,故答案为:2AgI+Fe=2Ag+ Fe2++2I-;AgNO;②通入 的过程中,因I-还原性强
3
于Fe2+, 先氧化还原性强的I-,若氧化产物只有一种,则该氧化产物只能是I,故反应的化学方程式为
2
FeI+Cl= I+FeCl ,若反应物用量比 时即 过量,先氧化完全部I-再氧化Fe2+,恰
2 2 2 2
好将全部I-和Fe2+氧化,故氧化产物为I、FeCl ,当 即 过量特别多,多余的氯气
2 3
会与生成的单质碘以及水继续发生氧化还原反应,单质碘的收率会降低,故答案为:FeI+Cl= I+FeCl ;
2 2 2 2
I、FeCl ;I 被过量的 进一步氧化;(2)先向 溶液中加入计量的 ,生成碘化物即含I-的
2 3 2
物质;再向混合溶液中(含I-)加入 溶液,反应得到 ,上述制备 的两个反应中I-为中间产物,
总反应为 与 发生氧化还原反应,生成 和 ,根据得失电子守恒、电荷守恒]及元素守恒配
平离子方程式即可得: ,故答案为:
。
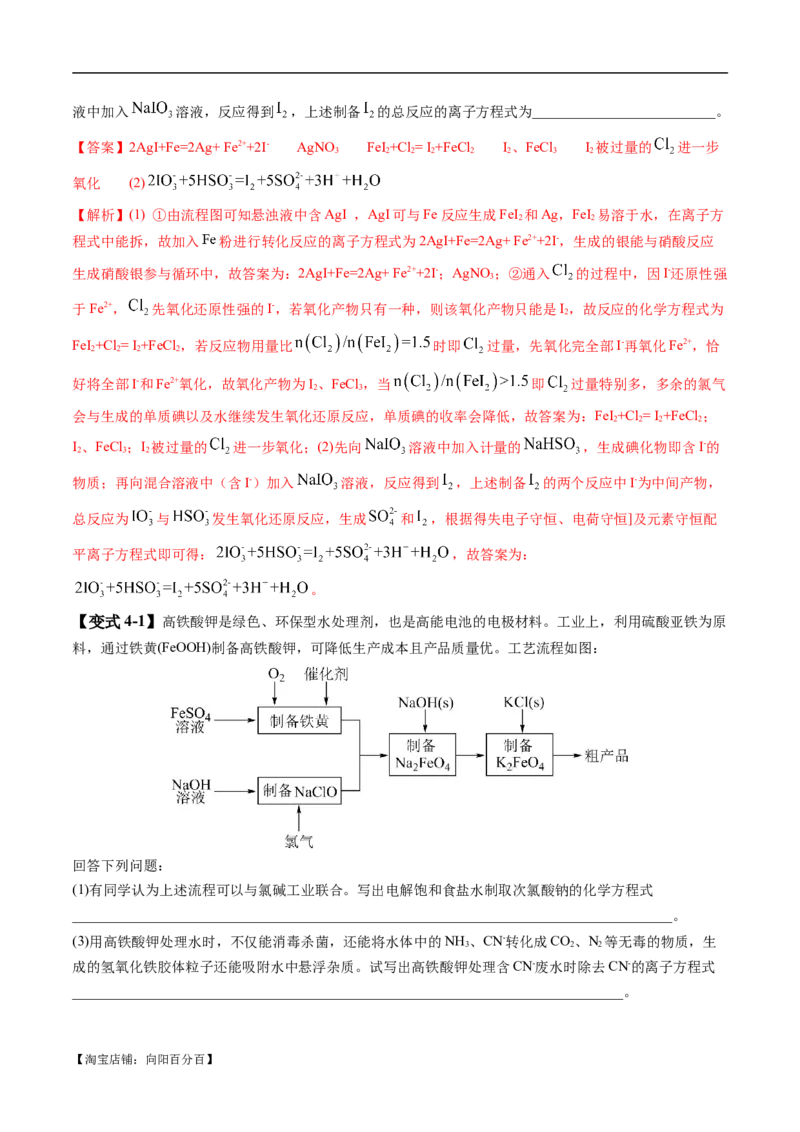
【变式4-1】高铁酸钾是绿色、环保型水处理剂,也是高能电池的电极材料。工业上,利用硫酸亚铁为原
料,通过铁黄(FeOOH)制备高铁酸钾,可降低生产成本且产品质量优。工艺流程如图:
回答下列问题:
(1)有同学认为上述流程可以与氯碱工业联合。写出电解饱和食盐水制取次氯酸钠的化学方程式
_____________________________________________________________________________________。
(3)用高铁酸钾处理水时,不仅能消毒杀菌,还能将水体中的NH 、CN-转化成CO、N 等无毒的物质,生
3 2 2
成的氢氧化铁胶体粒子还能吸附水中悬浮杂质。试写出高铁酸钾处理含CN-废水时除去CN-的离子方程式
______________________________________________________________________________。
【淘宝店铺:向阳百分百】【答案】(1)NaCl+H O NaClO+H ↑
2 2
(3)10FeO +6CN-+22H O=10Fe(OH) (胶体)+6CO +3N ↑+14OH-
2 3 2
【解析】实验室欲制备高铁酸钾,首先要分别制备铁黄和NaClO,将而二者混合后加入NaOH调节溶液
pH得到高铁酸钠,通过Na与K的置换可以得到高铁酸钾粗产品。根据图像分析制备过程中最佳的制备温
度和溶液pH;根据沉淀溶解平衡常数计算溶液中Fe3+的浓度;根据充电时的电池总反应方程式和充电时各
电极的得失电子情况书写电极方程式。(1)电解饱和食盐水制取次氯酸钠的化学方程式NaCl+H O
2
NaClO+H ↑;(3)高铁酸钾具有氧化性,可以将CN-氧化为氮气和二氧化碳而除去,本身被还原为氢氧化铁
2
胶体,在碱性溶液中二氧化碳变成碳酸根离子,反应的方程式为10FeO +6CN-+22H O=10Fe(OH) (胶体)
2 3
+6CO +3N ↑+14OH-。
2
【变式4-2】 和 都是锂离子电池的电极材料,可利用钛铁矿(主要成分为 ,还
含有少量MgO、 等杂质)来制备。工艺流程如下;
回答下列问题:
(2)“酸浸”后,钛主要以 形式存在,写出相应反应的离子方程式____________________________。
(5)写出“高温煅烧②”中由 制备 的化学方程式___________________________________。
(6)一种钛酸锂二次电池原理如图,放电时 由N极层状材料中脱出经由电解质嵌入M极层状材料中,充
电时N极电极反应方程式为________________________________________________________,放电时M极
每增重7g,负载中转移电子数为________________。
【答案】(3) 6Fe3++4SO +6H O+2Na++6MgO=Na Fe (SO )(OH) ↓+6Mg2+
2 2 6 4 4 12
(6)2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O
4 2 4 2
【解析】废料与硫酸、过氧化氢混合,硫酸把单质Fe、Cu、Mg的氧化物溶解,部分Ni溶解,转化得到的
离子有Fe2+、Cu2+、Mg2+,加入的HO 具有氧化性,可以促进Ni的溶解,使其全部转化为Ni2+,同时把存
2 2
在的Fe2+氧化为Fe3+;二氧化硅不溶于酸,则滤渣为二氧化硅;加入MgO、硫酸钠生成黄钠铁矾
[Na Fe (SO )(OH) ]沉淀;加入硫化氢,生成不溶于硫酸的硫化铜沉淀;加入NaF溶液,使Mg2+转化为
2 6 4 4 12
MgF 沉淀除去;加入NaOH使镍生成沉淀。(3)“除铁”时加入NaSO 溶液和MgO,根据元素守恒和电荷
2 2 4
守恒,离子方程式为6Fe3++4SO +6H O+2Na++6MgO=Na Fe (SO )(OH) ↓+6Mg2+;(6)NaClO具有强氧化
2 2 6 4 4 12
【淘宝店铺:向阳百分百】性,Cl元素由+1价降低到-1价,则Ni元素由NiSO 中+2价升高到NiOOH中的+3价,根据得失电子守恒
4
和元素守恒,化学方程式为2NiSO +NaClO+4NaOH=2NiOOH↓+NaCl+2Na SO +H O。
4 2 4 2
突破5 热重曲线的相关问题
【例6】硫酸铁铵[NH Fe(SO )·xHO]是一种重要铁盐。采用热重分析法测定硫酸铁铵晶体样品所含结晶
4 4 2 2
水数,将样品加热到 150 ℃时失掉 1.5 个结晶水,失重 5.6%。硫酸铁铵晶体的化学式为
。
【答案】NH Fe(SO )·12H O
4 4 2 2
【解析】
第一步 根据题给信息,确定硫酸铁铵发生的变化:NH Fe(SO )·xHO→NHFe(SO )·(x-1.5)H O
4 4 2 2 4 4 2 2
第二步 理解样品失重5.6%的含义,列出含x的代数式,求出x的值,确定硫酸铁铵的化学式
样品加热到 150 ℃时失掉 1.5 个结晶水,发生变化:NH Fe(SO )·xHO→NHFe(SO )·(x-1.5)H O+
4 4 2 2 4 4 2 2
1.5H O。固体失重5.6%,即失去水的质量占样品总质量的5.6%,列出关系式:×100%=5.6%,解得x=
2
12,故硫酸铁铵晶体的化学式为NH Fe(SO )·12H O。
4 4 2 2
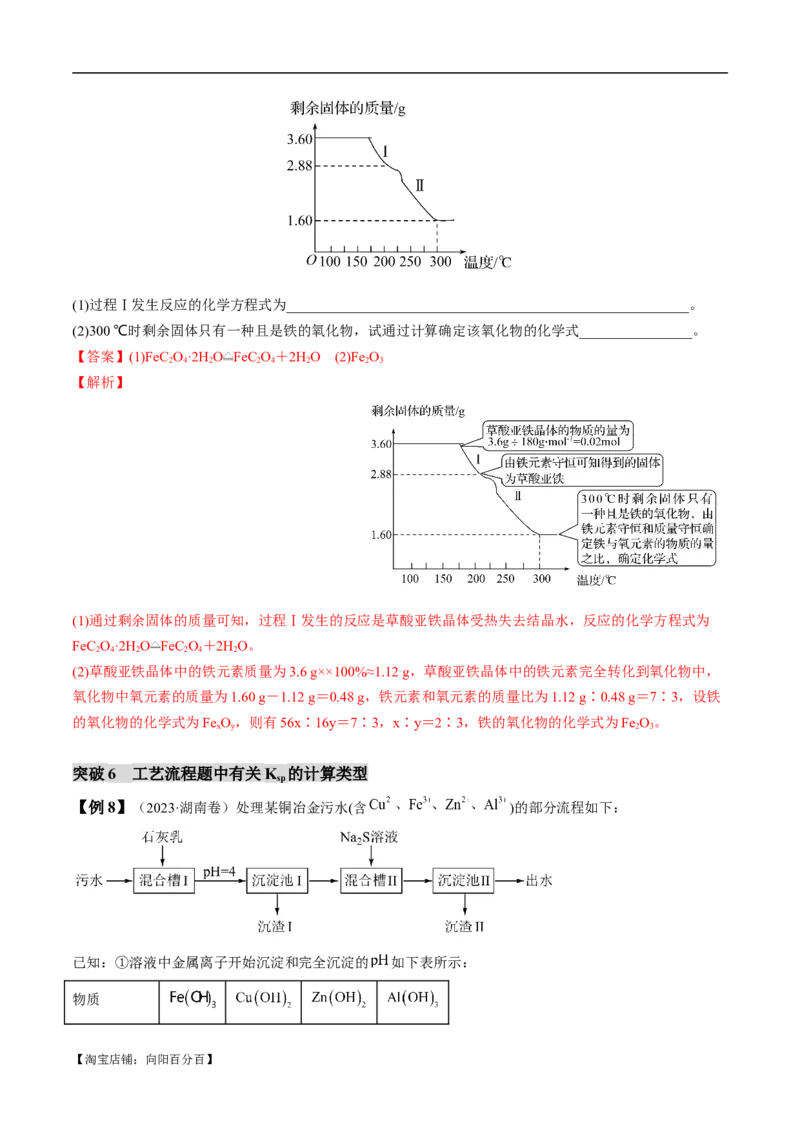
【例 7】在加热固体NH Al(SO )·12H O时,固体质量随温度的变化曲线如图所示:已知a点物质为
4 4 2 2
NH Al(SO ),b点物质为Al (SO ),下列判断正确的是( )
4 4 2 2 4 3
A.0~T ℃的过程变化是物理变化
B.c点物质是工业上冶炼铝的原料
C.a→b反应中生成物只有Al (SO ) 和NH 两种
2 4 3 3
D.Al (SO ) 能够净水,可用离子方程式表示为Al3++3OH-===Al(OH)
2 4 3 3
【答案】B
【解析】因为a点物质为NH Al(SO ) ,则0~T ℃的过程变化是失去结晶水生成NH Al(SO ) ,是化学变
4 4 2 4 4 2
化,A项错误;b点物质为硫酸铝,继续加热分解则在c点生成氧化铝,所以c点物质是工业上冶炼铝的原
料,B项正确;a→b发生的反应为硫酸铝铵分解生成硫酸铝、氨气和硫酸,C项错误;硫酸铝能够净水,
其原理是铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性可以吸附水中悬浮的杂质,D项错误。
【变式5-1】在空气中加热10.98 g草酸钴晶体(CoC O·2H O)样品,受热过程中不同温度范围内分别得到
2 4 2
一种固体物质,其质量如表。
温度范围/℃ 固体质量/g
150~210 8.82
290~320 4.82
890~920 4.50
【淘宝店铺:向阳百分百】(1)加热到210 ℃时,固体物质的化学式为_______________________________________。
(2)经测定,加热到210~310 ℃过程中的生成物只有CO 和钴的氧化物,此过程发生反应的化学方程式为
2
________________________________________________________________________。
【答案】 (1)CoC O (2)3CoC O+2O===Co O+6CO
2 4 2 4 2 3 4 2
【解析】(1)CoC O·2H O失去全部结晶水的质量为10.98× g=8.82 g,即加热到210 ℃时,固体物质是
2 4 2
CoC O 。(2)根据元素守恒,n(CO)=×2 mol=0.12 mol,质量为0.12 mol×44 g·mol-1=5.28 g,固体量减少
2 4 2
(8.82-4.82)g=4.00 g,说明有气体参加反应,即氧气参加,氧气的质量为(5.28-4.00)g=1.28 g,其物质的
量为 mol=0.04 mol,n(CoC O)∶n(O )∶n(CO)=∶0.04∶0.12=0.06∶0.04∶0.12=3∶2∶6,依据原子守
2 4 2 2
恒,3CoC O+2O===Co O+6CO。
2 4 2 3 4 2
【变式5-2】取26.90g ZnSO·6H O加热,剩余固体的质量随温度的变化如图2所示。750℃时所得固体的
4 2
化学式为( )
A.ZnO B.ZnSO C. ZnO(SO ) D.ZnSO·H O
4 3 4 2 4 2
【答案】C
【解析】750℃时剩余固体与680℃时一样,剩下13.43g,质量减少了 ,26.90g
ZnSO·6H O中水的质量 ,则还有S元素质量减少 ,26.90g
4 2
ZnSO·6H O中S元素的质量 ,则S元素还有剩余,故答案选择C。
4 2
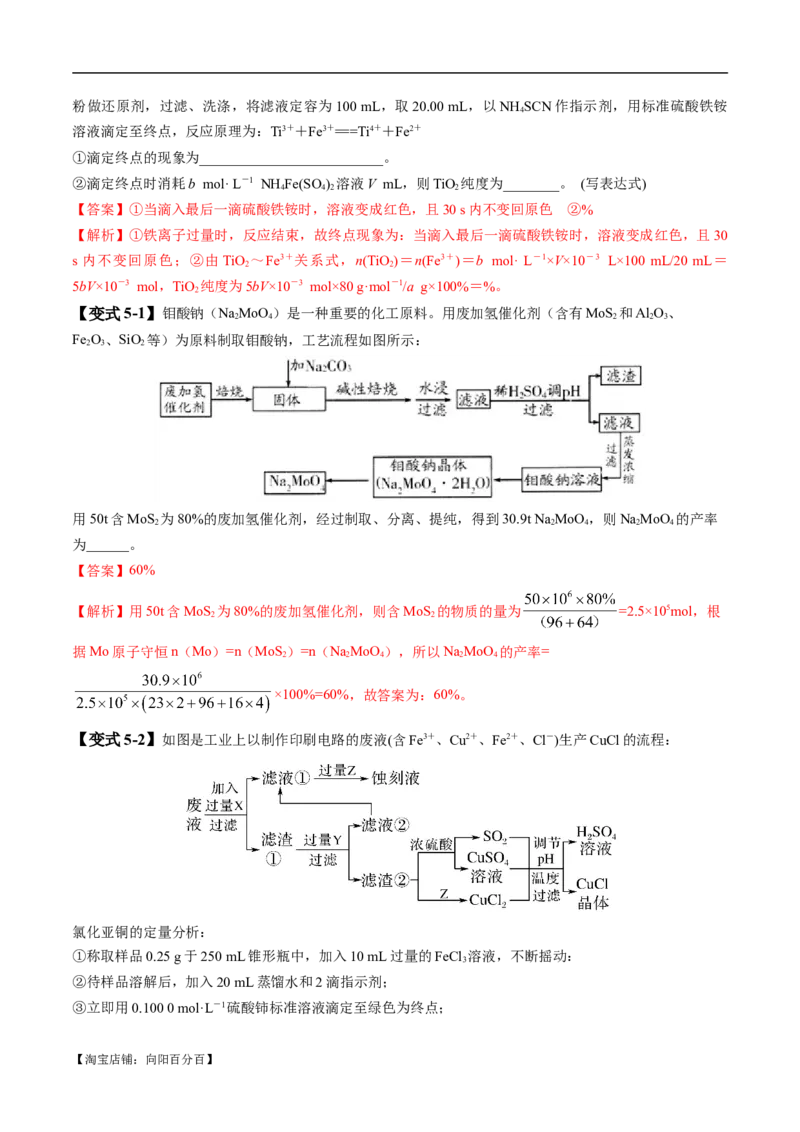
【变式5-3】称取3.60 g草酸亚铁晶体(FeC O·2H O,相对分子质量是180)用热重法对其进行热分解,得
2 4 2
到剩余固体的质量随温度变化的曲线如图所示,请分析图并回答下列问题:
【淘宝店铺:向阳百分百】(1)过程Ⅰ发生反应的化学方程式为_________________________________________________________。
(2)300 ℃时剩余固体只有一种且是铁的氧化物,试通过计算确定该氧化物的化学式________________。
【答案】(1)FeC O·2H O FeC O+2HO (2)Fe O
2 4 2 2 4 2 2 3
【解析】
(1)通过剩余固体的质量可知,过程Ⅰ发生的反应是草酸亚铁晶体受热失去结晶水,反应的化学方程式为
FeC O·2H O FeC O+2HO。
2 4 2 2 4 2
(2)草酸亚铁晶体中的铁元素质量为3.6 g××100%≈1.12 g,草酸亚铁晶体中的铁元素完全转化到氧化物中,
氧化物中氧元素的质量为1.60 g-1.12 g=0.48 g,铁元素和氧元素的质量比为1.12 g∶0.48 g=7∶3,设铁
的氧化物的化学式为Fe O,则有56x∶16y=7∶3,x∶y=2∶3,铁的氧化物的化学式为Fe O。
x y 2 3
突破6 工艺流程题中有关K 的计算类型
sp
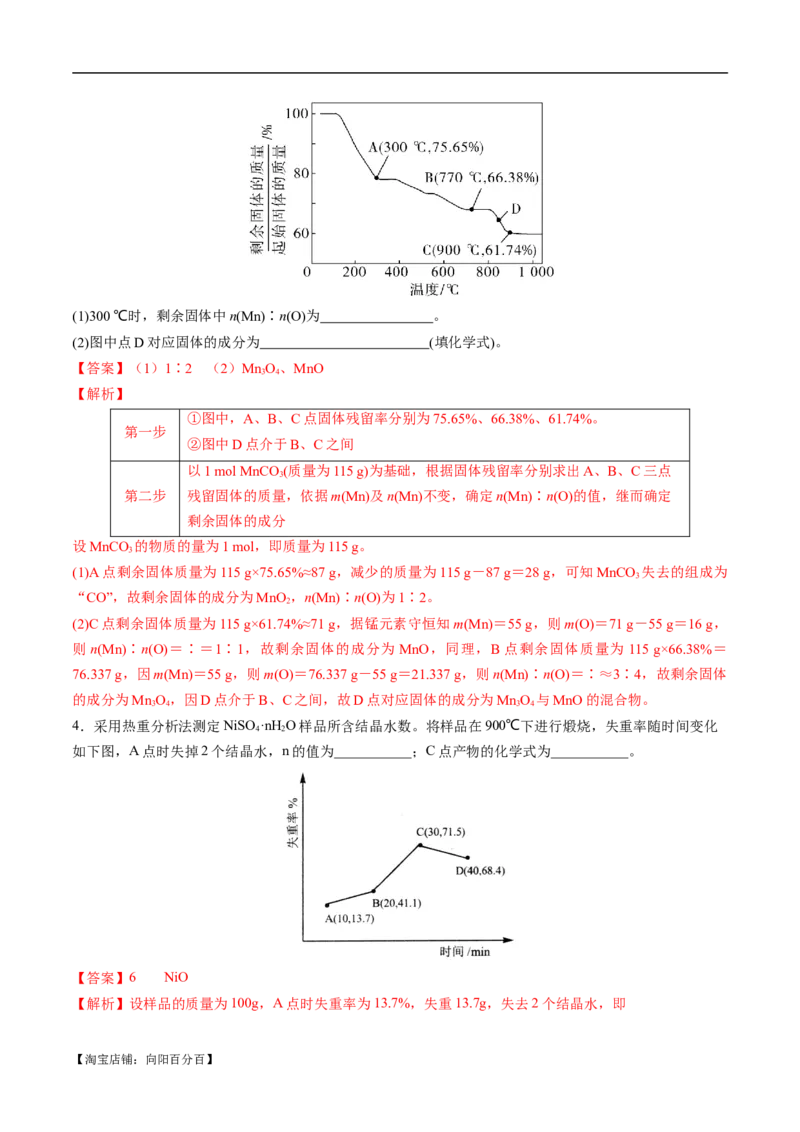
【例8】(2023·湖南卷)处理某铜冶金污水(含 )的部分流程如下:
已知:①溶液中金属离子开始沉淀和完全沉淀的 如下表所示:
物质
【淘宝店铺:向阳百分百】开始沉淀 1.9 4.2 6.2 3.5
完全沉淀 3.2 6.7 8.2 4.6
② 。
下列说法错误的是
A.“沉渣Ⅰ”中含有 和
B. 溶液呈碱性,其主要原因是
C.“沉淀池Ⅱ”中,当 和 完全沉淀时,溶液中
D.“出水”经阴离子交换树脂软化处理后,可用作工业冷却循环用水
【答案】D
【分析】污水中含有铜离子、三价铁离子、锌离子、铝离子,首先加入石灰乳除掉三价铁离子和铝离子,
过滤后,加入硫化钠除去其中的铜离子和锌离子,再次过滤后即可达到除去其中的杂质,以此解题。
【解析】A.根据分析可知氢氧化铁当pH=1.9时开始沉淀,氢氧化铝当pH=3.5时开始沉淀,当pH=4时,
则会生成氢氧化铝和氢氧化铁,即“沉渣I”中含有Fe(OH) 和Al(OH) ,A正确;
3 3
B.硫化钠溶液中的硫离子可以水解,产生氢氧根离子,使溶液显碱性,其第一步水解的方程式为:S2-
+H O HS-+OH-,B正确;
2
C.当铜离子和锌离子完全沉淀时,则硫化铜和硫化锌都达到了沉淀溶解平衡,则
⇌
,C正确;
D.污水经过处理后其中含有较多的钙离子,故“出水”应该经过阳离子交换树脂软化处理,达到工业冷
却循环用水的标准后,才能使用,D错误;
故选D。
【例9】工业上用重铬酸钠(Na Cr O)母液生产重铬酸钾(K Cr O)的工艺流程如图所示:
2 2 7 2 2 7
上述流程中KCr O 发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过
2 2 7
加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH) 沉淀时
3
Fe3+是否沉淀完全?________(填“是”或“否”)。{已知:K [Fe(OH) ]=4.0×10-38,K [Cr(OH) ]=6.0×10
sp 3 sp 3
-31}
【答案】是
【解析】Cr(OH) 开始出现沉淀时,溶液中c3(OH-)===2×10-26,若Fe3+沉淀完全时,c(Fe3+)应小于10
3
-5mol·L-1,此时溶液中c(Fe3+)== mol·L-1=2×10-12 mol·L-1<1×10-5 mol·L-1,说明Fe3+沉淀完全。
【淘宝店铺:向阳百分百】【例10】偏钒酸镁在化工“新型材料”光电领域有着重要的用途。以硼泥[主要成分是MgO(52.12%)还有
Fe O、FeO、Al O、SiO 等杂质]为原料设计制备偏钒酸镁的生产工艺如图所示:
2 3 2 3 2
“除杂”过程加入双氧水的目的是________________________________________________(用离子方程式表
示)。此过程中使Fe3+、Al3+浓度均小于1×10-6 mol·L-1,在室温下需调节pH的范围是:__________(已知:
K [Fe(OH) ]=1×10-39,K [Al(OH) ]=1×10-33,pH=9.3时,Mg2+开始沉淀)。
sp 3 sp 3
【答案】2Fe2++HO+2H+===2Fe3++2HO 5<pH<9.3
2 2 2
【解析】加入双氧水可以把Fe2+氧化为Fe3+,离子方程式为2Fe2++HO +2H+===2Fe3++2HO。因氢氧
2 2 2
化铝的溶解度大于氢氧化铁,根据K [Al(OH) ]=1×10-33,Fe3+、Al3+浓度均小于l×10-6mol·L-1时c(OH
sp 3
-)>mol·L-1=10-9mol·L-1,pH最小值为5,为防止Mg2+沉淀,控制pH的最大值为9.3,所以pH的范围是
5K [Fe(OH) ],Ga3+完全沉淀
2 3 3 sp 3 sp 3
时Fe3+已经完全沉淀,浓度小于 1×10-5mol·L-1,c(OH-)==mol·L-1=3×10-9mol·L-1,c(H+)=×10-
5mol·L-1,pH=-lg(×10-5)=5.48,Zn2+开始沉淀时c(OH-)== mol·L-1=4×10-8mol·L-1,c(H+)=×10-
6mol·L-1,pH=-lg(×10-6)=6.6,则pH应调节的范围为5.48