文档内容
模板 04 实验简答题答题规范
本节导航
识·题型解读 考情分析+命题预测/技巧解读
明·模板构建 答题模板+技巧点拨
通·模板运用 真题示例+模板答题+变式训练
练 ·模板演练 最新模拟、预测考向
实验试题中,语言表达题是常见的考查形式,考查内容包括仪器的作用、实验操作的目的和作用、
实验操作的描述、实验现象的描述等。此类试题在相对简单和陌生的研究对象及问题情境下,考查学
生信息获取与加工、逻辑推理与论证能力,如基于题给信息的原因分析;基于现象和原因的措施分析;
基于物质性质的原因分析;基于题给信息和物质性质的判断等。
一、实验操作类规范语言表述答题模板
1.实验操作目的或原因规范描述
实验操作目的或原因 规范描述
先通入N 或惰性气体的目的 除去装置中的空气,排除O 对实验的干扰
2 2
末端连接碱石灰干燥管的目的 防止空气中的CO 和水蒸气对实验的干扰
2
防止反应物的蒸气逸出脱离反应体系,从而提高反应物
冷凝回流操作的目的
的转化率
①减小压强,使液体沸点降低,更易分离出某种液体。
减压蒸馏的目的 ②防止加热时某些物质(如HO)的分解。如浓缩双氧水
2 2
需减压蒸馏
恒压滴液漏斗中支管的作用 平衡气压,使恒压滴液漏斗中的液体顺利滴下
①分离除杂:使杂质充分沉淀或溶解,提高纯度。②调
调节溶液pH的目的 控反应:使溶液呈酸性,提高氧化性,或使溶液呈碱
性,控制反应的发生①水洗:除去晶体表面水溶性的杂质;②“冰水洗
涤”:能洗去晶体表面的杂质离子,同时防止晶体在洗
沉淀的洗涤目的 涤过程中的溶解损耗;③用特定有机试剂清洗晶体:洗
去晶体表面的杂质,降低晶体的溶解度、有利于析出,
减少损耗等
“趁热过滤”的目的 防止降温过程中杂质析出,提高产品的纯度
2.基本操作规范答题
基本操作 答题规范
静置,取沉淀后的上层清液,加入××试剂(沉淀剂),若没有
证明沉淀完全的操作
沉淀生成,说明沉淀完全
沿玻璃棒向过滤器中的沉淀上加蒸馏水至没过沉淀,静置使
洗涤沉淀的操作
其全部滤出,重复操作2~3次
取最后一次洗涤液,加入××试剂(根据沉淀可能吸附的杂质
检验沉淀是否洗涤干净的操
离子,选择合适的检验试剂),若没有××(特征现象)出现,
作
证明沉淀已洗涤干净
蒸发浓缩→冷却结晶→过滤→洗涤(包括水洗、冰水洗、热水
从溶液中得到晶体的操作
洗、乙醇洗等)→干燥
3.化学实验中常见操作的目的、作用或原因
(1)沉淀水洗的目的:除去××杂质(可溶于水)
(2)沉淀用乙醇洗涤的目的:a.减小固体的溶解损失;b.除去固体表面吸附的杂质;c.乙醇挥发带走水分,
使固体快速干燥
(3)冷凝回流的作用及目的:防止××蒸气逸出而脱离反应体系,提高××物质的转化率
(4)控制溶液pH的目的:防止××离子水解;防止××离子沉淀;确保××离子沉淀完全;防止××物质溶解
等
(5)“趁热过滤”后,有时先向滤液中加入少量水,加热至沸腾,然后再“冷却结晶”出目标产物的原
因:稀释溶液,防止降温过程中杂质析出,提高产品的纯度
(6)加过量A试剂的原因:使B物质反应完全或提高B物质的转化率等
(7)加入氧化性试剂的目的:使××(还原性)物质转化为××物质
(8)温度不高于××℃的原因:温度过低反应速率较慢,温度过高××物质(如HO 、浓硝酸、NH HCO
2 2 4 3
等)分解或××物质(如浓硝酸、浓盐酸)挥发或××物质(如NaSO 等)氧化或促进××物质(如AlCl 等)水解。
2 3 3
(9)减压蒸馏(减压蒸发)的原因:减小压强,使液体沸点降低,防止××物质(如 HO 、浓硝酸、
2 2
NH HCO 等)受热分解
4 3
(10)蒸发、反应时的气体氛围:抑制××离子的水解(如蒸发AlCl 溶液得无水AlCl 时需在HCl气流中进
3 3
行,加热MgCl ·6H O得MgCl 时需在HCl气流中进行等)
2 2 2
(11)配制某溶液时事先煮沸水的原因:除去溶解在水中的氧气,防止某物质被氧化
(12)反应容器中和大气相通的玻璃管的作用:指示容器中压强大小,避免反应容器中压强过大
(13)加热的目的:加快反应速率或促进平衡向某个方向(一般是有利于生成目标产物的方向)移动(14)用平衡移动原理解释某现象的原因:溶液中存在××平衡,该平衡是××(平衡反应的特点),××(条件
改变)使平衡向××方向移动,产生××现象
4.化学实验中仪器或试剂作用
(1)有机物制备装置中长导管(或冷凝管)的作用:冷凝回流、导气
(2)有机物分离过程中加无水氯化钙的作用:干燥(除水)
(3)固液加热型制气装置中恒压漏斗上的支管的作用:保证反应容器(一般为圆底烧瓶)内压强与恒压漏
斗内压强相等(平衡压强),使恒压漏斗内的液体顺利滴下
(6)温度计的使用方法:蒸馏时温度计的液泡置于蒸馏烧瓶的支管口处,测定馏分的温度;制乙烯时温
度计的液泡置于反应液液面以下(不能接触瓶底),测定反应液的温度
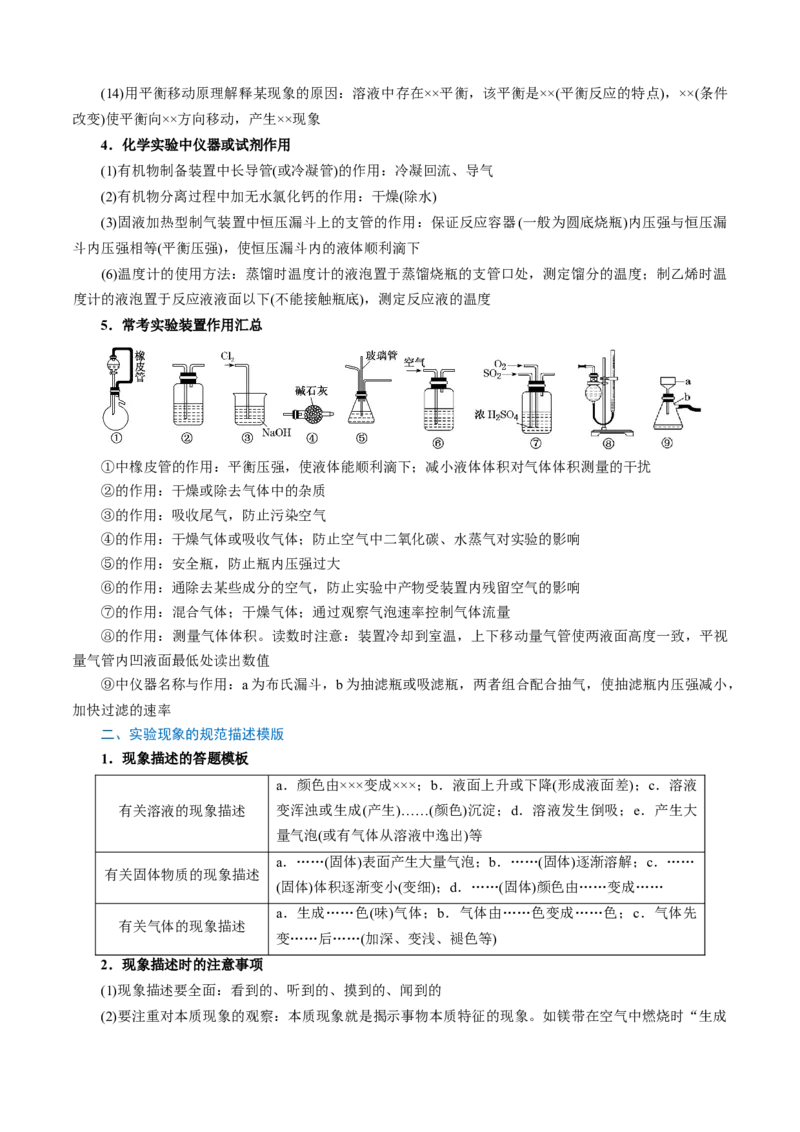
5.常考实验装置作用汇总
①中橡皮管的作用:平衡压强,使液体能顺利滴下;减小液体体积对气体体积测量的干扰
②的作用:干燥或除去气体中的杂质
③的作用:吸收尾气,防止污染空气
④的作用:干燥气体或吸收气体;防止空气中二氧化碳、水蒸气对实验的影响
⑤的作用:安全瓶,防止瓶内压强过大
⑥的作用:通除去某些成分的空气,防止实验中产物受装置内残留空气的影响
⑦的作用:混合气体;干燥气体;通过观察气泡速率控制气体流量
⑧的作用:测量气体体积。读数时注意:装置冷却到室温,上下移动量气管使两液面高度一致,平视
量气管内凹液面最低处读出数值
⑨中仪器名称与作用:a为布氏漏斗,b为抽滤瓶或吸滤瓶,两者组合配合抽气,使抽滤瓶内压强减小,
加快过滤的速率
二、实验现象的规范描述模版
1.现象描述的答题模板
a.颜色由×××变成×××;b.液面上升或下降(形成液面差);c.溶液
有关溶液的现象描述 变浑浊或生成(产生)……(颜色)沉淀;d.溶液发生倒吸;e.产生大
量气泡(或有气体从溶液中逸出)等
a.……(固体)表面产生大量气泡;b.……(固体)逐渐溶解;c.……
有关固体物质的现象描述
(固体)体积逐渐变小(变细);d.……(固体)颜色由……变成……
a.生成……色(味)气体;b.气体由……色变成……色;c.气体先
有关气体的现象描述
变……后……(加深、变浅、褪色等)
2.现象描述时的注意事项
(1)现象描述要全面:看到的、听到的、摸到的、闻到的
(2)要注重对本质现象的观察:本质现象就是揭示事物本质特征的现象。如镁带在空气中燃烧时“生成白色固体”是本质现象,因为由此现象可正确理解化学变化这个概念,而发出“耀眼的白光”则是非本质
现象。因此,观察实验现象要有明确的观察目的和主要的观察对象
(3)现象描述要准确
a.如A试管中……,B处观察到……
b.不能以结论代替现象。如铁丝在氧气中燃烧的实验现象是“火星四射,放出大量的热,生成黑色
固体”,而不能用结论“生成四氧化三铁”代替“生成黑色固体”
(4)格式要正确:按“现象+结论”叙述,不能“以结论代替现象”,忌结论现象不分
(5)汉字使用规范:如“溢出”“逸出”,注意“光”和“火焰”“烟”和“雾”等区别
3.实验现象的规范描述模版
(1)溶液:a.颜色由××色变成××色。b.液面上升或下降(形成液面差)。c.溶液变浑浊,或生成(产生)××色
沉淀。d.溶液发生倒吸。e.产生大量气泡或有气体从溶液中逸出。
(2)固体:a.固体表面产生大量气泡。b.固体逐渐溶解。c.固体体积逐渐变小(变细)。d.(固体)颜色由××
变成××。
(3)气体:a.生成××色(味)气体。b.气体由××色变成××色。c.先变××后××(加深、变浅、褪色)。
(4)滴定终点的判断:滴溶液(当滴入最后半滴××标准溶液)→观色变(溶液由××色变成××色)→半分钟(且
半分钟内不恢复原来颜色)。
三、物质检验和鉴别类的答题规范
1.离子的检验
取试样→加水溶解→加……试剂
⃗除干扰⃗分离
加……检验试剂→观察现象→得
单一离子 出结论
检验 以SO的检验为例:取少量溶液于试管中,加入足量稀盐酸,无明显现象,再加入
BaCl 溶液,若有白色沉淀产生,则证明有SO
2
取少量溶液于两支试管中,分别加入……试剂,现象是……的是……物质;取少量溶
液于两支试管中,分别加入……试剂,现象是……继续加入……试剂,现象是……的
是……物质
多种离子
检验某溶液中既含有Fe2+又含有Fe3+的方法:分别取少量溶液于两支试管中,向其
检验
中一支试管中滴加几滴KSCN溶液,溶液显血红色,则证明溶液中含有Fe3+,再向
另一支试管中滴加几滴铁氰化钾[K Fe(CN) ]溶液,有蓝色沉淀生成,则证明溶液中含
3 6
有Fe2+
2.固体的检验
** 错误的表达式 **取少许固体样品于两支试管中,加水溶解,分别再加入……试剂(微
热/振荡),现象是……的是……物质
答题
** 错误的表达式 **取少许固体样品于试管中,加水溶解,把样品分为两等份,一份
模板
加……试剂,现象是……的是……物质,另一份加……试剂,现象是……的是……物
质
实例 榴石矿石可以看作CaO、FeO、Fe O、Al O、SiO 组成。试设计实验证明榴石矿中含有
2 3 2 3 2FeO(试剂任选,说明实验操作与现象):取矿石少许于试管中,加稀硫酸充分反应后,
向其中滴加酸性高锰酸钾溶液,若紫色褪去,则证明矿石中含有FeO (不能加盐酸溶解)
3.气体检验
将气体通入(或通过) 试剂[×××溶液(或××固体)] 描述现象 得出结
单一气体检验
论
混合气体的检验 检验气体甲 除去气体甲 确定气体甲已除尽 检验气体乙
以“CO 气体检验”为例:将无色无味的气体通入澄清石灰水中,若溶液变
2
实例
浑浊,则证明该气体是CO
2
** 错误的表达式 **水蒸气最先检验;** 错误的表达式 **有干扰的气体先
微点拨
检验;** 错误的表达式 **关键词:如“少量”“除尽”等
4.物质的鉴别
①分别取固体分置于两支试管中加热或加入……试剂,现象是……的是……物
质
固体
②分别取固体分置于两支试管中溶于水形成溶液,加……试剂,现象是……的
是……物质
①分别取两溶液分置于两支试管中,分别加入……试剂,现象是……的是……
物质
溶液
②分别取两溶液分置于两支试管中,分别加入……试剂,现象是……继续加
入……试剂,现象是……的是……物质
取适量……溶液于两支洁净试管中,分别通入两种气体,能使……(试剂)……
(现象)的是……气体,不能使……(试剂)……(现象)的是……气体
气体
鉴别SO 和CO :取适量品红溶液于两洁净的试管中,分别通入两气体,能使
2 2
品红溶液褪色的是SO 气体,不能使品红溶液褪色的是CO
2 2
5.气体的验满和验纯操作
气体 方法
氧气验满 将带火星的木条平放在集气瓶口,若木条复燃,则气体已集满
二氧化碳验满 将燃着的木条平放在集气瓶口,若火焰熄灭,则气体已集满
氨气验满 将湿润的红色石蕊试纸放在集气瓶口,若试纸变蓝,则气体已集满
氯气验满 将湿润的碘化钾淀粉试纸放在集气瓶口,若试纸变蓝,则气体已集满
可燃性气体(如氢气) 用排水法收集一小试管的气体,用大拇指摁住管口移近火焰,放开手指,若
的验纯方法 听到尖锐的爆鸣声,则气体不纯;若听到轻微的“噗”的一声,则气体纯净
1. (2024·甘肃卷)某兴趣小组设计了利用 和 生成 ,再与 反应制备
的方案:(1)采用下图所示装置制备 ,仪器a的名称为_______;步骤I中采用冰水浴是为了_______;
(2)步骤Ⅱ应分数次加入 ,原因是_______;
(3)步骤Ⅲ滴加饱和 溶液的目的是_______;
(4)步骤Ⅳ生成 沉淀,判断 已沉淀完全的操作是_______;
(5)将步骤Ⅴ中正确操作或现象的标号填入相应括号中_______。
A.蒸发皿中出现少量晶体
B.使用漏斗趁热过滤
C.利用蒸发皿余热使溶液蒸干
D.用玻璃棒不断搅拌
E.等待蒸发皿冷却
【答案】(1)①. 恒压滴液漏斗 ②. 增大SO 的溶解度、增大HSO 的浓度,同时为步骤Ⅱ提供低温
2 2 3
(2)防止过多的MnO 与HSO 反应生成MnSO ,同时防止反应太快、放热太多、不利于控制温度低于
2 2 3 4
10℃
(3)除去过量的SO (或HSO )
2 2 3
(4)静置,向上层清液中继续滴加几滴饱和NaCO 溶液,若不再产生沉淀,说明Mn2+已沉淀完全
2 3
(5)D、A、E
【分析】步骤Ⅱ中 MnO 与 HSO 在低于 10℃时反应生成 MnS O ,反应的化学方程式为
2 2 3 2 6
MnO +2H SO =MnSO+2H O,步骤Ⅲ中滴加饱和Ba(OH) 除去过量的SO (或HSO ),步骤Ⅳ中滴入饱
2 2 3 2 6 2 2 2 2 3
和NaCO 溶液发生反应MnS O+Na CO=MnCO↓+Na SO ,经过滤得到NaSO 溶液,步骤Ⅴ中NaSO
2 3 2 6 2 3 3 2 2 6 2 2 6 2 2 6
溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥得到NaSO∙2HO。
2 2 6 2
【解析】(1)根据仪器a的特点知,仪器a为恒压滴液漏斗;步骤Ⅰ中采用冰水浴是为了增大SO 的溶解度、
2
增大HSO 的浓度,同时为步骤Ⅱ提供低温;
2 3
(2)由于MnO 具有氧化性、SO (或HSO )具有还原性,步骤Ⅱ应分数次加入MnO ,原因是:防止过多
2 2 2 3 2
的MnO 与HSO 反应生成MnSO ,同时防止反应太快、放热太多、不利于控制温度低于10℃;
2 2 3 4
(3)步骤Ⅲ中滴加饱和Ba(OH) 溶液的目的是除去过量的SO (或HSO ),防止后续反应中SO 与NaCO
2 2 2 3 2 2 3溶液反应,增加饱和NaCO 溶液的用量、并使产品中混有杂质;
2 3
(4)步骤Ⅳ中生成MnCO 沉淀,判断Mn2+已沉淀完全的操作是:静置,向上层清液中继续滴加几滴饱和
3
NaCO 溶液,若不再产生沉淀,说明Mn2+已沉淀完全;
2 3
(5)步骤Ⅴ的正确操作或现象为:将滤液倒入蒸发皿中→用酒精灯加热→用玻璃棒不断搅拌→蒸发皿中出现
少量晶体→停止加热→等待蒸发皿冷却→过滤、洗涤、干燥得到NaSO∙2HO,依次填入D、A、E。
2 2 6 2
2.(2024·新课标卷)吡咯类化合物在导电聚合物、化学传感器及药物制剂上有着广泛应用。一种合成
1-(4-甲氧基苯基)-2,5-二甲基吡咯(用吡咯X表示) 反的应和方法如下:
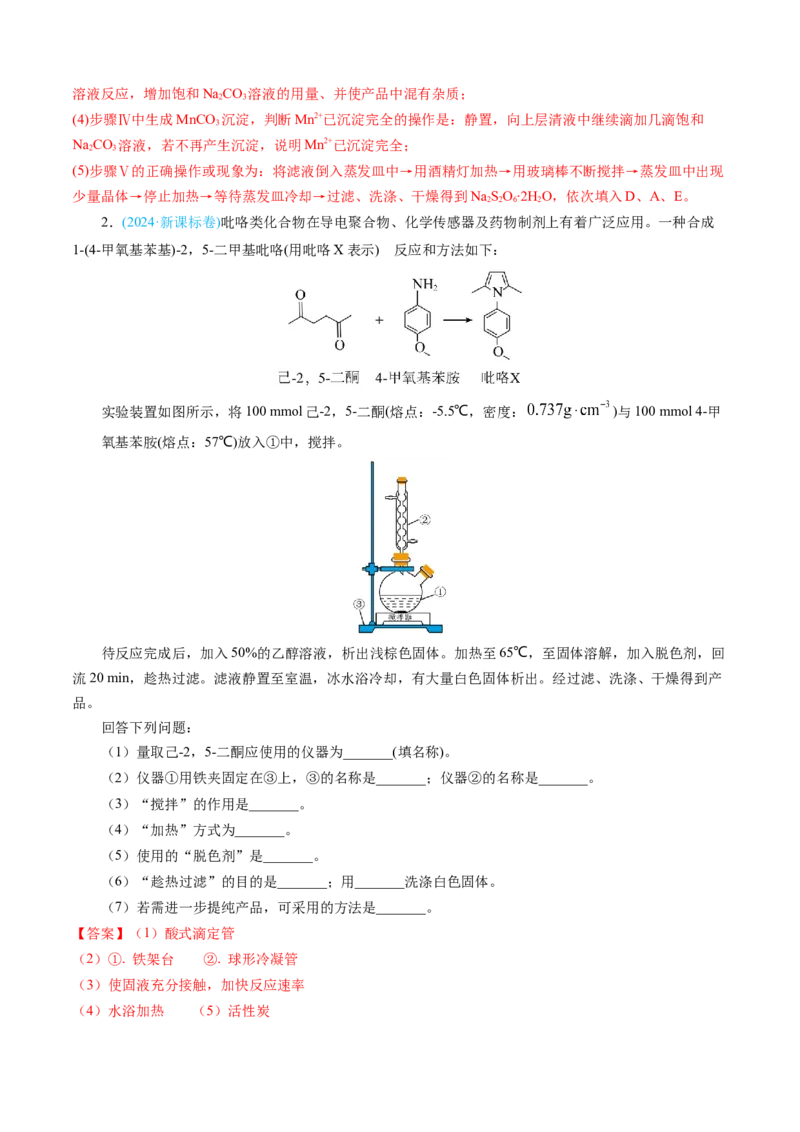
实验装置如图所示,将100 mmol己-2,5-二酮(熔点:-5.5℃,密度: )与100 mmol 4-甲
氧基苯胺(熔点:57℃)放入①中,搅拌。
待反应完成后,加入50%的乙醇溶液,析出浅棕色固体。加热至65℃,至固体溶解,加入脱色剂,回
流20 min,趁热过滤。滤液静置至室温,冰水浴冷却,有大量白色固体析出。经过滤、洗涤、干燥得到产
品。
回答下列问题:
(1)量取己-2,5-二酮应使用的仪器为_______(填名称)。
(2)仪器①用铁夹固定在③上,③的名称是_______;仪器②的名称是_______。
(3)“搅拌”的作用是_______。
(4)“加热”方式为_______。
(5)使用的“脱色剂”是_______。
(6)“趁热过滤”的目的是_______;用_______洗涤白色固体。
(7)若需进一步提纯产品,可采用的方法是_______。
【答案】(1)酸式滴定管
(2)①. 铁架台 ②. 球形冷凝管
(3)使固液充分接触,加快反应速率
(4)水浴加热 (5)活性炭(6)①. 防止产品结晶损失,提高产率 ②. 50%的乙醇溶液
(7)重结晶
【分析】将100 mmol己-2,5-二酮(熔点:-5.5℃,密度:0.727g·cm-3)与100 mmol 4-甲氧基苯胺(熔点:
57℃)放入两颈烧瓶中,利用球形冷凝管进行冷凝回流提高原料利用率,通过搅拌来提高反应速率,反应完
成后,加入50%的乙醇溶液,析出浅棕色固体(即含杂质的产品),加热至65℃,至固体溶解,加入脱色剂
(脱色剂为不溶于水和乙醇等溶剂的固体,如:活性炭),回流20min,趁热过滤,使产品尽可能多地进
入滤液,滤液静置至室温,冰水浴冷却,有大量白色固体析出,经过滤、洗涤、干燥得到产品。
【解析】(1)己-2,5-二酮的摩尔质量为114g·mol-1,根据题中所给数据可知,所需己-2,5-二酮的体积为
,又因为酮类对橡胶有腐蚀性,所以选用酸式滴定
管。
(2)③为铁架台;仪器②用于冷凝回流,为球形冷凝管。
(3)己-2,5-二酮的熔点为-5.5℃,常温下为液体,4-甲氧基苯胺的熔点为57℃,常温下为固体,搅拌可使固
液反应物充分接触,加快反应速率。
(4)由题给信息“加热至65℃”可知,应用水浴加热,这样便于控制温度,且受热更均匀。
(5)“脱色剂”的作用是吸附反应过程中产生的有色物质,结合题中信息,加入脱色剂后回流,趁热过滤,
保留滤液,即脱色剂为不溶于水和乙醇等溶剂的固体,所以可以选用活性炭作脱色剂。
(6)由题给信息可知,产品吡咯X为白色固体,加热至65℃可溶解在50%的乙醇溶液中,所以需趁热过滤,
使产品尽可能多地进入滤液,防止产品结晶损失,提高产率;由加入50%的乙醇溶液,析出浅棕色固体(即
含杂质的产品)可知,常温下产品不溶于50%的乙醇溶液,所以为减少溶解损失,洗涤时可用50%的乙醇溶
液。
(7)由产品的分离提纯过程可知,若需进一步提纯,可采用的方法为重结晶。
1. (2023·河北选考)配合物Na[Co(NO )](M=404 g·mol-1)在分析化学中用于K+的鉴定,其制备装置示意
3 2 6
图(夹持装置等略)及步骤如下:
①向三颈烧瓶中加入15.0 g NaNO 和15.0 mL热蒸馏水,搅拌溶解。
2
②磁力搅拌下加入5.0 g Co(NO)·6H O,从仪器a加入50%醋酸7.0 mL。冷却至室温后,再从仪器b缓
3 2 2
慢滴入30%双氧水8.0 mL。待反应结束,滤去固体。③在滤液中加入95%乙醇,静置40分钟。固液分离后,依次用乙醇、乙醚洗涤固体产品,称重。
已知:ⅰ.乙醇、乙醚的沸点分别是78.5 ℃、34.5℃;
ⅱ.NaNO 的溶解度数据如下表。
2
温度/℃ 20 30 40 50
溶解度/(g/100 g H O) 84.5 91.6 98.4 104.1
2
回答下列问题:
(2)步骤①中,用热蒸馏水的目的是 ________________________________。
(3)步骤③中,用乙醚洗涤固体产品的作用是 ________________________。
(4)实验室检验样品中钾元素的常用方法是:将铂丝用盐酸洗净后,在外焰上灼烧至与原来的火焰颜色相同
时,用铂丝蘸取样品在外焰上灼烧, ____________________________________________。
【答案】(2)增加NaNO 的溶解度
2
(3)加速产品干燥
(4)透过蓝色钴玻璃观察火焰的颜色,若呈紫色则含钾元素
【解析】三颈烧瓶中加入NaNO 和热蒸馏水,将物料溶解加入Co(NO )·6H O再加入醋酸,冷却至室温后,
2 3 2 2
再从仪器b缓慢滴入30%双氧水,待反应结束,滤去固体,在滤液中加入95%乙醇降低溶解度,析晶,过
滤洗涤干燥,得到产物。
(2)步骤①中,用热蒸馏水的目的是增加NaNO 的溶解度。
2
(3)步骤③中,用乙醚洗涤固体产品的作用是加速产品干燥。
(4)实验室检验样品中钾元素的常用方法是:将铂丝用盐酸洗净后,在外焰上灼烧至与原来的火焰颜色相同
时,用铂丝蘸取样品在外焰上灼烧,透过蓝色钴玻璃观察火焰的颜色,若呈紫色则含钾元素。
2.实验室用粗锌(含ZnS、ZnC 杂质)制备纯净干燥的H,用以还原WO 得到金属W的装置如图所示。
2 2 3
(1)装置a的作用是___________________________________。
(2)洗气瓶①、②、③中盛装的试剂分别为足量酸性KMnO 溶液、 ________________、浓硫酸。为了确保
4
实验科学性,洗气瓶①中的实验现象:有沉淀产生、 ________________________;写出酸性KMnO 溶液
4
与酸性气体发生反应的离子方程式为 ________________________________________。
(3)管式炉加热前,需要进行的操作是 __________________________________。
(4)结束反应时,先 ________(填字母)。
a.关闭活塞K b.停止加热
【答案】(1)安全瓶,防倒吸
(2)氢氧化钠溶液 (紫色)变浅(不能写褪色) 2MnO+5HS+6H+===5S↓+2Mn2++8HO、2MnO+10Cl-+
2 2
16H+===2Mn2++5Cl↑+8HO
2 2
(3)用试管在④处收集气体并点燃,通过声音判断气体纯度(4)b
【解析】H 还原WO 制备金属W,装置Q用于制备氢气,因盐酸易挥发,则①、②、③应分别用于除去
2 3
HS、HCl、氯气和水,得到干燥的氢气与WO 在加热条件下制备W,实验结束后应先停止加热再停止通
2 3
入氢气,以避免W被重新氧化,以此解答该题。
(1)装置a中没有试剂,作用是安全瓶,防倒吸。
(2)由分析,②中液体是用于除去氢气中的氯气,应为氢氧化钠溶液,为了确保实验科学性,要确保硫化氢
吸收完全,故洗气瓶①中的实验现象:有沉淀产生、紫色变浅但未褪色,高锰酸钾有强氧化性,与HS、
2
HCl反应,生成硫单质、氯气和二价锰离子,离子方程式为2MnO+5HS+6H+===5S↓+2Mn2++8HO、
2 2
2MnO+10Cl-+16H+===2Mn2++5Cl↑+8HO。
2 2
(3)可燃性气体点燃或者加热前需要验纯,故管式炉加热前,需要进行的操作是:用试管在④处收集气体并
点燃,通过声音判断气体纯度。
(4)实验结束后应先停止加热再停止通入氢气,以避免W被重新氧化,故选b。
3.无水氯化铬(CrCl )是有机合成和无机合成的重要原料,实验室中可采用含水氧化铬制备无水氯化铬。制
3
备步骤如下:
ⅰ.组装好装置,检验装置气密性,向瓷舟中加入Cr O·nHO。
2 3 2
ⅱ.向体系中通入干燥纯净的N 一段时间。
2
ⅲ.使N 通过CCl ,进入到硬质玻璃管中,同时打开管式炉,对反应物加热。
2 4
ⅳ.制备实验结束后,继续通入纯净的N,直至产物冷却为室温,硬质玻璃管右端有紫色薄片出现。
2
ⅴ.检测产品纯度,实验装置如右图所示:
已知相关部分物质的性质如下表:
无水氯化铬(CrCl ) 紫色晶体,950 ℃升华,易溶于水
3
Cr O 绿色粉末固体,熔点2 435 ℃,高温下能被O 氧化
2 3 2
CCl 无色液体,沸点:76~77 ℃
4
光气(COCl ) 无色气体,剧毒,遇水水解:COCl +HO===CO +2HCl
2 2 2 2
回答下列问题:
(1)步骤ⅰ中,检验装置B气密性的方法是 ___________________________________。
(2)步骤ⅱ中,通入纯净的N 时,请描述K、K、K 的关闭或打开状态:________________________。
2 1 2 3
(3)管式炉中,Cr O·nHO先失水转化为Cr O ,然后与CCl 反应,除目标产物外,还产生光气,生成目标
2 3 2 2 3 4
产物的化学方程式是_________________________。该实验中为了得到足够浓度的气态CCl ,可采取
4
的方法为_________________。
(4)反应过程中,通入N 的作用是 ________________________________。
2(5)装置C中NaOH溶液的作用是 _______________________________(用离子方程式表示)。
(6)该装置存在的弊端有 _______________________________________(填两条)。
【答案】 (1)关闭K 、K ,打开K ,在硬质玻璃管处微热,若装置C中导气管口有气泡冒出,停止微热,
1 2 3
导气管内有水柱上升,且较长时间不回落,则装置B气密性良好
(2)打开K、K,关闭K
1 3 2
(3)Cr O+3CCl =====2CrCl +3COCl 水浴加热装置A
2 3 4 3 2
(4)搅动CCl ,加快其挥发
4
(5)COCl +4OH-===CO+2Cl-+2HO
2 2
(6)装置B、C间缺少干燥装置;装置BC间导管太细,易堵塞(合理即可)
【解析】 三氯化铬易潮解,高温下易被氧化,因此反应前需要除去装置内的空气,先通入氮气,除去装
置中原有的空气,随后加热A中四氯化碳使其汽化为气态CCl 进入B中,加热条件下与Cr O 反应生成
4 2 3
CrCl ,生成的COCl 被NaOH溶液吸收。(1)检验装置B气密性的方法:关闭K 、K ,打开K ,在硬质玻
3 2 1 2 3
璃管处微热,若装置C中导气管口有气泡冒出,停止微热,导气管内有水柱上升,且较长时间不回落,则
装置B气密性良好。(2)通入纯净的N 时,需打开K、K,关闭K。(3)Cr O 与CCl 反应,生成CrCl 和光
2 1 3 2 2 3 4 3
气,Cr O +3CCl =====2CrCl +3COCl ;实验中为了得到足够浓度的气态CCl ,可采取的方法:水浴加
2 3 4 3 2 4
热装置A。(4)反应过程中,通入N 的作用:搅动CCl ,加快其挥发。(5)光气有毒,可用装置C中NaOH
2 4
溶液吸收,题中所给信息:COCl +HO===CO +2HCl,故与NaOH溶液反应的离子方程式为COCl +
2 2 2 2
4OH-===CO+2Cl-+2HO。(6)该装置存在的弊端有装置B、C间缺少干燥装置;装置B、C间导管太细,
2
易堵塞。
4.氢氧化亚铁为白色固体,难溶于水,在空气中极易被氧化为氢氧化铁。回答下列问题;
(一)制备氢氧化亚铁
(1)装置 A 中盛装生石灰的仪器的名称是_______。选择上图中的装置制备氢氧化亚铁,连接顺序为
________(按气流方向从左到右,填写装置标号)。装置C的作用是 _________________________。
(2)装置B中发生反应的离子方程式为 ______________________________。反应结束后,继续通一段时间
的N,目的是 ___________________________。
2
(二)灰绿色沉淀的成因
反应后将装置B中的固体过滤时,白色沉淀会逐渐转变为灰绿色,实验小组为探究灰绿色沉淀的成因,
查阅到以下资料;①Fe(OH) 沉淀具有较强的吸附性;②若存在固体杂质,会导致Fe(OH) 沉淀不够紧
2 2
密,沉淀与溶液的接触面积会更大。
甲同学猜测灰绿色可能是Fe(OH) 吸附Fe2+引起的,设计并完成了实验1~实验3。
2
实验 操作 试剂(均为0.1 mol·L-1) 实验现象ⅰ.1滴FeSO 溶液 玻璃片夹缝中有白色
4
1
ⅱ.4滴NaOH溶液 浑浊
玻璃片夹缝中有白色
ⅰ.4滴FeSO 溶液
4
2 浑浊,一段时间后变
向两片玻璃片中心
ⅱ.1滴NaOH溶液
为灰绿色
分别滴加试剂,面
ⅰ.2滴FeSO 溶液,1滴
对面快速夹紧 4
玻璃片夹缝中立即有
3 Fe (SO ) 溶液
2 4 3
灰绿色浑浊
ⅱ.2滴NaOH溶液
(3)依据甲同学的猜测,实验1中沉淀无灰绿色的原因是 _____________________________。
(4)实验3中立即出现灰绿色浑浊的原因是 _____________________________。
(5)根据以上实验探究,若尽可能制得白色 Fe(OH) 沉淀,需要控制的实验条件除了隔绝氧气外,还有
2
______________________________________。
【答案】 (1)三颈烧瓶 ACBD 做安全瓶,防倒吸
(2)Fe2++2NH +2HO===Fe(OH) ↓+2NH 防止拆除装置时残留的氨气逸出,污染空气
3 2 2
(3)NaOH溶液过量,反应后溶液中Fe2+浓度很小,不易被吸附在Fe(OH) 表面
2
(4)Fe(OH) 沉淀中混有Fe(OH) ,导致Fe(OH) 沉淀不够紧密,与溶液的接触面积增大,更容易吸附Fe2+
2 3 2
(5)保证NaOH溶液过量(或保证FeSO 溶液不足)
4
【解析】 装置A为氨气的发生装置,B为制备氢氧化亚铁的装置,C为防倒吸装置,连在AB之间,D
为NH 的尾气处理装置,据此回答。(1)装置A中盛装生石灰的仪器的名称是三颈烧瓶,制备氢氧化亚铁,
3
根据分析可知,装置的连接顺序为ACBD,装置C的作用是做安全瓶,防倒吸。(2)装置B中发生反应的离
子方程式为Fe2++2NH +2HO===Fe(OH) ↓+2NH,反应结束后,继续通一段时间的N,目的是防止拆除
3 2 2 2
装置时残留的氨气逸出,污染空气。(3)实验1中沉淀无灰绿色的原因是NaOH溶液过量,反应后溶液中
Fe2+浓度很小,不易被吸附在Fe(OH) 表面。(4)实验3中立即出现灰绿色浑浊的原因是Fe(OH) 沉淀中混有
2 2
Fe(OH) ,导致Fe(OH) 沉淀不够紧密,与溶液的接触面积增大,更容易吸附Fe2+。(5)若尽可能制得白色
3 2
Fe(OH) 沉淀,需要控制的实验条件除了隔绝氧气外,还有保证NaOH溶液过量(或保证FeSO 溶液不足)。
2 4
5.亚硫酰氯(SOCl )是一种重要化工试剂,被广泛应用于结晶水合物的脱水和有机合成。工业上合成方
2
法之一是:PCl (s)+SO (g)===POCl (l)+SOCl (l) ΔH=-101.4 kJ·mol-1。已知相关物质的熔、沸点及
5 2 3 2
水解性如表:
物质 熔点/℃ 沸点/℃ 水解性
POCl 1.2 105.5 易水解
3
SOCl -104.5 76 易水解
2
PCl 160(升华) 167 易水解
5
某小组在实验室模拟工业制亚硫酰氯设计如图实验。(1) 反应过程中C装置的烧瓶要放在冰水浴中,原因是 。
②判断PCl 已与SO 完全反应的实验现象是 。
① 5 2
(2)反应结束后,从双颈烧瓶中的液体得到较纯净的亚硫酰氯需进行的操作是 。
【答案】(1) 该反应放热,SOCl 沸点低(76 ℃),保持低温防止SOCl 汽化挥发
2 2
②固体完全消失(或B、C装置导管口冒出气泡的速率近似相等)
①
(2)对C装置双颈烧瓶中的液体进行蒸馏(或取出C装置双颈烧瓶中的液体进行蒸馏)
【解析】(1)①由题干信息可知,该反应放热,SOCl 沸点低(76 ℃),需保持低温防止SOCl 汽化挥发,
2 2
故反应过程中C装置的烧瓶要放在冰水浴中。②由题干信息可知,PCl 为固体,SO 为气体,POCl 和
5 2 3
SOCl 均为液体,则判断PCl 已与SO 完全反应的实验现象是固体完全消失(或B、C装置导管口冒出气泡
2 5 2
的速率近似相等)。(2)利用POCl 和SOCl 二者沸点相差较大的特点,反应结束后,从双颈烧瓶中的液
3 2
体得到较纯净的亚硫酰氯需进行的操作是对C装置双颈烧瓶中的液体进行蒸馏(或取出C装置双颈烧瓶中
的液体进行蒸馏)。
6.化学实验小组通过查阅相关资料,设计了以下制备无水氯化亚锡(SnCl )的实验方案:
2
a.将锡箔和浓盐酸(添加少量浓硝酸)装入三颈烧瓶,按如图组装好回流装置,在95 ℃回流反应;
b.在CO 气氛下蒸发浓缩SnCl 盐酸溶液,析出SnCl ·2H O晶体,抽滤;
2 2 2 2
c.用乙酸酐[(CHCO)O]脱去结晶水,得到无水SnCl 晶体,抽滤并用乙醚洗涤,真空干燥得到产品。
3 2 2
已知:Sn2+具有较强还原性且易水解。
(1)溶解锡箔时,向浓盐酸中添加少量浓硝酸的目的是 。
(2)采用回流装置的作用: 。
(3)用乙醚洗涤晶体的优点是 。
(4)实验室配制的氯化亚锡溶液如欲装瓶存放一段时间,需要向瓶中既加入盐酸又加入锡粒,目的分别是
。
【答案】(1)增强氧化性,加快溶解反应速率
(2)提高原料利用率、避免污染空气(答出一点即可)
(3)减少产品溶解损失且利于干燥固体
(4)加入盐酸抑制水解,加入锡粒防止氧化【解析】(1)溶解锡箔时,向浓盐酸中添加少量浓硝酸的目的是增强氧化性,加快溶解反应速率。(2)
采用回流装置,可以提高原料利用率、避免污染空气。(3)SnCl ·2HO不溶于乙醚,用乙醚洗涤晶体,
2 2
可以减少产品溶解损失且利于干燥固体。(4)Sn2+易水解,且Sn2+易被氧化为Sn4+,所以需要向瓶中既
加入盐酸又加入锡粒,加入盐酸抑制水解,加入锡粒防止氧化。
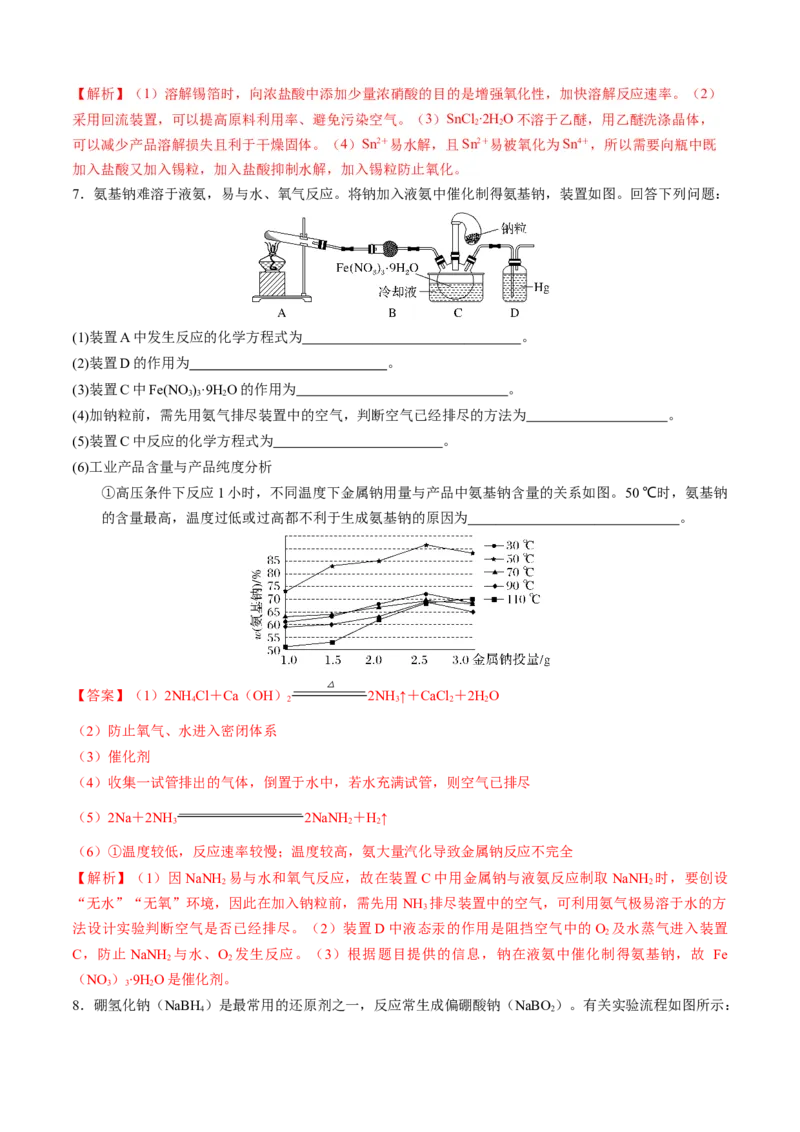
7.氨基钠难溶于液氨,易与水、氧气反应。将钠加入液氨中催化制得氨基钠,装置如图。回答下列问题:
(1)装置A中发生反应的化学方程式为 。
(2)装置D的作用为 。
(3)装置C中Fe(NO )·9H O的作用为 。
3 3 2
(4)加钠粒前,需先用氨气排尽装置中的空气,判断空气已经排尽的方法为 。
(5)装置C中反应的化学方程式为 。
(6)工业产品含量与产品纯度分析
①高压条件下反应1小时,不同温度下金属钠用量与产品中氨基钠含量的关系如图。50 ℃时,氨基钠
的含量最高,温度过低或过高都不利于生成氨基钠的原因为 。
△
【答案】(1)2NH Cl+Ca(OH) 2NH ↑+CaCl +2HO
4 2 3 2 2
(2)防止氧气、水进入密闭体系
(3)催化剂
(4)收集一试管排出的气体,倒置于水中,若水充满试管,则空气已排尽
(5)2Na+2NH 2NaNH +H↑
3 2 2
(6)①温度较低,反应速率较慢;温度较高,氨大量汽化导致金属钠反应不完全
【解析】(1)因NaNH 易与水和氧气反应,故在装置C中用金属钠与液氨反应制取NaNH 时,要创设
2 2
“无水”“无氧”环境,因此在加入钠粒前,需先用 NH 排尽装置中的空气,可利用氨气极易溶于水的方
3
法设计实验判断空气是否已经排尽。(2)装置D中液态汞的作用是阻挡空气中的O 及水蒸气进入装置
2
C,防止NaNH 与水、O 发生反应。(3)根据题目提供的信息,钠在液氨中催化制得氨基钠,故 Fe
2 2
(NO )·9HO是催化剂。
3 3 2
8.硼氢化钠(NaBH )是最常用的还原剂之一,反应常生成偏硼酸钠(NaBO )。有关实验流程如图所示:
4 2氢化钠 硼氢化钠 偏硼酸钠
Ⅰ.氢化钠的制备:
已知NaH能在潮湿的空气中自燃。甲同学用如图所示装置(每种装置只选一次)来制取NaH。
(1)装置的连接顺序是C→ →D→ ,X、Y分别是 、 。
(2)通入H ,点燃装置D处酒精灯之前的实验操作是 。若省略该操作,可能
2
导致的后果是 。
【答案】Ⅰ.(1)A B 碱石灰(或生石灰) 浓硫酸
(2)验纯或排尽装置中的空气 爆炸或仪器炸裂等
【解析】Ⅰ.(1)C装置中制取的氢气需要除杂和干燥,即除去水蒸气和氯化氢气体,应选择碱石灰(或
生石灰等),既可以吸收氯化氢也可以吸收水分,D装置制得的NaH能在潮湿的空气中自燃,还需要在D
装置之后连接一个干燥装置,则实验装置的连接顺序为C→A→D→B,A盛装的试剂X为碱石灰(或生石
灰等),B中盛装的试剂Y为浓硫酸。(2)通入H,点燃装置D处酒精灯之前的实验操作是验纯(或将
2
装置中空气排尽);若省略该操作,氢气中混有空气,可能导致的后果是爆炸(或仪器炸裂等)。
9.某合作学习小组进行以下实验探究。
①实验任务
通过测定溶液电导率,探究温度对AgCl溶解度的影响。
②查阅资料
电导率是表征电解质溶液导电能力的物理量。温度一定时,强电解质稀溶液的电导率随溶液中离子浓
度的增大而增大;离子浓度一定时,稀溶液电导率随温度的升高而增大。25 ℃时,K (AgCl)=1.8×10-10。
sp
③提出猜想
猜想a:较高温度的AgCl饱和溶液的电导率较大。
猜想b:AgCl在水中的溶解度S(45 ℃)>S(35 ℃)>S(25 ℃)。
④设计实验、验证猜想
取试样Ⅰ、Ⅱ、Ⅲ(不同温度下配制的AgCl饱和溶液),在设定的测试温度下,进行表1中实验1~3,
记录数据。
表1
实验序号 试样 测试温度/℃ 电导率/(μS·cm-1)
Ⅰ:25 ℃的AgCl饱和溶
1 25 A
1
液
Ⅱ:35 ℃的AgCl饱和溶
2 35 A
2
液
3 Ⅲ:45 ℃的AgCl饱和溶 45 A 3液
⑤数据分析、交流讨论
25 ℃的AgCl饱和溶液中,c(Cl-)=______mol·L-1。实验结果为A>A>A 。小组同学认为,此结果可
3 2 1
以证明③中的猜想a成立,但不足以证明猜想b成立。结合②中信息,猜想b不足以成立的理由有
______________________________________________________。
⑥优化实验
小组同学为进一步验证猜想b,在实验1~3的基础上完善方案,进行实验4和5。请完成表2中内容。
表2
实验序号 试样 测试温度/℃ 电导率/(μS·cm-1)
4 Ⅰ B
1
5 B
2
⑦实验总结
根据实验1~5的结果,并结合②中信息,小组同学认为猜想b也成立。猜想b成立的判断依据是
___________________________________________________________________。
【答案】⑤1.34×10-5 测试温度不同,根据电导率结果无法判断不同温度下饱和溶液的溶解度
45 ℃ Ⅱ 45 ℃ ⑦A>B>B
3 2 1
【解析】⑤由于AgCl饱和溶液中c(Ag+)=c(Cl-),因此25 ℃时,c(Cl-)== mol·L-1=×10-5 mol·L-
⑥
1≈1.34×10-5 mol·L-1。由于不同温度下的饱和溶液的浓度不同,因此实验1、2、3中,存在两个变量(温度
与浓度),因此不足以证明猜想b成立。⑥要证明AgCl在水中的溶解度S(45 ℃)>S(35 ℃)>S(25 ℃),则还
需要控制相同温度,不同浓度进行实验。⑦猜想b成立的判断依据是A>B>B。
3 2 1
10.亚硝酰氯(NOCl)可作为有机合成试剂。
已知:①2NO+Cl=====2NOCl。②沸点:NOCl为-6 ℃,Cl 为-34 ℃,NO为-152 ℃。③NOCl
2 2
易水解,能与O 反应。
2
某研究小组用NO和Cl 在如图所示装置中制备NOCl,并分离回收未反应的原料。
2
回答问题:
(1)通入Cl 和NO前先通入氩气,作用是___________________;仪器D的名称是___________。
2
(2)将催化剂负载在玻璃棉上而不是直接平铺在玻璃管中,目的是_______________________________。
(3)实验所需的NO可用NaNO 和FeSO 溶液在稀HSO 中反应制得,离子反应方程式为
2 4 2 4
________________________________。
(4)为分离产物和未反应的原料,低温浴槽 A的温度区间应控制在___________,仪器C收集的物质是
___________。
(5)无色的尾气若遇到空气会变为红棕色,原因是______________________________。
【答案】(1)排尽装置中的空气,防止NO、NOCl与空气中的O 反应,防止NOCl遇空气中的水而水解
2干燥管 (2)增大与气体的接触面积,加快反应速率 (3)NO+Fe2++2H+===NO↑+Fe3++HO (4)-34 ℃
2
<T≤-6 ℃或(-34 ℃,-6 ℃] Cl (5)与空气中的O 反应产生红棕色的NO
2 2 2
【解析】(1)通入Cl 和NO前先通入氩气,作用是排尽装置中的空气,防止 NO和NOCl与空气中的O 反
2 2
应,防止NOCl遇空气中的水而水解;仪器D的名称是干燥管;(2)目的是增大与气体的接触面积,加快反
应速率;(4)为分离产物和未反应的原料,低温浴槽A使NOCl冷凝,得到产品,则温度区间应控制在-34
℃<T≤-6 ℃或(-34 ℃,-6 ℃];再经过低温浴槽B降温,使Cl 冷凝,防止逸出,污染空气,仪器C收
2
集的物质是Cl;(5)剩下的气体为NO,与空气中的O 反应产生红棕色的NO 。
2 2 2
11.CaS是一种重要的工业原料,科研小组利用硫酸钙与焦炭高温制备 CaS,并探究其生成物,装置图如
图所示。实验过程中B、C、E、F都有明显的现象。已知CO不与酸性KMnO 溶液反应,各装置对气
4
体的吸收都是完全的。
(1)实验开始前先通一段时间氮气再加热,其目的是__________________________________。
(2)碱石灰的主要成分为___________________。
(3)已知反应中会产生SO ,B装置中KMnO 溶液褪色,写出装置B中反应的离子方程式:
2 4
_______________________________________________。
(4)能说明产物中有CO的实验现象是____________________________________________。
(5)通常选择固体原料在加热条件下制 CaS,而不能在水溶液中制取 CaS,请解释其原因:
_________________________________________________________________。
【答案】(1)将装置中的空气排尽,以免干扰实验 (2)CaO(NaOH、KOH 和 HO 可写,也可不写)
2
(3)2MnO+5SO +2HO===2Mn2++5SO+4H+ (4)E中出现红色固体,F中澄清石灰水变浑浊
2 2
(5)CaS遇水会发生水解
【解析】(3)装置B中SO 与KMnO 发生反应使KMnO 溶液褪色,MnO→Mn2+得5e-,SO →SO失2e-,
2 4 4 2
根据得失电子守恒,MnO、SO 的化学计量数分别为2、5,再根据电荷守恒和原子守恒配平可得反应的离
2
子方程式。(4)若产物中有CO,则装置E中一氧化碳与氧化铜共热反应生成铜和二氧化碳,生成的二氧化
碳会使F中澄清石灰水变浑浊。
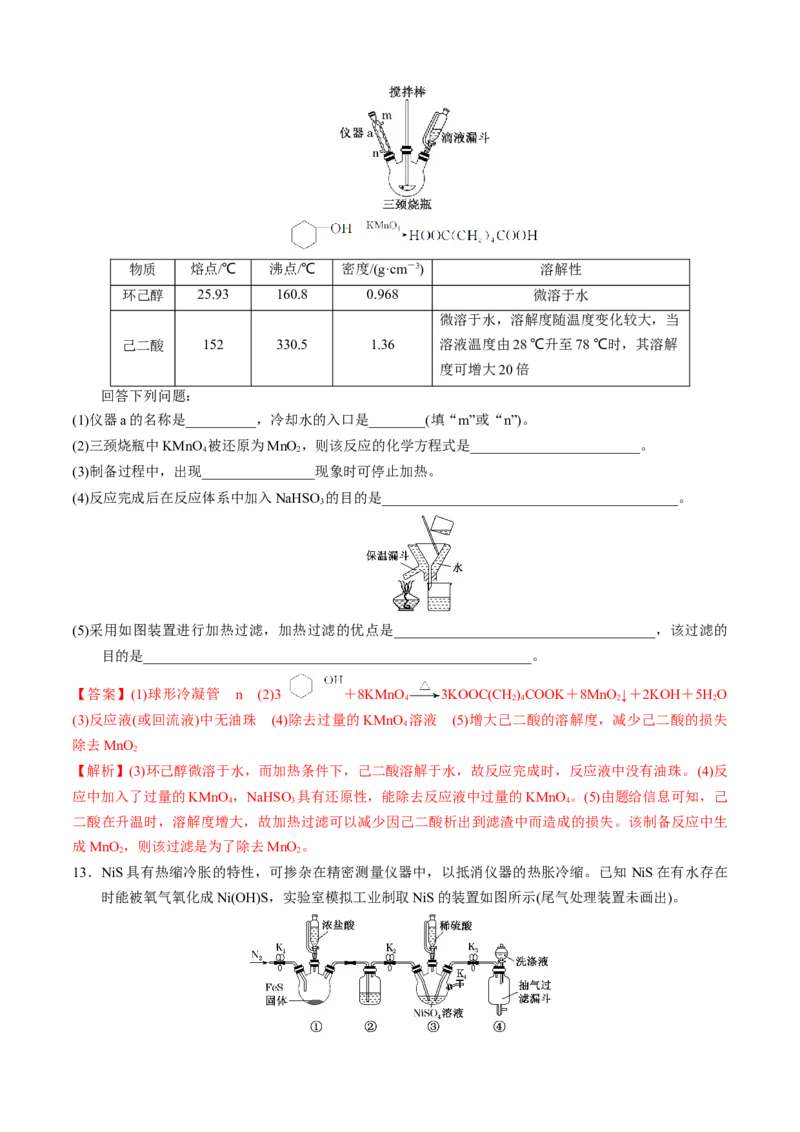
12.己二酸在化工生产、有机合成工业、医药、润滑剂制造等方面都有重要作用。某实验小组以环己醇
(OH)和KMnO 为主要原料制备己二酸,制备流程如下:
4
主要实验装置示意图、制备原理和部分物质的性质如下:物质 熔点/℃ 沸点/℃ 密度/(g·cm-3) 溶解性
环己醇 25.93 160.8 0.968 微溶于水
微溶于水,溶解度随温度变化较大,当
己二酸 152 330.5 1.36 溶液温度由28 ℃升至78 ℃时,其溶解
度可增大20倍
回答下列问题:
(1)仪器a的名称是__________,冷却水的入口是________(填“m”或“n”)。
(2)三颈烧瓶中KMnO 被还原为MnO ,则该反应的化学方程式是________________________。
4 2
(3)制备过程中,出现________________现象时可停止加热。
(4)反应完成后在反应体系中加入NaHSO 的目的是__________________________________________。
3
(5)采用如图装置进行加热过滤,加热过滤的优点是_____________________________________,该过滤的
目的是_______________________________________________________。
【答案】(1)球形冷凝管 n (2)3 +8KMnO 3KOOC(CH )COOK+8MnO ↓+2KOH+5HO
4 2 4 2 2
(3)反应液(或回流液)中无油珠 (4)除去过量的KMnO 溶液 (5)增大己二酸的溶解度,减少己二酸的损失
4
除去MnO
2
【解析】(3)环己醇微溶于水,而加热条件下,己二酸溶解于水,故反应完成时,反应液中没有油珠。(4)反
应中加入了过量的KMnO ,NaHSO 具有还原性,能除去反应液中过量的KMnO 。(5)由题给信息可知,己
4 3 4
二酸在升温时,溶解度增大,故加热过滤可以减少因己二酸析出到滤渣中而造成的损失。该制备反应中生
成MnO ,则该过滤是为了除去MnO 。
2 2
13.NiS具有热缩冷胀的特性,可掺杂在精密测量仪器中,以抵消仪器的热胀冷缩。已知 NiS在有水存在
时能被氧气氧化成Ni(OH)S,实验室模拟工业制取NiS的装置如图所示(尾气处理装置未画出)。操作步骤:
Ⅰ.按照如图所示连接装置,并检查气密性;
Ⅱ.打开K、K、K,关闭K,向装置①中通入N 排净装置中的空气;
1 2 4 3 2
Ⅲ.向①②③④中装入对应药品;
Ⅳ.关闭K、K,打开K、K,然后滴加酸溶液直至反应完全;
1 3 2 4
Ⅴ.关闭K、K,打开K,开启抽气机抽气,放出洗涤液洗涤,干燥。
2 4 3
回答下列问题:
(1)步骤Ⅰ检查气密性的方法:_______________________________________________。
(2)写出NiS接触空气生成Ni(OH)S的化学方程式:____________________________,装置①在滴加浓盐酸
前通入N,若没有这个操作则会对实验带来何种不利?________________________________。
2
(3)装置②的名称是__________,装置②中所加入的试剂应为________(填标号)。
A.浓硫酸 B.NaOH溶液
C.饱和NaHS溶液 D.酸性高锰酸钾溶液
(4)装置③中滴加稀硫酸的目的是___________________________________________。
(5)步骤Ⅴ洗涤沉淀应选用的洗涤试剂为________(填标号)。
A.无水酒精 B.煮沸过的蒸馏水
C.饱和NaS溶液 D.稀硫酸
2
(6)某同学根据实验推断出溶度积K (NiS)<K (FeS),他的推断依据可能是_________________________。
sp sp
请你设计实验方案验证该结论:_________________________________________________________。
【答案】(1)关闭滴液漏斗活塞并塞紧塞盖,关闭K 和K ,封闭抽气过滤漏斗下口,向装置④中分液漏斗
1 4
内加水后再打开其活塞与旋塞,液体不能顺利流下,则气密性良好(其他合理表达均可)
(2)4NiS+2HO+O===4Ni(OH)S 有水存在时装置中的氧气会将NiS氧化成Ni(OH)S,产品纯度降低
2 2
(3)洗气瓶 C
(4)酸化NiSO 溶液,抑制Ni2+水解,提高产品纯度
4
(5)B
(6)对比装置①中反应FeS+2H+===Fe2++HS↑和装置③中反应Ni2++HS===NiS↓+2H+,可知溶度积
2 2
K (NiS)<K (FeS) 两支试管中分别取等体积等浓度的FeSO 溶液、NiSO 溶液,分别逐滴滴加等浓度的
sp sp 4 4
NaS溶液,比较二者开始产生沉淀时所用NaS溶液的体积(或滴数),所用NaS溶液体积小的溶度积较小
2 2 2
(其他合理方案也可)
【解析】(2)根据题干信息可知,制备过程要隔绝空气,所以通入N 的目的是排除装置中的空气,若没有
2
该操作,则会发生反应4NiS+2HO+O===4Ni(OH)S,降低产品纯度。(3)装置③的反应环境是水溶液,可
2 2
以推知装置②的作用不是干燥,结合整套装置可以看出装置②可以除去HCl,故装置②是洗气瓶;浓硫酸、
酸性高锰酸钾溶液会氧化HS,NaOH能与HS发生反应,除去HS中的HCl应选饱和NaHS溶液。(4)Ni2+
2 2 2
水解能生成Ni(OH) 沉淀,使产品纯度降低,硫酸能抑制Ni2+水解。(5)沉淀表面是硫酸盐等杂质,酒精洗
2
涤硫酸盐的能力不如水,饱和NaS溶液和稀硫酸洗涤后固体表面仍然留有杂质,用煮沸过的蒸馏水最好,
2
防氧化又能洗去表面杂质,所以选 B。(6)分析实验装置的反应,对比装置①中反应FeS+2H+===Fe2++
HS↑,装置③中反应Ni2++HS===NiS↓+2H+,FeS可与酸性溶液反应生成Fe2+和HS,而Ni2+和HS在
2 2 2 2酸性溶液中反应生成NiS沉淀,可推测溶度积K (NiS)<K (FeS)。
sp sp