文档内容
参考答案:
1.A
【详解】A.聚丙烯的主要原料为丙烯,主要来源是石油的裂解,故A正确;
B.水晶、玛瑙的主要成分是二氧化硅,属于氧化物,不是硅酸盐,不属于硅酸盐工业产品,
故B错误;
C.人造刚玉的主要成分是三氧化二铝(或氧化铝),故C错误;
D.使燃料充分燃烧可以增大氧气的浓度或增大氧气的接触面积,空气的通入量增多会带走
热量,降低热效率,故D错误;
故答案为A。
2.D
A.向明矾溶液中逐滴加入Ba(OH) 溶液至生成沉淀,当Al3+完全沉淀时,SO2-还未沉淀完全,
2 4
继续加入Ba(OH) 溶液,Al(OH) 溶解,BaSO 增多,且BaSO 增加的质量大于Al(OH) 减
2 3 4 4 3
少的质量,故SO2-完全沉淀时,生成沉淀的质量最大,此时的离子反应方程式为
4
Al3++2SO2-+2Ba2++4OH-=2BaSO +AlO-+2H O,
4 4 2 2
B.不论CO 的量多少,与苯酚钠反应,都生成苯酚和碳酸氢钠,B错误
2
C.I还原性强于Fe2+,Cl 先与I反应,当nFeI :nCl 1:1时,发生反应
2 2 2
2ICl I 2Cl,C错误
2 2
D.硼酸为弱酸,离子方程式中保持化学式不拆,和NaOH溶液的反应为
H BO OH BOH,故D正确;
3 3 4
故选D。
3.D
【分析】W、X、Y、Z的原子序数依次增大且占据三个不同周期,W的原子序数最小,且
可以形成一个共价键,则W为H元素,则X、Y、Z占据两个不同周期,所以X一定为第
二周期元素,X可以形成两个共价键,应为O元素;Y可以形成+3价阳离子,且原子序数
大于O,则为Al元素;Z可以形成5个共价键,应为P元素。
【详解】A.P元素的最高价氧化物对应的水化物为H PO ,为三元弱酸,A正确;
3 4
B.X和Y组成的化合物为Al O ,由于AlCl 为共价化合物,工业上电解熔融态Al O 制备
2 3 3 2 3
铝单质,B正确;
学科网(北京)股份有限公司C.X、Y的简单氢化物分别为H O、AlH ,常温下H O为液体,AlH 为固体,所以AlH
2 3 2 3 3
的熔点更高,C错误;
D.Al3+最外层为8个电子,阴离子中形成两个共价键的O满足8电子稳定结构,由于阴离
子带三个单位负电荷,所以形成一个共价键的O也满足8电子稳定结构,D正确;
综上所述答案为C。
4.B
【详解】A.根据示意图可知,a与c相连后,a电极发生失电子的氧化反应所以作负极,考
虑到电解质溶液为pH=3的Li SO -H SO 溶液,所以a极的电极反应式为:
2 4 2 4
2H O4e O 4H;由于生成H+,所以a极附近的pH下降;A项正确;
2 2
B.根据示意图可知,a与c相连后,c为正极,发生得电子的还原反应,电极反应式应写作:
WO xHxe=H WO ;B项错误;
3 x 3
C.根据示意图,b与c若相连,b极为正极发生氧气的还原反应,考虑到电解质溶液为pH=3
的Li SO -H SO 溶液,所以电极反应式为:O 4H4e=2H O;C项正确;
2 4 2 4 2 2
D.连接a与c后,将太阳能转变成B中的化学能,再连接b,c后,就可将化学能再转变
成电能,最终实现了太阳能向电能的转化,D项正确;
答案选B。
5.D
【详解】A.试管中加入的AgNO 溶液过量,过量的Ag+与I-反应产生AgI沉淀,不能证明
3
AgCl会发生沉淀转化生成AgI沉淀,故无法证明溶度积常数K (AgCl)>K (AgI),A错误;
sp sp
B.乙醇具有挥发性,挥发的气体中含有乙醇及浓硫酸与乙醇发生氧化还原反应产生的SO
2
都具有还原性,二者都能使酸性高锰酸钾溶液褪色,因此不能证明反应产生了乙烯,B错误;
C.氨气的水溶液显碱性,能够使湿润的红色石蕊试纸变蓝色,而不是使湿润的蓝色石蕊试
纸变红色,C错误;
D.将CH CH Br与NaOH溶液共热,发生水解反应产生CH CH OH及NaBr,冷却后,取
3 2 3 2
出上层水溶液,先加HNO 酸化,再加AgNO 溶液有淡黄色沉淀即为AgBr沉淀,则可说明
3 3
有溴元素,D正确;
故合理选项是D。
6.C
【详解】A.盐酸滴定氨水,氨水逐渐减少,铵根离子增多,曲线①代表NH H O,曲
3 2
学科网(北京)股份有限公司线②代表
NH
,选项A正确;
4
B.a点溶液c(NH+)=c(NH •H O),溶液pH=9.26,呈现碱性,c(OH-)>c(H+)根据电
4 3 2
荷守恒,c(NH+)>c(Cl-),c(NH+)=c(NH •H O)>c(Cl-),选项B正确;
4 4 3 2
c(NH+)c OH-
C.K (NH •H O)= 4 ,a点时c(NH+)=c(NH •H O),K (NH •H O)
b 3 2 c(NH H O) 4 3 2 b 3 2
3 2
=c(OH-)=10-4.74,数量级为10-5,选项C错误;
D.滴定终点所得氯化铵溶液,溶液显酸性,若选择甲基橙为指示剂,滴定终点溶液的颜色
变化为黄色变为红色,选项D正确;
答案选C。
7.D
【详解】A.由M和N的结构简式可知,M和N不含有亲水基团,则M和N不易溶于水,
故A错误;
B. 在O→P的过程中,O中的羧基转化成羟基,发生了还原反应,故B错误;
C.戊烯有5种同分异构体,分别为1-戊烯,2-戊烯,2-甲基-1-丁烯,2-甲基-2-丁烯,3-甲基
-1-丁烯。1-戊烯的一氯代物有5种,2-戊烯的一氯代物有5种,2-甲基-1-丁烯的一氯代物有
4种,2-甲基-2-丁烯的一氯代物有3种,3-甲基-1-丁烯的一氯代物有4种,所以一氯戊稀总
共有5+5+4+3+4=21种,所以Q的链状同分异构体有20种,故C错误;
D.由R的结构简式可知,R可以与与Br 发生取代反应,R中含有碳碳双键,能与Br 发生
2 2
加成反应,故D正确;
故选D。
【点睛】有机反应中可以根据组成的变化判断反应类型,得氢失氧的过程为还原反应,得氧
失氢的反应为氧化反应,如羧基变为羟基,属于失去氧的反应,该过程为还原反应。
26(14分). 恒压滴液漏斗(或恒压分液漏斗)(1分) 防倒吸(1分) 降低Na S O 的溶
2 2 4
Δ
解度,有利于其结晶析出 HCOO-+2SO +3OH- S O2+CO2+2H O或HCOO-
2 2 4 3 2
Δ
+2SO +OH- S O2+CO +H O CD 淀粉溶液 87.0 取少量分解产物溶于足量的稀
2 2 4 2 2
盐酸中,静置,取上层清液,滴加几滴BaCl 溶液,若出现沉淀则说明产物中含有Na SO ,
2 2 4
反之则无
【分析】装置A反应产生SO ,进入C装置与甲酸、NaOH等反应生成Na S O ,装置D吸
2 2 2 4
学科网(北京)股份有限公司收多余的SO ,防止污染空气。
2
【详解】(1)容器a为带有恒压装置的分液漏斗,故名称为恒压分液漏斗或恒压滴液漏斗;
由于SO 进入C装置反应可能会产生倒吸,故装置B的作用为防倒吸;
2
(2)因为Na S O 易溶于水、不溶于甲醇,故甲醇的作用为降低Na S O 溶解度,有利于其结
2 2 4 2 2 4
晶析出;根据题意,HCOOH与SO 在碱性条件下反应生成Na S O ,HCOOH滴入后首先
2 2 2 4
与NaOH反应转化为HCOO-,故初步确定反应为:HCOO-+SO +OH-→ S O2-,S元素由
2 2 4
+4被HCOO-还原为+3,推测HCOO- 中C元素由+1被氧化为稳定+4价CO ,由于为碱性条
2
件,故此时应该生成CO2-,结合元素守恒确定生成物中有H O,故配平后方程式为:HCOO-
3 2
Δ Δ
+2SO +3OH- S O2+CO2+2H O(或HCOO-+2SO +OH- S O2+CO +H O);
2 2 4 3 2 2 2 4 2 2
(3)A.Na S O 具有强还原性,强氧化性HNO 能将其氧化为SO2-,故A不合理;
2 2 4 3 4
B.若甲酸与NaOH 物质的量之比为1:1,则此时恰好反应,若NaOH过量,则可以将CO
2
反应生成CO2-,有助于平衡正向移动,提高Na S O 产率,故B不合理;
3 2 2 4
C.Na S O 具有强还原性,在空气中易被氧化,故排尽空气可防止Na S O 被氧化,提高其
2 2 4 2 2 4
纯度,C合理;
D.Na S O 不溶于甲醇,故可用甲醇洗涤,D合理;
2 2 4
故答案选CD。
(4) 涉及I 的滴定,可以用淀粉溶液作指示剂,终点现象为溶液颜色由无色变为浅蓝色,故
2
此处填淀粉溶液;
根据已知方程式确定关系式:Na S O ~NaHSO ·HCHO~2I ,得
2 2 4 2 2
n(I ) 0.2000 mol/L×25.00 mL×10-3 L/mol
c(Na S O )= 2 = =2.5× 10-3 mol;
2 2 4
2 2
2.5×10-3 mol×174 g/mol
W(Na S O )= ×100%=87.0%,即Na S O 质量分数为87.0%;
2 2 4 2 2 4
0.5000 g
(5)检验SO2-,需加入稀盐酸排除SO2-等离子干扰,再加入BaCl 溶液观察现象,不能选用
4 3 2
稀硝酸,因为硝酸会将Na SO 、Na S O 、SO 等物质氧化成SO2-产生干扰,故选用试剂为:
2 3 2 2 3 2 4
稀盐酸和BaCl 溶液,具体操作为:取少量分解产物溶于足量的稀盐酸中,静置,取上层清
2
液,滴加几滴BaCl 溶液,若出现沉淀则说明产物中含有Na SO ,反之则无。
2 2 4
高温
27.(15分) 2Cr O +4Na CO +3O 4Na CrO +4CO 物质的粒度为60
2 3 2 3 2 2 4 2
学科网(北京)股份有限公司目 H SiO (1
2 3
分) 2CrO2+2H+ CrO2+H O 0.25mol·L−1 2.4×10−4 Na Cr O +CH OH+3H SO =2
4 2 7 2 2 2 7 3 2 4
⇌ 38m
Cr(OH)SO +CO ↑+Na SO +4H O 2 100%
4 2 2 4 2 33m
1
【分析】由流程可知,铬渣加入纯碱、空气和辅料氧化煅烧, Cr O 转化为 Na CrO ,存在
2 3 2 4
高温 高温
的副反应:SiO +Na CO Na SiO +CO ↑、Al O +Na CO 2NaAlO +CO ↑,且水浸之
2 2 3 2 3 2 2 3 2 3 2 2
后滤渣1中还原氧化铁和氢氧化钙,加入稀硫酸调节pH,除去溶液中的AlO -、SiO 2-,则
2 3
滤渣2为氢氧化铝、硅酸;滤液中存在2CrO2+2H+ CrO2+H O,经调节pH=a、蒸发结晶
4 2 7 2
后可生成重铬酸钠,然后加入甲醇、硫酸将重铬酸钠⇌还原为Cr(OH)SO ,据此分析解答。
4
【详解】(1)“焙烧”时 Cr O 转化为 Na CrO ,反应化学方程式是2Cr O +4Na CO +3O
2 3 2 4 2 3 2 3 2
高温 高温
4Na CrO +4CO ,故答案为:2Cr O +4Na CO +3O 4Na CrO +4CO ;
2 4 2 2 3 2 3 2 2 4 2
(2)由图可知,“水浸”过程中,物料的粒度(颗粒大小)为60目时铬残余量最小,则最佳的反
应条件为60目,故答案为:物质的粒度为60目;
(3)“滤渣2”的主要成分为Al(OH) 和H SiO ,“过滤2”后,将溶液pH调至a,a小于6.5,目
3 2 3
的是使CrO2转化为CrO2+H O,酸化时发生的反应为:2CrO2+2H+ CrO2+H O,若1L
4 2 7 2 4 2 7 2
10 ⇌ 10
酸化后所得溶液中含铬元素的质量为28.6g,CrO2有 转化为CrO2,说明铬元素有 转
4 11 2 7 11
化为CrO2,根据铬元素守恒,存在关系式:2Cr~2CrO2~CrO2,n(CrO2)
2 7 4 2 7 4 剩余
28.6g 10
= × =0.05mol,则n(CrO2)=0.25mol,因此酸化后所得溶液中
52g/mol 11 2 7
n
c(CrO2)= =0.25mol•L-1, 故答案为:H SiO ; 2CrO2+2H+ CrO2+H O;0.25mol•L-1;
2 7 V 2 3 4 2 7 2
⇌
(4)根据沉淀溶解平衡BaCrO CrO2+Ba2+,有K (BaCrO )=c(CrO2)×c(Ba2+)
4 4 sp 4 4
=1.2×10-10=5.0×10-7×c(Ba2+),⇌解得:c(Ba2+)=2.4×10-4mol/L,故答案为:2.4×10-4;
(5)CH OH 被氧化生成 CO ,根据流程图,Na Cr O 被还原为 Cr(OH)SO ,反应的化学方
3 2 2 2 7 4
程式为Na Cr O +3H SO +CH OH=2Cr(OH)SO +Na SO +CO ↑+4H O,故答案为:
2 2 7 2 4 3 4 2 4 2 2
Na Cr O +3H SO +CH OH=2Cr(OH)SO +Na SO +CO ↑+4H O;
2 2 7 2 4 3 4 2 4 2 2
(6)用m kg 的铬渣(含 Cr O 40%)制备 Cr(OH)SO ,最终得到产品m kg,由Cr原子守恒可
1 2 3 4 2
学科网(北京)股份有限公司m 40% 132m
知理论上生成产品的质量为 1 ×165g/mol×2kg= 1 kg,则产率为
152g/mol 152
m kg
2 38m 38m
132m ×100%= 2 ×100%,故答案为: 2 ×100%。
1kg 33m 33m
152 1 1
【点睛】解得本题的关键是要知道存在 2CrO2+2H+ CrO2+H O,本题的易错点为(3),要
4 2 7 2
注意铬元素的守恒关系的应用。 ⇌
28.(1)B
(2)第一步
4
(3) BCD < p2
9 2
(4) 2CO 12e12H C H 4H O 阳
2 2 4 2
【详解】(1)A.高温低压,平衡逆向移动,不能提高二氧化碳平衡转化率,A错误;
B.低温高压,平衡正向移动,能提高二氧化碳的平衡转化率,B正确;
C.高温高压不能确定平衡移动方向,C错误;
D.低温低压不能确定平衡移动方向,D错误;
故选B;
(2)反应速率较快的是第一步,理由是第一步反应的活化能小;
(3)①A.反应中全为气体物质,恒容容器中混合气体的密度始终保持不变,故不能说明
反应达到平衡,A不符合题意;
B.反应前后气体的总物质的量不同,故容器内混合气体的压强保持不变能说明反应达到平
衡,B符合题意;
C.反应速率:2v CO v H 说明正逆反应速率相等,说明达到平衡,C符合题意;
正 2 逆 2
D.同时断裂2molC—H和1molH—H能说明正逆反应速率相等,说明反应达到平衡,D符
合题意;
故选BCD;
②结合反应,温度相同时,压强增大,平衡逆向移动,甲烷的转化率降低,故由图乙可知,
压强p p 。
1 2
学科网(北京)股份有限公司CH g CO g 2CO g 2H g
4 2 2
起始时物质的量/mol 0.2 0.2 0 0
③ ,平衡时总物质的量为
改变时物质的量/mol 0.1 0.1 0.2 0.2
平衡时物质的量/mol 0.1 0.1 0.2 0.2
0.10.10.20.2mol0.6mol,则平衡时甲烷的平衡分压为 0.1 p ,二氧化碳的平衡分压
0.6 2
0.1 0.2 0.2
为 p ,一氧化碳的平衡分压为 p ,氢气的平衡分压为 p ,则X点对应温度下的
0.6 2 0.6 2 0.6 2
2 2
0.2 0.2
p p
K 0.6 2 0.6 2 4 p 2。
p 0.1 0.1 9 2
p p
0.6 2 0.6 2
(4)连接电源负极的一极为阴极,阴极电极反应为2CO 12e12H=C H 4H O;因为
2 2 4 2
阳极室中的氢离子需要进入阴极室,故该装置中使用的是阳离子交换膜。
35. a c sp CO(或N O、CS 等) N>O>C 高 NH 分子间形成氢键,使
2 2 2 3
411751030
NH 的沸点反常偏高 3∶2 三角锥形
3 N ·a3
A
【分析】根据核外电子排布规律判断微粒能量的大小;根据杂化轨道理论及等电子体理论分
析轨道杂化类型及分子的空间构型;根据元素性质及核外电子排布规律比较元素第一电离能;
根据晶胞结构及题干信息进行相关计算。
【详解】(1)氮原子核外有7个电子,a项电子排布能量最低;b项电子排布违背洪特规则;
c项中1s能级上电子发生跃迁,能量最高;d项中电子排布违背洪特规则。
故答案为a;c ;
(2)NO +的结构类似CO ,都是直线型结构,氮原子通过两个双键与两个O原子相连,氮
2 2
原子为sp杂化。与NO +互为等电子体的化合物有:CO 、CS 或N O等。
2 2 2 2
故答案为 sp ; CO (或N O、CS 等);
2 2 2
(3)氮原子由于2p轨道处于半充满状态,第一电离能反常偏大,故C、N、O三者的第一
电离能由大到小的顺序为:N>O>C;氮的电负性强,NH 分子之间形成氢键,使其沸点反
3
常偏高;砷的电负性弱,在AsH 分子间不能形成氢键,因而AsH 的沸点低。
3 3
故答案为N>O>C;高;NH 分子间形成氢键,使NH 的沸点反常偏高;
3 3
(4)在乙炔分子C≡C中含1个σ键2个π键,此外C−H间还有2个σ键,故σ键与π键数目之
比3∶2;AsCl 分子类似NH 的结构,As采取sp3杂化,故分子结构为三角锥形。
3 3
学科网(北京)股份有限公司故答案为3∶2;三角锥形;
1 1
(5)在BAs晶胞中B位于顶点和面心,故1个晶胞中含B的个数=8× +6× =4,As位于
8 2
4
晶胞内部有4个,故1个晶胞中含4个BAs;则晶胞质量m=ρ·(a×10−10)3= ×(11+75)g,
N
A
411751030
故晶胞的密度ρ= g·cm−3。
N ·a3
A
411751030
故答案为 。
N ·a3
A
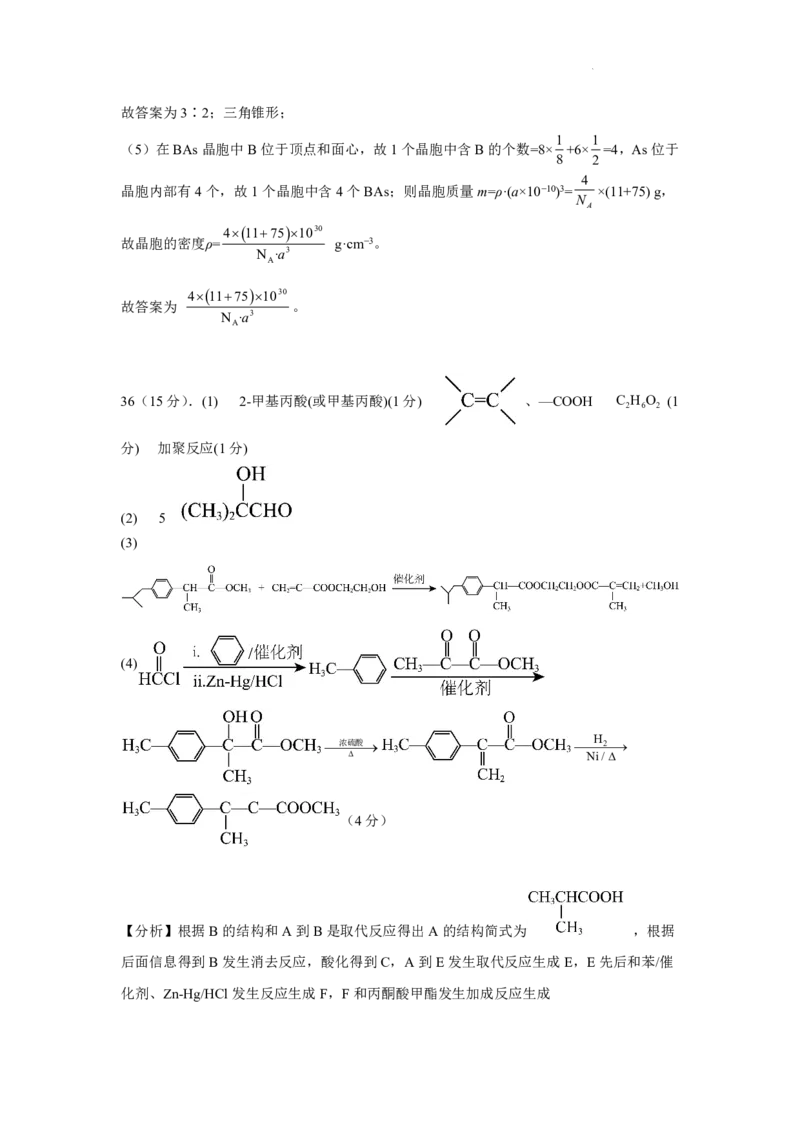
36(15分).(1) 2-甲基丙酸(或甲基丙酸)(1分) 、—COOH C H O (1
2 6 2
分) 加聚反应(1分)
(2) 5
(3)
(4)
浓硫酸 H 2
Ni/
(4分)
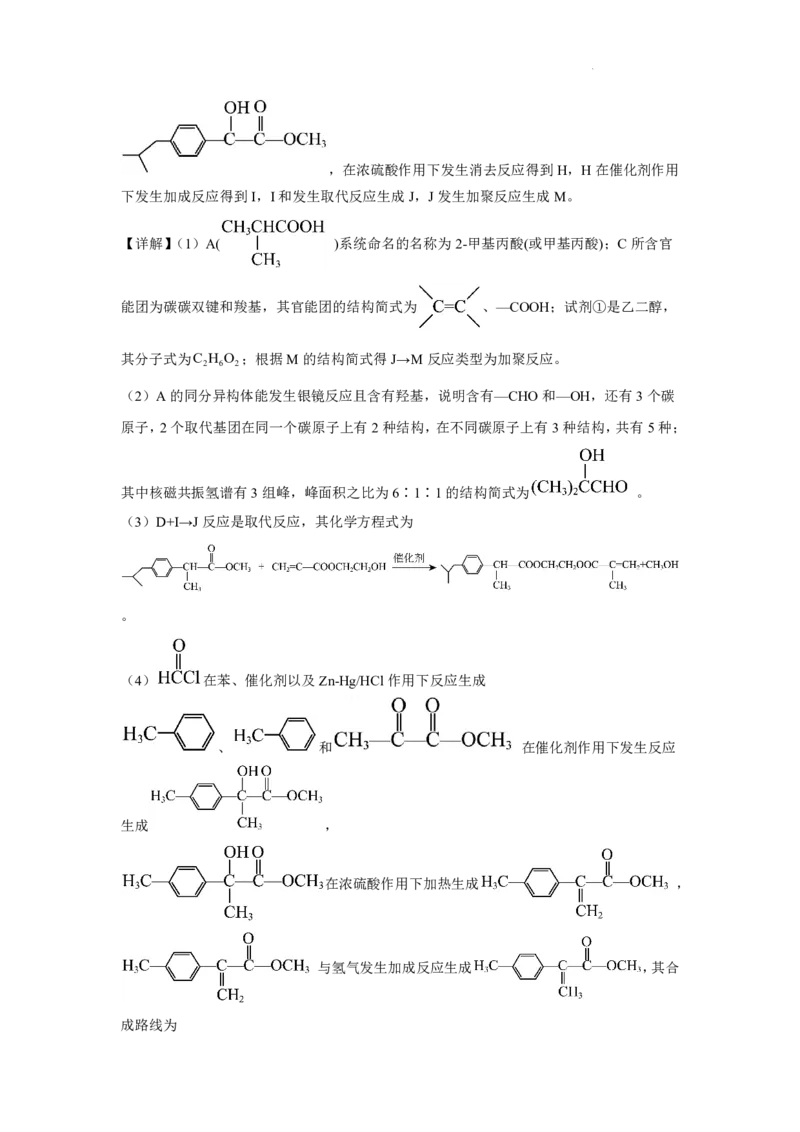
【分析】根据B的结构和A到B是取代反应得出A的结构简式为 ,根据
后面信息得到B发生消去反应,酸化得到C,A到E发生取代反应生成E,E先后和苯/催
化剂、Zn-Hg/HCl发生反应生成F,F和丙酮酸甲酯发生加成反应生成
学科网(北京)股份有限公司,在浓硫酸作用下发生消去反应得到H,H在催化剂作用
下发生加成反应得到I,I和发生取代反应生成J,J发生加聚反应生成M。
【详解】(1)A( )系统命名的名称为2-甲基丙酸(或甲基丙酸);C所含官
能团为碳碳双键和羧基,其官能团的结构简式为 、—COOH;试剂①是乙二醇,
其分子式为C H O ;根据M的结构简式得J→M反应类型为加聚反应。
2 6 2
(2)A的同分异构体能发生银镜反应且含有羟基,说明含有—CHO和—OH,还有3个碳
原子,2个取代基团在同一个碳原子上有2种结构,在不同碳原子上有3种结构,共有5种;
其中核磁共振氢谱有3组峰,峰面积之比为6∶1∶1的结构简式为 。
(3)D+I→J反应是取代反应,其化学方程式为
。
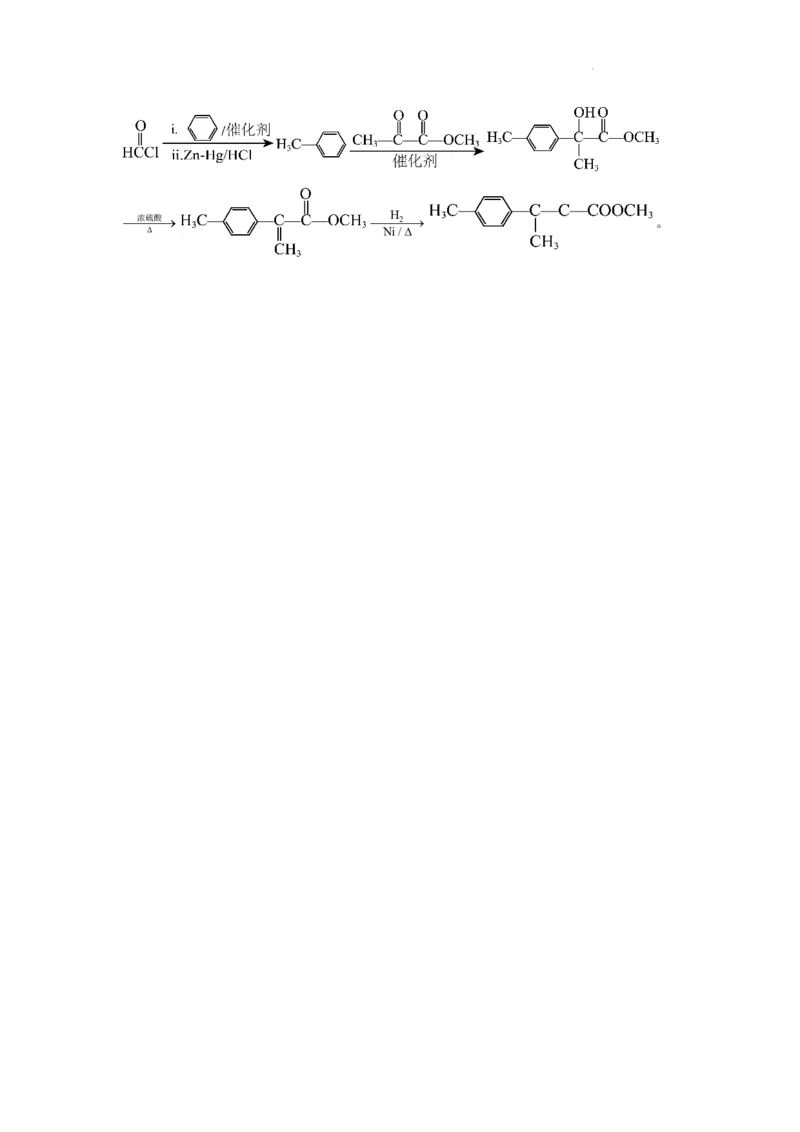
(4) 在苯、催化剂以及Zn-Hg/HCl作用下反应生成
、 和 在催化剂作用下发生反应
生成 ,
在浓硫酸作用下加热生成 ,
与氢气发生加成反应生成 ,其合
成路线为
学科网(北京)股份有限公司浓硫酸 H 2 。
Ni/
学科网(北京)股份有限公司学科网(北京)股份有限公司