文档内容
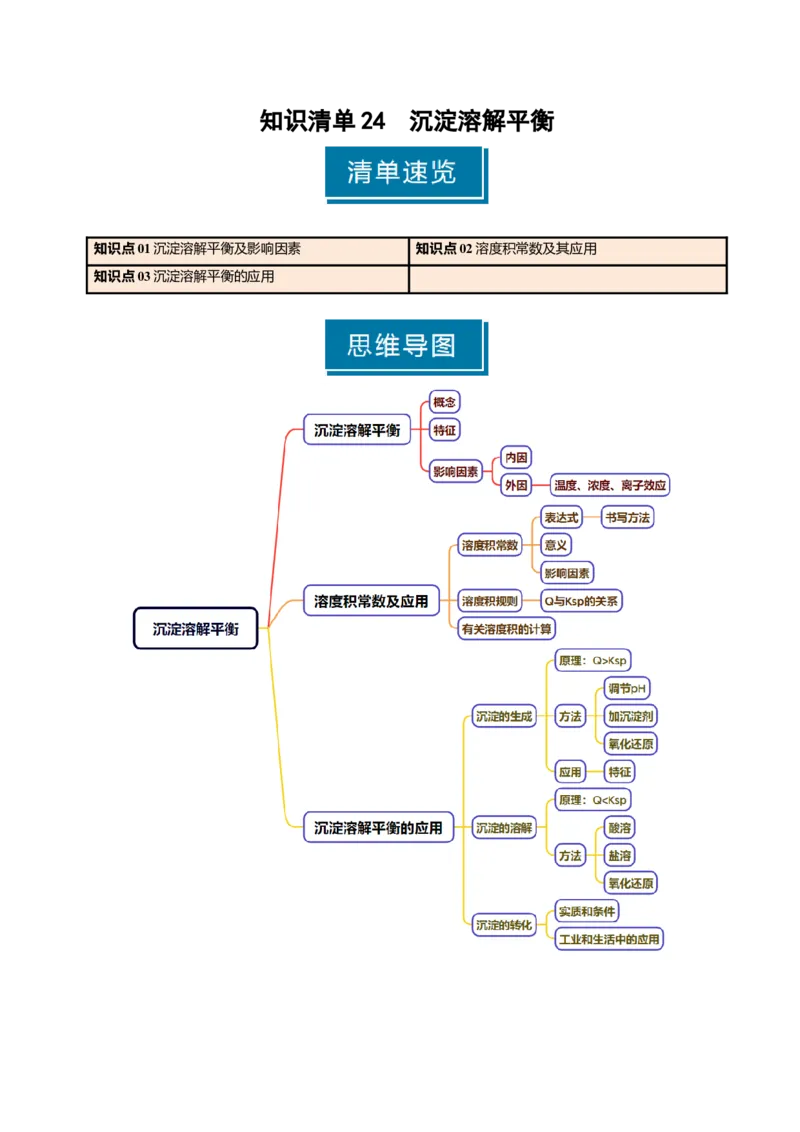
知识清单 24 沉淀溶解平衡
知识点01沉淀溶解平衡及影响因素 知识点02溶度积常数及其应用
知识点03沉淀溶解平衡的应用知识点 01 沉淀溶解平衡及影响因素
1.25 ℃时,溶解性与溶解度的关系
溶解性 易溶 可溶 微溶 难溶
溶解度 >10 g 1~10 g 0.01~1 g <0.01 g
2.难溶电解质的沉淀溶解平衡
(1)沉淀溶解平衡的概念
在一定温度下,当沉淀和溶解的速率相等时,形成电解质的饱和溶液,达到平衡状态,人们把这种
平衡称为沉淀溶解平衡。
(2)沉淀溶解平衡的特征
①动态平衡:v =v ≠0。
溶解 沉淀
②达到平衡时,溶液中离子的浓度保持不变。
③当改变外界条件时,溶解平衡将发生移动,达到新的平衡。
3.难溶电解质沉淀溶解平衡的影响因素
(1)内因(决定因素):难溶电解质本身的性质。
(2)外因:温度、浓度等条件的影响符合勒夏特列原理。
①温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解的方向移动。
②浓度:加水稀释,平衡向溶解的方向移动。
③离子效应:向平衡体系中加入难溶物相应的离子,平衡逆向移动。
④其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡
向溶解的方向移动。
(3)实例分析:
已知沉淀溶解平衡:Mg(OH) (s) Mg2+(aq)+2OH-(aq),请分析当改变下列条件时,对该沉淀溶
2
解平衡的影响,填写下表(浓度变化均指平衡后和原平衡比较):
条件改变 移动方向 c(Mg2+) c(OH-)
加少量水 正向移动 不变 不变
升温 正向移动 增大 增大
加MgCl (s) 逆向移动 增大 减小
2
加盐酸 正向移动 增大 减小
加NaOH(s) 逆向移动 减小 增大
(1)升高温度,沉淀溶解平衡一定正向移动。( × )
(2)NaCl溶解性很好,饱和NaCl溶液中不存在溶解平衡。( × )错因 易溶电解质作溶质时只要是饱和溶液也可存在溶解平衡。
(3)沉淀达到溶解平衡时,溶液中难溶电解质电离出的各个离子浓度均相等。( × )
错因 溶解平衡时,溶液中各离子浓度不再改变,不一定相等。
(4)室温下,AgCl在水中的溶解度小于在食盐水中的溶解度。( × )
错因 食盐水中c(Cl-)大,抑制AgCl的溶解,故AgCl在水中的溶解度大于在食盐水中的溶解度。
(5)沉淀溶解是吸热过程,降低温度,溶解平衡一定逆向移动。( × )
错因 少数沉淀(如氢氧化钙)溶解放热,升温逆向移动。
(6)Mg(OH) 在NaOH溶液中的溶解度与在水中一样。( × )
2
错因 OH-抑制Mg(OH) 的溶解,在NaOH溶液中溶解度小。
2
(7)BaSO===Ba2++SO和BaSO(s)Ba2+(aq)+SO(aq),两式所表示的意义相同。( × )
4 4
错因 前者为BaSO 的电离方程式,后者为BaSO 沉淀溶解平衡的离子方程式。
4 4
(8)难溶电解质达到沉淀溶解平衡时,保持温度不变,增加难溶电解质的量,平衡向溶解方向移动。( × )
错因 难溶电解质是固体,其浓度可视为常数,增加它的量对平衡无影响。
(1)利用生成沉淀的方法能否全部除去要沉淀的离子?
提示 不可能将要除去的离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于 1×10-5 mol·L
-1时,沉淀已经完全。
(2)试用平衡移动原理解释下列事实:
分别用等体积的蒸馏水和0.01 mol·L-1的盐酸洗涤AgCl沉淀,为什么用水洗涤造成的AgCl的损失
大于用稀盐酸洗涤的损失量?
提示 用水洗涤AgCl,AgCl(s)Ag+(aq)+Cl-(aq)平衡右移,AgCl的质量减少;而用盐酸洗涤AgCl
时,HCl电离产生的Cl-会使AgCl的溶解平衡向左移动,可以减少AgCl的溶解,因而损失较少。
知识点 02 溶度积常数及其应用
1.概念
在一定温度下,难溶电解质达到沉淀溶解平衡后的溶液为饱和溶液,其离子浓度不再发生变化,溶
液中各离子浓度幂之积为常数,叫做溶度积常数(简称溶度积),用K 表示。
sp
2.表达式
A B (s) mAn+(aq)+nBm-(aq) K =cm(An+)·cn(Bm-)。
m n sp
如Fe(OH) 的K =c(Fe3+)·c3(OH-)。
3 sp
3.意义
K 的大小反映难溶电解质在水中的溶解能力。
sp
(1)相同类型的难溶电解质,溶度积小的电解质,其溶解能力小。
(2)不同类型的难溶电解质,溶度积小的电解质,其溶解能力不一定比溶度积大的溶解能力小。4.影响因素
溶度积K 值的大小只与难溶电解质本身的性质和温度有关,与浓度无关。
sp
5.应用——溶度积规则
通过比较溶度积与溶液的离子积Q,如对于Ag S溶液来说,任意时刻的Q=c2(Ag+)·c(S2-)]的相对
2
大小,可以判断难溶电解质在给定条件下沉淀能否生成或溶解:
(1)Q>K ,溶液过饱和,有沉淀析出,直至溶液饱和,达到新的平衡。
sp
(2)Q=K ,溶液饱和,沉淀与溶解处于平衡状态。
sp
(3)Q1.8×10-10,故生成AgCl沉淀。
c
(4)K 既与难溶电解质的性质和温度有关,也与沉淀的量和溶液中离子浓度有关。( × )
sp
错因 K 只与难溶电解质的性质和温度有关,与沉淀的量和溶液中离子浓度无关。
sp
(5)常温下,向Mg(OH) 饱和溶液中加入NaOH固体,Mg(OH) 的K 不变。( √ )
2 2 sp
(6)25 ℃时,K (Ag CrO)K ,所以有AgCl沉淀生成。
sp
2.常温下,K =c(Cu2+)·c2(OH-)=2×10-20,计算有关Cu2+沉淀的pH。
sp
(1)某CuSO 溶液中c(Cu2+)=0.02 mol·L-1,如果生成Cu(OH) 沉淀,应调整溶液的pH,使之大于
4 2
__________。
(2)要使0.2 mol·L-1 CuSO 溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液
4
中加入NaOH溶液,使溶液的pH为________。
答案 (1)5 (2)6
解析 (1)根据题给信息,当c(Cu2+)·c2(OH-)=2×10-20时开始出现沉淀,则c(OH-)= mol·L-1=10-9
mol·L-1,c(H+)=10-5 mol·L-1,pH=5,所以要生成Cu(OH) 沉淀,应调整pH>5。
2
(2)要使Cu2+浓度降至=2×10-4 mol·L-1,c(OH-)= mol·L-1=10-8 mol·L-1,c(H+)=10-6 mol·L-1,此
时溶液的pH=6。
3.已知K (AgCl)=1.56×10-10,K (AgBr)=7.7×10-13,K (Ag CrO)=9.0× 10-12。某溶液中含有
sp sp sp 2 4
Cl-、Br-和CrO,浓度均为0.01 mol·L-1,向该溶液中逐滴加入0.01 mol·L-1的AgNO 溶液时,计算三
3
种阴离子沉淀的先后顺序。
答案 三种阴离子浓度均为0.01 mol·L-1时,分别产生AgCl、AgBr和Ag CrO 沉淀,所需要Ag+浓度依
2 4
次为c(Ag+)== mol·L-1=1.56×10-8 mol·L-1,c(Ag+)== mol·L-1=7.7×10-11 mol·L-1,c(Ag+)==
1 2 3
mol·L-1=3×10-5 mol·L-1,沉淀时Ag+浓度最小的优先沉淀,因而沉淀的顺序为Br-、Cl-、CrO。
4.K (CaCO)=2.8×10-9、K (CaSO)=9.1×10-6,溶解能力:CaSO 大于CaCO 。请用数据说明溶
sp 3 sp 4 4 3
解能力小的CaCO 能否转化为溶解能力大的CaSO?
3 4
答案 在CaCO 的饱和溶液中c(Ca2+)== mol·L-1≈5.3×10-5 mol·L-1,若向CaCO 饱和溶液中加入
3 3
NaSO 溶液,产生CaSO(s)时SO的最小浓度为c(SO)==≈0.17 mol·L-1,则当溶液中c(SO)大于0.17
2 4 4
mol·L-1时,CaCO (s)可以转化为CaSO(s)。
3 4
5.某温度下,溶液中含有I-、Cl-等离子,向其中滴加AgNO 溶液,当AgCl开始沉淀时,溶液中
3
=____________。[已知:K (AgCl)=1.6×10-10,K (AgI)=8×10-17]
sp sp
答案 5×10-7
解析 同一溶液中c(Ag+)相等,====5×10-7。
知识点 03 沉淀溶解平衡的应用
1.沉淀的生成(1)沉淀生成的原理
根据沉淀溶解平衡原理,如果加入与溶液中相同的离子,使平衡向沉淀方向移动,就可以生成沉淀。
(2)沉淀的方法
①调节pH法:
如工业原料氯化铵中含杂质氯化铁,使其溶解于水,再加入氨水调节 pH,使 Q[Fe(OH) ]>
3
K [Fe(OH) ]可使Fe3+转变为Fe(OH) 沉淀而除去。反应如下:Fe3++3NH ·H O===Fe(OH) ↓+3NH。
sp 3 3 3 2 3
②加沉淀剂法:
如以NaS、HS等作沉淀剂,使某些金属离子,如Cu2+、Hg2+等生成极难溶的硫化物CuS、HgS等
2 2
沉淀,即离子积Q>K 时,生成沉淀,也是分离、除去杂质常用的方法。
sp
a.通入HS除去Cu2+的离子方程式:HS+Cu2+===CuS↓+2H+。
2 2
b.加入NaS除去Hg2+的离子方程式:Hg2++S2-===HgS↓。
2
③同离子效应法:
增大沉淀溶解平衡体系中某种离子的浓度,使平衡向生成沉淀的方向移动,如向AgCl的饱和溶液
中加入饱和食盐水可继续生成AgCl沉淀。
④氧化还原法:
改变离子的存在形式,促使其转化为溶解度更小的难溶电解质,便于分离出来,例如通过氧化还原
反应将Fe2+氧化为Fe3+,从而生成更难溶的Fe(OH) 沉淀。
3
(3)沉淀生成的应用
在无机物的制备和提纯、废水处理等领域,常利用生成沉淀来达到分离或除去某些离子的目的。
2.沉淀的溶解
(1)沉淀溶解的原理
根据平衡移动原理,对于在水中难溶的电解质,如果能设法不断地移去平衡体系中的相应离子,
Q24c(SO 2-),在BaSO 饱和溶液中,c(SO 2-)≈1.0×10-
4 3 3 4 4 4
5mol·L-1,故当c(CO2-)>2.4×10-4 mol·L-1时,BaSO 转化为BaCO 。
3 4 3
2.将足量的ZnS粉末加入到10 mL 0.001 mol·L-1的CuSO 溶液中,是否有CuS沉淀生成?请通过计
4
算后回答。
已知:K (ZnS)=1.6×10-24,K (CuS)=6.3×10-36。
sp sp
提示:在ZnS沉淀溶解平衡体系中产生的硫离子浓度为c(S2-)==≈1.26×10-12
Q(CuS)=c(Cu2+)·c(S2-)=1.0×10-3×1.26×10-12=1.26×10-15
因为Q(CuS)>K (CuS),所以ZnS沉淀会转化为CuS沉淀。
sp
3.已知:25 ℃时,K (BaSO)=1.1×10-10,K (BaCO)=2.6×10-9。
sp 4 sp 3
(1)医学上进行消化系统的X射线透视时,常使用BaSO 作内服造影剂。胃酸酸性很强(pH约为1),
4
但服用大量BaSO 仍然是安全的,BaSO 不溶于酸的原因是(用溶解平衡原理解释)__________________
4 4
______________________________________________________________________。
万一误服了少量BaCO ,应尽快用大量0.5 mol·L-1 Na SO 溶液洗胃,如果忽略洗胃过程中NaSO
3 2 4 2 4
溶液浓度的变化,残留在胃液中的Ba2+浓度仅为________ mol·L-1。
(2)长期使用的锅炉需要定期除水垢,否则会降低燃料的利用率。水垢中含有 CaSO,可先用NaCO
4 2 3
溶液处理,使之转化为疏松、易溶于酸的CaCO ,而后用酸除去。
3
①CaSO 转化为CaCO 的离子方程式为____________________________________________。
4 3
②请分析CaSO 转化为CaCO 的原理:____________________________________________。
4 3
(3)牙齿表面由一层硬的组成为Ca (PO )OH的难溶物质保护着,它在唾液中存在下列平衡:
5 4 3
Ca (PO )OH(s)5Ca2+(aq)+3PO(aq)+OH-(aq)
5 4 3
进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是:
________________________________________________________________________。
已知Ca (PO )F的溶解度比Ca (PO )OH的溶解度小,请用离子方程式表示使用含氟牙膏防止龋齿
5 4 3 5 4 3
的原因:__________________________________________________________。
答案:(1)对沉淀溶解于平衡BaSO(s)Ba2+(aq)+SO(aq),H+不能减少Ba2+或SO的浓度,平衡不能向
4
沉淀溶解的方向移动 2.2×10-10
(2)①CaSO(s)+CO(aq)CaCO (s)+SO(aq)
4 3
②CaSO 存在沉淀溶解平衡,加入NaCO 溶液后,CO与Ca2+结合生成CaCO 沉淀,Ca2+浓度减小,使
4 2 3 3
CaSO 的沉淀溶解平衡向溶解的方向移动
4
(3)发酵生成的有机酸能中和 OH-,使平衡向右移动,加速牙齿腐蚀 Ca (PO )OH(s)+F-
5 4 3
(aq)Ca (PO )F(s)+OH-(aq)
5 4 3
4.(1)在粗制CuSO ·5H O晶体中常含有杂质Fe2+。
4 2
①在提纯时为了除去Fe2+,常加入合适的氧化剂,使Fe2+转化为Fe3+,下列物质可采用的是______。
A.KMnO B.HO C.氯水 D.HNO
4 2 2 3
②然后再加入适当物质调整溶液 pH至4,使Fe3+转化为Fe(OH) ,调整溶液pH可选用下列中的
3
______。A.NaOH B.NH ·H O C.CuO D.Cu(OH)
3 2 2
(2)甲同学怀疑调整溶液pH至4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计
算确定,他查阅有关资料得到如下数据,常温下Fe(OH) 的溶度积K =1.0×10-38,Cu(OH) 的溶度积K
3 sp 2 sp
=3.0×10-20,通常认为残留在溶液中的离子浓度小于 1.0×10-5 mol·L-1时就认定沉淀完全,设溶液中
CuSO 的浓度为 3.0 mol·L-1,则 Cu(OH) 开始沉淀时溶液的 pH 为______,Fe3+完全沉淀[即 c(Fe3
4 2
+)≤1.0×10-5 mol·L-1]时溶液的pH为______,通过计算确定上述方案_____________(填“可行”或“不
可行”)。
答案:(1)①B ②CD (2)4 3 可行
解析:K [Cu(OH) ]=c(Cu2+)·c2(OH-),则c(OH-)= =1.0×10-10 mol·L-1,则c(H+)=1.0×10-4 mol·L-
sp 2
1,pH=4。
Fe3+完全沉淀时:K [Fe(OH) ]=c(Fe3+)·c3(OH-),则c(OH-)= =1.0×10-11 mol·L-1。此时c(H+)=
sp 3
1×10-3 mol·L-1,pH=3,因此上述方案可行。