文档内容
第 06 讲 氧化还原反应
目录
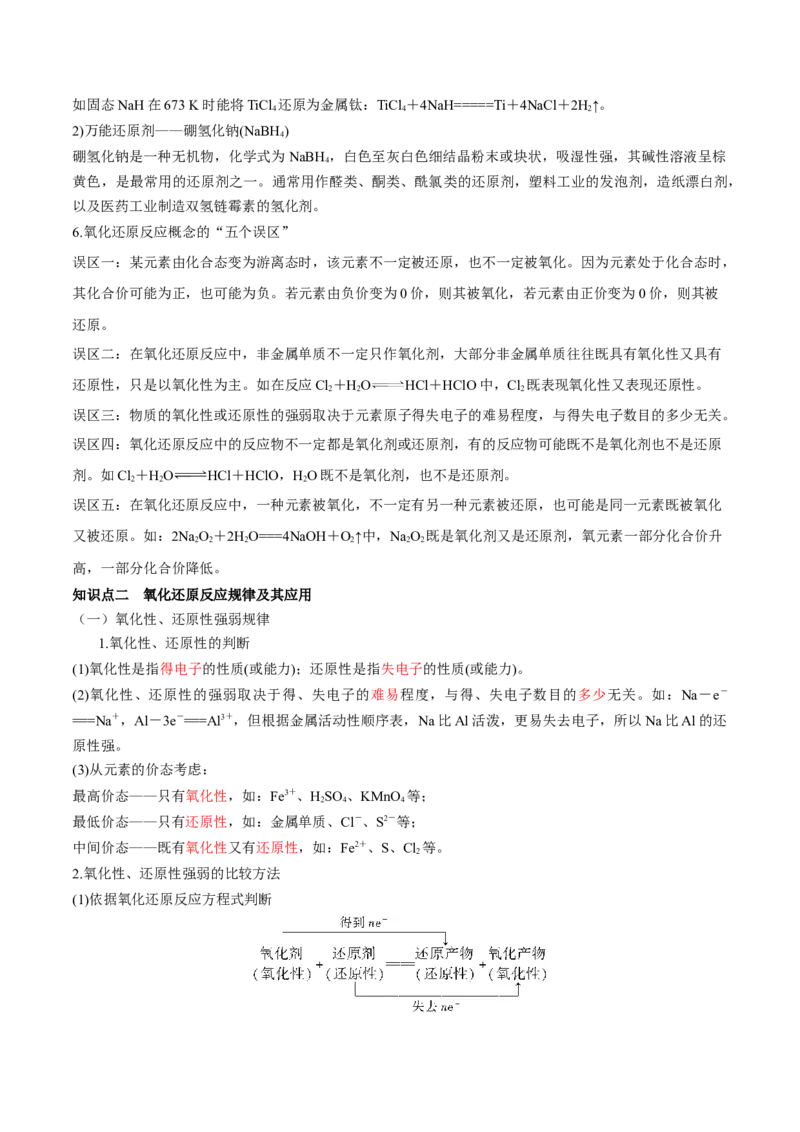
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查氧化还原反应的判断
高频考点2 考查氧化还原反应中相关概念的判断
高频考点3 考查氧化性、还原性强弱的判断
高频考点4 考查氧化还原规律及其应用
高频考点5 考查陌生氧化还原反应方程式的书写和配平
高频考点6 考查氧化还原反应的相关计算
正文第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 氧化还原反应的相关概念及其表示方法
1.氧化还原反应的本质和特征
2.基于双线桥理解氧化还原反应概念之间的关系
【名师总结】分析电子转移数目的关键——标出元素化合价
(1)基本方法:先标出熟悉元素的化合价,再根据化合物中正负化合价的代数和为零的原则求解其他元素的
化合价。
(2)熟记常见元素的化合价:一价氢、钾、钠、氟、氯、溴、碘、银;二价氧、钙、钡、镁、锌;三铝、四
硅、五价磷;说变价也不难,二三铁、二四碳、二四六硫都齐全;铜汞二价最常见。
(3)明确一些特殊物质中元素的化合价:
CuFeS :Cu、Fe、S;KFeO :Fe;LiNH、LiNH 、AlN:N;NaSO :S;MO:M;C O:C;
2 2 4 2 2 2 2 3 2
HCN:C、N;CuH:Cu、H;FeO:Fe;Si N:Si、N。
3 4
可概括为“氧、氧、得、降、还、还、还”。3.电子转移的表示方法
请分别用单线桥法和双线桥法表示Cu与稀硝酸反应中电子转移的方向和数目:
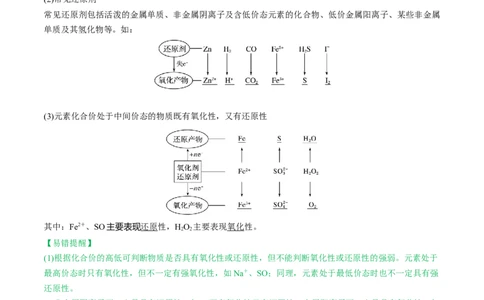
(1)双线桥法:①标变价 ②画箭头(反应物指向生成物) ③算数目 ④说变化。
【特别提醒】a.箭头从失电子元素的原子指向得电子元素的原子。
b.不标“得到”或“失去”,只标明电子转移的总数。
c.线桥只出现在反应物中。
(2)单线桥法:①标变价 ②画箭头(由失电子原子指向得电子原子) ③算数目(线桥上只标电子转移的
总数目,不标“得”“失”字样)
【特别提醒】a.箭头指向反应前后有元素化合价变化的同种元素的原子,且需注明“得到”或“失去”。
b.箭头的方向不代表电子转移的方向,仅表示电子转移前后的变化。
c.失去电子的总数等于得到电子的总数。
4.氧化还原反应与四种基本类型反应间的关系
【特别提醒】(1)有单质参与的化合反应是氧化还原反应。
(2)有单质生成的分解反应是氧化还原反应。
(3)有单质参加或生成的化学反应,不一定是氧化还原反应,如3O=====2O。
2 3
(4)所有的置换反应都是氧化还原反应。
(5)所有的复分解反应都不是氧化还原反应。
5.常见的氧化剂和还原剂
(1)常见氧化剂
常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:【特别提醒】
(1)O、O 在水溶液中的还原产物,其中酸性条件下是HO,中性、碱性条件下是OH-;而当还原产物
2 3 2
为固态时是O2-或O。
(2)浓硝酸的还原产物是NO ,稀HNO 的还原产物是NO。
2 3
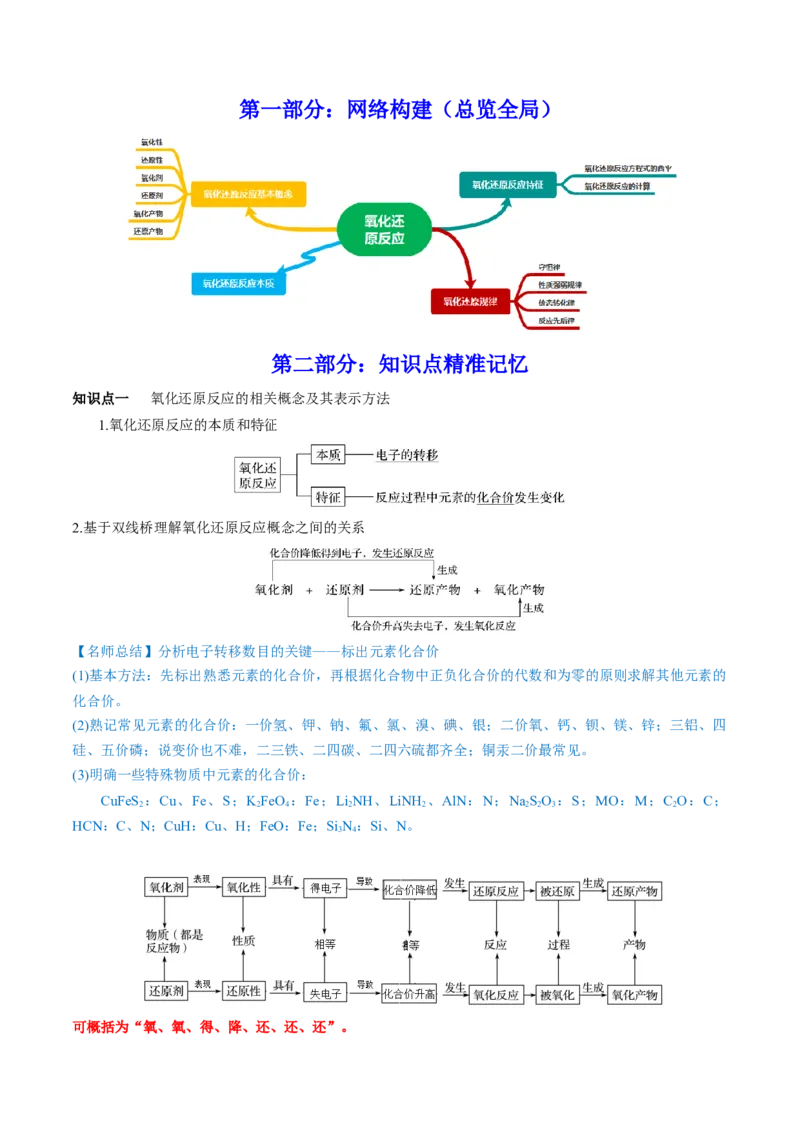
(2)常见还原剂
常见还原剂包括活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离子、某些非金属
单质及其氢化物等。如:
(3)元素化合价处于中间价态的物质既有氧化性,又有还原性
其中:Fe2+、SO主要表现还原性,HO 主要表现氧化性。
2 2
【易错提醒】
(1)根据化合价的高低可判断物质是否具有氧化性或还原性,但不能判断氧化性或还原性的强弱。元素处于
最高价态时只有氧化性,但不一定有强氧化性,如Na+、SO;同理,元素处于最低价态时也不一定具有强
还原性。
(2)非金属阴离子不一定只具有还原性,如O既有氧化性又有还原性。金属阳离子不一定只具有氧化性,如
Fe2+既有还原性又有氧化性。
(4)重要的还原剂——金属氢化物、NaBH
4
1)金属氢化物
①结构特点
电子式可表示为M+[H]-(M为碱金属)。
②强还原性
a.遇水强烈反应放出氢气,使溶液呈强碱性,如:NaH+HO===NaOH+H↑。
2 2
b.高温还原金属如固态NaH在673 K时能将TiCl 还原为金属钛:TiCl +4NaH=====Ti+4NaCl+2H↑。
4 4 2
2)万能还原剂——硼氢化钠(NaBH )
4
硼氢化钠是一种无机物,化学式为NaBH ,白色至灰白色细结晶粉末或块状,吸湿性强,其碱性溶液呈棕
4
黄色,是最常用的还原剂之一。通常用作醛类、酮类、酰氯类的还原剂,塑料工业的发泡剂,造纸漂白剂,
以及医药工业制造双氢链霉素的氢化剂。
6.氧化还原反应概念的“五个误区”
误区一:某元素由化合态变为游离态时,该元素不一定被还原,也不一定被氧化。因为元素处于化合态时,
其化合价可能为正,也可能为负。若元素由负价变为0价,则其被氧化,若元素由正价变为0价,则其被
还原。
误区二:在氧化还原反应中,非金属单质不一定只作氧化剂,大部分非金属单质往往既具有氧化性又具有
还原性,只是以氧化性为主。如在反应Cl+HO HCl+HClO中,Cl 既表现氧化性又表现还原性。
2 2 2
误区三:物质的氧化性或还原性的强弱取决于元素原子得失电子的难易程度,与得失电子数目的多少无关。
误区四:氧化还原反应中的反应物不一定都是氧化剂或还原剂,有的反应物可能既不是氧化剂也不是还原
剂。如Cl+HO HCl+HClO,HO既不是氧化剂,也不是还原剂。
2 2 2
误区五:在氧化还原反应中,一种元素被氧化,不一定有另一种元素被还原,也可能是同一元素既被氧化
又被还原。如:2NaO+2HO===4NaOH+O↑中,NaO 既是氧化剂又是还原剂,氧元素一部分化合价升
2 2 2 2 2 2
高,一部分化合价降低。
知识点二 氧化还原反应规律及其应用
(一)氧化性、还原性强弱规律
1.氧化性、还原性的判断
(1)氧化性是指得电子的性质(或能力);还原性是指失电子的性质(或能力)。
(2)氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的多少无关。如:Na-e-
===Na+,Al-3e-===Al3+,但根据金属活动性顺序表,Na比Al活泼,更易失去电子,所以Na比Al的还
原性强。
(3)从元素的价态考虑:
最高价态——只有氧化性,如:Fe3+、HSO 、KMnO 等;
2 4 4
最低价态——只有还原性,如:金属单质、Cl-、S2-等;
中间价态——既有氧化性又有还原性,如:Fe2+、S、Cl 等。
2
2.氧化性、还原性强弱的比较方法
(1)依据氧化还原反应方程式判断氧化性:氧化剂>氧化产物
还原性:还原剂>还原产物
口诀:比什么“性”找什么“剂”,“产物”之“性”小于“剂”。
(2)依据反应条件及反应的剧烈程度判断
当不同的氧化剂(或还原剂)与同一还原剂(或氧化剂)反应时,反应越易进行,则对应的氧化剂(或还原
剂)的氧化性(或还原性)越强,反之越弱。如:
MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO
4 2 2 2
O+4HCl(浓)=====2Cl+2HO
2 2 2
氧化性:KMnO >MnO>O
4 2 2
2Na+2HO===2NaOH+H↑ Mg+2HO Mg(OH) +H↑
2 2 2 2 2
还原性:Na>Mg
(3)依据被氧化还原的程度判断
相同条件下:
a.不同氧化剂作用于同一种还原剂,氧化产物价态高的其氧化性强。
例如:Fe+S FeS,2Fe+3Cl 2FeCl ,可以得出氧化性:Cl>S
2 3 2
b.不同还原剂作用于同一种氧化剂,还原产物价态低的其还原性强。例如:
→
(4)依据“三表”判断
a.根据元素周期表判断
b.根据金属活动顺序表
c.根据非金属活动性顺序表判断
――→
――→
(5)依据“两池”判断
a.原电池:一般情况下,两种不同的金属构成原电池的两极,其还原性:负极>正极。b.电解池:用惰性电极电解混合溶液时,在阴极先放电的阳离子的氧化性较强,在阳极先放电的阴离子的
还原性较强。
(6)依据“三度”判断(“三度”即:浓度、温度、酸碱度)
a.浓度:同一种物质浓度越大,氧化性(或还原性)越强。如氧化性:浓 HSO >稀HSO ,浓HNO>稀
2 4 2 4 3
HNO;还原性:浓盐酸>稀盐酸。
3
b.温度:同一种物质,温度越高其氧化性(或还原性)越强。如热的浓硫酸的氧化性比冷的浓硫酸的氧化性强。
c.酸碱度:同一种物质,所处环境酸(碱)性越强其氧化性(或还原性)越强。如KMnO 溶液的氧化性随溶液酸
4
性的增强而增强。
(二)价态归中、歧化规律及其应用
1.价态归中规律思维模型
含不同价态的同种元素的物质间发生氧化还原反应时,该元素价态的变化一定遵循“高价+低价―→中间
价”,而不会出现交叉现象。简记为“两相靠,不相交”。
例如,不同价态硫之间可以发生的氧化还原反应是
注:不会出现⑤中HS转化为SO 而HSO 转化为S的情况。
2 2 2 4
2.歧化反应规律思维模型
“中间价―→高价+低价”。
具有多种价态的元素(如氯、硫、氮和磷元素等)均可发生歧化反应,如:Cl +2NaOH===NaCl+NaClO+
2
HO。
2
3.应用
(1)判断同种元素不同价态物质间发生氧化还原反应的可能性,如浓HSO 与SO 不发生反应。
2 4 2
(2)根据化合价判断反应体系中的氧化剂、还原剂及氧化产物、还原产物。如对于反应 6HCl+
NaClO===NaCl+3Cl↑+3HO中,氧化剂为NaClO,还原剂为HCl,氧化产物和还原产物都为Cl。
3 2 2 3 2
(三)先后规律及其应用
1、规律
①同时含有几种还原剂时――→将按照还原性由强到弱的顺序依次反应。如:在FeBr 溶液中通入少量Cl
2 2
时,因为还原性Fe2+>Br-,所以Fe2+先与Cl 反应。
2
②同时含有几种氧化剂时――→将按照氧化性由强到弱的顺序依次反应。如:在含有Fe3+、Cu2+、H+的溶
液中加入铁粉,因为氧化性Fe3+>Cu2+>H+,所以铁粉先与Fe3+反应,然后依次为Cu2+、H+。
2、应用
3、常见的强弱顺序氧化性:MnO(H+)>Cl >Br >Fe3+>I >稀HSO >S,还原性:Mn2+