文档内容
第11讲 硫及其化合物
1.下列气体不能用浓硫酸干燥的是
A. B.CO C. D.
2
2.下列“实验结论”与“实验操作及现象”相符的一组是
选项 实验操作及现象 实验结论
A 向某溶液中加入 溶液,产生白色沉淀 该溶液中一定含有
B 向某溶液中加入KSCN溶液,溶液变为红色 该溶液中一定含有
C 向某溶液中加入 溶液,有白色沉淀生成 该溶液中一定含有
D 向某溶液中加入稀盐酸,有无色气体产生 该溶液中一定含有
3.下列事实表明浓硫酸具有脱水性的是
A.空气中敞口久置的浓硫酸质量增大
B.浓硫酸在加热的条件下与铜反应
C.用浓硫酸在纸上书写的字迹变黑
D.浓硫酸可用来干燥某些气体
4.关于硫及其化合物的下列说法正确的是
A.可用 洗涤试管内壁的S
B. 溶液与 溶液混合会产生黄色沉淀
C.浓 使胆矾变为白色,说明浓硫酸具有脱水性
D.含2mol 的浓硫酸与足量Zn反应,产生标准状况下的气体22.4L
5.下列关于SO 的叙述正确的是
2
A.SO 是无色、无臭、无毒的气体 B.SO 与NaOH反应生成NaSO
2 2 2 4
C.SO 能使紫色的KMnO 溶液褪色 D.SO 具有漂白性,可用于漂白食品
2 4 2
6.对下列事实的解释错误的是
A.在蔗糖中加入浓硫酸后出现黑色物质,说明浓硫酸具有脱水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定C.将一块打磨过的铝片投入浓硝酸中,铝片未见溶解,铝与浓硝酸不反应
D.浓硫酸露置于空气中,溶液浓度降低,是由于浓硫酸具有吸水性
7.二氧化硫是中国允许使用的还原性漂白剂。对食品有漂白和对植物性食品内的氧化酶有强烈的抑制作
用。中国规定可用于葡萄酒和果酒,最大使用量0.25 g·kg-1,残留量不得超过0.05 g·kg-1。下列说法正确的
是
A.因为SO 具有漂白性,所以它能使品红溶液、酸性KMnO 溶液和石蕊溶液褪色
2 4
B.能使品红溶液褪色的不一定是SO
2
C.SO 、漂白粉、活性炭、NaO 都能使红墨水褪色,其原理相同
2 2 2
D.SO 和Cl 混合使用,将会有更强的漂白能力
2 2
8.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.lmol SO 与足量的O 反应,产生的SO 数目为 N
2 2 3 A
B.某浓硝酸中n(HNO)= 2mol,该浓硝酸与足量的铜完全反应可生成1molNO
3 2
C.lmolFe 与S完全反应,转移电子数为2N
A
D.标准状况下,11.2L 的SO 中含有的分子数为0.5N
3 A
9.工业常用接触法制备硫酸,其流程如图所示。下列叙述正确的是
A.燃烧黄铁矿时,若氧化剂与还原剂物质的量之比为 ,则固体产物为
B.制备 温度低于400℃时, 催化氧化反应速率较小
C.工业上,可以用98.3%的浓硫酸除去 中少量 杂质
D.其他条件相同时,采用低压空气比高压空气反应速率大
10.通常条件下,将气体X和气体 同时通入盛有 溶液的洗气瓶中(如图所示),若洗气瓶中有沉淀
生成,关于气体X的正确组合为① ② ③ ④ ⑤ ⑥
A.①②③④⑥ B.②③④⑤⑥ C.①③④⑤ D.②③⑤⑥
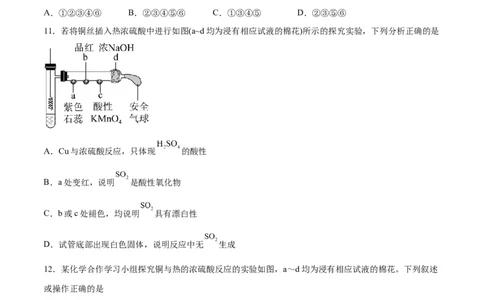
11.若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是
A.Cu与浓硫酸反应,只体现 的酸性
B.a处变红,说明 是酸性氧化物
C.b或c处褪色,均说明 具有漂白性
D.试管底部出现白色固体,说明反应中无 生成
12.某化学合作学习小组探究铜与热的浓硫酸反应的实验如图,a~d均为浸有相应试液的棉花。下列叙述
或操作正确的是
A.a处溶液先变红后褪色B.b、c处分别验证了SO 的漂白性、还原性,d处利用SO 的酸性
2 2
C.当试管Ⅰ中消耗0.64gCu时,则被还原的HSO 的质量为1.96g
2 4
D.将试管Ⅰ与试管Ⅱ分离后,向试管Ⅰ中加入适量蒸馏水,验证有Cu2+生成
13.下列实验中,所得现象和结论均对应且正确的是
选项 实验 现象 结论
A 向某溶液中滴加硝酸酸化的BaCl 溶液 有白色沉淀产生 该溶液中可能含SO
2
B 将少量氯气通入KI—淀粉溶液 溶液变蓝 还原性:I-<Cl-
C 向pH试纸上滴加一滴浓硫酸 pH试纸先变红后变黑 浓硫酸具有强氧化性
D 向溴水中通入足量SO 气体 溴水褪色 SO 具有氧化性
2 2
14.如图是一种综合处理SO 废气的工艺流程。下列说法正确的是
2
A.操作Ⅱ发生反应的离子方程式为4Fe2++4H++O=4Fe3++2HO
2 2
B.溶液b中阳离子只有Fe2+
C.溶液a转化为溶液b的反应中,SO 被还原
2
D.加入FeO可以使溶液c转化为溶液a
15.几种无机物之间的转化关系如图所示(反应条件省略,部分产物省略)。下列推断不正确的是
A.若L为强酸,则E可能为NH Cl、F为Ca(OH)
4 2
B.若L为强酸,则E可能为NaS、F为HSO
2 2 4
C.若L为弱酸,则E可能为Mg、F与K为CO
2
D.若L为强酸,则E可能为NaSO 溶液、F为浓HSO
2 3 2 4
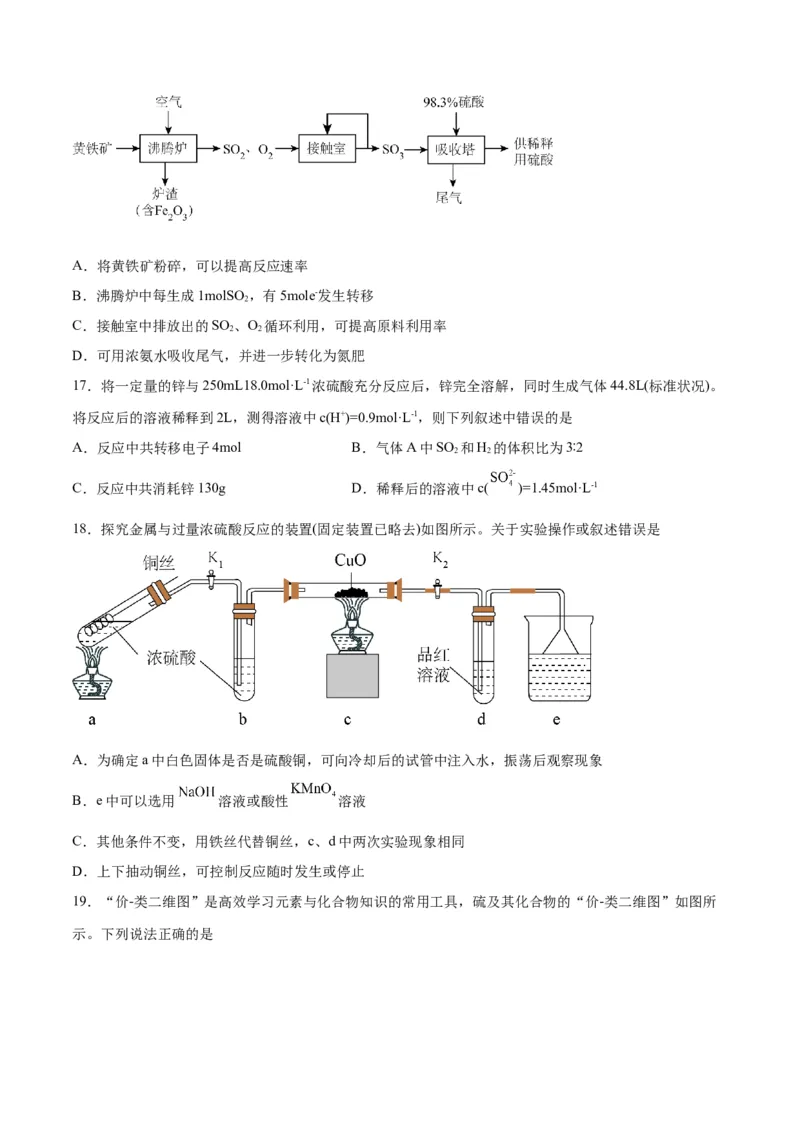
16.以黄铁矿(主要成分为FeS,其中硫的化合价为-1价)生产硫酸的工艺流程如下图,下列说法不正确的
2
是A.将黄铁矿粉碎,可以提高反应速率
B.沸腾炉中每生成1molSO ,有5mole-发生转移
2
C.接触室中排放出的SO 、O 循环利用,可提高原料利用率
2 2
D.可用浓氨水吸收尾气,并进一步转化为氮肥
17.将一定量的锌与250mL18.0mol·L-1浓硫酸充分反应后,锌完全溶解,同时生成气体44.8L(标准状况)。
将反应后的溶液稀释到2L,测得溶液中c(H+)=0.9mol·L-1,则下列叙述中错误的是
A.反应中共转移电子4mol B.气体A中SO 和H 的体积比为3∶2
2 2
C.反应中共消耗锌130g D.稀释后的溶液中c( )=1.45mol·L-1
18.探究金属与过量浓硫酸反应的装置(固定装置已略去)如图所示。关于实验操作或叙述错误是
A.为确定a中白色固体是否是硫酸铜,可向冷却后的试管中注入水,振荡后观察现象
B.e中可以选用 溶液或酸性 溶液
C.其他条件不变,用铁丝代替铜丝,c、d中两次实验现象相同
D.上下抽动铜丝,可控制反应随时发生或停止
19.“价-类二维图”是高效学习元素与化合物知识的常用工具,硫及其化合物的“价-类二维图”如图所
示。下列说法正确的是A.硫在过量的空气中燃烧直接生成Y
B.在实验中可用M检验
C.硫酸型酸雨的pH小于 是因为酸雨中含有X
D. 与M反应生成Z与N,说明Z的酸性比 弱
20.向100mLNaOH溶液中通入一定量的SO 气体,充分反应后,再向所得溶液中逐滴加入0.2mol•L-1的盐
2
酸,产生SO 的体积与所加盐酸体积之间关系如图所示。下列判断正确的是
2
A.通入SO 后,所得溶液的溶质成分的物质的量之比为n(NaHSO):n(Na SO )=1:1
2 3 2 3
B.通入SO 的体积为336mL
2
C.通入SO 后,所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na SO )=1:3
2 2 3
D.原NaOH溶液的浓度为0.2mol•L-1
21. 是中学化学常见的气体,可用于制造硫酸、杀菌、防腐等。某学习小组用铜粉与浓硫酸共热反应
制取 气体并探究 与镁粉反应的含硫产物。相关实验装置如图所示(部分加热装置及夹持装置已略
去)。回答下列问题:(1) 的制取
①仪器a的名称为 ;仪器a中发生反应的化学方程式为 。
②向仪器a中加入一定量的浓硫酸后,加热至250℃,产生大量气体,溶液显蓝色,仪器a底部有较多灰白
色沉淀,该灰白色沉淀可能是 。
③装置B的作用是 。
④有同学认为装置D有缺陷,请你写出改进措施: 。
(2)探究 与镁粉反应的含硫产物
操作步骤 实验现象 解释或结论
取反应后的固体于试管中,向反应后的固体中慢慢滴加 固体物质部分溶解,有大 未溶解的固体为硫
稀盐酸至过量,充分反应 量气体产生 单质
含硫产物中无
将产生的气体先通入盛有品红溶液的试管中 ①
②该反应的离子方
将产生的气体再通入盛有 溶液的试管中 有黑色沉淀生成
程式为
(3)根据上述实验现象及结论可知,除发生反应 外,还发生的反应有 。
22.在印染工业中,连二亚硫酸钠(Na SO)因能使染好的布褪色,而使布能重新染色,故而俗称保险粉,
2 2 4
其可溶于水,但不溶于甲醇。工业制备流程如下:请回答下列问题:
(1)流程①步骤中需在耐高温的坩埚中进行,常用来制做耐高温坩埚的金属氧化物化学式为 。
(2)由锌块制备锌粉的目的是 ;向锌液中鼓入M气体,使液态锌雾化,冷却得到粒度约为
180μm的锌粉,鼓入气体M为常见的化合物,则M的化学式为 ;分散系A为 (填“溶
液”“胶体”或“悬浊液”)。
(3)流程②步骤中的化学方程式为 。
(4)流程③的分离方法步骤为 、洗涤、干燥,洗涤所用试剂是 ;过滤前加入NaCl固体
的作用是 。
(5)将等体积0.04 mol·L-1AgNO 溶液和0.02 mol·L-1碱性NaSO 溶液混合,两者恰好完全反应,反应后溶液
3 2 2 4
中有纳米级的银粉生成,写出反应的离子方程式 。