文档内容
第 13 讲 硫及其化合物
第一部分:高考真题感悟
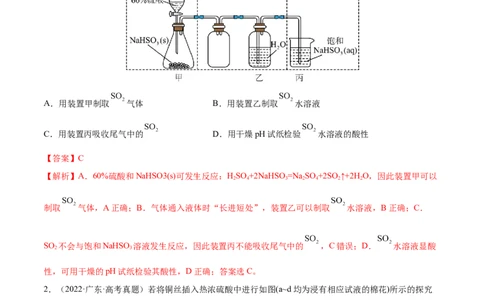
1.(2022·江苏·高考真题)实验室制取少量 水溶液并探究其酸性,下列实验装置和操作不能达到实验
目的的是
A.用装置甲制取 气体 B.用装置乙制取 水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验 水溶液的酸性
【答案】C
【解析】A.60%硫酸和NaHSO3(s)可发生反应:HSO +2NaHSO =Na SO +2SO↑+2H O,因此装置甲可以
2 4 3 2 4 2 2
制取 气体,A正确;B.气体通入液体时“长进短处”,装置乙可以制取 水溶液,B正确;C.
SO 不会与饱和NaHSO 溶液发生反应,因此装置丙不能吸收尾气中的 ,C错误;D. 水溶液显酸
2 3
性,可用干燥的pH试纸检验其酸性,D正确;答案选C。
2.(2022·广东·高考真题)若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究
实验,下列分析正确的是A. 与浓硫酸反应,只体现 的酸性
B.a处变红,说明 是酸性氧化物
C.b或c处褪色,均说明 具有漂白性
D.试管底部出现白色固体,说明反应中无 生成
【答案】B
【解析】A.铜和浓硫酸反应过程中,生成CuSO 体现出浓硫酸的酸性,生成SO 体现出浓硫酸的强氧化
4 2
性,故A错误;B.a处的紫色石蕊溶液变红,其原因是SO 溶于水生成了酸,可说明SO 是酸性氧化物,
2 2
故B正确;C.b处品红溶液褪色,其原因是SO 具有漂白性,而c处酸性高锰酸钾溶液褪色,其原因是
2
SO 和KMnO 发生氧化还原反应,SO 体现出还原性,故C错误;D.实验过程中试管底部出现白色固体,
2 4 2
根据元素守恒可知,其成分为无水CuSO ,而非蓝色的CuSO ·5H O,其原因是浓硫酸体现出吸水性,将反
4 4 2
应生成的HO吸收,故D错误;综上所述,正确的是B项。
2
3.(2017·海南,2)分别将足量下列气体通入稀NaS溶液中,可以使溶液变浑浊的是( )
2
A.CO B.SO C.HCl D.CO
2 2
【答案】B
【解析】A项,CO不与NaS发生反应,因此没有沉淀产生,错误;B项,SO 具有氧化性,与NaS发生
2 2 2
氧化还原反应,即SO +2S2-+4H+===3S↓+2HO,正确;C项,利用酸性强的制取酸性弱的,即发生2H
2 2
++S2-===H S,没有沉淀产生,错误;D项,不产生沉淀,错误。
2
4.(2021·山东,8)工业上以SO 和纯碱为原料制备无水NaHSO 的主要流程如图,下列说法错误的是( )
2 3
A.吸收过程中有气体生成
B.结晶后母液中含有NaHCO
3
C.气流干燥湿料时温度不宜过高
D.中和后溶液中含NaSO 和NaHCO
2 3 3
【答案】B
【解析】根据流程图分析可知,吸收过程中有二氧化碳生成,A正确;结晶后母液中含饱和NaHSO 和过
3
量的二氧化硫形成的亚硫酸,没有NaHCO ,假设产物中存在NaHCO ,则其会与生成的NaHSO 发生反应,
3 3 3且NaHCO 溶解度较低,若其残留于母液中,会使晶体不纯,假设不成立,B错误;NaHSO 高温时易分解
3 3
变质,所以气流干燥过程中温度不宜过高,C正确;结合上述分析可知,中和后溶液中含 NaSO 和
2 3
NaHCO ,D正确。
3
5.(2017·江苏,4)下列制取SO 、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是(
2
)
【答案】B
【解析】A项,稀HSO 与铜片不反应,错误;B项,SO 能使品红溶液褪色,体现其漂白性,正确;C项,
2 4 2
SO 密度比空气大,导管应“长进短出”,错误;D项,SO 不与饱和NaHSO 反应,无法吸收SO ,错误。
2 2 3 2
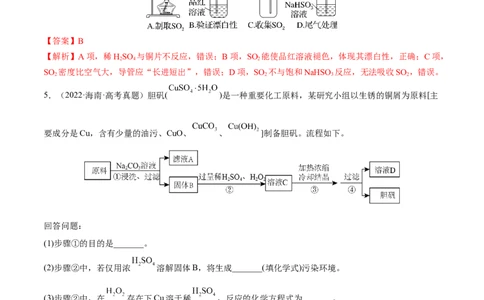
5.(2022·海南·高考真题)胆矾( )是一种重要化工原料,某研究小组以生锈的铜屑为原料[主
要成分是Cu,含有少量的油污、CuO、 、 ]制备胆矾。流程如下。
回答问题:
(1)步骤①的目的是_______。
(2)步骤②中,若仅用浓 溶解固体B,将生成_______(填化学式)污染环境。
(3)步骤②中,在 存在下Cu溶于稀 ,反应的化学方程式为_______。
(4)经步骤④得到的胆矾,不能用水洗涤的主要原因是_______。
(5)实验证明,滤液D能将 氧化为 。
ⅰ.甲同学认为不可能是步骤②中过量 将 氧化为 ,理由是_______。
ⅱ.乙同学通过实验证实,只能是 将 氧化为 ,写出乙同学的实验方案及结果_______(不要求写具体操作过程)。
【答案】(1)除油污
(2)
(3)
(4)胆矾晶体易溶于水
(5)溶液 C 经步骤③加热浓缩后双氧水已完全分解 取滤液,向其中加入适量硫化钠,使铜离子恰
好完全沉淀,再加入 ,不能被氧化
【解析】由流程中的信息可知,原料经碳酸钠溶液浸洗后过滤,可以除去原料表面的油污;滤渣固体B与
过量的稀硫酸、双氧水反应,其中的CuO、CuCO、Cu(OH) 均转化为CuSO ,溶液C为硫酸铜溶液和稀
3 2 4
硫酸的混合液,加热浓缩、冷却结晶、过滤后得到胆矾。
(1)原料表面含有少量的油污,NaCO 溶液呈碱性,可以除去原料表面的油污,因此,步骤①的目的是:除
2 3
去原料表面的油污。
(2)在加热的条件下,铜可以与浓硫酸发生反应生成CuSO 、SO 和HO,二氧化硫是一种大气污染物,步
4 2 2
骤②中,若仅用浓HSO 溶解固体B,将生成SO 污染环境。
2 4 2
(3)步骤②中,在HO 存在下Cu溶于稀HSO ,生成CuSO 和HO,该反应的化学方程式为Cu+ HO+
2 2 2 4 4 2 2 2
HSO =CuSO+2H O。
2 4 4 2
(4)胆矾是一种易溶于水的晶体,因此,经步骤④得到的胆矾,不能用水洗涤的主要原因是:胆矾晶体易溶
于水,用水洗涤会导致胆矾的产率降低。
(5)ⅰ. H O 常温下即能发生分解反应,在加热的条件下,其分解更快,因此,甲同学认为不可能是步骤②
2 2
中过量HO 将I-氧化为I,理由是:溶液C经步骤③加热浓缩后HO 已完全分解。
2 2 2 2 2
ⅱ. I-氧化为I 时溶液的颜色会发生变化;滤液D中含有CuSO 和HSO ,乙同学通过实验证实,只能是
2 4 2 4
Cu2+将I-氧化为I,较简单的方案是除去溶液中的Cu2+,然后再向其中加入含有I-的溶液,观察溶液是否变
2
色;除去溶液中的Cu2+的方法有多种,可以加入适当的沉淀剂将其转化为难溶物,如加入NaS将其转化为
2
CuS沉淀,因此,乙同学的实验方案为取少量滤液D,向其中加入适量NaS溶液,直至不再有沉淀生成,
2
静置后向上层清液中加入少量KⅠ溶液;实验结果为:上层清液不变色,证明I-不能被除去Cu2+的溶液氧
化,故只能是Cu2+将I-氧化为I。
2第二部分:最新模拟精练
完卷时间:50分钟
一、选择题(共12*5分)
1.(2022·全国·模拟预测)下图是有关二氧化硫性质的实验装置图,下列说法正确的是
A.a中紫色石蕊先变红后褪色
B.b中品红溶液褪色,加热后又恢复红色
C.c中氢硫酸溶液出现黄色浑浊,体现 的还原性
D.d中溴水褪色,体现了二氧化硫漂白性
【答案】B
【解析】A.二氧化硫溶于水变为亚硫酸,亚硫酸显酸性,能使紫色石蕊变红,但二氧化硫不能漂白石蕊,
因此a中紫色石蕊变红,不褪色,故A错误;B.b中品红溶液褪色,由于二氧化硫的漂白是暂时性漂白,
加热后又恢复红色,故B正确;C.c中氢硫酸溶液出现黄色浑浊,二氧化硫中硫化合价降低,体现 的
氧化性,故C错误;D.d中溴水褪色,二氧化硫与溴水发生氧化还原反应,体现了二氧化硫氧化性,故D
错误。综上所述,答案为B。
2.(2022·江苏·模拟预测)含硫矿物如黄铁矿(FeS )、黄铜矿、芒硝在工业上有着重要的用途。收集黄铜
2
矿炼铜过程中产生的SO 制备SO ,其反应为2SO (g)+O(g) 2SO (g) 。指定条件
2 3 2 2 3
下,下列物质转化不能实现的是A.SO HSO B.FeS SO
2 2 4 2 3
C.SO NH HSO D.NH HSO (NH )SO
2 4 3 4 3 4 2 4
【答案】B
【解析】A.SO 具有还原性,Cl 具有强氧化性,两者发生氧化还原反应生成HCl和HSO ,可实现转化,
2 2 2 4
故A不符合题意;B.FeS 和O 反应只能生成SO ,不可实现转化,故B符合题意;C.SO 和NH HSO
2 2 2 2 4 3
中S元素化合价都为+4,SO 溶于水生成亚硫酸与氨水发生复分解反应可得NH HSO ,可实现转化,故C
2 4 3
不符合题意;D.根据强酸制弱酸,NH HSO 与HSO 反应可生成(NH )SO 和HSO ,可实现转化,故D
4 3 2 4 4 2 4 2 3
不符合题意;答案选B。
3.(2022·北京海淀·二模)下列关于实验现象的解释或结论中,不正确的是
选项 实验操作 试剂A 现象 结论
A 酸性KMnO 溶液 紫色褪去 SO 具有还原性
4 2
B 新制氯水 黄绿色褪去 SO 具有漂白性
2
C HS溶液 出现淡黄色浑浊 SO 具有氧化性
2 2
盐酸酸化的BaCl 无明显变化,一段时间后产 硫元素从+4价被氧化
D 2
溶液 生白色沉淀 到+6价
【答案】B
【解析】A.酸性高锰酸钾溶液可氧化二氧化硫,紫色褪色,可知二氧化硫具有还原性,A项正确;B.氯
水可氧化二氧化硫,黄绿色褪去,可知二氧化硫具有还原性,与漂白性无关,B项错误;C.二氧化硫可
氧化硫化氢,出现淡黄色浑浊,可知SO 具有氧化性,C项正确;D.二氧化硫与盐酸酸化的BaCl 溶液不
2 2
反应,无明显变化,一段时间后产生白色沉淀为硫酸钡,可知硫元素从+4价被氧化到+6价,D项正确;
答案选B。
4.(2022·天津南开·三模)下列叙述不正确的是
A.食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用
B.大气污染物主要包括氮氧化物、硫氧化物、二氧化碳等
C.将垃圾进行分类处理,可实现资源的合理利用
D.硫酸铝可用于去除污水中的细小悬浮物
【答案】B
【解析】A.二氧化硫具有漂白性和还原性,食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用,A正确;B.大气中的污染物不包含二氧化碳,B错误;C.垃圾是放错了地方的资源,将垃圾进行
分类处理,可实现资源的合理利用,C正确;D.硫酸铝溶于水后铝离子水解生成氢氧化铝胶体,胶体具
有吸附性,能去除污水中的细小悬浮物,D正确;故选B。
5.(2022·上海普陀·二模)NaS俗称硫化碱,是重要的工业原料。工业制备原理:NaSO +2C
2 2 4
NaS+2CO↑,下列说法正确的是
2 2
A.还原性:C>Na S B.NaSO :俗称芒硝
2 2 4
C.反应1mol碳,生成22.4LCO D.该反应在常温下进行
2
【答案】A
【解析】A.C是反应物,化合价升高,做还原剂,NaS是生成物,做还原产物,故还原性:C>Na S,故
2 2
A项正确;B.NaSO :俗称无水芒硝,故B项错误;C.标准状况下,反应1mol碳,生成22.4LCO ,故
2 4 2
C项错误;D.常温下NaSO 与C不反应,故D项错误;故答案选A。
2 4
6.(2022·江苏南通·模拟预测)SO 具有较强的还原性,能将铜离子、银离子等还原。氯化亚铜(CuCl)是
2
一种重要化工原料,难溶于水,在潮湿空气中易水解氧化。实验室制备CuCl的反应原理为SO +2CuSO
2 4
+2NaCl+2HO=2CuCl↓+2HSO +NaSO ,用下列装置进行实验,不能达到实验目的的是
2 2 4 2 4
A.用装置甲制取SO B.用装置乙制取CuCl
2
C.用装置丙将CuCl与母液分离 D.用装置丁干燥CuCl
【答案】D
【解析】A.用浓硫酸与亚硫酸钠可以制取二氧化硫气体,图示装置合理,故A不选;B.根据反应SO +
2
2CuSO +2NaCl+2HO=2CuCl↓+2HSO +NaSO 可知,用装置乙可制取CuCl,故B不选;C.CuCl难溶
4 2 2 4 2 4
于水,可用装置丙避光将CuCl与母液分离,故C不选;D.氯化亚铜(CuCl)难溶于水,在潮湿空气中易水
解氧化,通过装置丁干燥CuCl,CuCl会被氧化,无法达到实验目的,故D选;故选D。
7.(2022·北京·人大附中三模)向2mL0.2mol/LCuSO 溶液中滴加0.2mol/LNa SO 溶液时溶液变绿,继续
4 2 3
滴加产生棕黄色沉淀,经检验棕黄色沉淀中不含 。通过实验探究棕黄色沉淀的成分。
实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体实验2:
已知: , (白色) 。
下列同学对实验现象的分析正确的是
A.实验1中加入稀 后溶液变蓝可证实棕黄色沉淀中含有
B.实验2中加入KI溶液后产生白色沉淀,可证实棕黄色沉淀中含有
C.实验2中加入淀粉溶液后无明显现象,说明不存在
D.在 的存在下, 与 发生了氧化还原反应,产生CuI沉淀和 ,说明棕黄色沉淀中含有
和
【答案】B
【解析】A.加入稀硫酸后,溶液变蓝,说明溶液中有Cu2+,可能固体中就有Cu2+,不能说明棕黄色沉淀
中含有Cu+,A错误;B.根据已知条件Cu2+ CuI↓(白色) + I ,加入KI溶液后出现白色沉淀,说明棕
2
黄色沉淀中含有Cu2+,B正确;C.淀粉遇碘单质变蓝,实验2加入淀粉无明显现象,说明不存在碘单质,
不能说明不存在Cu2+,C错误;D.根据实验2中沉淀A为BaSO,且加入淀粉无现象,则溶液中无I,
4 2
Cu2+ CuI↓(白色)+I ,I 与SO 反应生成碘离子和硫酸根,硫酸根与氯化钡f生成白色沉淀BaSO 不,
2 2 4
是Cu2+与SO 反应,D错误;故选B。
8.(2022·上海徐汇·三模)双氧水( )与下列溶液反应,不能体现 氧化性的是
A.酸性 溶液 B.淀粉KI溶液
C.溶有 的 溶液 D.盐酸酸化的 溶液
【答案】A【解析】A.双氧水与酸性高锰酸钾溶液反应时,双氧水为反应的还原剂,反应中被氧化为氧气,表现还
原性,故A符合题意;B.双氧水与淀粉碘化钾溶液中的碘化钾反应时,双氧水为反应的氧化剂,反应中
被还原为水,表现氧化性,故B不符合题意;C.双氧水与溶有二氧化硫的氯化钡溶液中的二氧化硫反应
时,双氧水为反应的氧化剂,反应中被还原为水,表现氧化性,故C不符合题意;D.双氧水与盐酸酸化
的氯化亚铁溶液中的氯化亚铁反应时,双氧水为反应的氧化剂,反应中被还原为水,表现氧化性,故D不
符合题意;故选A。
9.(2022·江苏·模拟预测)硫难溶于水,微溶于酒精,易溶于CS。硫的氧化物、氢化物、硫酸在工业中
2
有很多应用。高压发电系统常用 作为绝缘气体,该气体分子呈正八面体结构,如图所示。“热化学硫
碘循环分解水”是一种利用硫酸、碘等来获取氢能源的方法。硫元素的几种化合物存在下列转化关系。下
列说法正确的是
浓HSO SO NaSO 溶液 NaSO 溶液 S
2 4 2 2 3 2 2 3
A.反应①中生成的SO 具有漂白性,可使溴水褪色
2
B.反应②中若SO 过量,就会生成NaHSO
2 3
C.反应④中生成 S 既是氧化产物,也是还原产物
D.反应④中当消耗 1mol 稀硫酸时,电子转移为4mol
【答案】B
【解析】A.SO 具有漂白性,但使溴水褪色反应原理为:Br +SO+2H O=2HBr+HSO ,与漂白性无关,
2 2 2 2 2 4
是因为其还原性,A错误;B.反应②中若SO 过量,则将发生反应NaSO +SO+H O=2NaHSO ,B正确;
2 2 3 2 2 3
C.反应④中NaSO 歧化生成S,反应原理为:NaSO+H SO (稀)=Na SO +S↓+SO ↑+H O,S元素化合价
2 2 3 2 2 3 2 4 2 4 2 2
降低,S为还原产物,C错误;D.反应④中的化学方程式为NaSO+H SO (稀)=Na SO +S↓+SO ↑+H O,
2 2 3 2 4 2 4 2 2
由方程式可知,反应消耗 1mol 稀硫酸时,转移2mol电子,D错误;故答案为:B。
10.(2021·北京·模拟预测)实验小组设计图所示装置,验证SO 性质,对实验现象分析不正确的是
2
A.通入SO 一段时间后,试管内时的CCl 溶液逐渐褪色,说明SO 具有还原性
2 4 2B.一段时间后试管内有白色沉淀,说明SO 与BaCl 反应生成BaSO 沉淀
2 2 3
C.试管中的红色花瓣颜色变浅,说明SO 溶于水具有漂白性
2
D.滴有酚酞的NaOH溶液红色变浅,说明SO 能与碱溶液反应
2
【答案】B
【解析】硫酸和NaSO 发生复分解反应产生SO ,SO 与溴、水在氯化钡溶液和溴的四氯化碳分界处发生
2 3 2 2
氧化还原反应生成硫酸、HBr,一段时间后溴的四氯化碳溶液褪色,证明二氧化硫有还原性,硫酸与氯化
钡产生硫酸钡沉淀,湿润的二氧化硫使红色花瓣褪色,说明二氧化硫有漂白性,与NaOH溶液反应消耗
NaOH,滴有酚酞的NaOH溶液褪色。A.由分析可知,一段时间后试管内Br 的CCl 溶液褪色,则SO 和
2 4 2
Br 、HO发生氧化还原反应,说明SO 具有还原性,故A正确;B.由分析可知沉淀为BaSO,故B错误;
2 2 2 4
C.SO 有漂白性,根据试管中的红色花瓣褪色,说明SO 具有漂白性,故C正确;D.滴有酚酞的NaOH
2 2
溶液红色变浅,NaOH物质的量减少,则说明SO 能与碱溶液反应,故D正确。答案为B。
2
11.(2022·辽宁·抚顺市第二中学模拟预测)在实验室进行铁粉和硫粉混合加热的实验,产物又进行了系
列实验,流程如下。下列说法正确的是
A.气体A和D含有同一物质,且均为氧化产物
B.硫元素一共参加了3个氧化还原反应
C.沉淀F可以和NaOH溶液在加热的条件下反应
D.若固体B中加浓硫酸,发生反应时被氧化的和被还原的均为同一种元素
【答案】BC
【解析】首先铁粉和硫粉反应生成FeS,S和O 反应生成SO ,FeS与稀硫酸反应生成FeSO 和HS,HS
2 2 4 2 2
和HSO (浓)反应生成S、SO 和HO。A.由以上分析可知,气体A中SO 是氧化产物,气体D中SO 是
2 4 2 2 2 2
还原产物,A错误;B.由以上分析可知,铁粉和硫粉反应生成FeS,S和O 反应生成SO ,HS和
2 2 2
HSO (浓)反应生成S、SO 和HO,反应中S元素化合价都发生改变,故硫元素一共参加了3个氧化还原反
2 4 2 2
应,B正确;C.沉淀F是S,S与NaOH加热条件下反应生成NaS、NaSO 和HO,C正确;D.固体B
2 2 3 2
为FeS,FeS和浓硫酸反应生成Fe (SO )、S、SO 和HO,其中被氧化的元素为Fe和S,被还原的元素为
2 4 3 2 2
S,故发生反应时被氧化的和被还原的均不为同一种元素,D错误;故选BC。
12.(2022·河北·模拟预测)将SO 分别通入无氧、有氧的浓度均为0.1mol•L-1的BaCl 溶液和Ba(NO ) 溶
2 2 3 2液中,除BaCl 溶液(无氧)外,都产生白色沉淀。实验测得各溶液pH变化曲线如图。下列说法不正确的是
2
A.曲线a所示溶液pH降低的原因:SO +H O HSO H++HSO
2 2 2 3
B.依据曲线b可推知0.2mol•L-1KNO 溶液(无氧)能氧化SO
3 2
C.曲线c所示溶液中发生反应的离子方程式为:2Ba2++2SO+O +2H O=BaSO↓+4H+
2 2 2 4
D.曲线d所表示的过程中NO 是氧化SO 的主要微粒
2
【答案】D
【解析】A.曲线a表示无氧环境下,氯化钡溶液 pH变化减小,说明二氧化硫与水反应生成了弱酸亚硫
酸,溶液pH降低的原因是SO +H O HSO H++HSO ,A选项正确;B.根据曲线b可知,0.1
2 2 2 3
mol·L-1的Ba(NO ) 在无氧环境下可以氧化二氧化硫,对比曲线a可知,是硝酸根离子的作用;依据该实验
3 2
预测0.2 mol·L-1的KNO 溶液(无氧)也可以氧化SO ,B选项正确;C.曲线c表示有氧环境下,氯化钡溶液
3 2
pH变化较大,则说明二氧化硫被氧气氧化为强酸硫酸,反应的方程式是2Ba2+
+2SO+O +2H O=2BaSO↓+4H+,C选项正确;D.氯化钡、硝酸钡在有氧环境下,pH变化几乎相同,所以
2 2 2 4
不能说明曲线d所表示的过程中NO 是氧化SO 的主要微粒,D选项错误;故选D。
2
二、主观题(共3小题,共40分)
13.(2022·海南·模拟预测)(10分)在印染工业中,连二亚硫酸钠( )能使染好的布褪色,也能使
布重新染色,故俗称保险粉。实验室模拟工业生产保险粉的工艺流程如图所示:已知: 为白色固体,易溶于水,难溶于乙醇,在空气中极易被氧化,在碱性介质中稳定。
(1)工业上获得锌粉的方法为:将锌块加热熔化得到锌液,向锌液中不断鼓入 气体,冷却后可获得锌粉。
鼓入 气体的目的除了防止氧化外,还有_________________。
(2)在步骤I中,控制反应温度比较适宜的方法是___________加热(填“水浴”“油浴”或“砂浴”)。
(3)已知: 与 性质相似,当pH大于10.5时开始溶解,写出步骤II中碱性较强时
溶解的离子方程式:_________________________________。
(4)已知:水溶液温度低于52℃时 以 形态结晶,碱性溶液中温度高于52℃时
脱水成无水盐。
步骤III的操作过程为:在无氧减压的环境中,将 碱性溶液于60℃左右蒸发至有大量晶体析出,趁
热过滤、洗涤、减压干燥。趁热过滤的目的是___________;操作中常选用无水乙醇洗涤,其优点是
___________、___________。
(5) 碱性溶液与 溶液反应有纳米银生成,该反应能用于 的纯度测定。若10mL
碱性溶液与20mL 溶液恰好完全反应,则该反应的离子方程式为
___________。
【答案】(1)雾化锌液,获得锌粉或将锌液形成小颗粒(2分)
(2)水浴(1分)
(3) [写 也可](2分)
(4)避免在52℃以下析出 (1分) 降低 的溶解度,减少 的损失
(1分) 乙醇易挥发,容易干燥(1分)
(5) (2分)
【解析】锌粉的悬浊液中通入二氧化硫生成ZnS O,ZnS O 溶液加入氢氧化钠溶液控制pH在8.2~10.5生
2 4 2 4成NaSO、Zn(OH) 沉淀,过滤出沉淀;在无氧减压的环境中,将 碱性溶液于60℃左右蒸发至有
2 2 4 2
大量晶体析出,趁热过滤、洗涤、减压干燥得 固体。
(1)将锌块加热熔化得到锌液,向锌液中不断鼓入 气体,鼓入 气体的目的是防止氧化外、雾化锌液,
冷却后可获得锌粉。
(2)在步骤I中,控制反应温度在35~45℃,温度较低,比较适宜的方法是水浴加热。
(3)当pH大于10.5时 和氢氧化钠反应生成偏锌酸钠,步骤II中碱性较强时 溶解的离子方
程式为 ;
(4)水溶液温度低于52℃时 以 形态结晶,趁热过滤的目的是避免在52℃以下析出
; 为白色固体,易溶于水,难溶于乙醇,在空气中极易被氧化,选用无水乙醇洗
涤,其优点是降低 的溶解度,减少 的损失;乙醇易挥发,容易干燥;
(5) 碱性溶液与 溶液反应生成银,若10mL 碱性溶液与20mL
溶液恰好完全反应,根据得失电子守恒,S元素化合价由+3升高为+4,生成亚硫酸根离
子,则该反应的离子方程式为 。
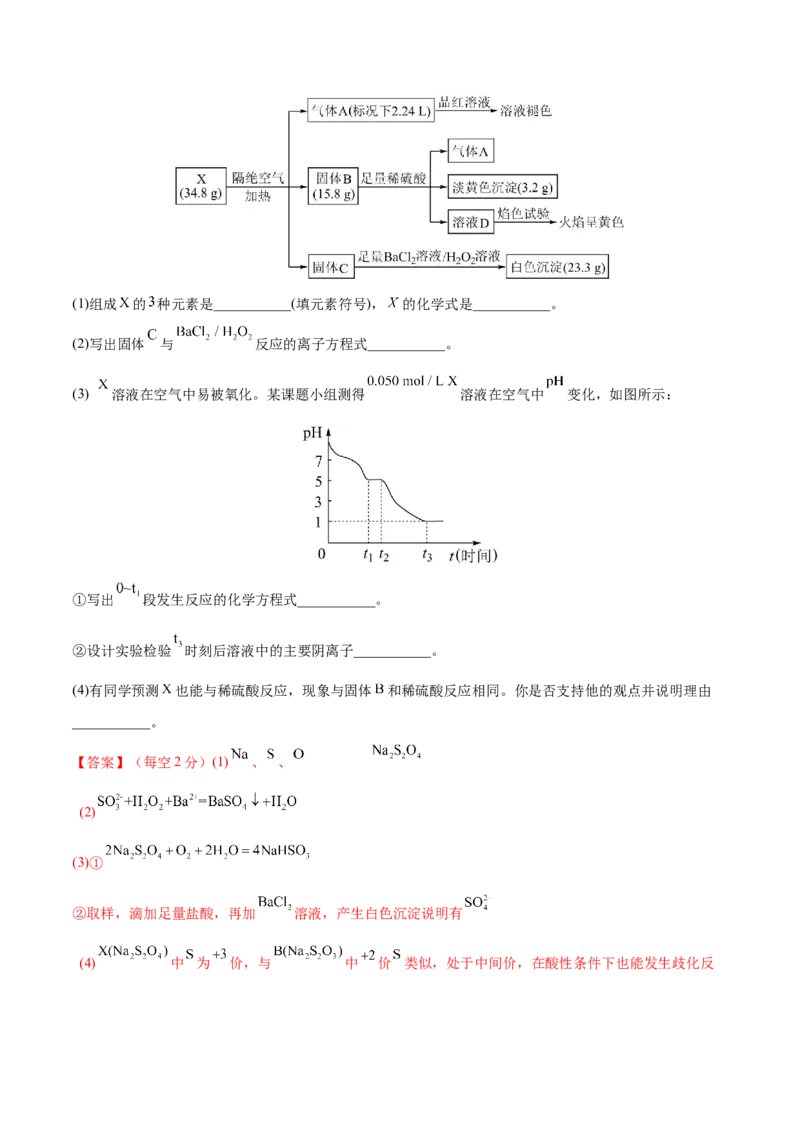
14.(2021·浙江·模拟预测)(12分)为了探究某盐 (仅含三种短周期元素,摩尔质量介于
)的组成和性质,设计并完成了如下实验。已知: 、 、 均为纯净物, 、 组成元素
相同。请回答:(1)组成 的 种元素是___________(填元素符号), 的化学式是___________。
(2)写出固体 与 反应的离子方程式___________。
(3) 溶液在空气中易被氧化。某课题小组测得 溶液在空气中 变化,如图所示:
①写出 段发生反应的化学方程式___________。
②设计实验检验 时刻后溶液中的主要阴离子___________。
(4)有同学预测 也能与稀硫酸反应,现象与固体 和稀硫酸反应相同。你是否支持他的观点并说明理由
___________。
【答案】(每空2分)(1) 、 、
(2)
(3)①
②取样,滴加足量盐酸,再加 溶液,产生白色沉淀说明有
(4) 中 为 价,与 中 价 类似,处于中间价,在酸性条件下也能发生歧化反应生成 和 。
【解析】(1)气体A能使品红溶液褪色,则A为二氧化硫且物质的量为0.1mol,溶液D的焰色实验为黄色,
说明含有钠元素,因此组成 的 种元素是Na、S、O,固体C在双氧水作用下与足量氯化钡反应,说明
固体C为亚硫酸钠,且根据生成硫酸钡沉淀23.3g即物质的量为0.1mol,得到亚硫酸钠物质的量为
n(Na SO )=0.1mol,固体B加稀硫酸反应生成二氧化硫、黄色沉淀S(物质的量为0.1mol)和溶液D(硫酸钠),
2 3
则固体B为硫代硫酸钠,根据NaSO~S,因此n(Na SO)=0.1mol,即质量为15.8g,气体A(SO )物质的
2 2 3 2 2 3 2
量为0.1mol,根据元素守恒得到n(Na)=0.2mol+0.2mol=0.4mol,n(S)=0.1mol+0.2mol+0.1mol=0.4mol,
n(O)=0.3mol+0.3mol+0.2mol=0.8mol,因此 的化学式是NaSO;故答案为:NaSO。
2 2 8 2 2 8
(2)根据前面得到固体 为亚硫酸钠,其与 反应的离子方程式 ;
故答案为: 。
(3)① 溶液在空气中易被氧化,在空气中酸性逐渐增强,因此 段发生反应的化学方程式
;故答案为: 。
②在 时刻溶液的pH=1,说明生成了二元强酸,因此溶液中的主要阴离子是硫酸根,一般检验方法是取样,
滴加足量盐酸,再加 溶液,产生白色沉淀说明有 ;故答案为:取样,滴加足量盐酸,再加
溶液,产生白色沉淀说明有 。
(4) 中 为 价,与 中 价 类似,处于中间价,在酸性条件下也能发生歧化反应
生成 和 ,因此 也在酸性条件下发生歧化反应;故答案为: 中 为 价,与
中 价 类似,处于中间价,在酸性条件下也能发生歧化反应生成 和 。
15.(2020·全国·模拟预测)(18分)硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存
在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。(1)图1中与图2中M、N对应的物质分别是_______、_______。
(2)X与Y反应中氧化剂与还原剂的物质的量之比为_______。
(3)Na SO 溶液易变质,实验室检验NaSO 溶液是否变质的基本操作是_______。
2 3 2 3
(4)SO 和氯水都有漂白性,有人为增强漂白效果,将Cl 和SO 混合使用,结果适得其反,几乎没有漂白效
2 2 2
果,用离子方程式表示其原因:_______。
(5)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做
原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO
4
方案乙:由Cu→CuO→CuSO
4
①方案甲,中铜和浓硫酸反应的化学方程式是_______。该反应体现了浓硫酸的_______性。
②这两种方案,你认为哪一种方案更合理?_______。理由是_______
【答案】(每空2分)(1) CaSO•2H O、NaSO •10H O CuFeS
4 2 2 4 2 2
(2)1:2
(3)取少量溶液于试管中,向其中加入过量稀盐酸,再滴加BaCl 溶液,如果产生白色沉淀,证明混有
2
NaSO
2 4
(4)Cl +SO+2H O=2Cl-+SO +4H+
2 2 2
(5) Cu+2H SO (浓) CuSO +SO↑+2H O 强氧化性、酸性 方案乙 无污染产生,原料
2 4 4 2 2
利用率高
【解析】(1)图2中M为+6价的硫元素对应的盐,对应图1中的物质为CaSO•2H O、NaSO •10H O,N
4 2 2 4 2
为-2价的硫元素对应的盐,对应图1中的物质为CuFeS;
2
(2)X为HS、Y为SO ,发生归中反应得到S单质,SO 做氧化剂,化合价降低4,HS做还原剂,化合价
2 2 2 2
升高2,由升降相等,则反应中氧化剂与还原剂的物质的量之比为1:2;
(3)Na SO 溶液易被氧气氧化为NaSO 而变质,即检验硫酸根是否存在即可,实验操作为:取少量溶液于
2 3 2 4试管中,向其中加入过量稀盐酸,再滴加BaCl 溶液,如果产生白色沉淀,证明混有NaSO ;
2 2 4
(4)二氧化硫与氯气和水发生氧化还原反应生成盐酸和硫酸,离子方程式:Cl+SO+2H O=2Cl-+SO
2 2 2
+4H+;
(5)①铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫与水,反应方程式为:Cu+2H SO (浓)
2 4
CuSO +SO↑+2H O,反应中硫元素的化合价部分降低生成二氧化硫,部分不变存在与硫酸铜中,浓硫酸表
4 2 2
现强氧化性与酸性;
②方案①生成二氧化硫,污染空气,硫元素不能完全利用,方案②与方案①相比,没有污染产生且原料的
利用率高,故方案②更合理。