文档内容
第 20 讲 晶体结构与性质
(模拟精练+真题演练)
完卷时间:50分钟
可能用到的相对原子质量:C 12 N 14 F 19 Fe 56 Ni 59
一、选择题(每小题只有一个正确选项,共12×5分)
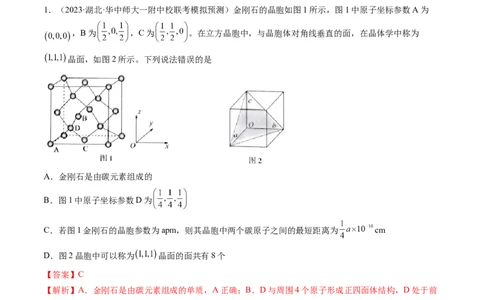
1.(2023·湖北·华中师大一附中校联考模拟预测)金刚石的晶胞如图1所示,图1中原子坐标参数A为
,B为 ,C为 。在立方晶胞中,与晶胞体对角线垂直的面,在晶体学中称为
晶面,如图2所示。下列说法错误的是
A.金刚石是由碳元素组成的
B.图1中原子坐标参数D为
C.若图1金刚石的晶胞参数为apm,则其晶胞中两个碳原子之间的最短距离为 cm
D.图2晶胞中可以称为 晶面的面共有8个
【答案】C
【解析】A.金刚石是由碳元素组成的单质,A正确;B.D与周围4个原子形成正四面体结构,D处于前
面、下面和左面的1/4,D原子的坐标参数为 ,B正确;C.金刚石晶胞中两个碳原子之间的最短
距离是体对角线的 ,为 cm,C错误;D.图2晶胞中共有8个顶点,4条体对角线,由(1,1,1)
晶面定义可知,晶胞中可以称为 晶面的面共有8个,D正确;故选C。
2.(2023·辽宁·校联考模拟预测)几种晶体的晶胞结构如图所示。已知: 、 均为立方晶胞。
下列说法错误的是A.相同条件下,熔点:
B.另一种 晶胞结构中,当 处于体心时,则 处于棱心
C. 晶胞中a点原子坐标参数为 ,则b点原子坐标参数为
D.三种晶体中,Ca的配位数均为8
【答案】D
【解析】A. 半径小于 , 的离子键强于 的, 熔点更高,A项正确;B.另一种 晶
胞结构中,当 处于体心时, 处于顶角、O处于棱心,B项正确;C.由 晶胞结构及a点原子坐标
参数为 ,可知 点原子坐标参数为, ,C项正确;D. 中 的配位数为12,D项
错误;故答案为:D。
3.(2023·天津南开·南开中学校考模拟预测)下列表述中正确的有
①晶体与非晶体的根本区别在于固体是否具有规则的几何外形
②非极性分子往往具有高度对称性,如 这样的分子
③利用超分子的分子识别特征,可以分离 和
④接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出来的大,是由于氢键的影响
⑤设 为阿伏加德罗常数的值,含 碳原子的金刚石晶体中共价键个数为
⑥熔融状态能导电,熔点在 左右的晶体一定为离子晶体
A.2个 B.3个 C.4个 D.5个
【答案】B
【解析】①晶体与非晶体的根本区别在于晶体有自范性,与是否有规则的几何外形无关,如:玻璃,故①
错误;②PCl 为三角锥形分子,HO 为书页形分子,PCl 、HO 分子的正负电荷重心不重合,为极性分子,
3 2 2 3 2 2
故②错误;③C 和C 的混合物加入一种空腔大小适合C 的“杯酚”中可进行分离,这是利用超分子的
60 70 60
分子识别特征,故③正确;④接近水的沸点的水蒸气的相对分子质量测定值比用化学式HO计算出来的相
2
对分子质量大一些,其主要原因是接近水的沸点的水蒸气中水分子间因氢键而形成了“缔合分子”,故④
正确;⑤金刚石中每个C原子形成4个共价键,每个共价键被2个C原子共用,所以每个C原子占有的共
价键个数为4× =2,2.4g金刚石中n(C)= =0.2mol,则碳原子个数为0.2mol×2N /mol=0.4N ,故
A A
⑤正确;⑥熔融状态能导电,熔点在1000℃左右的晶体可能是金属晶体,故⑥错误;故选:B。4.(2023·湖北荆州·沙市中学校考模拟预测)快离子导体是一类具有优良导电能力的固体电解质。图
1(Li SBF )和图2是潜在的快离子导体材料的结构示意图。温度升高时,NaCl晶体出现缺陷,晶体的导电
3 4
性增强。该晶体导电时,③迁移的途径有两条:
途径1:在平面内挤过2、3号氯离子之间的狭缝(距离为x)迁移到空位。
途径2:挤过由1、2、3号氯离子形成的三角形通道(如图3,小圆的半径为y)迁移到空位。
已知:氯化钠晶胞参数a=564pm,r(Na+)=95pm,r(Cl-)=185pm, =1.4, =1.7。
下列说法不正确的是
A.第二周期元素中第一电离能介于B和F之间的元素有4种
B.图1所示晶体中,每个Li+与4个呈四面体结构的离子相邻
C.氯化钠晶体中,Na+填充在氯离子形成的正八面体空隙中
D.温度升高时,NaCl晶体出现缺陷,晶体的导电性增强,该晶体导电时,③迁移的途径可能性更大的是
途径1
【答案】D
【解析】A.第二周期元素第一电离能从左向右呈增大趋势,由于Be的2s轨道全满,N的2p轨道半满,
结构稳定,造成Be和N比同周期相邻元素的第一电离能高,因此第一电离能介于B和F之间的有Be、
C、N、O共4种,A正确;B.由图1所示晶体结构可知,Li+位于棱心,正四面体结构的离子在体心,则
每个Li+与4个呈四面体结构的离子相邻,B正确;C. NaCl晶胞中Na+周围有3个Cl-,则在NaCl晶体
中,Na+周围等距离最近有6个C1-,6个C1-构成正八面体结构,即Na+填充在C1-堆积而成的八面体空隙
中,C正确;D.该三角形为等边三角形,边长等于图2中面对角线长度,故三角形边长=
,即 ,r(Cl-)=185pm,解得x=24.8pm;内部虚线部分
三角形的顶角为120°、两腰长为r(Cl )+y、底长为282 pm,边角关系有 [ r(Cl )+y]=282 pm,解得
y= 47.2pm;由于挤过由1、2、 3号氯离子形成的三角形通道y的值大于挤过2、3号氯离子之间的狭缝x
值,所以Na+如果能挤过,那么挤过由1、2、 3号氯离子形成的三角形通道相对容易些,即迁移可能性更
大的途径是途径2,D错误;
故选D。
5.(2023·湖北武汉·湖北省武昌实验中学校考模拟预测)砷化镓(GaAs)是优良的半导体材料,熔点为
1238℃,用于制作太阳能电池的材料,其结构如图所示,其中以原子1为原点,原子2的坐标为(1,1,
1)。下列有关说法中错误的是A.原子3的坐标为( , , ) B.Ga的配位数为4
C.GaAs为共价晶体 D.若将Ga换成Al,则晶胞参数将变小
【答案】A
【解析】A.由图可知,原子3在x、y、z轴上的投影分别为 ,坐标为 ,A错误;B.根据
晶胞结构可知,Ga的配位数为4,B正确;C.GaAs的熔点为1238℃,硬度大,熔点高硬度大,故晶体类
型为共价晶体,C正确;D.Ga原子半径比Al小,则若将Ga换成Al,则晶胞参数将变小,D正确;故选
A。
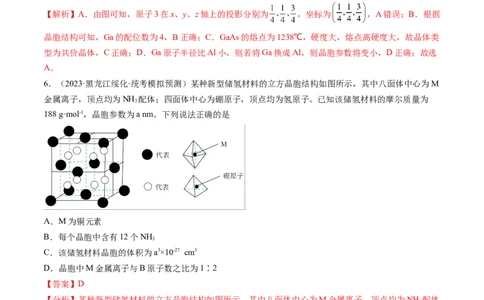
6.(2023·黑龙江绥化·统考模拟预测)某种新型储氢材料的立方晶胞结构如图所示,其中八面体中心为M
金属离子,顶点均为NH 配体;四面体中心为硼原子,顶点均为氢原子。已知该储氢材料的摩尔质量为
3
188 g·mol-1,晶胞参数为a nm。下列说法正确的是
A.M为铜元素
B.每个晶胞中含有12个NH
3
C.该储氢材料晶胞的体积为a3×10-27 cm3
D.晶胞中M金属离子与B原子数之比为1∶2
【答案】D
【分析】某种新型储氢材料的立方晶胞结构如图所示,其中八面体中心为M金属离子,顶点均为NH 配体,
3
八面体位于顶点和面心,八面体的个数为8× +6× =4,1个八面体中有1个M和6个NH ,晶胞中含
3
4个M和24个NH ;四面体中心为硼原子,顶点均为氢原子,四面体位于体内,四面体的个数为8,1个
3
四面体中有1个B和4个H,晶胞中含8个B和32个H;
【解析】A.晶胞中M、NH 、B、H的个数之比为4∶24∶8∶32=1∶6∶2∶8,晶体的化学式为
3
M(NH)(BH),该储氢材料的摩尔质量为188g/mol,M的相对原子质量为188-6×17-2×15=56,M为Fe元
3 6 4 2
素,A项错误;B.1个八面体中有6个NH ,1个晶胞中含4个八面体,则每个晶胞中含有4×6=24个
3
NH ,B项错误;C.晶胞参数为anm=a×10-7cm,该储氢材料晶胞的体积为(a×10-7cm)3=a3×10-21cm3,C项错
3误;D.晶胞中M金属离子与B原子数之比为4∶8=1∶2,D项正确;答案选D。
7.(2023·山东聊城·校联考三模)BP晶体是一种超硬耐磨的涂层材料,其合成途径之一为
、 。下列说法正确的是
A.BP晶体为离子晶体 B. 的电子式为
C.第一电离能: D. 为正四面体结构,键角为
【答案】D
【解析】A.BP晶体是一种超硬耐磨的涂层材料,则它为原子晶体,A项错误;B.C最外层四个电子需
要共用4对电子达饱和,即C与每个S共用两对电子,B项错误;C.P、S、Cl为同周期从左往右第一电
离能逐渐增大,但P为半充满结构难失电子所以其第一电离能P>S。第一电离能:Cl>P>S,C项错误;
D.P 形成正四面体,每个面为正三角形所以键角即为三角形的内角为60°,D项正确;故选D。
4
8.(2023·辽宁葫芦岛·统考二模)某铁氮化合物晶体的晶胞结构如图所示。若晶胞中距离最近的两个铁原
子距离为apm,阿佛伽德罗常数的值为N ,则下列说法不正确的是
A
A.若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为棱心、面心和体心
B.该化合物化学式为Fe N
4
C.N原子的分数坐标为( , , )
D.该晶体的密度为 g/cm3
【答案】A
【解析】A.由题干晶胞示意图可知,若以氮原子为晶胞顶点,则铁原子在晶胞中的位置为棱心和体心,A
错误;B.由题干晶胞示意图可知,一个晶胞中含有Fe个数为: =4,N原子个数为1,故该化
合物化学式为Fe N,B正确;C.由题干晶胞示意图可知,N原子位于体心上,故N原子的分数坐标为( ,
4
, ),C正确;D.由B项分析可知,一个晶胞中含有Fe个数为: =4,N原子个数为1,设
晶胞的边长为dpm,若晶胞中距离最近的两个铁原子距离为apm,即有 ,解得d= ,则该晶体的密度为 = g/cm3,D正确;故答案为:A。
9.(2023·湖北武汉·华中师大一附中校考模拟预测)一种由镍、氟和钾三种元素组成的化合物晶体结构如
图所示,下列说法错误的是
A.该晶体中Ni的化合价为+2 B.与镍等距离且最近的 有6个
C.图中A、B原子间的距离为 D.该晶体的密度为
【答案】B
【解析】A.根据晶胞结构可知该晶体中 个数为 , 个数为 ,Ni的个数
为 ,根据正负化合价代数和为0,可知Ni应为+2价,选项A正确;B.晶胞中a与c不相等,因此
与镍等距离且最近的 不是6个,选项B错误;C.图中A位于棱边 处,B原子位于中心,二者之间的
距离为 pm,选项C正确;D.该晶胞的化学式为 ,晶胞质量为426/ ,晶胞体
积为 ,因此该晶体的密度为 ,选项D正确;答案选B。
10.(2023·北京海淀·北京市十一学校校考三模)硅酸盐是地壳岩石的主要成分,在硅酸盐中,四面体
(如图甲为俯视投影图)通过共用顶角氧原子可形成六元环(图乙)、无限单链状(图丙)、无限双链状(图
丁)等多种结构。石棉是由钙、镁离子以离子数 的比例与单链状硅酸根离子形成的一种硅酸盐。下列说法不正确的是
A.大多数硅酸盐材料硬度高与硅氧四面体结构有关
B.六元环的硅酸盐阴离子化学式
C.石棉的化学式为
D.双链状硅酸盐中硅氧原子数之比为
【答案】D
【解析】A.硅氧四面体结构是指由一个硅原子和四个氧原子组成的四面体结构。这种结构因其内部化学
键的结构和特性而具有稳定性。硅氧四面体结构中的硅原子与四个氧原子形成了共价键,共享电子对使每
个原子都充满了电子。这种共价键结构使得硅氧四面体结构比单纯的硅或氧分子更加稳定,所以硅氧四面
体结构决定了大多数硅酸盐材料硬度高,故A正确;B.六元环的硅酸盐阴离子中Si元素显+4价,O元素
显-2价,所以六元环的硅酸盐阴离子化学式为 ,故B正确;C.石棉中钙、镁离子之比为1∶3,
其中Mg元素、Ca元素显+2价,Si元素显+4,O元素显-2价,所以,该石棉的化学式可表示为
,故C正确;D.由图丁可知,双链硅酸盐中有两种硅氧四面体,且数目之比为1∶1,一种
与单链硅酸盐中硅氧原子个数比相同,其中硅原子个数为1,氧原子个数为 ,个数比为1∶3;
另一种,硅原子个数为1,O原子个数为 ,个数比为1∶2.5,所以双链状硅酸盐中硅氧原子数
之比为2∶5.5,故D错误;故选D。
11.(2023·湖北·校联考模拟预测)复合催化剂 可以实现常压合成乙二醇。下列有关叙述正
确的是
A. 和石墨烯互为同素异形体 B. 和 均为传统无机非金属材料
C.石英玻璃具有各向异性 D. 的立体构型为正四面体形
【答案】A
【解析】A. 和石墨烯为结构不同的碳单质,互为同素异形体,故A正确;B. 为新型无机非金属
材料,故B错误;C.玻璃为非晶态物质,不具有晶体的各向异性,故C错误;D. 中铜离子采
用 杂化,立体构型为平面正方形,故D错误;故选:A。
12.(2023·山东济南·山东省实验中学校考模拟预测)黑砷在催化电解水方面受到关注,其晶体结构如图
所示,与石墨类似。下列说法正确的是A.黑砷中As—As键的强度均相同
B.黑砷与C 都属于混合型晶体
60
C.黑砷与石墨均可作为电的良导体
D.黑砷单层中As原子与As—As键的个数比为1∶3
【答案】C
【解析】A.根据图知,黑砷中存在的As−As键的键长不同,则键能不同,故A错误;B.C 属于分子晶
60
体,黑砷晶体结构类似于石墨,石墨晶体中既有共价键,又有金属键,还有范德华力,为混合晶体,所以
黑砷属于混合晶体,故B错误;C.黑砷晶体结构与石墨类似,石墨是电的良导体,则黑砷能也是电的良
导体,故C正确;D.根据图知,黑砷晶体每层原子之间组成六元环结构,一个正六边形有6个As,每个
As相邻的3个As以As−As相结合,既A每个As属于3个正六边形,实际属于这个正六边形的As原子数
为 ,同理,一个正六边形六条边,但每个As−As属于相邻两个正六边形,则实际属于这个正六边
形的As−As为 ,故黑砷单层中As原子与As−As键个数比为2:3,故D不正确;故答案选C。
二、主观题(共3小题,共40分)
13.(12分)(2023·山东烟台·统考二模)硅材料和铝材料在生产生活中应用广泛。回答下列问题:
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a. 、b.
、c. ,半径由大到小的顺序为___________(填标号);第三周期元素中,第一
电离能介于A1和P之间的元素有___________种。
(2) 是一种高介电常数材料。已知: 中 键角120°, 中 键角
111°。共价键的极性Si—N___________C—N(填“>”、“=”或“<”)。下列划线原子与 中N原子
杂化类型相同的是___________(填标号)。
A. B. C. D.
(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝
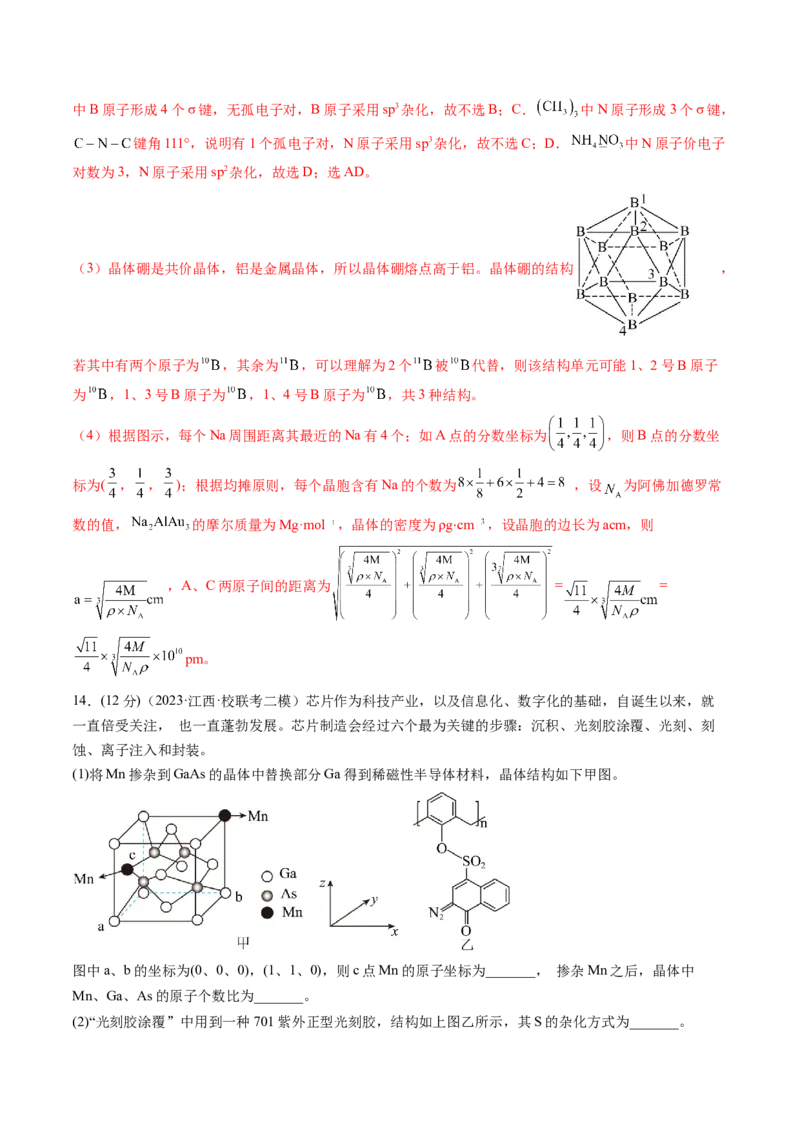
的原因是___________。晶体硼的结构单元是正二十面体,每个单元中有12个硼原子,结构如图。若其中
有两个原子为 ,其余为 ,则该结构单元有___________种。(4)已知合金 的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空
隙中填入 四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。
每个Na周围距离其最近的Na有___________个;以晶胞参数为单位长度建立的坐标系可以表示晶胞中各
原子的位置,称为原子的分数坐标,如A点的分数坐标为 ,则B点的分数坐标为___________;
设 为阿佛加德罗常数的值, 的摩尔质量为Mg·mol ,晶体的密度为ρgcm ,则A、C两原
子间的距离为___________pm(列出计算表达式)。 ⋅
【答案】(除标注外,每空1分)(1)cab 3
(2)> AD
(3)晶体硼为共价晶体,铝为金属晶体 (2分) 3
(4)4 ( , , ) (2分) (2分)
【解析】(1)电子层数越多半径越大,质子数相同、电子层数也相同时,电子数越多半径越大,由硅原
子核形成的三种微粒:a. 、b. 、c. ,半径由大到小的顺序为
> > ;同周期元素从左到右第一电离能有增大趋势,第三周期元
素中,Mg的3s能级全充满、P的3p能级半充满,结构稳定,第一电离大于同周期相邻元素,第一电离能
介于A1和P之间的元素有Mg、Si、S共3种元素。
(2)C的电负性大于Si,共价键的极性Si—N>C—N。 中 键角120°,说明N原子采用
sp2杂化。A. 中Al原子形成3个σ键,无孤电子对,Al原子采用sp2杂化,故选A;B.中B原子形成4个σ键,无孤电子对,B原子采用sp3杂化,故不选B;C. 中N原子形成3个σ键,
键角111°,说明有1个孤电子对,N原子采用sp3杂化,故不选C;D. 中N原子价电子
对数为3,N原子采用sp2杂化,故选D;选AD。
(3)晶体硼是共价晶体,铝是金属晶体,所以晶体硼熔点高于铝。晶体硼的结构 ,
若其中有两个原子为 ,其余为 ,可以理解为2个 被 代替,则该结构单元可能1、2号B原子
为 ,1、3号B原子为 ,1、4号B原子为 ,共3种结构。
(4)根据图示,每个Na周围距离其最近的Na有4个;如A点的分数坐标为 ,则B点的分数坐
标为( , , );根据均摊原则,每个晶胞含有Na的个数为 ,设 为阿佛加德罗常
数的值, 的摩尔质量为Mg·mol ,晶体的密度为ρgcm ,设晶胞的边长为acm,则
⋅
,A、C两原子间的距离为 = =
pm。
14.(12分)(2023·江西·校联考二模)芯片作为科技产业,以及信息化、数字化的基础,自诞生以来,就
一直倍受关注, 也一直蓬勃发展。芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻
蚀、离子注入和封装。
(1)将Mn掺杂到GaAs的晶体中替换部分Ga得到稀磁性半导体材料,晶体结构如下甲图。
图中a、b的坐标为(0、0、0),(1、1、0),则c点Mn的原子坐标为_______, 掺杂Mn之后,晶体中
Mn、Ga、As的原子个数比为_______。
(2)“光刻胶涂覆”中用到一种701紫外正型光刻胶,结构如上图乙所示,其S的杂化方式为_______。(3)“光刻”时,紫外负型光刻胶常含有-N (叠氮基), 在紫外光下形成的阴离子 的等电子体有______ (填
3
化学式,任写一种),其空间构型为_______。
(4)一种Ag HgI 固体导电材料为四方晶系,其晶胞参数为apm、apm 和2a pm,晶胞沿x、y、z的方向投
2 4
影(如图所示),A、B、C表示三种不同原子的投影。其中代表Hg原子是_______ “A”、“B”、“C”)。设
N 为阿伏加德罗常数的值,Ag HgI 的摩尔质量为Mg·mol-1,该晶体的密_______g·cm-3(用代数式表示)。
A 2 4
【答案】(除标注外,每空2分)(1)(0, , ) 5:27:32
(2)sp3(1分)
(3)N O、CO、CS(任写一种) 直线形(1分)
2 2 2
(4)B ×1030
【解析】(1)由图可知,c点锰原子在x、y、z轴上的投影坐标分别为0、 、 ,则c点Mn的原子坐标
为(0, , );根据“均摊法”,晶胞中含 个Mn、 个Ga、4个As,掺杂
Mn之后,晶体中Mn、Ga、As的原子个数比为5:27:32;
(2)图中硫原子形成4个共价键且无孤电子对,为sp3杂化;
(3)等电子体是指价电子数和原子数相同的分子、离子或原子团,阴离子 的等电子体有NO、CO、
2 2
CS 等;阴离子 的中心原子N原子的价层电子对数为 ,为sp杂化,空间构型为直线形;
2
(4)由投影可知,A为位于晶胞内部,原子数为8;B原子位于顶点和体心,根据“均摊法”,晶胞中含
个B;C原子位于棱上和六个面上,晶胞中含 个C;结合化学式Ag HgI 可知,
2 4
ABC分别为I、Hg、Ag,晶体密度为 。
15.(16分)(2023·天津河北·统考二模)坐落在河北区的华为天津区域总部项目计划于2023年12月底竣工。
石墨烯液冷散热技术系华为公司首创,所使用材料石墨烯是一种二维碳纳米材料。
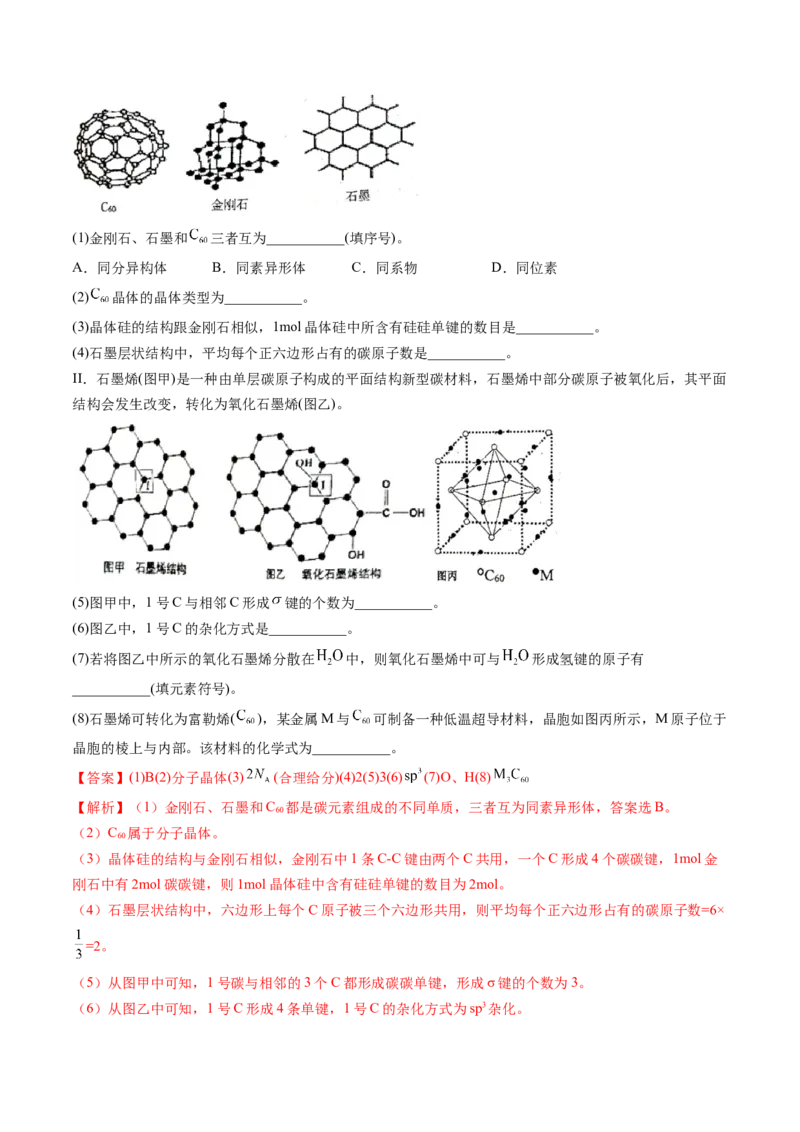
I. 、金刚石、石墨的结构模型如图所示(石墨仅表示出其中的一层结构):(1)金刚石、石墨和 三者互为___________(填序号)。
A.同分异构体 B.同素异形体 C.同系物 D.同位素
(2) 晶体的晶体类型为___________。
(3)晶体硅的结构跟金刚石相似,1mol晶体硅中所含有硅硅单键的数目是___________。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是___________。
II.石墨烯(图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面
结构会发生改变,转化为氧化石墨烯(图乙)。
(5)图甲中,1号C与相邻C形成 键的个数为___________。
(6)图乙中,1号C的杂化方式是___________。
(7)若将图乙中所示的氧化石墨烯分散在 中,则氧化石墨烯中可与 形成氢键的原子有
___________(填元素符号)。
(8)石墨烯可转化为富勒烯( ),某金属M与 可制备一种低温超导材料,晶胞如图丙所示,M原子位于
晶胞的棱上与内部。该材料的化学式为___________。
【答案】(1)B(2)分子晶体(3) (合理给分)(4)2(5)3(6) (7)O、H(8)
【解析】(1)金刚石、石墨和C 都是碳元素组成的不同单质,三者互为同素异形体,答案选B。
60
(2)C 属于分子晶体。
60
(3)晶体硅的结构与金刚石相似,金刚石中1条C-C键由两个C共用,一个C形成4个碳碳键,1mol金
刚石中有2mol碳碳键,则1mol晶体硅中含有硅硅单键的数目为2mol。
(4)石墨层状结构中,六边形上每个C原子被三个六边形共用,则平均每个正六边形占有的碳原子数=6×
=2。
(5)从图甲中可知,1号碳与相邻的3个C都形成碳碳单键,形成σ键的个数为3。
(6)从图乙中可知,1号C形成4条单键,1号C的杂化方式为sp3杂化。(7)只有电负性较大的非金属元素与氢元素才可形成氢键,氧化石墨烯中的O能与水分子中的H形成氢
键,氧化石墨烯中的H也可与水分子中的O形成氢键,能与HO形成氢键的原子有H、O。
2
(8)根据均摊法,该晶胞中M原子的个数为 ×12+9=12,C 个数为8× +6× =4,则该材料的化学式为
60
MC 。
3 60
1.(2023·辽宁·统考高考真题)晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方
体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
A.图1晶体密度为 g∙cm-3 B.图1中O原子的配位数为6
C.图2表示的化学式为 D. 取代产生的空位有利于 传导
【答案】C
【解析】A.根据均摊法,图1的晶胞中含Li:8× +1=3,O:2× =1,Cl:4× =1,1个晶胞的质量为
g= g,晶胞的体积为(a×10-10cm)3=a3×10-30cm3,则晶体的密度为 g÷(a3×10-30cm3)=
g/cm3,A项正确;B.图1晶胞中,O位于面心,与O等距离最近的Li有6个,O原子的配
位数为6,B项正确;C.根据均摊法,图2中Li:1,Mg或空位为8× =2。O:2× =1,Cl或Br:4×
=1,Mg的个数小于2,根据正负化合价的代数和为0,图2的化学式为LiMgOCl Br ,C项错误;D.进
x 1-x
行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料,说明Mg2+取代产生的空位有利于Li+的传
导,D项正确;答案选C。
2.(2022·北京·高考真题)2022年3月神舟十三号航天员在中国空间站进行了“天宫课堂”授课活动。其
中太空“冰雪实验”演示了过饱和醋酸钠溶液的结晶现象。下列说法不正确的是
A.醋酸钠是强电解质
B.醋酸钠晶体与冰都是离子晶体
C.常温下,醋酸钠溶液的
D.该溶液中加入少量醋酸钠固体可以促进醋酸钠晶体析出
【答案】B【解析】A.醋酸钠在水溶液中能完全电离,醋酸钠是强电解质,故A正确;B.醋酸钠晶体是离子晶体,
冰是分子晶体,故B错误;C.醋酸钠是强碱弱酸盐,常温下,醋酸钠溶液的 ,故C正确;D.过
饱和醋酸钠溶液处于亚稳态,加入少量醋酸钠固体可以促进醋酸钠晶体析出,形成饱和溶液,故D正确;
选B。
3.(2022·江苏·高考真题)我国古代就掌握了青铜(铜-锡合金)的冶炼、加工技术,制造出许多精美的青铜
器;Pb、 是铅蓄电池的电极材料,不同铅化合物一般具有不同颜色,历史上曾广泛用作颜料,下列
物质性质与用途具有对应关系的是
A.石墨能导电,可用作润滑剂
B.单晶硅熔点高,可用作半导体材料
C.青铜比纯铜熔点低、硬度大,古代用青铜铸剑
D.含铅化合物颜色丰富,可用作电极材料
【答案】C
【解析】A.石墨是过渡型晶体,质软,可用作润滑剂,故A错误
B.单晶硅可用作半导体材料与空穴可传递电子有关,与熔点高无关,故B错误;C.青铜是铜合金,比纯
铜熔点低、硬度大,易于锻造,古代用青铜铸剑,故C正确;D.含铅化合物可在正极得到电子发生还原
反应,所以可用作电极材料,与含铅化合物颜色丰富无关,故D错误;故选C。
4.(2022·湖北·统考高考真题) 在高温高压下可转变为具有一定导电性、高硬度的非晶态碳玻璃。下
列关于该碳玻璃的说法错误的是
A.具有自范性 B.与 互为同素异形体
C.含有 杂化的碳原子 D.化学性质与金刚石有差异
【答案】A
【解析】A.自范性是晶体的性质,碳玻璃为非晶态,所以没有自范性,A错误;B.碳玻璃和 均是由
碳元素形成的不同的单质,所以是同素异形体,B正确;C.碳玻璃具有高硬度,与物理性质金刚石类似,
因而结构具有一定的相似性,所以含有 杂化的碳原子形成化学键,C正确;D.金刚石与碳玻璃属于同
素异形体,性质差异主要表现在物理性质上,化学性质上也有着活性的差异,D正确;故选A。
5.(2022·山东·高考真题) 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存
在 键、 键。下列说法错误的是
A. 的熔点高于 B.晶体中所有化学键均为极性键
C.晶体中所有原子均采取 杂化 D.晶体中所有原子的配位数均相同
【答案】A
【分析】Al和Ga均为第ⅢA元素,N属于第ⅤA元素,AlN、GaN的成键结构与金刚石相似,则其为共
价晶体,且其与金刚石互为等电子体,等电子体之间的结构和性质相似。AlN、GaN晶体中,N原子与其
相邻的原子形成3个普通共价键和1个配位键。
【解析】A.因为AlN、GaN为结构相似的共价晶体,由于Al原子的半径小于Ga,N—Al的键长小于N—Ga的,则N—Al的键能较大,键能越大则其对应的共价晶体的熔点越高,故GaN的熔点低于AlN,A说
错误;B.不同种元素的原子之间形成的共价键为极性键,故两种晶体中所有化学键均为极性键,B说法
正确;C.金刚石中每个C原子形成4个共价键(即C原子的价层电子对数为4),C原子无孤电子对,故
C原子均采取sp3杂化;由于AlN、GaN与金刚石互为等电子体,则其晶体中所有原子均采取sp3杂化,C
说法正确;D.金刚石中每个C原子与其周围4个C原子形成共价键,即C原子的配位数是4,由于AlN、
GaN与金刚石互为等电子体,则其晶体中所有原子的配位数也均为4,D说法正确。综上所述,本题选
A。
6.(2021·湖北·统考高考真题)某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该
合金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是
A.该晶胞的体积为a3×10-36cm-3 B.K和Sb原子数之比为3∶1
C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 apm
【答案】B
【解析】A.该晶胞的边长为 ,故晶胞的体积为 ,A项错误;B.该
晶胞中K的个数为 ,Sb的个数为 ,故K和Sb原子数之比为3∶1,B项正确;
C.以面心处Sb为研究对象,与Sb最邻近的K原子数为8,C项错误;D.K和Sb的最短距离为晶胞体对
角线长度的 ,即 ,D项错误。故选B。