文档内容
第二十六、二十七讲 弱电解质的电离、盐类的水解
【基础巩固】
1.下列事实与盐类水解无关的是( )
A.MgCO 可以除去MgCl 酸性溶液中的Fe3+ B.氯化铁溶液常用作铜印刷电路板的腐蚀剂
3 2
C.常用热的纯碱溶液除去油污 D.长期施用硫酸铵易使土壤酸化
2.(2023·浙江·统考高考真题)氯化铁是一种重要的盐,下列说法不正确的是
A.氯化铁属于弱电解质 B.氯化铁溶液可腐蚀覆铜板
C.氯化铁可由铁与氯气反应制得 D.氯化铁溶液可制备氢氧化铁胶体
3.(2023·上海宝山·统考二模)下列变化规律正确的是
A.HCl、HBr、HI热稳定性由弱到强
B.HCO、HClO、CHCOOH的酸性由弱到强
2 3 3
C.物质的量浓度相等的NaCl、MgCl 、AlCl 三种溶液的pH值由小到大
2 3
D.等物质的量的乙烷、乙烯、乙炔充分燃烧,所耗用氧气的量由多到少
4.(2023·浙江金华·浙江省丽水中学校联考一模)下列说法一定正确的是
A.相同温度下,1L0.02mol·L-1的NaCl溶液和2L0.01mol·L-1NaCN溶液中的离子总数相等
B.常温下,将pH=2的一元酸HA溶液与pH=12的一元碱BOH溶液等体积混合,所得溶液pH=7
C.25℃时,向10mL0.1mol·L-1HA溶液中加入0.1mol·L-1的NaOH溶液,当水电离出的c(H+)=1.0×10-
7mol·L-1时,滴加氢氧化钠溶液的体积可能出现两种情况,则HA为弱酸
D.将冰醋酸加水稀释,冰醋酸的电离度逐渐增加,但电离常数K 不变,c(H+)逐渐增大,导电性逐渐增
a
强。
5.(2023·浙江·校联考一模)已知25℃时, 。某体系中,膜只允许未电离的HA自由通
过(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是A.溶液Ⅰ和Ⅱ中的 不相等 B.溶液Ⅰ中
C.溶液Ⅱ中的HA的电离度为 D.溶液Ⅰ、Ⅱ中水电离出的 之比为
6.(2023·浙江·高三统考专题练习)下列实验操作正确的是
A.选用图1滴定管量取17.60mLNaCl溶液
B.如图2所示,记录滴定终点读数为19.90mL
C.中和滴定时,选用图1滴定管盛装NaOH标准溶液
D.可用图3装置进行KMnO 溶液滴定未知浓度的FeSO 溶液实验
4 4
7.(2023·河南·校联考模拟预测)食用级NaHSO 产品用作防腐剂、抗氧化剂等。根据常温时下列实验得
3
到的粒子浓度关系正确的是
实
实验操作和现象 粒子浓度的关系
验
向蓝色石蕊试纸上滴入2滴0.1 mol ·L-1NaHSO 溶液,试
① 3 c(Na+) >c( ) >c( ) >c(HSO )
纸变红 2 3
向10 mL0.1 mol ·L-1NaHSO 溶液中加入等体积等浓度的 c(Na+)-c( ) -c( ) -c(H SO )
② 3 2 3
NaOH溶液 =0.05 mol ·L-1
向0.1 mol ·L-1NaHSO 溶液中加入等浓度的NaOH溶液至
③ 3 c( ) +c( )=c(Na+)
pH=7
A.①③ B.②③ C.①② D.①②③
8.(2023·上海金山·统考二模)常温下酸性:HSO >HClO。SO 与足量Ca(ClO) (aq)反应的离子方程式为
2 2
A.SO +HO+ClO-=HSO +HClO
2 2
B.SO +HO+Ca2++2ClO-=CaSO↓+2HClO
2 2 3
C.SO +HO+Ca2++ClO-=CaSO↓+Cl-+2H+
2 2 4D.SO +HO+Ca2++3ClO-=CaSO↓+Cl-+2HClO
2 2 4
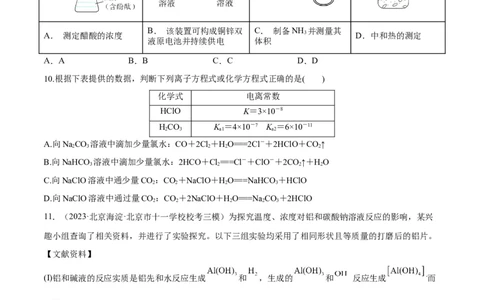
9.(2023·陕西西安·西北工业大学附属中学校考模拟预测)用如图所示装置(夹持装置省略)进行实验,操
作正确且能达到目的的是
B. 该装置可构成铜锌双 C. 制备NH 并测量其
A. 测定醋酸的浓度 3 D.中和热的测定
液原电池并持续供电 体积
A.A B.B C.C D.D
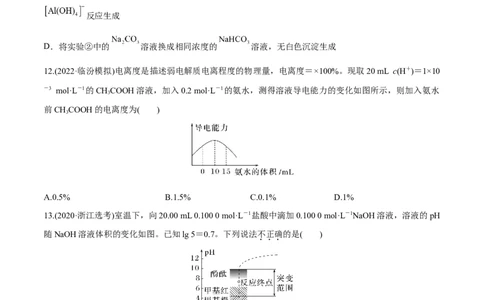
10.根据下表提供的数据,判断下列离子方程式或化学方程式正确的是( )
化学式 电离常数
HClO K=3×10-8
HCO K =4×10-7 K =6×10-11
2 3 a1 a2
A.向NaCO 溶液中滴加少量氯水:CO+2Cl+HO===2Cl-+2HClO+CO↑
2 3 2 2 2
B.向NaHCO 溶液中滴加少量氯水:2HCO+Cl===Cl-+ClO-+2CO↑+HO
3 2 2 2
C.向NaClO溶液中通少量CO:CO+NaClO+HO===NaHCO+HClO
2 2 2 3
D.向NaClO溶液中通过量CO:CO+2NaClO+HO===Na CO+2HClO
2 2 2 2 3
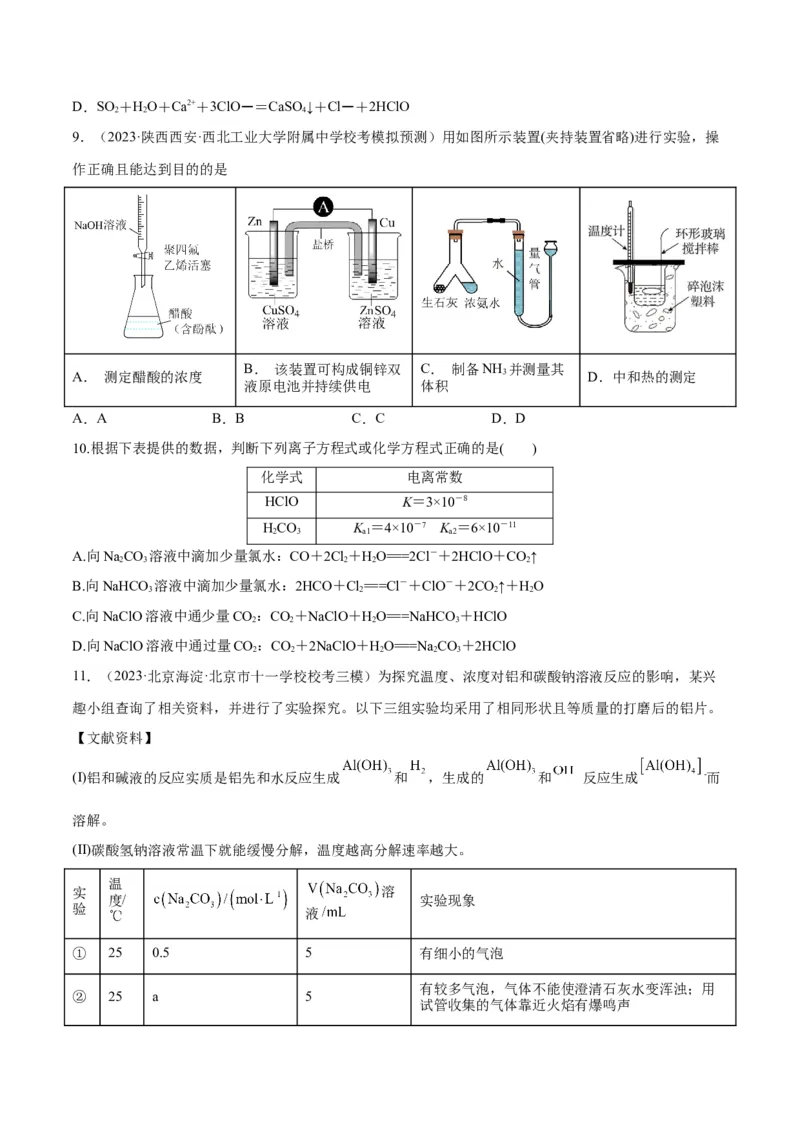
11.(2023·北京海淀·北京市十一学校校考三模)为探究温度、浓度对铝和碳酸钠溶液反应的影响,某兴
趣小组查询了相关资料,并进行了实验探究。以下三组实验均采用了相同形状且等质量的打磨后的铝片。
【文献资料】
(I)铝和碱液的反应实质是铝先和水反应生成 和 ,生成的 和 反应生成 -而
溶解。
(II)碳酸氢钠溶液常温下就能缓慢分解,温度越高分解速率越大。
温
实 溶
度/ 实验现象
验
液
① 25 0.5 5 有细小的气泡
有较多气泡,气体不能使澄清石灰水变浑浊;用
② 25 a 5
试管收集的气体靠近火焰有爆鸣声有大量白色絮状沉淀和气泡,气体可使澄清石灰
③ 80 2.0 5 水变浑浊;气体通过 溶液除杂后用试管收
集,靠近火焰有爆鸣声
下列说法不正确的是
A.
B.实验③的反应速率比实验②更大的原因之一是实验③中 浓度更大
C.实验③中的气体为 混合气体,白色沉淀的产生可能是由于 往溶液上方移动时与
反应生成
D.将实验②中的 溶液换成相同浓度的 溶液,无白色沉淀生成
12.(2022·临汾模拟)电离度是描述弱电解质电离程度的物理量,电离度=×100%。现取20 mL c(H+)=1×10
-3 mol·L-1的CHCOOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电能力的变化如图所示,则加入氨水
3
前CHCOOH的电离度为( )
3
A.0.5% B.1.5% C.0.1% D.1%
13.(2020·浙江选考)室温下,向20.00 mL 0.100 0 mol·L-1盐酸中滴加0.100 0 mol·L-1NaOH溶液,溶液的pH
随NaOH溶液体积的变化如图。已知lg 5=0.7。下列说法不正确的是( )
A.NaOH与盐酸恰好完全反应时,pH=7
B.选择变色范围在pH突变范围内的指示剂,可减小实验误差
C.选择甲基红指示反应终点,误差比甲基橙的大
D.V(NaOH)=30.00 mL时,pH=12.3
14.H SO 是一种弱酸,实验室欲用 0.01 mol·L-1的 NaSO 溶液滴定 I 溶液,发生的反应为 I +
2 2 3 2 2 3 2 22NaSO===2NaI+NaSO,下列说法合理的是( )
2 2 3 2 4 6
A.该滴定可用甲基橙作指示剂
B.Na SO 是该反应的还原剂
2 2 3
C.该滴定可选用如图所示装置
D.该反应中每消耗2 mol Na SO,电子转移数为4N
2 2 3 A
15.X、Y、Z、W分别是HNO 、NH NO 、NaOH、NaNO 四种强电解质中的一种。下表是常温下浓度均为
3 4 3 2
0.01 mol·L-1的X、Y、Z、W溶液的pH。
0.01 mol·L-1的溶液 X Y Z W
pH 12 2 8.5 4.5
(1)X、W的化学式分别为____________、_____________________。
(2)W在溶液中的电离方程式为_____________________________________________________。
(3)25 ℃时,Z溶液的pH>7的原因是_______________________________(用离子方程式表示)。
(4)将X、Y、Z各1 mol同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为
________________________________________________________________________。
(5)Z 溶液与 W 溶液混合加热,可产生一种无色无味的单质气体,该反应的化学方程式为
_________________________________________________________________________________。
17.(2023秋·山东青岛·高三青岛二中校考期末)化学反应速率是描述化学反应进行快慢程度的物理量。
下面是某同学测定化学反应速率并探究其影响因素的实验。
I.测定化学反应速率,该同学利用如图装置测定化学反应速率。
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是 ;
(2)该反应有黄色固体生成,并且伴有刺激性,能使品红溶液褪色的气体生成。请写出该反应的离子方程式: 。
(3)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比
实际值偏小,其原因是 。
II.为探讨化学反应速率的影响因素,设计的实验方案如下表。(已知2NaSO+I =Na SO+2NaI,其中
2 2 3 2 2 4 6
NaSO 溶液均足量)
2 2 3
体积V/mL
实验
时间/s
序号
NaSO 溶液 淀粉溶液 碘水 水
2 2 3
① 10.0 2.0 4.0 0.0 t
1
② 8.0 2.0 4.0 2.0 t
2
③ 6.0 2.0 4.0 V t
x 3
表中V= mL,比较t、t、t 大小,试推测该实验结论:
x 1 2 3
III.氧化还原滴定原理同中和滴定原理相似,为了测定某未知浓度的NaHSO 溶液的浓度,现用0.1000mol/L
3
的酸性KMnO 溶液进行滴定,离子方程式:2 +5 +H+=2Mn2++5 +3H O;回答下列问题:
4 2
(1)用KMnO 进行滴定时,判断滴定终点的现象是 。
4
(2)下列操作会导致测定结果偏低的是 。
A.酸式滴定管水洗后未用待测液润洗 B.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C. 滴定管尖嘴部分有气泡,滴定后消失 D.观察读数时,滴定前仰视,滴定后俯视
(3)根据下表中测定的实验数据,计算NaHSO 溶液的物质的量浓度(写出计算过程,结果保留4位有效数
3
字) 。
实验编
待测NaHSO 溶液的体积/mL KMnO 溶液的体积/mL
3 4
号
1 20.00 15.98
2 20.00 17.00
3 20.00 16.02
【拔高练习】
1.(2023·山东·统考高考真题)鉴别浓度均为 的 、 三种溶液,仅用
下列一种方法不可行的是A.测定溶液 B.滴加酚酞试剂
C.滴加 溶液 D.滴加饱和 溶液
2.(2023·上海徐汇·统考二模)在相同温度时100mL 0.01mol/L的醋酸溶液与10mL 0.1mol/L的醋酸溶液
相比较,下列数值前者大于后者的是
A.中和时所需NaOH的量 B.溶液的导电能力
C.H+的物质的量 D.CHCOOH的物质的量
3
3.(2023·浙江·校联考模拟预测)已知:室温下氢硫酸 的电离常数 , ;
和 的 分别为 、 ,下列说法不正确的是
A.反应 的平衡常数 的数值为
B.可以用 除去污水中的
C.从上述数据可得出 难溶于稀硫酸中
D. 的 溶液中加入等体积 的 溶液,则有:
4.某温度下,重水(D O)的离子积常数为1.6×10-15,若用定义pH一样规定pD=-lgc(D+),则在该温度
2
下,下列叙述正确的是( )
A.纯净的重水中,c(D+) ·c(OD-)>1.0×10-14
B.1 L溶解有0.01 mol DCl的重水溶液,其pD=2
C.1 L溶解有0.01 mol NaOD的重水溶液,其pD=12
D.纯净的重水中,pD=7
5.(2023·上海浦东新·统考二模)将pH传感器、氯离子传感器、氧气传感器分别插入盛有氯水的广口瓶
中,用强光照射,测得的实验数据如图所示。下列说法正确的是A.图甲中pH减小是由于光照促进了HClO的电离
B.图乙中 增大主要是由于反应消耗了水
C.图丙中氧气的体积分数增大是由于HClO的分解
D.该体系中存在两个电离平衡和两个化学平衡
6.(2023·浙江·校联考模拟预测)下列对于各实验操作及对应的实验现象分析正确的是
操作 现象 分析
适当升高 溶液的温度(不考 升温,对 、 电离的促进程度小于对
A 溶液 降低
虑 分解) 水解的促进程度
向盛有 溶液的试 管口产生红棕
B 被 还原为
色气体
管加入
25℃,测定 溶
C ,
液的
从2.5上升 打开盖后, 浓度(或压强)降低,促进
D 打开瓶盖,测定可乐溶液的 变化
到4.5左右 分解
A.A B.B C.C D.D
7.(2023·河北·校联考一模)下列离子方程式,不能正确解释相应现象的是
A.长期放置的 溶液中含有 :
B. 溶液中 :
C.向 溶液中加入适量 得到蓝色沉淀:
D.长期放置的 溶液中出现红棕色固体:8.(2023·河北·校联考一模)下列离子方程式,不能正确解释相应现象的是
A.长期放置的 溶液中含有 :
B. 溶液中 :
C.向 溶液中加入适量 得到蓝色沉淀:
D.长期放置的 溶液中出现红棕色固体:
9.(2023·北京海淀·清华附中校考三模)工业酸性废水中的 可转化为 除去,实验室用电解法模
拟该过程,结果如下表所示(实验开始时溶液体积为50 mL, 的起始浓度、电压、电解时间均相
同)。下列说法中,不正确的是
实验 ① ② ③
阴、阳极均为 阴、阳极均为石墨,滴加1 mL 阴极为石墨,阳极为铁,滴加1
电解条件
石墨 浓硫酸 mL浓硫酸
的去除
0.922 12.7 57.3
率/%
A.对比实验①②可知,降低pH可以提高 的去除率
B.实验②中, 在阴极放电的电极反应式是
C.实验③中, 去除率提高的原是
D.实验③中,理论上电路中每通过6 mol电子,则 被还原
10.常温下,向10 mL 1 mol·L-1一元酸HA溶液中,不断滴加1 mol·L-1的NaOH溶液,所加碱的体积与-
lg c (H+)的关系如图所示。c (H+)为溶液中水电离的c(H+)。下列说法不正确的是( )
水 水A.常温下,K(HA)的数量级为10-4
a
B.a、b两点pH均为7
C.从a点到b点,水的电离程度先增大后减小
D.溶液的导电性逐渐增强
11.(2023·上海松江·统考二模)常温下,向1LpH=10的NaOH溶液中持续通入CO,通入的CO 体积
2 2
(V)与溶液中水电离出的OH-离子浓度的关系如图所示。下列叙述不正确的是( )
A.a点溶液中:水电离出的c(H+)=1×10-10mol·L-1
B.b点溶液中:c(H+)=1×10-7mol·L-1
C.c点溶液中:c(Na+)>c(CO 2-)>c(HCO-)
3 3
D.d点溶液中:c(Na+)=2c(CO 2-)+c(HCO-)
3 3
12.(2023·浙江杭州·校联考模拟预测)对碳酸氢钠溶液进行一系列实验,根据现象得出的结论不正确的
是
选
实验操作 实验现象 实验结论
项
溶液变浑 与 反应生成 ,可说明
A 往饱和 溶液中通入
浊 溶解度小于
电离产生的 与 结合促进
溶液与 产生沉淀
B 并有气泡 平衡正移。使 增大,从面
溶液混合 冒出
产生 气体将 溶液加少 溶液的碱 稀释可以破坏 之间的氢键,使得 增
C
量水稀释 性增强 大,碱性增强
溶液pH 加热促进 和 的电离,使 增大,pH
D 将 溶液加热 先减小后
增大 减小,后由于分解生成 ,溶液pH增大
A.A B.B C.C D.D
13.(2022·新疆一模)化学上把外加少量酸、碱,而pH基本不变的溶液,称为缓冲溶液。
Ⅰ.现有25 ℃时,浓度均为0.10 mol/L的CHCOOH和CHCOONa的缓冲溶液,pH=4.76,回答下列问
3 3
题:[25 ℃时K(CHCOOH)=1.75×10-5,K 为盐的水解常数]
a 3 h
(1)25 ℃时K (CHCOO-)=____________(写表达式),计算K (CHCOO-)=____________(保留三位有效数
h 3 h 3
字)。
(2)该缓冲溶液中离子浓度由大到小的顺序是_________________________________________。
(3)向 1.0 L 上述缓冲溶液中滴加几滴 NaOH 稀溶液(忽略溶液体积的变化),反应后溶液中 c(H+)=
____________mol/L。
(4)改变下列条件,能使CHCOONa稀溶液中保持增大的是____________。
3
a.升温 b.加入NaOH固体 c.稀释
d.加入CHCOONa固体
3
Ⅱ.人体血液里主要通过碳酸氢盐缓冲体系()维持pH稳定。已知正常人体血液在正常体温时,HCO 的一级
2 3
电离常数K =10-6.1,≈,lg2=0.3。由题给数据可算得正常人体血液的pH约为____________,当过量的
a1
酸进入血液中时,血液缓冲体系中的值将____________(填“变大”“变小”或“不变”)。
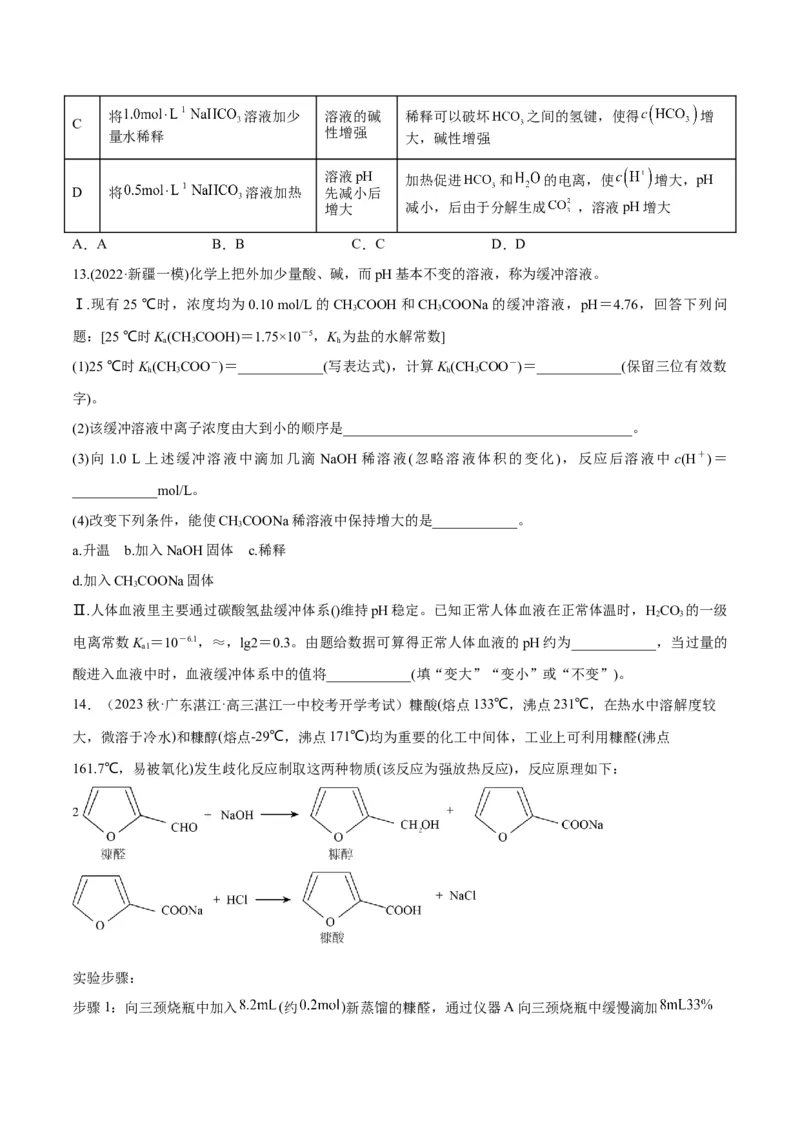
14.(2023秋·广东湛江·高三湛江一中校考开学考试)糠酸(熔点133℃,沸点231℃,在热水中溶解度较
大,微溶于冷水)和糠醇(熔点-29℃,沸点171℃)均为重要的化工中间体,工业上可利用糠醛(沸点
161.7℃,易被氧化)发生歧化反应制取这两种物质(该反应为强放热反应),反应原理如下:
实验步骤:
步骤1:向三颈烧瓶中加入 (约 )新蒸馏的糠醛,通过仪器A向三颈烧瓶中缓慢滴加的 溶液。搅拌并保持反应温度为8~12℃,回流 ,得到粗产品。
步骤2:将粗产品倒入盛有 水的烧杯中,然后将液体转移至分液漏斗中,用乙醚萃取4次,分液得到
水层和醚层。
步骤3:向水层中分批滴加25%的盐酸,调至溶液的 ,冷却、结晶、抽滤、冷水洗涤,得到糠酸粗
品;向醚层中加入无水碳酸钾干燥,过滤除掉碳酸钾后,分离乙醚(乙醚的沸点为34.6℃)和糠醇。
回答下列问题:
(1)仪器A的名称为 。与直形冷凝管相比,使用仪器B的优点是 。
(2)该反应必须严格控制反应温度为8~12℃,实验中采用了哪些保障措施? 。
(3)步骤3中分离乙醚和糠醇的实验操作为 。
(4)步骤3中洗涤粗糠酸用冷水的原因是 。进一步将粗糠酸提纯,应采用的方法是
。
(5)取 提纯后的糠酸样品,配成 溶液,准确量取 于锥形瓶中,加入几滴酚酞溶液,用
标准溶液滴定,平行滴定三次,平均消耗 标准溶液 。糠酸的纯度为
。该中和滴定实验中,若其他实验操作均正确,则下列实验操作造成测得的糠酸的纯度比实际偏低的是
(填标号)。
A.蒸馏水洗净后,末用 标准溶液润洗碱式滴定管
B.指示剂酚酞溶液滴加过多(酚酞是一种弱酸)
C.锥形瓶内壁用蒸馏水洗净后,再用配制好的糠酸样品溶液润洗2~3次,将润洗液倒掉,再装入
糠酸样品溶液,进行中和滴定
D.滴定前仰视碱式滴定管液面读数,滴定后俯视碱式滴定管液面读数