文档内容
专题 10 化学反应速率与平衡
第 27 练 化学平衡
1.在已经处于化学平衡的体系中,如果下列物理量发生变化,其中一定能表明平衡发生了移动的是(
)。
A.反应混合物的浓度 B.反应物的转化率
C.正、逆反应速率 D.反应混合物的压强
2.对于可逆反应:2SO (g)+O(g) 2SO (g),在一定温度下其平衡常数为K,下列条件的变化中,
2 2 3
能使K发生变化的是( )
A.缩小容器体积 B.降低体系温度
C.保持体积不变,充入O D.使用合适的催化剂
2
3.已知下列反应在某温度下的平衡常数:
H(g)+S(s) HS(g) K
2 2 1
S(s)+O(g) SO (g) K
2 2 2
则在该温度下反应H(g)+SO (g) O(g)+HS(g)的平衡常数为( )
2 2 2 2
A.K +K B.K -K C.K ×K D.K /K
1 2 1 2 1 2 1 2
4.在恒温下的密闭容器中,有可逆反应2NO(g)+O (g) 2NO (g) ΔH<0,不能说明反应已达
2 2
到平衡状态的是( )
A.正反应生成NO 的速率和逆反应生成O 的速率相等
2 2
B.反应器中压强不随时间变化而变化
C.混合气体颜色深浅保持不变
D.混合气体平均相对分子质量保持不变
5.可逆反应N+3H 2 NH 的正、逆反应速率可用各反应物或生成物浓度的变化来表示,下列
2 2 3
各关系中能说明反应已达到最大限度(即化学平衡)的是( )
A.N 将完全转化为NH B.N、H 和NH 的物质的量浓度相等
2 3 2 2 3
C.N、H 和NH 的物质的量浓度不再变化 D.正反应和逆反应的速率都为零
2 2 3
6.一定温度下的定容密闭容器中发生反应:A(s)+2B(g) C(g)+D(g),能说明该反应达到平衡
状态的是( )
A.v(B)∶v(C)∶v(D)=2∶1∶1B.Δn(A)∶Δn(B)∶Δn(C)∶Δn(D)=1∶2∶1∶1
C.混合气体的平均相对分子质量不再改变
D.混合气体总物质的量不再改变
7.一定条件下,在体积为1 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g)
Z(g),下列叙述能证明该反应已达到化学平衡状态的是( )
A.X的百分含量不再发生变化
B.c(X)∶c(Y)∶c(Z)=2∶1∶1
C.容器内原子总数不再发生变化
D.同一时间内消耗2n mol X的同时生成n mol Z
8.在一个不传热的固定容积的密闭容器中,可逆反应mA(气)+nB(气) pC(气)+qD(气)当m、
n、p、q为任意整数时,不能作为达到平衡的标志是( )
A.体系的压强不再改变 B.体系的温度不再改变
C.各组分的浓度不再改变 D.各组分的质量分数不再改变
9.在下列可逆反应中,增大压强或降低温度,均可使平衡正向移动的是( )
A.2SO (g)+O(g) 2SO (g) ΔH<0
2 2 3
B.4NH (g)+5O(g) 4NO(g)+6H O(g)ΔH<0
3 2 2
C.2NH (g) N(g)+3H(g) ΔH>0
3 2 2
D.SO (g)+NO (g) SO (g)+NO(g) ΔH<0
2 2 3
10.可逆反应N+3H 2NH (正反应为放热反应)达到平衡后,下列方法能使平衡向正反应方向移
2 2 3
动的是( )
A.升高温度 B.增大压强 C.增加氨气 D.使用催化剂
11.已知反应:COCl (g) CO(g)+Cl (g) ,当反应达到平衡时,下列能提高COCl 转化率
2 2 2
的措施的是( )
A.恒容通入惰性气体 B.增加CO浓度
C.加催化剂 D.恒压通入惰性气体
1.在一定温度下,固定的容积中,对反应A(s)+ 2B(g) 3C (g),不能说明该反应已达到平衡的
是( )
A.C生成的速率与C分解的速率相等
B.单位时间内消耗a mol A,同时生成3a mol C
C.容器内的压强不再变化D.混合气体的密度不再变化
2.在一定温度下,在恒定容积的密闭容器中进行的可逆反应A(g)+B (g) 2AB(g)达到化学平衡
2 2
的标志是( )
A.容器内的总压强不随时间而变化
B.反应速率v(A )=v(B )= v(AB)
2 2
C.单位时间内有nmol A 生成的同时就有2nmol AB生成
2
D.容器内混合气体的密度不随时间而变化
3.在一密闭容器中进行如下反应:2SO (g)+O(g) 2SO (g),已知反应过程中某一时刻SO 、
2 2 3 2
O、SO 的浓度分别为0.2 mol/L、0.1 mol/L、0.2 mol/L,当反应达平衡时,可能存在的数据是( )
2 3
A.SO 为0.4 mol/L、O 为0.2 mol/L B.SO 、SO 均为0.15 mol/L
2 2 2 3
C.SO 为0.25 mol/L D.SO 为0.4 mol/L
3 3
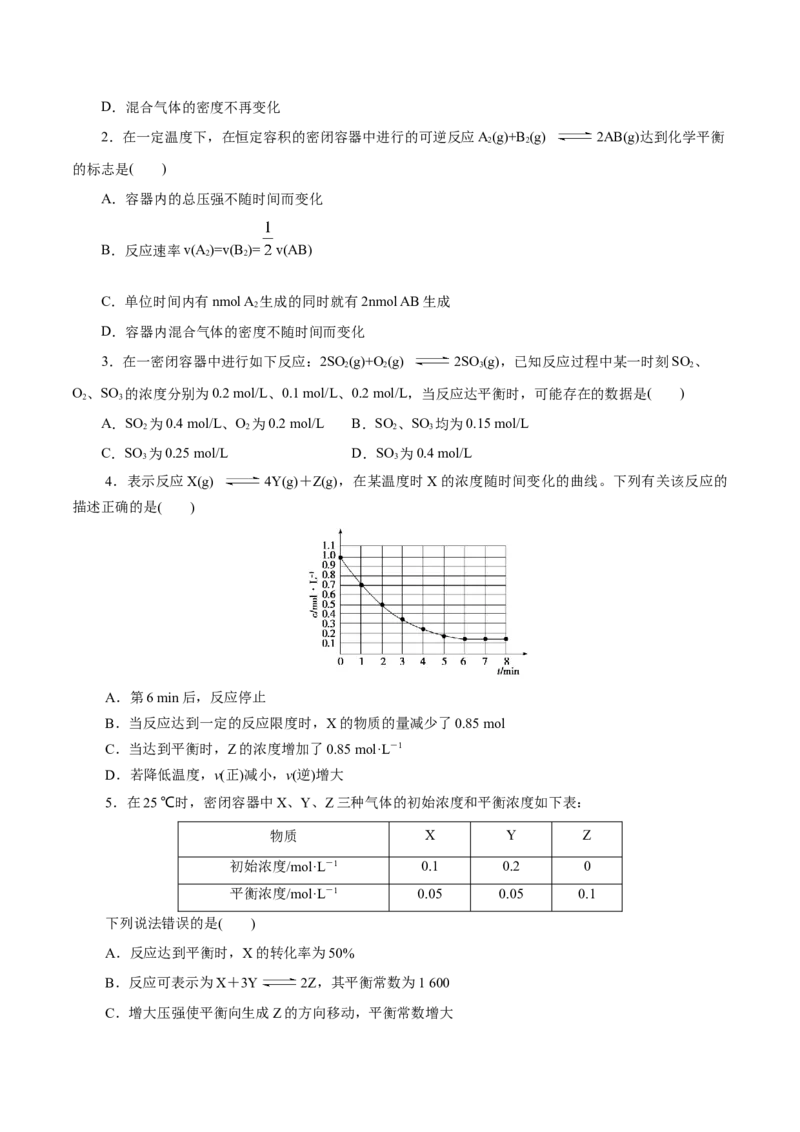
4.表示反应X(g) 4Y(g)+Z(g),在某温度时X的浓度随时间变化的曲线。下列有关该反应的
描述正确的是( )
A.第6 min后,反应停止
B.当反应达到一定的反应限度时,X的物质的量减少了0.85 mol
C.当达到平衡时,Z的浓度增加了0.85 mol·L-1
D.若降低温度,v(正)减小,v(逆)增大
5.在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 X Y Z
初始浓度/mol·L-1 0.1 0.2 0
平衡浓度/mol·L-1 0.05 0.05 0.1
下列说法错误的是( )
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y 2Z,其平衡常数为1 600
C.增大压强使平衡向生成Z的方向移动,平衡常数增大D.改变温度可以改变此反应的平衡常数
6.一定温度下,将2 mol A和2 mol B两种气体混合放入体积为2 L的密闭刚性容器中,发生反应
3A(g)+B(g) xC(g)+2D(g),2 min末反应达到平衡,生成0.8 mol D,并测得C的物质的量浓度为
0.4 mol·L-1,下列说法正确的是( )
A.x的值为1
B.A的平衡转化率为40%
C.此温度下该反应的平衡常数K的数值等于0.5
D.A和B的平衡转化率相等
7.在一密闭容器中发生反应:2A(g)+2B(g) C(s)+3D(g) ΔH<0,达到平衡时采取下列措施,
可以使正反应速率v 增大、D的物质的量浓度c(D)增大的是( )
正
A.移走少量C B.扩大容积,减小压强
C.缩小容积,增大压强 D.体积不变,充入“惰”气
8.在一密闭容器中,反应 3A(g)+B(s) 2Cg)+D(g) 达到平衡后,改变以下条件,下列说
法正确的是( )
A.增加A的浓度,平衡向正反应方向移动,平衡常数增大
B.升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动
C.恒温恒容充入Ne,容器内压强增大,V(正)、V(逆)均增大
D.增加B的用量,正、逆反应速率不变,平衡不移动
9.10mL0.1mol•L-1KI溶液与5mL0.1mol•L-1FeCl 溶液发生反应:2Fe3+(aq)+2I-(aq) 2Fe2+(aq)
3
+I (aq),达到平衡。下列说法不正确的是( )
2
A.加入少量氯化钾固体,平衡不移动
B.加适量水稀释,平衡正向移动
C.经过CCl 多次萃取分离后,向水溶液中滴加KSCN溶液,若溶液出现血红色,证明该化学反应存
4
在限度
D.该反应的平衡常数K=
10.等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达平衡:X(g)
+2Y(g) 3Z(g) H<0,当改变某个条件并达到新平衡后,下列叙述正确的是( )
A.升高温度,X△的体积分数减小
B.增大压强,Z的浓度不变
C.保持容器体积不变,充入一定量的惰性气体,Y的浓度不变D.保持容器体积不变,充入一定量的Z,X的体积分数增大
10.将5mL0.005mol·L-1FeCl 溶液和5mL0.015mol·L-1KSCN溶液混合,达到平衡后混合液呈红色。再
3
将混合液分为5等份,分别进行如下实验:
实验①:滴加4滴水,振荡
实验②:滴加4滴饱和FeCl 溶液,振荡
3
实验③:滴加4滴1mol·L-1KCl溶液,振荡
实验④:滴加4滴1mol·L-1KSCN溶液,振荡
实验⑤:滴加4滴6mol·L-1NaOH溶液,振荡
下列说法不正确的是( )
A.实验②中溶液颜色比实验①中深
B.对比实验①和③,可证明增加反应物中某些离子的浓度,平衡发生逆向移动
C.对比实验①和④,可证明增加反应物浓度,平衡发生正向移动
D.对比实验①和⑤,可证明减少反应物浓度,平衡发生逆向移动
11.T℃时,将2.0molA(g)和2.0molB(g)充入体积为1L的密闭容器中,在一定条件发生下述反应:
A(g)+B(g) 2C(g)+D(s) H<0;t 时刻时A物质的量为1.2mol,t 时刻时C(g)浓度为2.0mol/L并保持
1 2
不变。下列说法正确的是( △ )
A.t 时刻的逆反应速率 > t 时刻的正反应速率
1 2
B.T℃时该反应的化学平衡常数K=2
C.T 时刻反应达到平衡,然后缩小容器体积,平衡逆向移动
2
D.T℃时,若将A(g)、B(g)各1.0mol充入同样容器,平衡后,A的转化率为50%
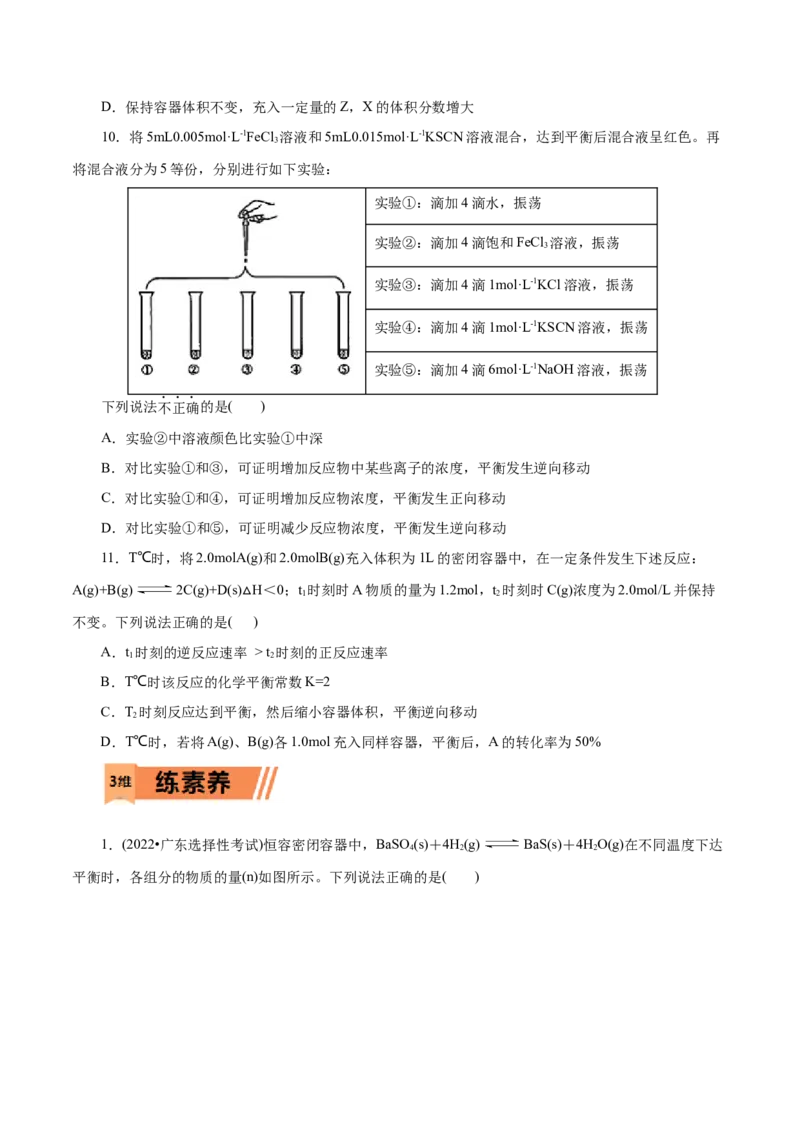
1.(2022•广东选择性考试)恒容密闭容器中,BaSO(s)+4H(g) BaS(s)+4HO(g)在不同温度下达
4 2 2
平衡时,各组分的物质的量(n)如图所示。下列说法正确的是( )A.该反应的ΔH<0
B.a为n(H O)随温度的变化曲线
2
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入BaSO,H 的平衡转化率增大
4 2
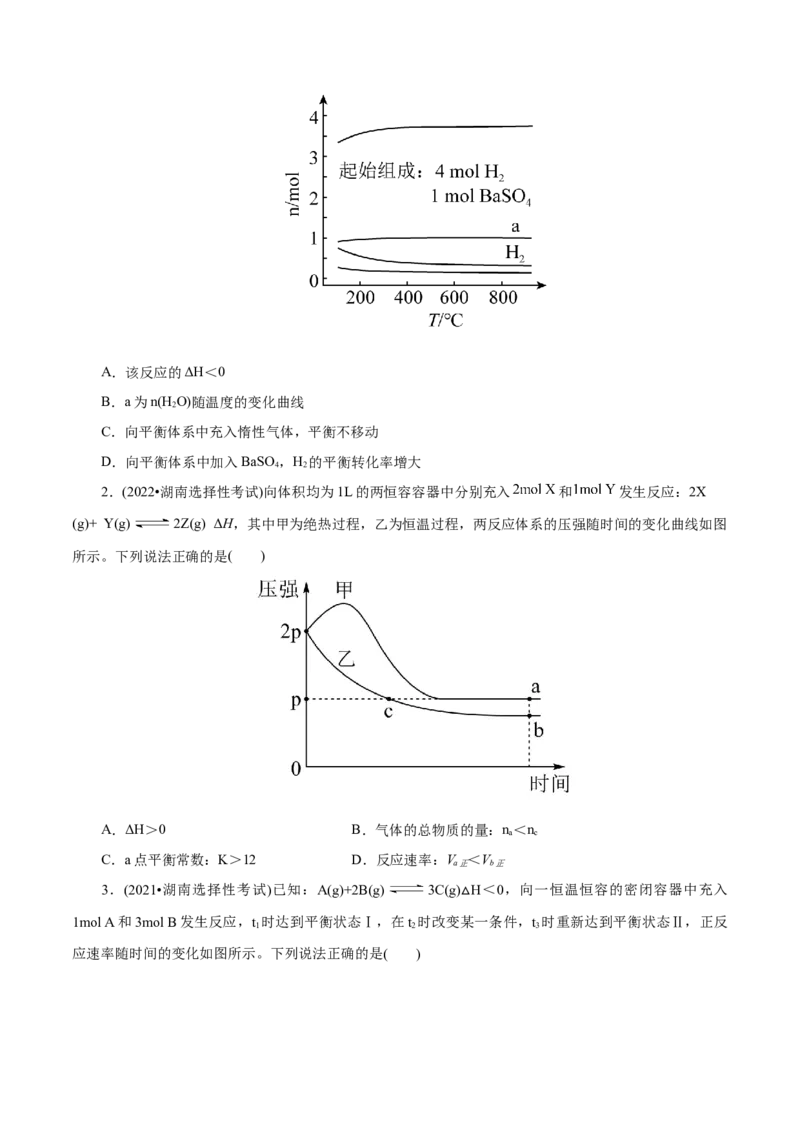
2.(2022•湖南选择性考试)向体积均为1L的两恒容容器中分别充入 和 发生反应:2X
(g)+ Y(g) 2Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图
所示。下列说法正确的是( )
A.ΔH>0 B.气体的总物质的量:n<n
a c
C.a点平衡常数:K>12 D.反应速率:V <V
a正 b正
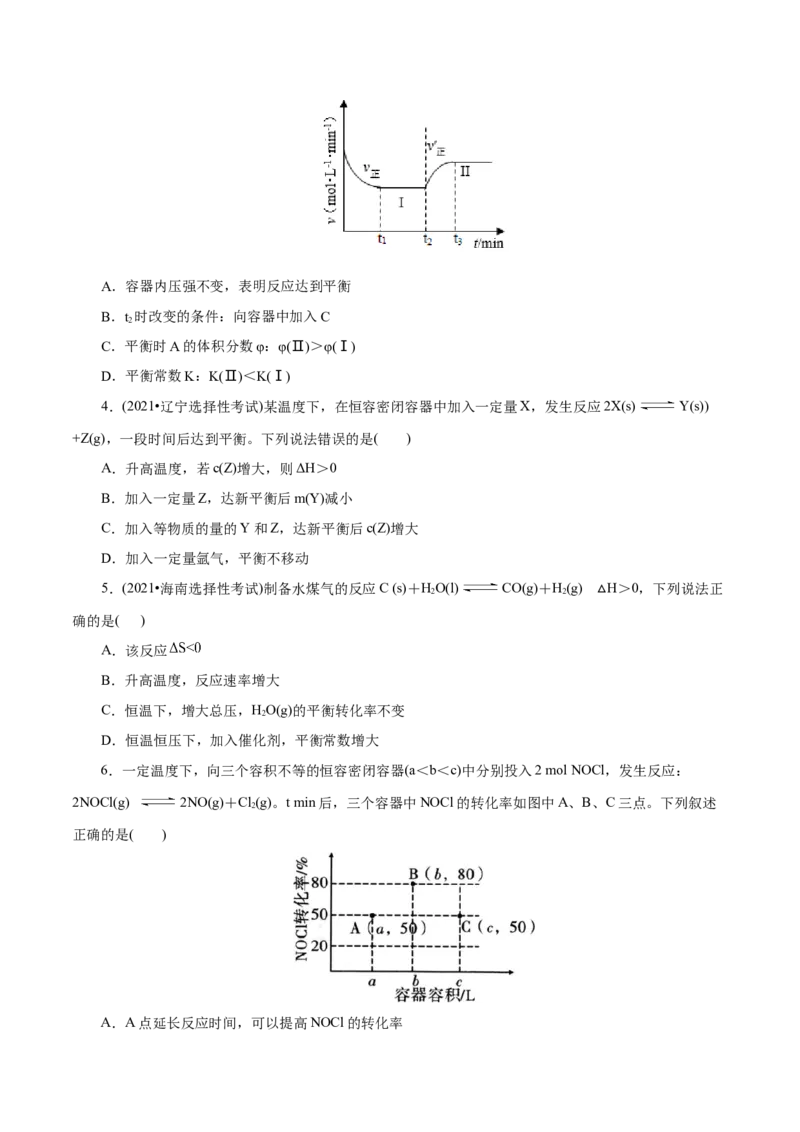
3.(2021•湖南选择性考试)已知:A(g)+2B(g) 3C(g) H<0,向一恒温恒容的密闭容器中充入
1mol A和3mol B发生反应,t 时达到平衡状态Ⅰ,在t 时改变某△一条件,t 时重新达到平衡状态Ⅱ,正反
1 2 3
应速率随时间的变化如图所示。下列说法正确的是( )A.容器内压强不变,表明反应达到平衡
B.t 时改变的条件:向容器中加入C
2
C.平衡时A的体积分数φ:φ(Ⅱ)>φ(Ⅰ)
D.平衡常数K:K(Ⅱ)<K(Ⅰ)
4.(2021•辽宁选择性考试)某温度下,在恒容密闭容器中加入一定量X,发生反应2X(s) Y(s))
+Z(g),一段时间后达到平衡。下列说法错误的是( )
A.升高温度,若c(Z)增大,则ΔH>0
B.加入一定量Z,达新平衡后m(Y)减小
C.加入等物质的量的Y和Z,达新平衡后c(Z)增大
D.加入一定量氩气,平衡不移动
5.(2021•海南选择性考试)制备水煤气的反应C (s)+HO(l) CO(g)+H(g) H>0,下列说法正
2 2
确的是( ) △
A.该反应
B.升高温度,反应速率增大
C.恒温下,增大总压,HO(g)的平衡转化率不变
2
D.恒温恒压下,加入催化剂,平衡常数增大
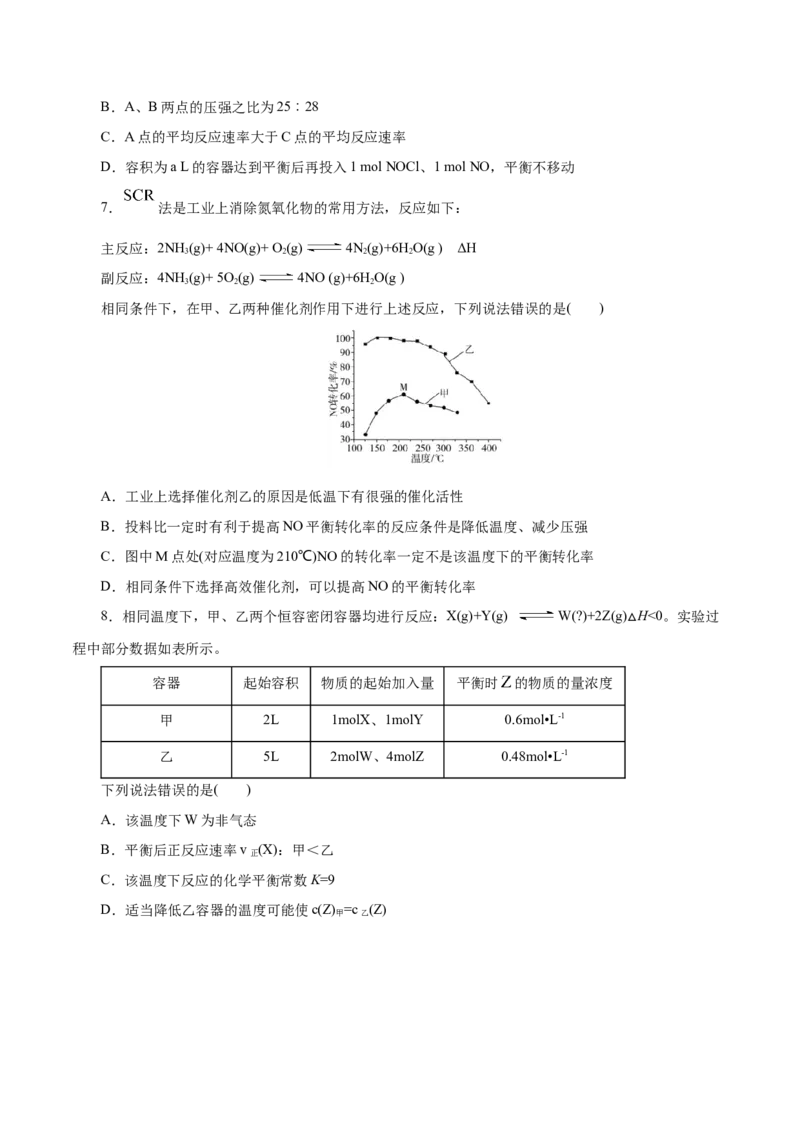
6.一定温度下,向三个容积不等的恒容密闭容器(a<b<c)中分别投入2 mol NOCl,发生反应:
2NOCl(g) 2NO(g)+Cl(g)。t min后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述
2
正确的是( )
A.A点延长反应时间,可以提高NOCl的转化率B.A、B两点的压强之比为25︰28
C.A点的平均反应速率大于C点的平均反应速率
D.容积为a L的容器达到平衡后再投入1 mol NOCl、1 mol NO,平衡不移动
7. 法是工业上消除氮氧化物的常用方法,反应如下:
主反应:2NH (g)+ 4NO(g)+ O (g) 4N(g)+6HO(g ) ΔH
3 2 2 2
副反应:4NH (g)+ 5O (g) 4NO (g)+6HO(g )
3 2 2
相同条件下,在甲、乙两种催化剂作用下进行上述反应,下列说法错误的是( )
A.工业上选择催化剂乙的原因是低温下有很强的催化活性
B.投料比一定时有利于提高NO平衡转化率的反应条件是降低温度、减少压强
C.图中M点处(对应温度为210℃)NO的转化率一定不是该温度下的平衡转化率
D.相同条件下选择高效催化剂,可以提高NO的平衡转化率
8.相同温度下,甲、乙两个恒容密闭容器均进行反应:X(g)+Y(g) W(?)+2Z(g) H<0。实验过
程中部分数据如表所示。 △
容器 起始容积 物质的起始加入量 平衡时 的物质的量浓度
甲 2L 1molX、1molY 0.6mol•L-1
乙 5L 2molW、4molZ 0.48mol•L-1
下列说法错误的是( )
A.该温度下W为非气态
B.平衡后正反应速率v (X):甲<乙
正
C.该温度下反应的化学平衡常数K=9
D.适当降低乙容器的温度可能使c(Z) =c (Z)
甲 乙