文档内容
第 26 讲 难溶电解质的溶解平衡
目录
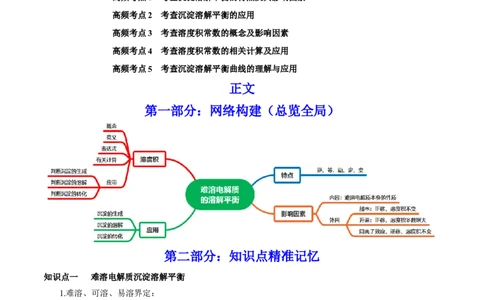
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查沉淀溶解平衡的特点及其影响因素
高频考点2 考查沉淀溶解平衡的应用
高频考点3 考查溶度积常数的概念及影响因素
高频考点4 考查溶度积常数的相关计算及应用
高频考点5 考查沉淀溶解平衡曲线的理解与应用
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 难溶电解质沉淀溶解平衡
1.难溶、可溶、易溶界定:
20 ℃时,电解质在水中的溶解度与溶解性存在如下关系:
2.沉淀溶解平衡
(1)含义
在一定温度下的水溶液中,当难溶电解质沉淀溶解和生成的速率相等时,即建立了沉淀溶解平衡状态。
(2)溶解平衡的建立
溶质溶解的过程是一个可逆过程:固体溶质 溶液中的溶质
(3)特点(同其他化学平衡):逆、等、定、动、变(适用平衡移动原理)
3.影响沉淀溶解平衡的因素
(1)内因:难溶电解质本身的性质,这是决定因素。
(2)外因
①浓度:加水稀释,平衡向沉淀溶解的方向移动;
②温度:绝大多数难溶电解质的溶解是吸热过程,升高温度,平衡向沉淀溶解的方向移动;
③同离子效应:向平衡体系中加入难溶电解质溶解产生的离子,平衡向生成沉淀的方向移动;
④其他:向平衡体系中加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子时,平衡向沉淀
溶解的方向移动。
(3)实例:以AgCl(s) Ag+(aq)+Cl-(aq)为例,填写外界条件对溶解平衡的影响。
外界条件 移动方向 平衡后c(Ag+) 平衡后c(Cl-) K
sp
升高温度 正向 增大 增大 增大
加水稀释 正向 不变 不变 不变
加入少量AgNO(s) 逆向 增大 减小 不变
3
通入HCl(g) 逆向 减小 增大 不变
通入HS(g) 正向 减小 增大 不变
2
4.沉淀溶解平衡的应用
(1)沉淀的生成
①调节pH法
如除去 NH Cl 溶液中的 FeCl 杂质,可加入氨水调节 pH 至 7~8,离子方程式为 Fe3++
4 3
3NH ·H O===Fe(OH) ↓+3NH。
3 2 3②沉淀剂法:如用HS沉淀Cu2+,离子方程式为HS+Cu2+===CuS↓+2H+。
2 2
(2)沉淀的溶解
①酸溶解法:如CaCO 溶于盐酸,离子方程式为CaCO +2H+===Ca2++HO+CO↑。
3 3 2 2
②盐溶液溶解法:如Mg(OH) 溶于NH Cl溶液,离子方程式为Mg(OH) +2NH===Mg2++2NH ·H O。
2 4 2 3 2
③氧化还原溶解法:如不溶于盐酸的硫化物Ag S溶于稀HNO。
2 3
④配位溶解法:如AgCl溶于氨水,离子方程式为AgCl+2NH ·H O===[Ag(NH )]++Cl-+2HO。
3 2 3 2 2
(3)沉淀的转化
①实质:沉淀溶解平衡的移动(沉淀的溶解度差别越大,越容易转化,易溶的转化为难溶的)。
如AgNO 溶液――→AgCl(白色沉淀)――→AgBr(浅黄色沉淀)――→AgI(黄色沉淀)――→Ag S(黑色沉淀)。
3 2
②沉淀转化的三种情况
1)难溶的物质转化为更难溶的物质较易实现。
2)K 相差不大时,K 小的物质可以转化为K 大的物质。如K (BaCO)=5.1×10-9>K (BaSO)=1.1×10-
sp sp sp sp 3 sp 4
10,通过增大CO的浓度,可以实现BaSO(s)+CO(aq) BaCO (s)+SO(aq)。
4 3
3)K 相差很大时,K 小的物质不能转化为K 大的物质。
sp sp sp
③应用
a.锅炉除垢:将 CaSO 转化为易溶于酸的 CaCO ,离子方程式为 CaSO(s)+CO(aq) CaCO (s)+
4 3 4 3
SO(aq)。
b.矿物转化:CuSO 溶液遇PbS转化为CuS,离子方程式为Cu2+(aq)+PbS(s) CuS(s)+Pb2+(aq)。
4
【易错提醒】(1)沉淀溶解平衡移动过程是固体溶解和析出的相互转化过程,属于物理变化,但遵循勒夏特
列原理。
(2)沉淀溶解达到平衡时,再加入该难溶物对平衡无影响。
(3)用沉淀法除杂不可能将杂质离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于 1×10-5
mol·L-1时,沉淀已经完全。
(4)对于化学式中阴、阳离子个数比不同的难溶物,不能直接根据 K 的大小来确定其溶解能力的大小,需
sp
通过计算转化为溶解度。
知识点二 溶度积常数
1.溶度积和离子积
以A B (s) mAn+(aq)+nBm-(aq)为例:
m n
溶度积 离子积
概念 沉淀溶解的平衡常数 溶液中有关离子浓度幂的乘积
符号 K Q
sp c
K (A B )=cm(An+)·cn(Bm-),式中的 Q(A B )=cm(An+)·cn(Bm-),式
表达式 sp m n c m n
浓度都是平衡浓度 中的浓度都是任意浓度
应用 判断在一定条件下沉淀能否生成或溶解①Q>K :溶液过饱和,有沉淀析出
c sp
②Q=K :溶液饱和,处于平衡状态
c sp
③Q<K :溶液未饱和,无沉淀析出
c sp
2.K 的影响因素
sp
(1)内因:难溶物质本身的性质,这是主要决定因素。
(2)外因
①浓度:加水稀释,平衡向溶解方向移动,但K 不变。
sp
②温度:绝大多数难溶盐的溶解是吸热过程,升高温度,平衡向溶解方向移动,K 增大。
sp
③其他:向平衡体系中加入可与体系中某些离子反应生成更难溶物质或更难电离物质或气体的离子时,平
衡向溶解方向移动,但K 不变。
sp
【易错提醒】(1)K 只与难溶电解质的性质和温度有关,与沉淀的量无关。
sp
(2)溶液中离子浓度的变化只能使溶解平衡移动,并不能改变溶度积。
(3)沉淀的生成和溶解相互转化的条件是离子浓度的大小,改变反应所需的离子浓度,可使反应向着所需的
方向转化。
(4)K 小的难溶电解质也能向K 大的难溶电解质转化,需看溶液中生成沉淀的离子浓度的大小。
sp sp
知识点三 水溶液中的离子平衡图像分析
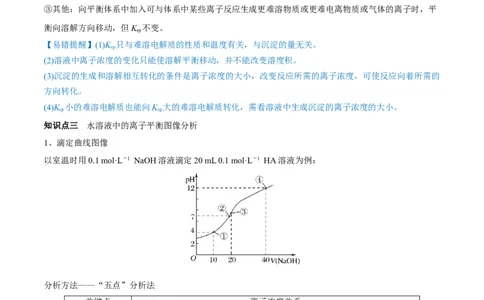
1、滴定曲线图像
以室温时用0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1 HA溶液为例:
分析方法——“五点”分析法
关键点 离子浓度关系
原点为HA的单一溶液,0.1 mol·L-1 HA溶液pH>1说明HA是弱酸;
原点(点O)
c(HA)>c(H+)>c(A-)>c(OH-)
反应一半点 两者反应生成等物质的量的NaA和HA混合液,此时溶液pH<7,说明HA
(点①)
的电离程度大于A-的水解程度,c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-)
中性点 此时溶液pH=7,溶液显中性,酸没有完全被中和,c(Na+)=c(A-)>c(HA)
(点②)
>c(H+)=c(OH-)
恰好完全反 此时二者恰好完全反应生成NaA,NaA为强碱弱酸盐,溶液显碱性,c(Na
应点(点③)
+)>c(A-)>c(OH-)>c(HA)>c(H+)过量点 此时,NaOH溶液过量,得到NaA与NaOH等物质的量的混合液,溶液显
(点④)
碱性,c(Na+)>c(OH-)>c(A-)>c(H+)
2、分布曲线图像
分布曲线是指以pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标的关系曲线。
一元弱酸(以CHCOOH为例) 二元弱酸(以草酸HC O 为例)
3 2 2 4
δ 为CHCOOH分布系数,δ 为CHCOO- δ 为HC O 分布系数、δ 为HC O分布
0 3 1 3 0 2 2 4 1 2
分布系数 系数、δ 为C O分布系数
2 2
随着pH增大,溶质分子浓度不断减小,离子浓度逐渐增大,酸根离子增多。根据分
布系数可以书写一定pH时所发生反应的离子方程式
同一pH条件下可以存在多种溶质微粒。根据在一定pH的微粒分布系数和酸的起始
浓度,就可以计算各成分在该pH时的平衡浓度
3、沉淀溶解平衡图像
1)沉淀溶解平衡曲线类似于溶解度曲线,曲线上任一点都表示饱和溶液,都是相应温度下恰好生成沉淀
时的离子浓度,同一温度下有相同的K 。
sp
2)分析沉淀溶解平衡图像的三步骤
(1)明确图像中纵、横坐标的含义
(2)理解图像中线上的点、线外点的含义
(3)抓住K 的特点,结合选项分析判断
sp
第三部分:典型例题剖析
高频考点1 考查沉淀溶解平衡的特点及其影响因素
例1.(2022·山东日照·模拟预测)某同学设计实验探究影响沉淀溶解平衡的因素,有关实验操作如下:
ⅰ.取规格相同的两支试管①和②,先向试管①中加入少量 黄色固体,并插入电导率测试仪,然后分别
加入等体积 饱和溶液;ⅱ.向试管①和②中分别滴入1滴 溶液,观察沉淀变化情况,一段
时间后向①中滴入少量蒸馏水,测得溶液电导率变化如图2所示。下列说法错误的是
A.滴加 溶液①②中产生 固体 B.b到c过程中①中固体质量减小
C.c点时溶液中 :①=② D.b点:
【答案】C
【解析】A.向 饱和溶液加入KI溶液,I-浓度增大,溶解平衡 逆向移动,①②中产生
固体,A正确;B.b到c过程中加水稀释平衡正向移动,①中固体质量减小,B正确;C.向①中加
水稀释c(I-)减小,则 增大,c点时溶液中 :①>②,C错误;D.b点为试管①加入蒸馏水稀
释促进 溶解,平衡正向移动,此时浓度商小于平衡常数,则Qc= ,D正确;
故选:C。
【易错提醒】(1)沉淀溶解平衡移动过程是固体溶解和析出的相互转化过程,属于物理变化,但遵循勒夏特
列原理。
(2)沉淀溶解达到平衡时,再加入该难溶物对平衡无影响。
(3)难溶电解质不一定是弱电解质,如BaSO、AgCl等都是强电解质。
4
(4)用沉淀法除杂不可能将杂质离子全部通过沉淀除去。一般认为残留在溶液中的离子浓度小于 1×10-5
mol·L-1时,沉淀已经完全。
【变式训练】(2021·辽宁葫芦岛·高三阶段练习)下列有关 沉淀溶解平衡的说法中错误的是
A. 的溶度积常数表达式
B. 难溶于水,溶液中没有 和SO
C.升高温度, 的溶解度增大D.向 悬浊液中加入 固体, 溶解的量减少
【解析】A.BaSO 难溶于水,悬浊液中存在BaSO(s) Ba2+(aq)+SO (aq),根据溶度积数学表达式,
3 3
推出K =c(Ba2+)×c(SO ),故A说法正确;B.BaSO 虽难溶于水,BaSO 在水中溶解度较小,但溶液中有
sp 3 3
极少量的Ba2+和SO ,故B说法错误;C.多数物质的溶解度随着温度升高而升高,升高温度,BaSO 的
3
溶解度增大,故C说法正确;D.BaSO 悬浊液中存在BaSO(s) Ba2+(aq)+SO (aq),加入NaSO 固
3 3 2 3
体,溶液中c(SO )增大,c(Ba2+)减少,BaSO 溶解的量减少,故D说法正确;答案为B。
3
【答案】B
高频考点2 考查沉淀溶解平衡的应用
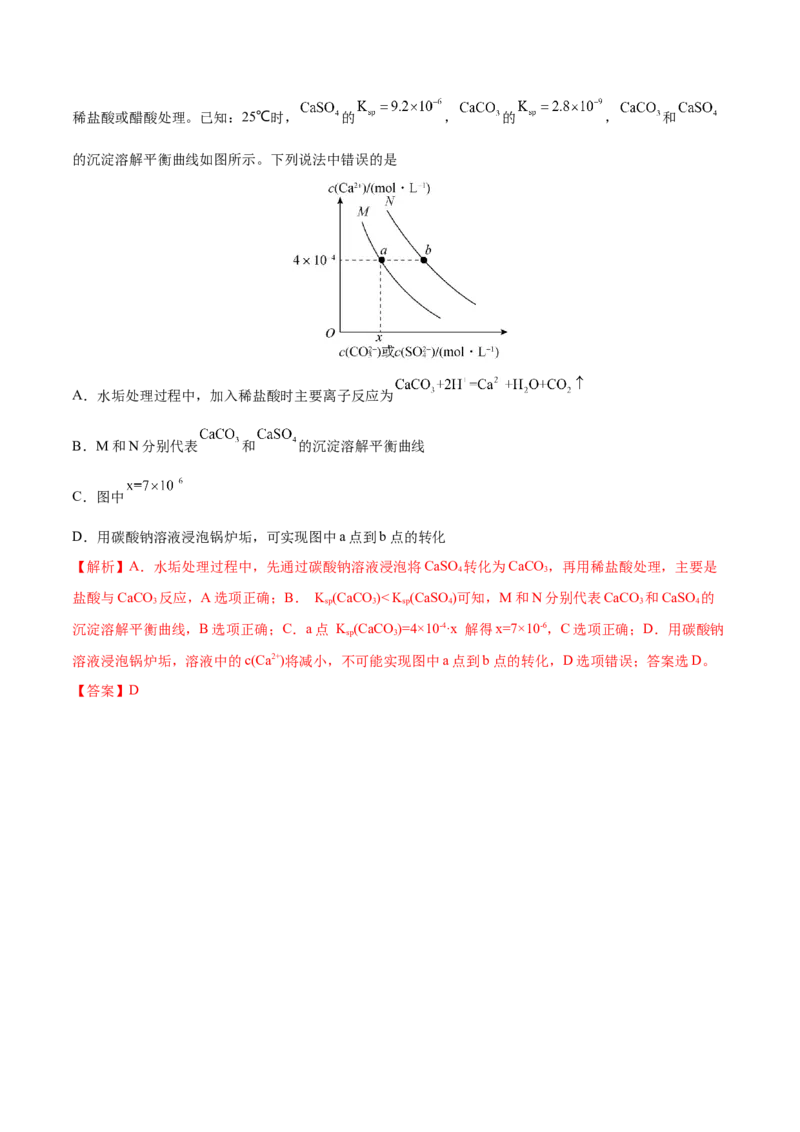
例2.(2022·全国·高三专题练习)往锅炉注入NaCO 溶液浸泡,将水垢中的CaSO 转化为CaCO ,再用盐
2 3 4 3
酸除去,下列叙述中正确的是 ( )
A.温度升高,NaCO 溶液的K 和c(H+)均会增大
2 3 w
B.CaSO 能转化为CaCO ,说明K (CaCO)>K (CaSO)
4 3 sp 3 sp 4
C.CaCO 溶解于盐酸而CaSO 不溶,是因为硫酸酸性强于盐酸
3 4
D.沉淀转化的离子方程式为CO(aq)+CaSO(s ) CaCO (s)+SO(aq)
4 3
【解析】温度升高,水的电离平衡正向移动,K 增大;温度升高,NaCO 的水解平衡正向移动,c(OH-)
w 2 3
增大,c(H+)减小,A项错误。一般说来溶解度小的沉淀易转化成溶解度更小的沉淀,故
K (CaCO)5∶4
C.向混合溶液中逐滴加入0.1 mol·L-1 NaOH溶液,最先看到红褐色沉淀
D.向混合溶液中加入适量氯水,并调节pH到3~4过滤,可获较纯净的CuSO 溶液
4
【解析】在pH=5的溶液中氢氧根的浓度是10-9 mol·L-1,铁离子的浓度是0.5 mol·L-1,则浓度商=1×10
-27>4×10-38,所以有氢氧化铁沉淀产生,则Fe3+不能大量存在,A正确;由于在溶液中金属阳离子均水解,
则混合溶液中c(SO)∶[c(Fe3+)+c(Fe2+)+c(Cu2+)]>5∶4,B正确;
根据三种物质的溶度积常数可知分别形成沉淀时需要氢氧根的浓度分别是、、 ,因此向混合溶液中逐滴
加入0.1 mol·L-1 NaOH溶液,首先生成氢氧化铁沉淀,则最先看到红褐色沉淀,C正确;向混合溶液中加
入适量氯水,并调节pH到3~4过滤,得到的是硫酸、盐酸和CuSO 的混合溶液,D错误。
4
【答案】D
【规律总结】(1)已知溶度积求溶液中的某种离子的浓度,如K =a的饱和AgCl溶液中c(Ag+)=c(Cl-)=
sp
mol·L-1。
(2)已知溶度积溶液中某离子的浓度,求溶液中的另一种离子的浓度,如某温度下 AgCl的K =a,在0.1
sp
mol·L-1的NaCl溶液中加入过量的AgCl固体,达到平衡后c(Ag+)=10a mol·L-1。【变式训练】(2021·全国·高三专题练习)还原沉淀法是处理含铬(含Cr O和CrO)工业废水的常用方法,
2
过程如下:
CrO――→Cr O――→Cr3+――→Cr(OH) ↓
2 3
已知转换过程中的反应为:2CrO(aq)+2H+(aq) Cr O(aq)+HO(l)。转化后所得溶液中铬元素的含量为
2 2
28.6 g/L,CrO有10/11转化为Cr O,下列说法不正确的是( )
2
A.溶液颜色保持不变,说明上述可逆反应达到平衡状态
B.若用绿矾(FeSO ·7H O)作还原剂,处理1 L废水,至少需要458.7 g
4 2
C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5
D.常温下K [Cr(OH) ]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5 mol·L-1,应调溶液的pH=5
sp 3
【解析】A.存在平衡:2CrO(aq,黄色)+2H+(aq) Cr O(aq,橙色)+HO(l),如颜色不变,说明浓度
2 2
不变,则达到平衡状态,故A说法正确;B.若用绿矾作还原剂,处理1 L废水,设需要x mol
FeSO ·7H O,由得失电子数目相等可知×(6-3)=x·(3-2),解得x=1.65,m(FeSO ·7H O)=1.65 mol×278
4 2 4 2
g/mol=458.7 g,故B说法正确;C.转化后所得溶液中铬元素含量为28.6 g/L,则1 L废水中n(Cr)=28.6
g÷52 g/mol=0.55 mol,CrO有10/11转化为Cr O,则酸化后c(CrO)=0.55 mol·L-1×(1-10/11)=0.05 mol·L-
2
1,c(CrO)=0.55 mol·L-1×10/11×1/2=0.25 mol·L-1,常温下转换反应的平衡常数K=1×1014,则
2
c(CrO)/[c2(CrO)·c2(H+)]=1×1014,解得c(H+)=1×10-6 mol·L-1,所以pH=6,故C说法错误;D.常温下
2
K [Cr(OH) ]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5 mol·L-1,则c(Cr3+)×c3(OH-)=1×10-32,
sp 3
解得c(OH-)=1×10-9 mol·L-1,pH=5,故D说法正确。
【答案】C
高频考点5 考查沉淀溶解平衡曲线的理解与应用
例5.(2022·广西柳州·模拟预测)难溶盐MA在水中溶解为吸热过程,其沉淀溶解平衡曲线如图所示。下
列说法错误的是
A.图中温度
B. 温度下, 值为C.在 温度下,加适量的NaA固体可使饱和溶液由p点变到n点
D.向q点的饱和溶液中滴加NaA溶液,立即析出MA沉淀
【解析】A.难溶盐MA在水中溶解为吸热过程,温度越高离子浓度越大,溶液离子浓度:T K 。
c sp
③曲线下方区域的点均为不饱和溶液,此时Q