文档内容
第 28 讲 物质的分离、提纯和检验
目录
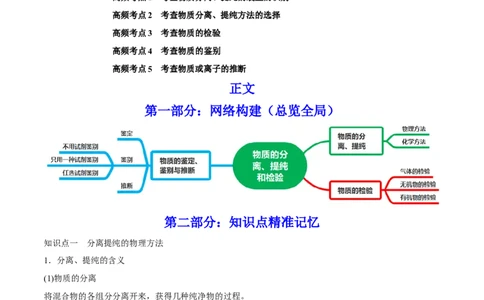
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
第三部分:典型例题剖析
高频考点1 考查物质分离、提纯的装置的识别
高频考点2 考查物质分离、提纯方法的选择
高频考点3 考查物质的检验
高频考点4 考查物质的鉴别
高频考点5 考查物质或离子的推断
正文
第一部分:网络构建(总览全局)
第二部分:知识点精准记忆
知识点一 分离提纯的物理方法
1.分离、提纯的含义
(1)物质的分离
将混合物的各组分分离开来,获得几种纯净物的过程。
(2)物质的提纯
将混合物中的杂质除去而得到纯净物的过程,又叫物质的净化或除杂。
2.物理方法中物质分离与提纯的常见实验装置
(1)过滤
适用范围 把不溶性固体与液体进行分离
注意 一贴 滤纸紧贴漏斗内壁滤纸上缘低于漏斗口
二低
液面低于滤纸上缘
事项 烧杯紧靠玻璃棒
三靠 玻璃棒下端紧靠三层滤纸处
漏斗下端紧靠烧杯内壁
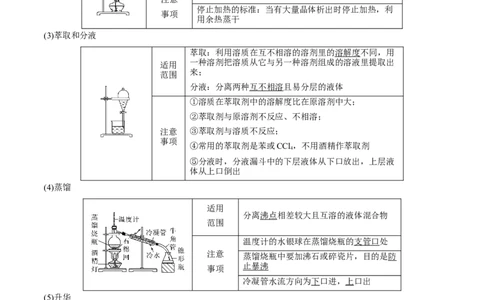
(2)蒸发
适用
分离易溶性固体的溶质和溶剂
范围
玻璃棒的作用:搅拌,防止液体局部过热而飞溅
注意
停止加热的标准:当有大量晶体析出时停止加热,利
事项
用余热蒸干
(3)萃取和分液
萃取:利用溶质在互不相溶的溶剂里的溶解度不同,用
适用 一种溶剂把溶质从它与另一种溶剂组成的溶液里提取出
范围 来;
分液:分离两种互不相溶且易分层的液体
①溶质在萃取剂中的溶解度比在原溶剂中大;
②萃取剂与原溶剂不反应、不相溶;
注意 ③萃取剂与溶质不反应;
事项
④常用的萃取剂是苯或CCl ,不用酒精作萃取剂
4
⑤分液时,分液漏斗中的下层液体从下口放出,上层液
体从上口倒出
(4)蒸馏
适用
分离沸点相差较大且互溶的液体混合物
范围
温度计的水银球在蒸馏烧瓶的支管口处
注意 蒸馏烧瓶中要加沸石或碎瓷片,目的是防
事项 止暴沸
冷凝管水流方向为下口进,上口出
(5)升华
适用
分离某种组分易升华的固体混合物
范围
注意 如NaCl固体中的I 可用该方法分离,但NH Cl
2 4
事项 固体中的I 2 不能用升华的方法分离
(6)洗气适用范围 除去气体中的杂质
注意事项 长管进气,短管出气
(7)过滤装置的创新——抽滤
由于水流的作用,使装置a、b中气体的压强减小,
故使过滤速率加快
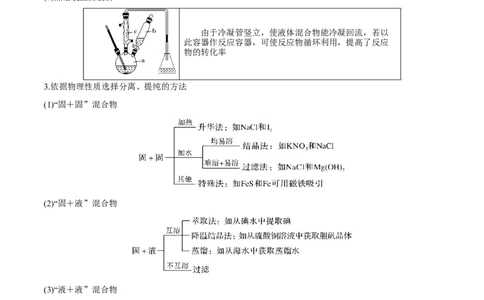
(8)蒸馏装置的创新
由于冷凝管竖立,使液体混合物能冷凝回流,若以
此容器作反应容器,可使反应物循环利用,提高了反应
物的转化率
3.依据物理性质选择分离、提纯的方法
(1)“固+固”混合物
(2)“固+液”混合物
(3)“液+液”混合物
知识点二 分离提纯的化学方法
1.化学方法分离、提纯物质遵循的“四原则”、“四必须”
(1)“四个原则”:一是不增加新的杂质;二是不减少被提纯物质;三是被提纯物质与杂质易分离;四是被
提纯物质易复原。(2)“四个必须”:一是除杂试剂必须过量;二是过量试剂必须除尽;三是除杂途径必须最佳;四是除去多
种杂质时必须考虑加入试剂的先后顺序。
2.分离提纯常用的化学方法
方法 原理 举例说明
电解精炼铜,将含杂质的粗铜作阳极,精铜作阴
电解法 利用电解原理分离和提纯物质
极,电解液为含铜离子的溶液
Cl-、SO、CO及能形成弱碱的金属阳离子可加入
沉淀法 将杂质离子转化为沉淀
适当的沉淀剂,使离子生成沉淀,过滤除去
将气体混合物通过洗气装置而 让混合气体通过盛有饱和食盐水的洗气瓶除去Cl
洗气法 2
除去杂质气体 中的少量HCl
酸碱溶解法 利用酸或碱将杂质溶解除去 用盐酸除去SiO 中的CaCO
2 3
氧化还原法 利用氧化还原反应除去杂质 用酸性KMnO 溶液除去CO 中SO
4 2 2
水解法 利用水解反应原理除去杂质 可用 CuO 、 Cu(OH) 等除去CuCl 溶液中的FeCl
2 2 3
CO、HCO、SO、HSO、NH等与H+或OH-反应
气化法 将杂质离子转化为气体
生成气体除去
用加热法除去固体混合物中易
热分解法 除去NaCl中的NH Cl
分解的物质 4
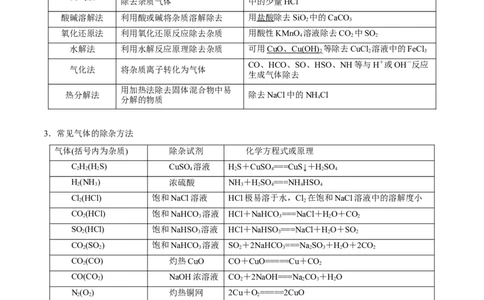
3.常见气体的除杂方法
气体(括号内为杂质) 除杂试剂 化学方程式或原理
C H(H S) CuSO 溶液 HS+CuSO ===CuS↓+HSO
2 2 2 4 2 4 2 4
H(NH ) 浓硫酸 NH +HSO ===NH HSO
2 3 3 2 4 4 4
Cl(HCl) 饱和NaCl溶液 HCl极易溶于水,Cl 在饱和NaCl溶液中的溶解度小
2 2
CO(HCl) 饱和NaHCO 溶液 HCl+NaHCO ===NaCl+HO+CO
2 3 3 2 2
SO (HCl) 饱和NaHSO 溶液 HCl+NaHSO===NaCl+HO+SO
2 3 3 2 2
CO(SO ) 饱和NaHCO 溶液 SO +2NaHCO ===Na SO +HO+2CO
2 2 3 2 3 2 3 2 2
CO(CO) 灼热CuO CO+CuO=====Cu+CO
2 2
CO(CO ) NaOH浓溶液 CO+2NaOH===Na CO+HO
2 2 2 3 2
N(O ) 灼热铜网 2Cu+O=====2CuO
2 2 2
CH(CH===CH 、 CH===CH +Br ―→CHBrCHBr
4 2 2 2 2 2 2 2
溴水
CHCH) HCCH+2Br ―→CHBr —CHBr
2 2 2
4.常见固体或溶液的除杂方法
物质(括号内为杂质) 除杂试剂或方法 化学方程式或原理 分离方法
NaCO 固体(NaHCO ) 加热 2NaHCO =====NaCO+HO+CO↑ —
2 3 3 3 2 3 2 2
加适量BaCl 溶
NaCl溶液(Na SO ) 2 NaSO +BaCl ===BaSO ↓+2NaCl 过滤
2 4 液 2 4 2 4
NaCl固体(NH Cl) 加热 NH Cl=====NH ↑+HCl↑ —
4 4 3FeCl 溶液(FeCl ) 加过量铁粉 2FeCl +Fe===3FeCl 过滤
2 3 3 2
FeCl 溶液(FeCl ) 通Cl 2FeCl +Cl===2FeCl —
3 2 2 2 2 3
NaHCO 溶液(Na CO) 通CO NaCO+CO+HO===2NaHCO —
3 2 3 2 2 3 2 2 3
Cu(NO ) 溶液(AgNO) 加过量铜粉 2AgNO+Cu===Cu(NO)+2Ag 过滤
3 2 3 3 3 2
I(SiO) 加热 I 升华、冷却、凝华,得I —
2 2 2 2
加过量NaOH溶
Fe O(AlO) Al O+2NaOH===2NaAlO +HO 过滤
2 3 2 3 液 2 3 2 2
NH Cl溶液(FeCl ) 加适量氨水 FeCl +3NH ·H O=Fe(OH) ↓+3NH Cl 过滤
4 3 3 3 2 3 4
KNO 固体(NaCl) 水 根据二者的溶解度随温度的变化不同 降温结晶
3
加适量NaOH溶
NaCl溶液(MgCl ) MgCl +2NaOH===Mg(OH) ↓+2NaCl 过滤
2 液 2 2
C(CuO) 加过量稀盐酸 CuO+2HCl===CuCl +HO 过滤
2 2
CuO(Fe) 磁铁 Fe能被磁铁吸引 —
CuS(FeS) 加过量稀盐酸 FeS+2HCl===FeCl +HS↑ 过滤
2 2
加过量NaOH溶
镁粉(铝粉) 2Al+2NaOH+2HO=2NaAlO +3H↑ 过滤
液 2 2 2
知识点三 常见物质的检验
1.物质检验的要求和一般步骤
1)物质检验对反应的一般要求
(1)反应要有良好的选择性,反应速率要快,并能反应完全。
(2)反应要有明显的外部特征,如:溶液颜色的改变、沉淀的生成或溶解、气体的生成等。
(3)要排除干扰物质的影响。
2)物质检验的基本步骤
(1)对试样进行外观观察:对试样进行外观观察的主要目的是利用被检验物质的颜色和状态,对可能含有的
某些组分进行推断,进而排除某些组分存在的可能性。
(2)试样的准备:不论是固体试样,还是液体试样,都只能取少量用于配制溶液或用于检验,要留有一定量
的试样备用。
(3)检验:在进行检验时,除了要考虑各离子的特征反应外,最重要的是要选取适当的措施排除离子之间可
能存在的干扰。只要排除干扰的方法得当,就可以设计出正确的实验方案
3)物质检验的原理
(1)依据物质的特殊性质进行检验。如物质的颜色、气味、溶解性等。
(2)依据物质间反应时所产生的特殊的反应现象。即所选的试剂和被检验的物质在发生化学反应时,必须能
够产生下列现象中的一种:①变色;②放出气体(通常指产生气体的气味或在溶液中反应时产生的气泡);
③生成沉淀等。
4)物质检验的方法
(1)物理方法:依据物理性质,如颜色、气味、溶解性、磁性等,通过观察、实验分析、判断,得出结论。
(2)化学方法:利用物质的特殊化学性质及反应时产生的特征现象。即所选的试剂与被检验的物质反应时要
有明显实验现象(如放出气体、生成沉淀或颜色改变),通过观察、分析,得出结论。5)答题要领:
(1)不用原瓶操作:鉴别的目的是为了以后的使用,若用原瓶操作,会污染原瓶中的试剂。要有“各取少许”字
样。
(2)不“指名道姓”:结论的得出,来自实验现象,在加入试剂之前,该物质是未知的,应该叙述为“若……(现象),
则证明有……”,叙述时不可出现“取某某物质加入某某试剂……”的字样,一般回答顺序为:各取少许→溶
解→加入试剂→描述现象→得出结论。
6)常见气体的检验
气体 检验特征性质 注意事项
O 使带火星的木条复燃 —
2
纯净的H 在空气中燃烧发出淡蓝色火焰,
2
H 在火焰上方罩一个干而冷的烧杯,烧杯的内 产物只有水
2
壁有水雾生成
在空气中燃烧产生淡蓝色火焰,在火焰上方
CH 罩一个干而冷的烧杯,烧杯的内壁有水雾生 产物有二氧化碳和水
4
成,同时生成能使澄清石灰水变浑浊的气体
在空气中燃烧产生淡蓝色火焰,生成能使澄
CO 产物只有二氧化碳
清石灰水变浑浊的气体
在空气中燃烧火焰明亮,有黑烟,可使溴
CH===CH —
2 2
水、酸性KMnO 溶液褪色
4
无色,有刺激性气味;能使品红溶液褪色, CO 也能使澄清石灰水变浑浊;SO
2 2
SO 加热后恢复红色;能使酸性KMnO 溶液褪 的漂白原理与新制氯水的漂白原理
2 4
色;能使溴水褪色;能使澄清石灰水变浑浊 不同
能使澄清石灰水变浑浊,能使燃着的木条熄 应注意区别,SO 也能使澄清石灰水
2
CO
2
灭 变浑浊,N 也能使燃着的木条熄灭
2
NO 无色气体,接触空气时立即变为红棕色 —
黄绿色,有刺激性气味,能使湿润的淀粉碘
Cl Cl 有毒,注意闻气味的方法
2 2
化钾试纸变蓝
NO 的颜色与溴蒸气相近,NO 溶于
2 2
红棕色,有刺激性气味,通入水中生成无色
NO AgNO 溶液无沉淀生成,而溴蒸气
2 3
溶液并产生无色气体,水溶液显酸性
溶于AgNO 溶液有淡黄色沉淀生成
3
无色,有刺激性气味,在潮湿的空气中形成
HCl极易溶于水,做相关实验时应
HCl 白雾;用蘸有浓氨水的玻璃棒靠近时冒白
防倒吸
烟;通入AgNO 溶液时有白色沉淀生成
3
无色,有刺激性气味,能使湿润的红色石蕊
NH 极易溶于水,做相关实验时应
3
NH 试纸变蓝;用蘸有浓盐酸的玻璃棒靠近时冒
3
防倒吸
白烟
7)常见离子的检验离子 检验方法
Cl-、Br 与稀HNO 酸化的AgNO 溶液反应,若产生白色、浅黄色或者黄色沉淀,则有
3 3
-、I- Cl-、Br-或者I-
SO 先加稀HCl酸化,再加BaCl 溶液,若产生白色沉淀,则有SO
2
做焰色反应实验,若火焰为黄色,则有Na+;透过蓝色钴玻璃观察,火焰为浅
Na+、K+
紫色,则有K+
先加足量的NaOH溶液,再加热,①用湿润的红色石蕊试纸靠近试管口,若试
NH 纸变蓝色,则有NH;②用蘸有浓盐酸的玻璃棒靠近试管口,若产生白烟,则
有NH
①先加KSCN溶液,无明显现象,再通入Cl ,若溶液变红色,则有Fe2+;②
2
Fe2+ 滴加NaOH溶液,若产生白色沉淀,且白色沉淀迅速变成灰绿色,最终变成红
褐色,则有Fe2+;③滴加K[Fe(CN) ]溶液,若产生蓝色沉淀,则有Fe2+
3 6
①滴加KSCN溶液,若溶液变红色,则有Fe3+;②滴加苯酚溶液,若溶液变紫
Fe3+
色,则有Fe3+;③滴加NaOH溶液,若立即产生红褐色沉淀,则有Fe3+
8)常见有机物的检验
(1)常用的检验有机物的试剂
有机物的性质主要是由其官能团决定的,有机物的检验,主要是官能团的检验,常用的试剂有:
①酸性KMnO 溶液:含碳碳双键或碳碳三键的有机化合物、苯的同系物、醇、苯酚、醛、甲酸、甲酸的酯
4
或盐、葡萄糖、麦芽糖等皆可使之褪色。
②溴水:含碳碳双键或碳碳三键的有机化合物、酚、醛、甲酸、甲酸的酯或盐、葡萄糖与溴水反应使溴水褪
色;苯的同系物、四氯化碳等可萃取溴水中的溴,使溴水褪色。
③银氨溶液:含醛基的有机物皆可发生银镜反应(注意发生反应和形成银镜的条件)。
④新制的Cu(OH) (碱性):a.含醛基的物质与其混合加热煮沸生成砖红色沉淀;b.羧酸可使其溶解得蓝色溶液;c.
2
多羟基化合物(丙三醇、葡萄糖等)使之溶解得绛蓝色溶液。
⑤FeCl 溶液遇苯酚显紫色;蛋白质(含苯环)与浓硝酸作用变黄色(颜色反应);淀粉与I 作用显蓝色。
3 2
(2)常见有机物的检验
①苯:能与液溴、铁屑反应,产生HBr,形成白雾。能与浓硫酸、浓硝酸的混合物反应,生成黄色的苦杏仁气味
的油状(密度大于1 g·cm-3)难溶于水的硝基苯。
②甲苯:取两份甲苯,一份滴入溴水,振荡后上层呈橙色;另一份滴入酸性KMnO4溶液,振荡,紫色褪去。
③卤代烷:与NaOH溶液(或NaOH的醇溶液)共热后,先用硝酸酸化,再滴加AgNO 溶液,产生白色沉淀的为氯
3
代烷,产生淡黄色沉淀的为溴代烷,产生黄色沉淀的为碘代烷。
④乙醇:加入金属钠,有气泡产生;与乙酸、浓硫酸共热产生果香味。
⑤苯酚:滴加过量的浓溴水,有白色沉淀;或滴加少量FeCl 溶液,溶液呈紫色。
3
⑥乙醛或葡萄糖:加入银氨溶液,水浴加热,产生银镜;或加入新制的Cu(OH) 加热至沸腾,有砖红色沉淀生成。
2
⑦乙酸:使石蕊溶液变红;或加入NaCO 或NaHCO 溶液有气泡产生;或加入新制的Cu(OH) 溶解得蓝色溶液;
2 3 3 2
或与乙醇、浓硫酸共热,产生果香味。⑧乙酸乙酯:加入滴有酚酞的NaOH溶液加热,红色变浅或消失。
⑨淀粉:滴加碘水,呈蓝色。
⑩蛋白质:灼烧,有烧焦羽毛气味;或加入浓硝酸微热,出现黄色。
(3)检验与鉴别有机物的四种主要方法
①检验有机物溶解性:通常是加水检查、观察是否能溶于水。例如:用此法可以鉴别乙酸与乙酸乙酯、乙醇
与氯乙烷、甘油与油脂等。
②检查液态有机物的密度:观察不溶于水的有机物在水中浮沉情况,可知其密度比水的密度小还是大。例如,
用此法可以鉴别硝基苯与苯、四氯化碳与1-氯丁烷。
③检查有机物燃烧情况:如观察是否可燃(大部分有机物可燃,四氯化碳和少数有机物不可燃)、燃烧时黑烟的
多少(可区分乙烷、乙烯和乙炔,己烯和苯,聚乙烯和聚苯乙烯)、燃烧时的气味(如识别聚氯乙烯和蛋白质)。
④检查有机物的官能团:结构决定性质,官能团体现结构,选取典型试剂检验对应的官能团是有机物检验的关
键。
知识点四 常见物质的鉴定、鉴别和推断
1.概念:
(1)鉴别是指对两种或两种以上的物质进行定性辨认。
(2)鉴定是指用化学方法来确定未知物质的组成,各组成部分一定要逐一检验出来,鉴定又分为定性和
定量两种。
(3)推断是通过已知实验事实,根据性质分析推理出物质的组成、结构或名称。
2.物质鉴别的思路
(1)鉴别主要是寻找各物质的特殊现象,包括颜色、状态、气味、反应情况等。
(2)如果要加入试剂进行鉴别,一定要先取样,不能直接对样品进行鉴别。
(3)选用鉴别方法时先简单后复杂,先考虑物理方法后化学方法。
3.物质鉴别的原则
操作简便 能用物理方法鉴别的不用化学方法,能用一种试剂鉴别的不用多种试剂
现象明显 使待鉴别的物质之间的现象对比度较大
防止干扰 区别Cl-和SO时,只能用BaCl 溶液不能用AgNO 溶液
2 3
4.物质鉴别的一般类型和方法
分类 鉴别方法
①先依据外观特征,鉴别出其中的一种或几种,然后再利用它或它们去鉴别其
他几种物质
②若均无明显外观特征,可考虑能否用加热或焰色反应等方法鉴别出一种或几
不用试剂
种物质
③若以上两种方法都不能鉴别时,可考虑两两混合或相互滴加,记录反应现
象,分析确定
只用一种 ①先分析被鉴别物质的水溶性、密度、颜色等,初步将被鉴别物质确定或分组
试剂
②在鉴别多种酸、碱、盐的溶液时,可依据“相反原理”确定试剂进行鉴别。即被鉴别的溶液多数呈酸性时,可选用碱或水解呈碱性的盐溶液作试剂;若被
鉴别的溶液多数呈碱性时,可选用酸或水解呈酸性的盐溶液作试剂
③可考虑用已检出的物质为试剂做后续鉴别
此类题目不限制所加试剂的种类或在指定范围内选择试剂,可有多种解法,题
任选或限
目考查的形式往往是从众多的鉴别方案中选择最佳方案,其要求是操作步骤简
选试剂
单,试剂选用最少,现象最明显
5.推断
1)推断是通过已知实验事实,根据性质分析推理出物质的组成、结构或名称。
2)推断与鉴别、鉴定的区别在于:鉴别、鉴定中的每一步都靠自己设计,可以尽自己的长处选比较熟悉的
知识;推断则不然,条件已给出,虽只回答结论,但环上套环,答题者必须根据题设的用意回答问题,往往
思考难度大。
第三部分:典型例题剖析
高频考点1 考查物质分离、提纯的装置的识别
例1.(2022·广东广州·三模)下列实验装置不能用于物质分离提纯的是
A B C D
【变式训练】(2022·江苏·模拟预测)已知氨水可以与溴反应:3Br +8NH•H O=N↑+6NHBr+8H O。下
2 3 2 2 4 2
面提纯粗溴苯(含溴苯、溴和苯),同时得到NH Br晶体的原理与装置不能达到实验目的的是
4
A.用装置甲除去溴苯中的溴 B.用装置乙分离甲中反应后的混合液
C.用装置丙蒸干溶液得到NH Br晶体 D.用装置丁分离溴苯与苯
4
高频考点2 考查物质分离、提纯方法的选择
例2.(2022·湖南·永州市第一中学高三期中)为提纯下列物质,除杂药品和分离方法错误的是
选项 被提纯的物质(杂质) 除杂药品 分离方法A 蛋白质溶液(葡萄糖) 硫酸铜溶液 盐析、过滤、洗涤、溶解
B 溴苯(溴) NaOH溶液 分液
C NH Cl溶液(FeCl ) 氨水 过滤
4 3
D 苯甲酸(NaCl) 水 重结晶
【变式训练】(2022·湖南师大附中高三阶段练习)为提纯下列物质,除杂药品和分离方法都正确的是
被提纯的物质(杂质) 除杂药品 分离方法
A 乙醇(乙酸) CaO 蒸馏
B KBr溶液(KI) 氯水、CCl 萃取、分液
4
C 氯化铝溶液(氯化铁) 氨水 过滤
D CO(SO ) 饱和NaCO 溶液 洗气
2 2 2 3
高频考点3 考查物质的检验
例3.下列关于某无色溶液中离子检验的操作、现象与结论对应正确的是
检验操作 现象 结论
产生白色沉
A 加入盐酸酸化的氯化钡
淀
一定有SO
B 加入酚酞溶液 溶液显红色 一定有
产生无色气
C 加入足量稀盐酸
体
一定有CO
产生白色沉
D 加入硝酸银 一定有
淀
【变式训练】(2022·山东·泰安市基础教育教学研究室高三期末)下列关于离子检验的说法中正确的是
A.向某溶液中加入稀盐酸,将产生的无色无味气体通入澄清石灰水中,石灰水变浑浊,则原溶液中一定
含有 或
B.向某溶液中加入 溶液有白色沉淀产生,再加稀盐酸,沉淀不消失,则原溶液中一定有
C.向溶液中先加入 溶液,再滴加 溶液,溶液变红,则原溶液中含 而不含
D.向某溶液中加入 溶液产生白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定有高频考点4 考查物质的鉴别
例4.(2022·四川绵阳·模拟预测)下列各组 物质能用一种试剂鉴别的是
A.乙酸、乙醇、苯 B.硝基苯、溴乙烷、四氯化碳
C.硝基苯、溴苯、苯 D.乙烷、乙烯、乙炔
【变式训练】(2022·上海普陀·二模)下列实验合理的是
A.用新制氢氧化铜悬浊液(必要时可加热)鉴别甲酸与乙酸
B.用澄清石灰水鉴别SO 与CO
2 2
C.用淀粉-KI试纸鉴别碘水与FeCl 溶液
3
D.用湿润的pH试纸测定CHCOONa的pH
3
高频考点5 考查物质或离子的推断
例5.(2022·上海静安·二模)某强酸性溶液中可能存在Al3+、Fe2+、NH 、Ba2+、Cl-、CO 、SO 、NO
中的若干种。为确定溶液的组成进行了如下实验:
ⅰ. 取100mL原溶液,加入足量Ba(NO ) 溶液,有白色沉淀a和无色气体b生成,过滤得滤液c。
3 2
ⅱ. 往滤液c中加入足量的NaOH溶液并加热,可得气体d和沉淀e,过滤得滤液f。
ⅲ. 取滤液f,通入少量的CO,有白色沉淀g生成。
2
下列有关判断正确的是
A.试液中一定没有Ba2+、CO 、NO 、Cl-
B.试液中一定有Fe2+、NH 、SO
C.气体b和气体d在一定条件下能反应生成盐
D.沉淀g一定含有Al(OH) ,可能含有BaCO
3 3
【变式训练】(2022·浙江绍兴·模拟预测)下列方案设计、现象、解释或结论有错误的是
选
实验操作 实验现象 解释或结论
项
摘下几根火柴头浸于水中,一定时间后取适量溶液于试管
A 出现白色沉淀 火柴头含有氯元素
中,加 溶液、稀硝酸和 溶液。
向 的 溶液中加入几滴 溶液,制得新
B 绛蓝色溶液 牙膏中存在甘油
制 然后加入适量牙膏
C
将石蜡油与碎瓷片混合加强热,产生的气体通入酸性重铬酸 酸性重铬酸钾 石蜡油加强热产生钾钾溶液中 溶液褪色 的气体是不饱和烃
取 溶液于试管中,滴加 白色沉淀转化 溶解度大于
D
为黄色沉淀
溶液,待不再出现白色沉淀后,再滴加 溶液